UPLC-MS 同时测定赤芍中五个指标成分的含量
2015-01-11李月婷侯靖宇王爱民
胡 杰,李月婷,侯靖宇,王爱民,黄 勇*
1 贵阳医学院药学院 贵州省药物制剂重点实验室;2 贵阳医学院 民族药与中药开发应用教育部工程研究中心,贵阳 550004
赤芍为毛茛科植物芍药(Paeoniae lactiflora Pall.)或川赤芍(Paeoniae veitchii Lynch)的干燥根[1]。其味苦、微寒、归肝经,具有清热凉血、散瘀止痛之功效,是中药中具有代表性的活血化瘀药物,在临床上应用广泛。现代药理研究发现,赤芍具有多方面的作用,如抗血栓形成、抗血小板聚集、抗菌、抗炎、抗病毒等[2]。鉴于赤芍药效作用广泛、成分多样,宜选用多指标成分测定的方法,较为全面、综合地反映和控制赤芍的质量[3-5]。文献报道,赤芍的主要有效部位为芍药总苷,其中包括芍药内酯苷、氧化芍药苷、芍药苷、苯甲酰芍药苷等[6]。本实验采用UPLC-MS 联用技术对12 批不同产地赤芍药材中芍药内酯苷、氧化芍药苷、芍药苷、苯甲酰芍药苷和没食子酸5 种指标成分进行含量测定,为赤芍药材的质量控制提供参考依据[7]。
1 仪器与材料
1.1 实验仪器
ACQUITY 系统超高效液相色谱-三重四级杆串联质谱仪,包括二元梯度泵、自动进样器、柱温箱、三重四级杆质量分析器和Masslynx4.1 质谱工作站(美国waters 公司)。
1.2 实验材料
没食子酸(1)和葛根素(6)对照品(均购自中国食品药品检定研究院,批号分别为110831-200803、0752-9605,纯度≥98%);氧化芍药苷(2)、芍药内酯苷(3)、芍药苷(4)、苯甲酰芍药苷(5)对照品(均购自中药固体制剂制造技术国家工程研究中心,批号分别为Y10-130912、S37-100126、110736–200934、B14-130912,纯度≥98%);乙腈、甲酸为色谱纯,甲醇为分析纯。
赤芍药材来源见表1,由贵阳医学院药学院药用植物学与生药学教研室龙庆德副教授鉴定为毛茛科植物芍药(P.lactiflora Pall.)或川赤芍(P.veitchii Lynch)的干燥根。
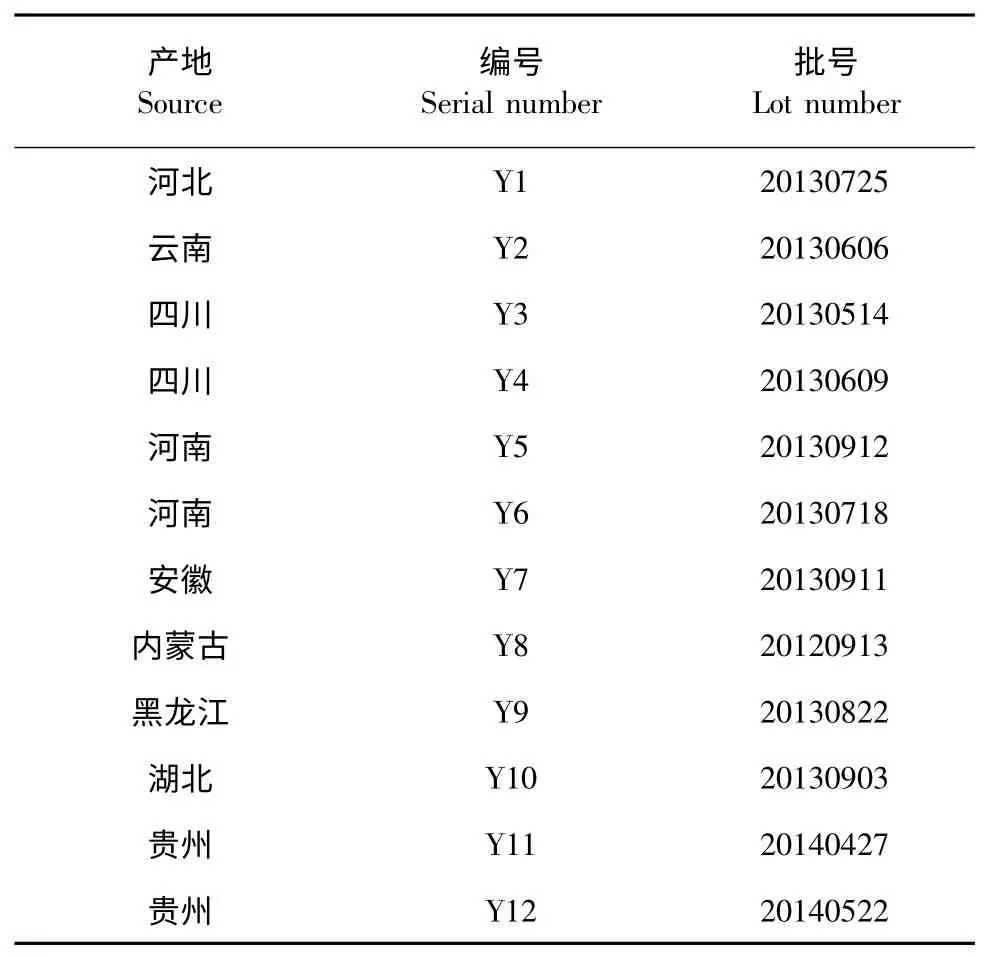
表1 赤芍药材来源表Table 1 Source of Radix Paeoniae Rubra
2 方法与结果
2.1 色谱条件
色谱柱为Acquity UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm);流动相0.1%甲酸乙腈溶液(A)-0.1%甲酸水溶液(B),梯度洗脱(0~3.0 min,5%~25%A;3.1~4.0 min,25%~90%A;4.1~5.0 min,90%~5%A);流速0.35 mL/min;柱温45 ℃;进样量1 μL;分析时间为5 min。
2.2 质谱条件
采用电喷雾离子源(ESI),毛细管电压3 KV,离子源温度120 ℃,去溶剂气(氮气)650 L/h,去溶剂气温度350 ℃,碰撞气(氩气)0.18 mL/min;选择性离子监测(SIR)模式进行正负离子同步监测;没食子酸等六种成分用于定量分析的监测离子见表2。
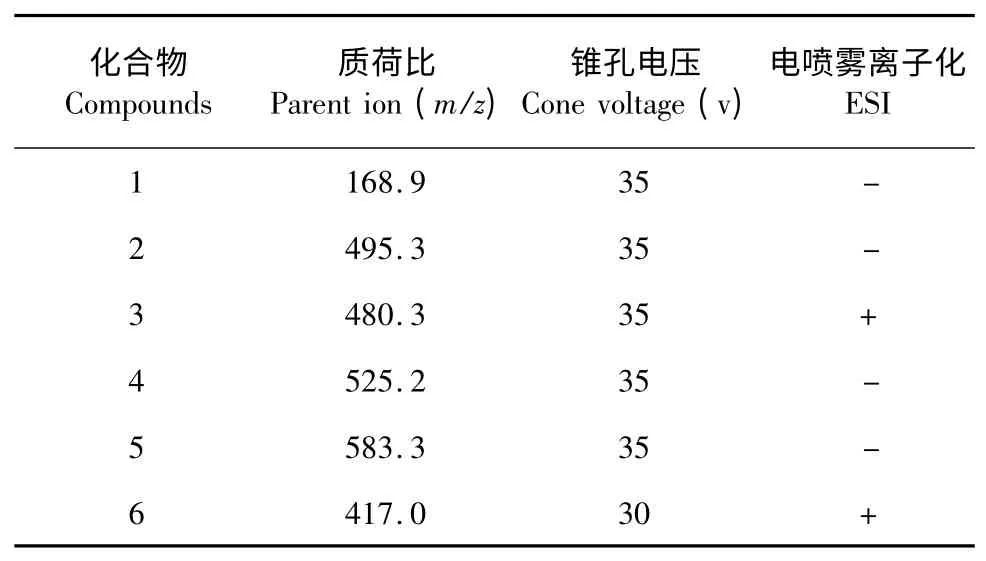
表2 质谱分析条件Table 2 MS analysis condition
2.3 溶液配制
2.3.1 对照品溶液
分别精密称取1~5 对照品10 mg,各置10 mL棕色容量瓶中,用甲醇溶解并定容,制得1 mg/mL的1~5 对照品储备液;精密称取内标6 对照品10 mg,置于10 mL 容量瓶中,用甲醇溶解并定容,从10 mL 容量瓶中吸取2 mL 溶液置于100 mL 容量瓶中,用甲醇定容,制得0.02 mg/mL 的6 对照品储备液。
2.3.2 供试品溶液
精密称取供试品约1.0 g,置于具塞锥形瓶中,加入甲醇25 mL,称定重量,浸泡4 h,超声30 min,再称定重量,用甲醇补足减失的重量,摇匀,滤过,离心(15000 g)10 min,取上清液进样。
2.4 专属性试验
分别精密称取1~6 对照品适量,制成1~6 浓度分别为20.0、20.5、20.1、21.4、20.2 和20 μg/mL的混合对照品溶液。精密吸取混合对照品溶液和赤芍药材溶液各1 μL,分别进样,结果见图1。供试品溶液中被测定化合物与6 个对照品的保留时间相同。比较被测定成分和对照品的质谱图,两者一致,表明本法专属性良好。
2.5 线性试验
分别取“2.3”项下1~5 对照品储备液适量,制成1~5 浓度分别为31.25、2.78、30.75、75.04、40.36 μg/mL 的混合对照品溶液。依次逐级稀释,再分别加如一定量的20 μg/mL 的葛根素内标,制得6个浓度的系列浓度线性工作液,分别进样测定。以对照品浓度c(X)为横坐标,色谱峰面积与内标峰面积比值As/Ai(Y)为纵坐标,进行线性回归。回归方程、定量限(LOQ)和检测限(LOD)等结果见表3。
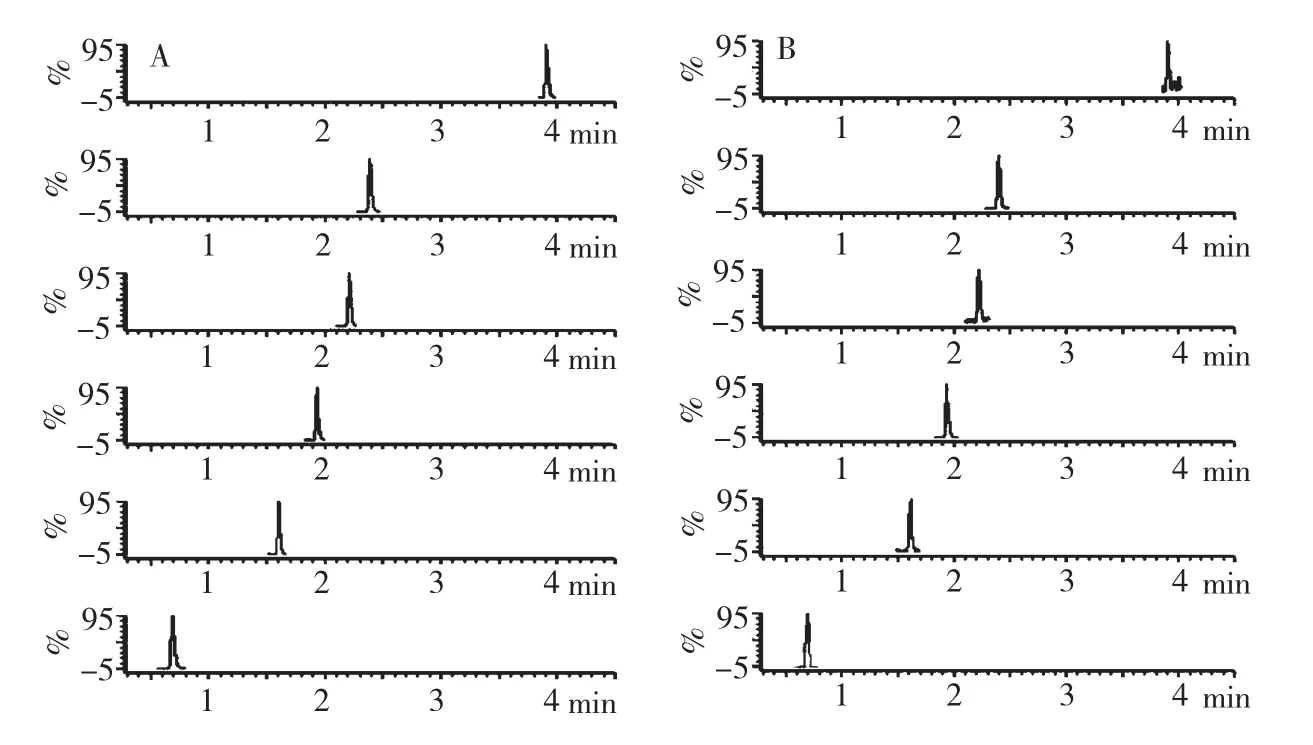
图1 混合对照品溶液(A)和供试品溶液(B)的UPLC-MS 选择离子色谱图Fig.1 UPLC-MS selected ion chromatograms of reference substances(A)and sample(B)
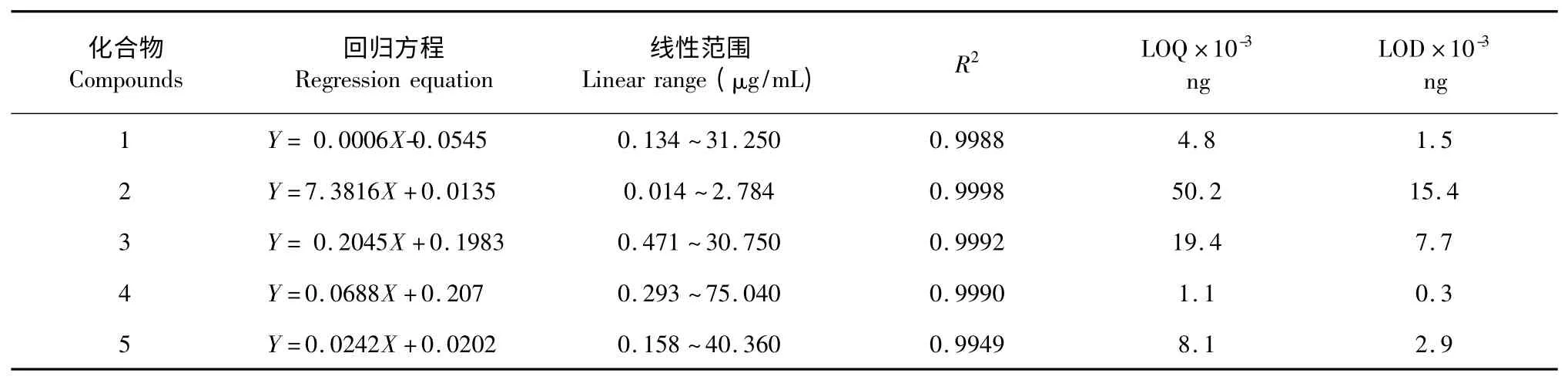
表3 5 种成分的线性关系Table 3 Linear relationships of the 5 investigated compounds
2.6 重复性试验
取同批赤芍药材,按“2.3”项下方法平行制备6份供试品溶液,分别进样测定,计算1~5 含量的RSD 分别为4.60%、3.71%、4.32%、4.05% 和4.45%,表明本方法重复性良好。
2.7 精密度试验
同批的供试品溶液,连续测定3 d,每天进样6次,测定峰面积并计算含量,结果1~5 的日内和日间RSD(%,n=6)分别为4.80%、4.67%、3.27%、4.37%和2.84%,表明仪器精密度良好。
2.8 稳定性试验
取同一供试品溶液,分别于处理后0、2、4、8、12 h 进样分析,1~5 含量的RSD 分别为4.20%、3.83%、4.03%、4.17%和2.61%,表明供试品溶液在12 h 内稳定性良好。
2.9 回收率试验
精密称取9 份已知含量的赤芍样品适量,平均分为3 组,分别精密吸取125、250 和375 μL 的混合标准溶液(1~5 浓度分别为5.00、1.28、7.53、18.76和2.52 μg/mL)样品测定,制成低、中、高浓度的质控样品,室温挥干,按“2.3”项下方法制备供试品溶液,分别进样测定,结果见表4。
2.10 样品测定
按“2.3”项下方法制备12 批样品的供试品溶液,分别进样测定,计算得样品中1~5 的含量,结果见表5。
除Y3 和Y4 外,其余批次的药材皆符合《中国药典》对赤芍药材的质量要求1。12 批药材里,Y6中芍药苷的含量最高,但五个有效成分综合含量最高的是Y9。
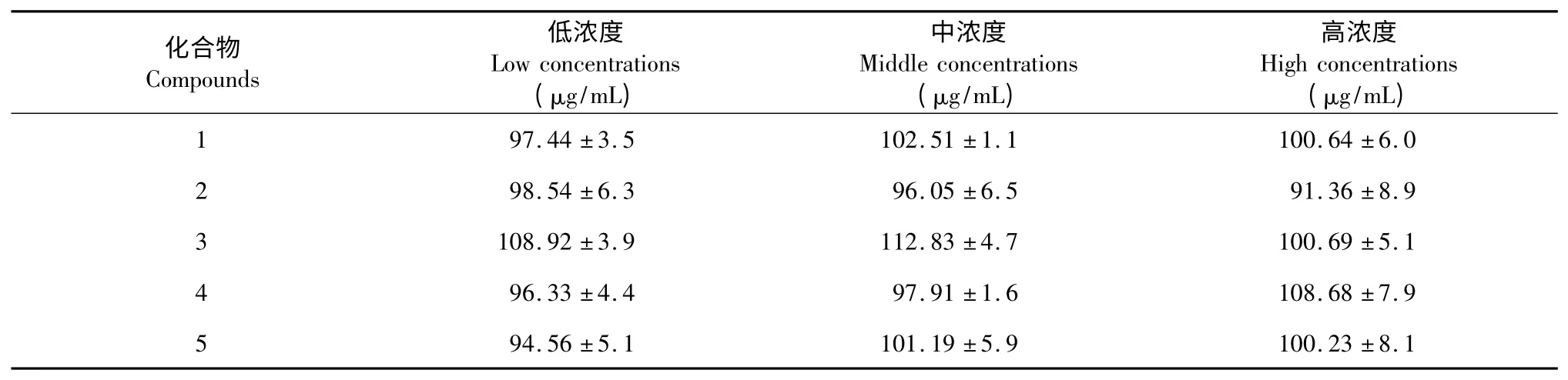
表4 回收率试验结果(%,n=3)Table 4 Testing results of recovery(%,n=3)
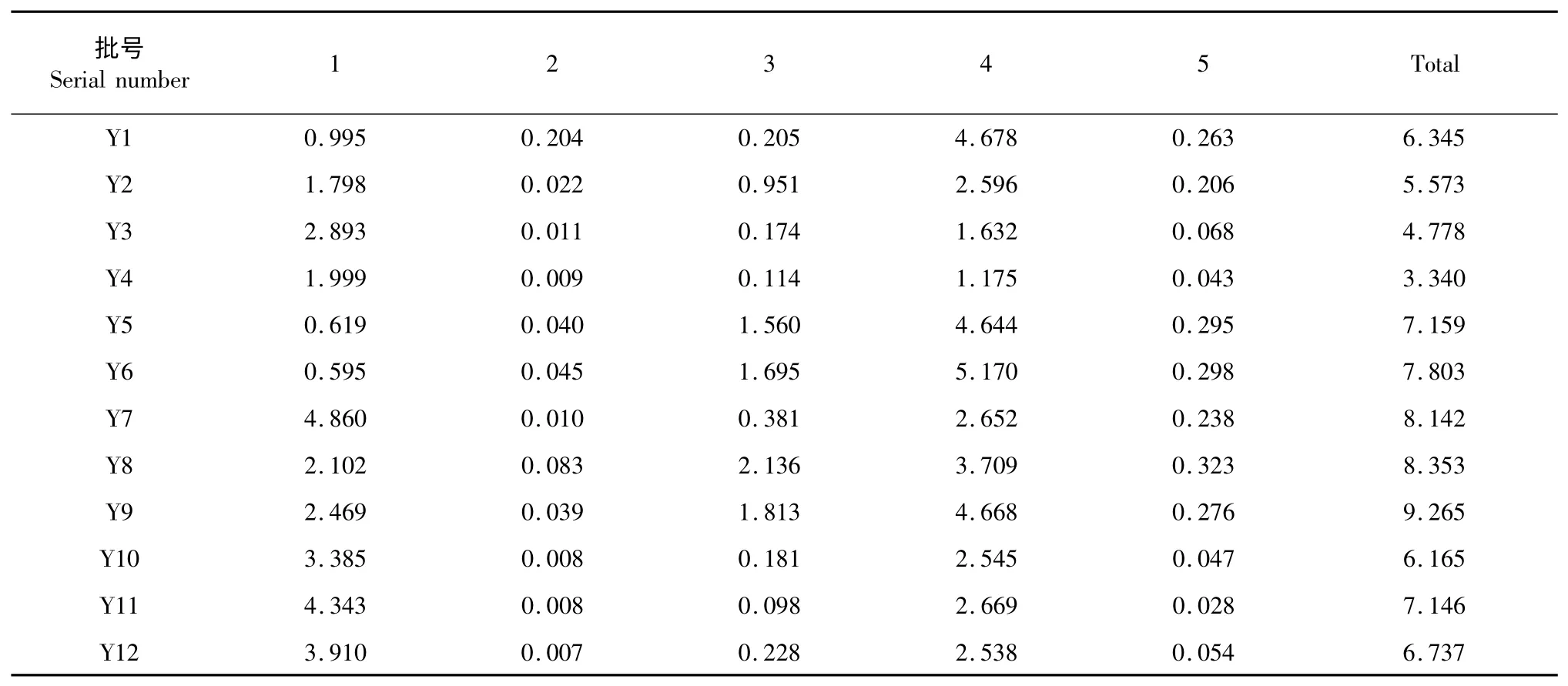
表5 12 批赤芍药材中5 个成分的含量(%,n=3)Table 5 Determination of 5 compounds from 12 batches of Radix Paeoniae Rubra samples(%,n=3)
3 讨论
目前,大多机构遵循《中国药典》,通过测定中药中某一有效成分的含量来评价该药材的优劣[1,8]。但中药作为一种多疗效多靶点的复杂天然药物,单一成分的含量并不能体现其真实药效,因此,对中药有效部位中包含的各成分综合测定,能够实现对该中药质量较全面地评价[6,9]。
本实验采用UPLC-MS 联用技术,将UPLC 对中药复杂成分的高分离度与MS 的高灵敏度、高选择性以及能够提供相对分子量与结构信息的优点结合起来,建立了应用UPLC-MS 同时测定赤芍药材中5个指标成分的方法[10]。该方法具有专属性强、灵敏度高、稳定性好的优点,并且分析速度快,仅5 min就能够完成检测工作,较大地提高了分析效率,为中药复杂样品检测分析、质量控制提供了一种更高效的方法[11]。
1 Chinese Pharmacopoeia Commission(国家药典委员会).Pharmacopoeia of the People’s Republic of China(中华人民共和国药典).Beijing:China Medical Science Press,2010.Vol I,11.
2 Hsieh CL,Yen GC.Antioxidant actions of Du Zhong(Eucommia umoides Oliv.)toward oxidative damage in biomolecules.Life Sci,2000,66:1387-1400.
3 Li YM(李咏梅),Gong Y(龚元).The latest research progression for the chemical constituents and pharmacology of Polygonum capitatum.J Guizhou Univ,Nat Sci(贵州大学学报,自科版),2007,24:205.
4 Huang Y(黄勇),He F(何峰),Zheng L(郑林),et al.Determination of eight marker compounds in flowers of Polygonum orientale by UPLC-MS/MS.Chin Pharm J(中国医药工业杂志),2012,43:70-73.
5 Xiong AZ(熊爱珍),Yang L(杨莉),Yang XJ(杨雪晶),et al.Simultaneous quantitation adonifoline and senecionine in Senecio herbs by UPLC-MS.Chin J Chin Mater Med(中国中药杂志),2011,36:702-705.
6 Ji LX(冀兰鑫),Huang H(黄浩),Li CZ(李长志),et al.Review in research of Radix Paeoniae Rubra.Drug Eval Res(药物评价研究),2010,(3):233-236.
7 Zhao HX(赵焕新),Bai H(白虹),Li W(李巍),et al.Chemical constituents from Polygonum capitatum.Nat Prod Res Dev(天然产物研究与开发),2011,23:262-266.
8 Zhou XG,Chen SX,Wei DH,et al.Determination of paeoniflorin and albiflorin contents in different germplasms and parts of Paeonia lactiflora Pall.Medicinal Plant,2013,4:70-73.
9 Zheng L(郑林),Mou JL(牟景丽),Tang L(唐丽).Simultaneous determination of two components of Xin Shao extract in rat plasma by UPLC-MS and their pharmacokinetics and absolute bioavailability.Chin Hosp Pharm J(中国新药杂志),2014,23:819-823.
10 Li YJ(李勇军),Luo HF(骆洪峰),Wang YL(王永林),et al.Studies on the chemical constituents of flavonoids from Polygonum capitatum.Chin Pharm J(中国药学杂志),2000,35:300-302.
11 Ma B(马冰),Wang J(王晶),Liu CM(刘春明),et al.RPHPLC method comparative study of different extraction methods on the content of plaeoniflorin from Radix Paeoniae Rubra.Lishizhen Med Mater Med Res(时珍国医国药),2013,24:1820-1822.
