甜荞麦壳原花色素微波辅助提取工艺研究
2015-01-08温志英
温志英,刘 晶,江 柳
河北经贸大学生物科学与工程学院,石家庄 050061
荞麦属蓼科双子叶植物,有甜荞麦(Fagopyrum esculentumMoench)和苦荞麦(Fagopyrum tataricumGaertn)两个主要栽培品种。我国是世界荞麦主要生产国之一,也是世界荞麦的起源中心,产量和总种植面积均居世界第二位[1]。在我国,荞麦籽粒多制粉后食用,而荞麦壳没有得到充分利用,一部分制成荞麦枕头,剩余的就进行基肥或者焚烧[2]。
国内外研究证实荞麦壳中富含黄烷醇类聚合物——原花色素[3-5]。原花色素(Proanthocyanidins,简称PC),是一类以黄烷-3-醇为主要结构单元的缩合多酚类化合物,由儿茶素、表儿茶素聚合而成,它普遍存在于植物的根、茎、叶、花、果实和树皮中,已发现的原花色素含量较高的植物超过600 种[6,7]。植物中的原花色素多数是不同聚合度的混合物,具有很强的生物活性,能够清除人体内过剩自由基,提高人体免疫能力,并具有较强的抗氧化能力,可作为防癌、抗突变、防治心血管疾病药物的主要有效成分和用作安全无毒的新型天然抗氧化剂[8]。现已在临床医学、化妆品、保健食品等领域得到应用[9]。国内有关原花色素的研究中,以葡萄籽、花生红衣为来源的原花色素研究得最为深入、广泛[10-13]。但有关荞麦壳中原花色素的研究少有文献涉及。
目前原花色素多采用传统的有机溶剂提取[14],本实验旨在以甜荞麦壳为原料,应用微波辅助提取技术[15]对甜荞麦壳中原花色素的提取方法进行研究,不仅速度快、成本小,且提高了提取率,同时结合响应曲面法优化了提取工艺条件,这可为合理有效地综合利用荞麦壳资源、构建农业固体废弃物资源利用的绿色模式提供有价值的参考。
1 材料与仪器
1.1 试剂与材料
甜荞麦壳:市售,产地为内蒙古。
儿茶素标准品:中国药品生物制品检定所(批号877-200001);颗粒活性碳,国药化学试剂有限公司;无水乙醇、甲醇:天津市红岩化学试剂厂;香草醛、石油醚:天津市津东天正精细化学试剂厂;浓盐酸:北京化学试剂公司。以上试剂均为分析纯。
1.2 仪器与设备
BS124S 电子天平,北京赛多利斯仪器系统有限公司;HH-4 型恒温水浴锅,金坛市科兴仪器厂;RA-8 微波萃取仪,上海博奥微波能设备有限公司;DFY-300 g 摇摆式高速中药粉碎机,温岭市大德中药机械有限公司;SHD-Ⅲ型循环水式多用真空泵,保定市高新区阳光科教仪器厂;722E 型分光光度计,上海光谱仪器有限公司;72-1 型电热恒温干燥箱,湖北省黄石市医疗器械厂。
2 实验方法
2.1 原料处理
甜荞麦壳在60 ℃下干燥24 h,在粉碎机中进行粉碎,过80 目筛,按1∶20(m/V)的比例加入石油醚并在30 ℃浸泡脱脂5 h,在真空泵中进行抽滤,滤渣在通风橱里除去残留的石油醚24 h,得脱脂甜荞麦壳粉末,干燥器中保存备用。
2.2 原花色素的提取
准确称取脱脂后的甜荞麦壳粉末1.0 g,置于150 mL 具塞三角瓶中,加入一定体积一定浓度的乙醇溶液,水浴30 min,微波提取,真空泵抽滤,活性炭脱色30 min,过滤,定容。利用香草醛-盐酸法测定原花色素含量。
2.3 原花色素得率的测定
采用香草醛-盐酸法[16,17]:取待测液1 mL,依次加入4%香草醛-甲醇溶液6 mL,浓盐酸3 mL,混匀后于室温条件下显色15 min,波长500 nm 处测定吸光度,用4%香草醛甲醇液做空白对照。整个过程注意避光操作。
儿茶素标准曲线的绘制:精确称取儿茶素标准样品配制1.0 mg/mL 标准溶液,分别取0、0.5、1、1.5、2、2.5 mL,定容10 mL,以香草醛-浓盐酸法测吸光度,绘制儿茶素标准曲线。

式中:C—查标准曲线对应的原花色素的含量(mg/mL);V—待测定样品液的体积,mL;m—样品质量,g;n—样品溶液稀释倍数。5.98%—甜荞麦壳水分含量。
2.4 单因素实验
称取甜荞麦壳粉1.0 g,以乙醇溶液为提取液,以甜荞麦壳原花色素得率作为提取原花色素的标准,分别考察料液比、乙醇体积分数、水浴温度,微波功率和微波时间对甜荞麦壳原花色素得率的影响。
2.5 Plackett-Burman 实验设计
在5 个单因素实验基础上,利用Minitab 16 软件的Plackett-Burman 设计对甜荞麦壳原花色素微波提取工艺影响因素的显著性进行考察,选取5 个影响因子,以得率为响应值进行二级水平试验。Plackett-Burman 实验因素水平表见表1。

表1 Plackett-Burman 实验因素水平及编码Table 1 Factors and levels of Plackett-Burman design
2.6 响应面法设计
根据响应面分析软件提供的模型,以原花色素得率为响应值,在单因素实验和Plackett-Burman 实验基础上,设计乙醇体积分数、微波时间、微波功率为因素,进行3 因素3 水平的响应面实验分析,优化甜荞麦壳原花色素的微波辅助提取条件。数据运用Design-Expert 7.0 统计软件处理。
3 结果分析
3.1 儿茶素标准曲线
配制1.0 mg/mL 儿茶素标准溶液,以吸光度为横坐标,儿茶素质量浓度为纵坐标,以香草醛—盐酸法绘制儿茶素标准曲线,并求出其线性回归方程为y=0.263x-0.007,R2=0.999。
3.2 单因素实验
3.2.1 乙醇体积分数对甜荞麦壳原花色素得率的影响
由图1A 可知,随着乙醇浓度增大,原花色素得率呈上升趋势,这是由于以乙醇-水溶液作为提取剂,能加速原花色素与多糖、蛋白质分子之间氢键的断裂,使原花色素分子顺利游离至细胞外,从而增大原花色素得率。乙醇体积分数为30%时原花色素得率最大,之后乙醇体积分数继续增大,原花色素得率呈下降趋势,原因主要是由于亲脂性强的成分溶出量增加,导致原花色素与乙醇-水分子的结合率降低,原花色素得率随之降低。
3.2.2 料液比对甜荞麦壳原花色素得率的影响
从传质速率的角度讲,料液比的提高必然会在较大程度上提高传质推动力,但也提高了生产成本及后续处理难度,故料液比不宜太高。由图1B 可知,在料液比为1∶30 g/mL 之前,得率随料液比的增大而增大,在1∶30 g/mL 时达到最大,但在1∶30 g/mL 之后,得率稍有下降。因此,可选择料液比1∶30 g/mL。

图1 乙醇体积分数(A)、料液比(B)、微波功率(C)、微波时间(D)、水浴温度(E)对荞麦壳原花色素得率的影响Fig.1 Effects of ethanol concentration (A),solid to liquid ratio (B),microwave power (C),microwave time (D)and bath temperature (E)on the yield of proanthocyanidins
3.2.3 微波功率对甜荞麦壳原花色素得率的影响
微波功率主要是影响升温速度,功率越大温度升高越快。从图1C 可以看出,微波火力在160 W时,得率最大,自此之后逐渐减小。由此可见,当微波时间一定时,微波火力的增加可能会导致部分活性成分损失,原花色素得率下降。
3.2.4 微波时间对甜荞麦壳原花色素得率的影响
由图1D 可以看出,随着微波萃取时间延长,原花色素的得率在30 s 时得率达到最高,时间再延长,得率下降,故适宜的萃取时间是30 s。微波时间与原花色素得率高低密切相关。由于原花色素是热不稳定物质,微波时间过长会导致原花色素分解而使得率下降。
3.2.5 水浴温度对甜荞麦壳原花色素得率的影响
由图1E 可知,在水浴温度70 ℃以前,随着水浴温度升高,原花色素得率不断增高,表明升高温度有利于原花色素的溶出。当温度达到70 ℃时原花色素的得率达到最高,温度再继续升高,得率下降,表明温度过高会破坏原花色素,不利于提取。故综合考虑,适宜的水浴温度是70 ℃。
3.3 Plackett-Burman 实验结果及分析
利用Minicab 16 软件的Plackett-Burman 实验设计对微波提取甜荞麦壳原花色素单因素实验结果进行分析,针对水浴温度、微波功率、微波时间、料液比、乙醇体积分数5 个因素共进行12 次实验,各重复三次,取其平均值。Plackett-Burman 实验设计及响应值见表2,方差分析见表3。
从表3 可以看出,各因素对响应值(甜荞麦壳原花色素得率)影响显著性的顺序为:微波时间>乙醇浓度>微波功率>料液比>水浴温度。而其中微波时间、乙醇体积分数和微波功率对甜荞麦壳原花色素提取液的吸光值具有显著的影响(P<0.05),料液比与水浴温度对响应值的影响并不显著。回归方程为:

表2 Plackett-Burman 实验设计及响应值Table 2 Plackett-Burman experimental design and results

表3 Plackett-Burman 实验方差分析表Table 3 Variance analysis of Plackett-Burman design
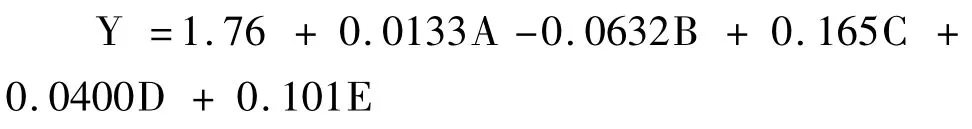
根据单因素和Plackett-Burman 实验结果,确定料液比为1∶30 g/mL,水浴温度70 ℃,在下面的响应面实验中重点考察微波功率、微波时间、乙醇体积分数对原花色素得率的影响。
3.4 响应面优化提取工艺
根据Plackett-Burman 实验设计,确定料液比为1∶30 g/mL,水浴温度70 ℃,改变乙醇体积分数、微波功率和微波时间三个因素,每个因素选取最佳参数及左右共三个水平进行响应面分析。采用软件Design-Expert 7.0 中的Box-Benhnken 实验设计原理,以得率为响应值,设计三因素三水平实验,见表4。
采用软件Design-Expert 7.0 中 的 Box-Benhnken 实验设计原理,以得率为响应值,响应面分析方案与结果见表5。
3.4.1 模型的建立及显著性检验
响应面二次回归方程方差分析见表6,由表6可以看出,A、B、C、A2、B2、C2项达到极显著水平,A-B交互项影响达到极显著水平。各因素对提取甜荞麦壳原花色素得率影响大小关系为:微波时间(B)>乙醇体积分数(A)>微波功率(C)。

表4 Box-Benhnken 实验设计因素与水平Table 4 Factors and levels of Box-Benhnken analysis

表5 微波辅助提取原花色素实验方案与结果Table 5 Design and results of response surface experiments

表6 响应面二次回归方程方差分析Table 6 Regression model of variance analysis results

利用Design-Expert 软件对表5 数据进行多元回归拟合,得到得率(Y)对乙醇体积分数(A)、微波时间(B)和微波功率(C)的二次多项回归模型:

该方程的相关系数R2=0.9999,Adj R2=0.9997,模型拟合程度良好。由表6 可知,整体模型达极显著水平(P<0.01),表明该二次方程模型极显著,不同处理间的差异高度显著。失拟项不显著(P=0.1639),表明模型选择合适。因此可以利用此模型对不同条件下的甜荞麦壳原花色素得率进行预测。
3.4.2 提取工艺的响应面分析与优化

图2 乙醇浓度和微波时间(A)、微波功率和微波时间(B)、乙醇浓度和微波功率(C)对原花色素得率影响的响应面图Fig.2 Response surface plots showing the mutual effects of ethanol concentration and microwave time (A),microwave power and microwave time (B),microwave power and ethanol concentration (C)on the yield of proanthocyanidins
用Design-Expert 软件,根据回归方程分析作响应面图2。可以看出,原花色素得率最初会随三个因素的逐渐增大而升高,超过实验所取的各因素中心值时,原花色素得率会随因素的增大而下降。由图2A、图2B 可知,微波时间表现出的响应曲线明显比乙醇体积分数和微波功率的响应曲线陡峭,说明微波时间对原花色素得率影响最显著,由图2C 可知,乙醇浓度和微波功率交互作用不够显著。这与二次回归方程方差分析结果一致。
3.4.3 最佳工艺条件的确定及验证实验
根据二次回归的数学模型分析结果,最优条件为微波时间27.27 s,乙醇体积分数33.27%,微波功率274.35 W。为了验证响应面法的可行性,将单因素实验所得最佳条件和响应面二次回归所得最佳条件进行实验,每个实验进行三次平行实验,结果见表7。结果表明,响应面所得工艺为最佳工艺,实际得率为2.27%,说明此模型可靠。考虑到具体实验的可行性,将提取条件确定为乙醇体积分数35%,微波时间28 s,微波功率280 W,实际得率为2.21%。
4 结论
4.1 利用Plackett-Burman 设计对甜荞麦壳原花色素微波提取工艺影响因素的显著性进行考察,其中微波时间、乙醇体积分数和微波功率对甜荞麦壳原花色素提取液的吸光值具有显著的影响(P<0.05)。
4.2 甜荞麦壳原花色素优化的数学回归模型为:Y=2.18 +0.21A-0.22B+0.097C+0.012AB-5 ×10-3AC-0.010BC-0.31A2-0.41B2-0.11C2,此模型在实验范围内能较准确地预测原花色素的得率。
4.3 结合实际可行性,甜荞麦壳原花色素微波提取最佳提取条件为:料液比为1∶30 g/mL,乙醇体积分数35%,水浴温度70 ℃,微波提取时间28 s,微波功率280 W,在此条件下甜荞麦壳原花色素得率为2.21%。

表7 验证实验结果Table 7 Verification results of proanthocyanidins extraction
1 Yu S (余霜),Li G (李光),Chen QF (陈庆富).SWOT analysis on the development of buckwheat seed industry in China.Seed(种子),2012,31(3):84-87.
2 Zhang C (张超),Li JX (李冀新).Process of buckwheat hull.Sci Technol Cereal Oil Food(粮油食品科技),2006,14(3):8-10.
3 Li FH,Yuan Y,Yang XL,et al.Phenolic profiles and antioxidant activity of buckwheat (Fagopyrum esculentumM?enchand Fagopyrum tartaricumL.Gaerth)hulls,brans and flours.J Integr Agric,2013,12:1684-1693.
4 Quettier-Deleu C,Gressier B,Vasseur J,et al.Phenolic compounds and antioxidant activities of buckwheat (Fagopyrum esculentumMoench)hulls and flour.J Ethnopharmacol,2000,72(1-2):35-42.
5 Mukoda T,Sun B,Ishiguro A.Antioxidant activities of buckwheat hull extract toward various oxidative stressin vitroandin vivo.Biol Pharm Bull,2001,24:209-213.
6 Monagas M,Quintanilla-Lopez JE,Gomez-Cordoves C,et al.MALDI-TOF MS analysis of plant proanthocyanidins.J Pharm Biomed Anal,2009,51:358-372.
7 Wang Y (王洋),Gao Z (高哲),Li Y (李晔),et al.Research progress on analysis of proanthocyanidins.J Food Safety Quality(食品安全质量检测学报),2012,3:130-135.
8 Shi B(石碧),Du X(杜晓).The progress on research and utilization of plant proathocyanidins.J Sichuan Univ,Eng Sci Ed(四川大学学报,工程科学版),2006,38(5):16-24.
9 Zhang CG(张长贵),Dong JB (董加宝),Xie WR(谢伍容).Research progress on antioxidative bioactivities of proanthocyanidins.Cereal Oil(粮食与油脂),2009,6:10-12.
10 Tang HB(唐洪波),Ma BJ(马冰洁),Li YP(李艳平).Study on extracting proanthocyanidins from grade seed.Cereal Oil Proc(粮油加工),2008,10:72-75.
11 Fan JL(樊金玲),Luo L(罗磊),Wu T(武涛),et al.Comparison of antioxidant activity of proanthocyanidins from seed of sea buckthorn and grape.Food Machinery(食 品 与 机械),2007,23(2):26-30.
12 Wang QL(王庆玲),Dong J(董娟),Ji H(姬华),et al.The review about procyanidin from peanut red skin.Food Res Dev(食品研究与开发),2011,32:184-186.
13 Cui XX (崔晓霞),Zhang XL(张小丽),Luo SQ(罗书勤),et al.Study on extraction technique of proanthocyanidins from larch bark.Nat Prod Res Dev(天然产物研究与开发),2012,24:127-130.
14 Zhang Y(张妍),Wu XX(吴秀香).Research progress on procyanidins.Pharmacol Clin Chin Mater Med(中药药理与临床),2011,27:112-116.
15 Fu RJ (傅荣杰),Feng Y(冯怡).Application of microwave extraction in Chinese traditional medicine and natural product.Chin J Chin Mater Med(中国中药杂志),2003,28:804-807.
16 The Ministry of Health Legal System and Supervision (卫生部法制与监督司).Health Food Inspection and Technical specification,2003.274-275.
17 Zheng YL(郑永丽),Li MQ(李梦青).Determination content of proanthocyanidins with spectrophotomeric method.Guangzhou Chem Ind(广州化工),2010,38:197-198.
