制备工艺对果胶/壳聚糖复合膜力学性能的影响
2015-01-06王虹霞丁克毅
王虹霞, 丁克毅, 刘 军
(西南民族大学 化学与环境保护学院,四川 成都 610041)
制备工艺对果胶/壳聚糖复合膜力学性能的影响
王虹霞, 丁克毅, 刘 军*
(西南民族大学 化学与环境保护学院,四川 成都 610041)
采用5种不同工艺制备果胶/壳聚糖(PEC/CS)复合膜,研究了成膜因素对膜力学性能的影响,并利用FT-IR、XRD、SEM表征其结构。结果表明:先将壳聚糖/果胶在乙酸溶液中生成絮状沉淀,再用甲酸溶解后制备的复合膜光滑透明,拉伸强度能达到45.38 MPa。FT-IR分析显示,果胶和壳聚糖通过-COOH和-NH2之间的静电作用和氢键作用生成复合物。XRD分析显示,果胶的加入降低了壳聚糖的结晶度,形成网络结构,提高了复合膜整体的力学性能。SEM分析显示,果胶/壳聚糖复合絮状沉淀的表面,可见明显纵横交错的条痕,说明果胶和壳聚糖分子之间发生了复合反应。
果胶,壳聚糖,复合膜,力学性能,形成机理
果胶和壳聚糖均是天然高分子线性多糖,无毒,具有良好的生物相容性和可降解性[3]。在适当体系下,果胶和壳聚糖之间会发生复合反应,生成果胶/壳聚糖聚电解质复合凝胶[1-3]。当前,药用胶囊的主要原料是明胶。由于“疯牛病”、“口蹄疫”等动物性传染病的蔓延引起的恐慌,加之“毒胶囊”事件后,市场对明胶胶囊的代替品——植物胶囊的需求日趋强烈。但是商品化的植物胶囊和动物性胶囊比,制品易脆,材料成型性差,崩解时间不易控制,因而难以保证药效。为此,目前已有较多的对植物多糖类物质改性以制备优质药用胶囊的研究报道,但多数集中在植物纤维素类的改性上,对果胶研究较少。四川本地大量生产柑橘,而柑橘果皮中含有丰富的果胶。作者采用4种不同方法制备PEC/CS复合膜,研究制备工艺对复合膜力学性能的影响,并探讨了复合膜的形成机理。
1 材料与方法
1.1 主要原料
果胶:酯化度66-69%,相对分子质量50 000~ 150 000,医用级,衢州果胶有限公司产品;壳聚糖,脱乙酰度≥85%,相对分子质量10 000~50 000,天津市瑞金特化学品公司产品。
1.2 主要设备及仪器
AL104分析天平:梅勒-脱利多仪器有限公司产品;S212恒速搅拌器:上海申顺生物科技有限公司产品;DHG-9240A电热恒温鼓风干燥箱:上海-恒科科技有限公司产品;AGS-J电子万能试验机:中国扬州拓实实验机械有限公司产品;NICOLET is50傅立叶变换红外吸收光谱仪:美国DIGILAB公司产品;UV-1950紫外分光光度计:北京普析通用仪器有限公司产品;XRD-6 X射线衍射仪:北京普析通用仪器有限公司产品;QUANTA 250扫描电镜:FEI香港有限公司产品。
1.3 试样制备
1.3.1 果胶膜、壳聚糖膜的制备称一定量的果胶粉末溶于去离子水中配制质量分数为2.0%的果胶水溶液,用体积分数1.0%的醋酸配制质量分数为2.0%的壳聚糖醋酸溶液,过滤,脱泡,涂膜,于45℃烘干后备用。
1.3.2 甲酸溶解絮状沉淀的复合膜制备用体积分数1.0%的醋酸配制质量分数为1.0%的壳聚糖醋酸溶液,搅拌下按果胶、壳聚糖质量比为5∶1、3∶1、2∶1、1∶1、2∶3、1∶2加入质量分数为2.0%的果胶水溶液,继续搅拌2 h,得到的白色絮状沉淀。用蒸馏水将其洗涤至中性后溶于pH=1.0的甲酸中,过滤,脱泡,涂膜,于45℃烘干后备用。
1.3.3 不同pH复合膜制备用体积分数1.0%的醋酸配制100 mL pH=1.5、2.5、3.5、4.5、5.5,质量分数为0.4%的壳聚糖醋酸溶液。在搅拌下加入等量等浓度的果胶水溶液,再搅拌10 min后,测得pH=2、3、4、5、6,脱泡,涂膜,于45℃烘干后备用。
1.3.4 不等比果胶/壳聚糖复合膜制备用体积分数1.0%的醋酸配制质量分数0.4%的壳聚糖醋酸溶液,在搅拌下按照壳聚糖占复合物20%、30%、40%、50%、60%的量加入等量的果胶水溶液,再搅拌10 min后,用饱和NaOH溶液调节成膜液pH=5,脱泡,涂膜,于45℃烘干后备用。
1.3.5 等比果胶/壳聚糖复合膜制备用体积分数1.0%的醋酸配制100 mL质量分数为0.2%、0.3%、0.4%、0.5%、0.6%的壳聚糖醋酸溶液,在搅拌下加入等量等浓度的果胶水溶液,再搅拌10 min后,用饱和NaOH溶液调节成膜液pH=5,脱泡,涂膜,于45℃烘干后备用。
1.3.6 果胶/壳聚糖复合絮状沉淀对果胶膜的增强用体积分数1.0%的醋酸配制100 mL质量分数为0.2%、0.4%、0.6%、0.8%、1.0%的壳聚糖醋酸溶液,在搅拌下加入等量等浓度的果胶水溶液,搅拌5 h后静置5 h,再加入5 g质量分数2.0%的果胶溶液,混合均匀,用饱和NaOH溶液调节成膜液pH=5。脱泡,涂膜,于45℃烘干后备用。
1.4 性能测试与结构表征
1.4.1 力学性能测试复合膜的拉伸强度和断裂伸长率按国家标准(GB/T 1040)进行测量。用标准样刀将膜切成4 mm×75 mm哑铃型长条,于室温、相对湿度65%的环境中调湿36 h至恒重,用万能测试仪测定膜的拉伸强度及断裂伸长率,拉引速度设定为1 mm/s,每种膜测定3个样取平均值。
1.4.2 结构表征UV分析:制备体积分数0.5%的果胶-乙酸溶液与同浓度的壳聚糖—乙酸溶液和pH 1.0甲酸溶解PEC/CS(1∶1)絮状沉淀溶液,分别以乙酸和甲酸做对照做吸光度测试;FT-IR分析:将1 cm×1 cm果胶膜、壳聚糖膜、果胶/壳聚糖复合膜分别置于光谱仪的探针处测试,间隔2 cm-1,测试范围4 000~400 cm-1;XRD分析:电压36 kV,电流20 mA,功率2 kW,扫描速度4°(2θ)/min;SEM分析:样品喷金后观察膜表面。
2 结果与讨论
2.1 复合膜的力学性能分析
2.1.1 甲酸溶解絮状沉淀制备的复合膜的力学性能为得到较为纯净的果胶/壳聚糖复合膜材料,实验先制备了果胶/壳聚糖反应白色絮状沉淀,再将该沉淀洗涤滤出,得到较为纯净的复合产物后,用酸溶解,涂膜。但是PEC/CS絮状沉淀在纯乙酸中都不溶解,而甲酸也是有机酸,易挥发,所以选择甲酸溶解PEC/CS絮状沉淀涂膜。果胶和壳聚糖的相对含量对复合膜力学性能的影响见图1。
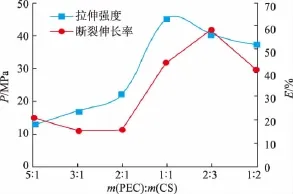
图1 甲酸溶解絮状沉淀的复合膜的力学性能Fig.1 Mechanical property of the membrane prepared by dissolving flocculent precipitate with formic acid solution
壳聚糖分子是刚性分子,具有很好的力学性能,拉伸强度可达(96.32±13.13)MPa[3];而果胶是柔性分子,成膜性能也较差。因此,壳聚糖的加入可以提高复合膜的拉伸强度。当果胶和壳聚糖的质量比为1:1时拉伸强度最大,为45.38 MPa,是动物明胶胶囊膜材料拉伸强度的0.68~1.30倍[7]。
2.1.2 不同pH复合膜的力学性能为了研究成膜液pH值对复合膜力学性能的影响,试验了5个pH条件下成膜时力学性能变化。

图2 不同pH复合膜的力学性能Fig.2 Mechanical property of the membrane prepared by different pH
从图2可以看出,膜的力学性能受成膜溶液pH的影响比较明显。在pH<3时形成的膜,具有较好的拉伸强度,最大能达到20.05 MPa。这是由于在pH值较低的环境下,果胶与壳聚糖之间主要以氢键作用为主。随着成膜液pH值的升高,膜的拉伸强度在pH=5时再次达到一个最大值10.02 MPa。当pH继续增大为6时,果胶与壳聚糖之间主要以经典斥力为主,形成的膜表面有较多的花斑状区域,这说明在该条件下,果胶和壳聚糖的相容性很差[8]。类似,复合膜的断裂伸长率随pH值的变化与其拉伸强度变化基本一致。在pH=5的环境下,复合膜的断裂伸长率达到最大67.37%,这说明此时果胶/壳聚糖复合膜具有一定的韧性。
2.1.3 不等比果胶/壳聚糖复合膜的力学性能为进一步考察壳聚糖的浓度及在复合膜中含量对膜力学性能的影响,采用降低果胶和壳聚糖反应液的浓度来去除涂膜液中气泡。
从图3可以看出,随着壳聚糖在复合膜中浓度的增加,膜复合的的拉伸强度和断裂伸长率均增加。这是由于随着壳聚糖的增加,体系中与—COOH反应的—NH2数量增多,形成的复合结构越稳定复杂,从而拉伸强度增大。而当壳聚糖质量分数超过50%之后,拉伸强度和断裂伸长率并没有因过量的壳聚糖破坏已形成的稳定结构而降低,这是因为过量的壳聚糖均匀地填充在复合结构中,由于壳聚糖自身特性使复合膜的力学性能继续增大。
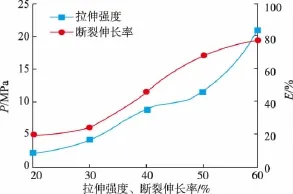
图3 不等比果胶/壳聚糖复合膜的力学性能Fig.3 Mechanical property of the membrane made of very low concentration and different proportion
2.1.4 等比果胶/壳聚糖复合膜的力学性能果胶、壳聚糖以相同比例,在总质量分数较低时直接复合成膜,膜的力学性能随总质量分数的变化见图4。

图4 等比果胶/壳聚糖复合膜的力学性能Fig.4 Mechanical property of the membrane made of very low concentration and same proportion
从图4可以看出,同比例果胶和壳聚糖溶液在极低浓度下制成的薄膜,拉伸强度随果胶、壳聚糖混合浓度的增加呈上升趋势,但总体力学性能比较低,均在10 MPa以下;复合膜的断裂伸长率表现为先减小后增大。
2.1.5 果胶/壳聚糖复合絮状沉淀增强果胶膜的力学性能为了研究果胶对同比例极低浓度果胶/壳聚糖复合物的增强作用,先用同比例极低浓度的果胶、壳聚糖溶液生成少量白色絮状沉淀,再向其中填充5 g质量分数为2%的果胶,使果胶均匀分散在絮状沉淀中,以起到增强作用。
从图5可以看出,同比例果胶和壳聚糖溶液在极低浓度下反应后,再填充高浓度果胶所制成的复合膜,拉伸强度先增加后减小。在两者质量分数均为0.2%时,反应生成的白色絮状聚合物量少,对膜的拉伸强度影响不大。随着反应液浓度的增加,生成的果胶/壳聚糖白色絮状聚合物增多,制成的复合膜,拉伸强度也增大,当两者质量分数均达到0.8%时,拉伸强度最大已达到18.74 MPa,但是超过该浓度后拉伸强度又减小。这是由于两者质量分数均大于0.8%时,添加果胶后,溶液中产生较多气泡,制成的复合膜中会有气泡孔洞,影响膜的拉伸强度。综合考虑,当果胶、壳聚糖的质量分数均为0.8%时,用果胶增强后的复合膜拉伸强度和断裂伸长率最佳,具有较好的刚性和韧性。
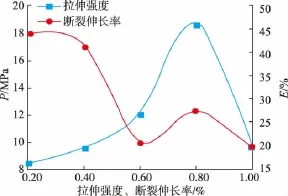
图5 同比例果胶/壳聚糖复合絮状沉淀对果胶膜增强的力学性能Fig.5 Mechanical property of composite membrane of composite flocculent precipitate made of very low and same proportion PEC/CS concentrations enhance PEC membrane
综合图4与图5还可以看出,在相同成膜液浓度下,添加果胶后的复合膜拉伸强度均比不添加果胶制的复合膜拉伸强度大,最大增强率达到62.3%,也说明填充果胶对复合膜的拉伸强度起到了一定的增强作用。
从以上5种复合膜的力学性能变化可知,复合膜的拉伸强度并不是随着某一单组份含量的变化而成比例变化,这从宏观上证明了复合膜中两组份并不是以其中任一种组份为股价的简单混合,而是两组份之间产生了一定的相互作用的结果,作者选择了拉伸强度为45.38 MPa的PEC/CS复合膜和PEC膜、CS膜做了结构分析试验。
2.2 复合膜的结构分析
2.2.1 UV分析由于PEC/CS絮状沉淀在纯乙酸中仍是絮状,说明其不溶解,同样也不溶于盐酸等无机酸,而在pH=1.0的甲酸溶液呈澄清透明溶液,故实验选择了挥发性较好的甲酸溶解PEC/CS絮状沉淀涂膜。PEC/CS复合物在pH 1.0甲酸中溶解后的状态与pH 1.0乙酸中直接溶解的PEC、CS体系的差别,从下面紫外分析可知。

图6 PEC/CH3COOH溶液(a)、CS/CH3COOH溶液(b)和PEC/CS/HCOOH溶液(c)的UV图谱Fig.6 UV spectra of PEC/CH3COOH(a)、CS/CH3COOH(b)and PEC/CS/HCOOH(c)
从紫外吸收光谱图图6可以看出,pH 1.0乙酸中直接溶解的PEC、CS体系的λm在229 nm、223 nm处吸收峰是由于分子中含有—OH、—NH2等杂原子基团发生n-δ*跃迁,PEC/CS复合物在pH1.0甲酸中溶解后的λm=256 nm,这是果胶和壳聚糖分子中—COOH和—NH2发应,在酸性环境中形成O=C—N:共轭结构的吸收峰。
2.2.2 FT-IR光谱分析果胶和壳聚糖间相互作用主要发生在果胶的—COOH和壳聚糖的—NH2之间。实验一般都选用醋酸溶液溶解壳聚糖,溶解后壳聚糖的—NH2变成—NH3+,不影响壳聚糖本身的性质。作者选择了拉伸强度为45.38 MPa的果胶/壳聚糖复合膜与单纯的果胶膜、壳聚糖膜做了红外吸收光谱如图7所示。
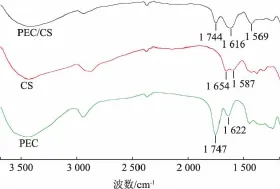
图7 PEC、CS和PEC/CS的红外吸收光谱图Fig.7 IR spectra of PEC、CS and PEC/CS
从图7可以看出,PEC、CS和PEC/CS复合膜的红外吸收光谱大体相似,但各自具有其主要特征峰:在 PEC的 IR谱图中,1 747 cm-1归属为—COCH3中羰基的伸缩振动吸收;1 622 cm-1归属为—COOH中羰基的伸缩振动吸收;在CS的IR谱图中,1 654 cm-1归属于酰胺一级结构的伸缩振动吸收;1 587 cm-1归属为酰胺二级结构的伸缩振动吸收;在PEC/CS谱图中,δN-H峰移动到1 569 cm-1,为—NH3+对称弯曲振动,表明果胶与壳聚糖的相互作用使氨基的化学环境发生变化。1 747 cm-1处的νC=O峰大大减弱,1 616 cm-1处出现—COO-不对称伸缩振动[5]吸收峰,是发生—COOH和—NH2的次价键反应形成的。这是由于果胶与壳聚糖之间存在着分子内和分子间相互作用。事实上,复合物的稳定可能通过带正电荷的壳聚糖和带负电荷的果胶之间的静电作用获得,还可能在果胶内—COOH和壳聚糖内—NH2之间,以及其官能团,诸如—OH,—OCH3,—COOCH3之间存在分子内氢键作用获得[9]。
2.2.3 X射线衍射分析当X射线通过晶体时,每一种结晶物质都有自己的独特的衍射花样。当其结构发生改变时,所对应的结晶峰也会发生变化。所以可以通过XRD图谱上结晶峰的变化来判断果胶、壳聚糖是否发生复合反应。
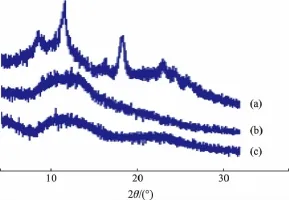
图8 CS膜(a)、PEC膜和PEC/CS复合膜(b)的XRD图Fig.8 XRD of CS membrane(a)、PEC membrane(b)and PEC/CS composite membrane(c)
从图8可以看出,若壳聚糖分子、果胶分子之间没有相互作用或相互作用很弱,则在其复合膜中会出现各自的结晶区,共混复合膜的衍射图谱则按混合组分的衍射峰相对强度简单叠加。由于果胶的加入,复合膜中壳聚糖的结晶峰发生了明显的变化。在各种果胶/壳聚糖复合膜中均找不到属于壳聚糖在18°和24°的衍射峰,而10.5°处的结晶峰也明显减弱。这是因为果胶的加入扰乱了壳聚糖链原有的规整排列,果胶羧基和壳聚糖氨基之间通过氢键作用[10],而对壳聚糖分子原来的结晶形成干扰,复合过程形成的网络结构降低了壳聚糖的结晶度。
2.2.4 扫描电镜(SEM)图分析将果胶溶液加入到迅速搅拌的壳聚糖溶液中,立即产生白色絮状沉淀。采用扫描电镜(SEM)在20.00 V电压下对果胶/壳聚糖(质量比1∶1)反应生成的白色絮状沉淀和甲酸溶解白色絮状沉淀制备的复合膜表面放大1 600倍进行分析,结果如图9所示。

图9 PEC/CS(质量比1∶1)复合絮状沉淀(a)、极低浓度果胶/壳聚糖复合絮状沉淀增强果胶膜 (b)和甲酸溶解PEC/CS(1∶1)复合絮状沉淀复合膜(c)的SEM图Fig.9 SEM photographs of PEC/CS (1∶1)composite flocculentprecipitate (a)、Composite flocculent precipitate made of very low PEC/CS concentrations enhance PEC membrane(b)、PEC/ CS(1∶1)composite floc membrane(c)
从图9(a)可以看出,果胶/壳聚糖复合絮状沉淀表面可见明显纵横交错的条痕,说明果胶与壳聚糖分子间存在相互作用,这一作用可归结为分子链间形成了更多的氢键及致密复杂的网状结构。从图9(b)可以看出,果胶/壳聚糖絮状沉淀有序填充在果胶膜中,对果胶膜起到一定的增强作用。从图9(c)可以看出,甲酸溶解果胶/壳聚糖絮状沉淀制备的PEC/CS复合膜表面均匀致密平整,说明果胶与壳聚糖之间有很好的相容性,这种良好的相容性所产生的协同效应明显地改善了复合膜的拉伸强度。
3 结语
采用不同工艺制备果胶/壳聚糖复合膜,通过复合膜的力学性能确定最佳制备工艺,进一步研究了复合膜的透光性、水蒸气透过率、溶胀性、体外降解及抗菌性等性能,提高了膜的综合性能,为果胶/壳聚糖复合膜在食品包装、药用胶囊等方面的应用提供了参考。
[1]Jindal M,Kumar V,Rana V,et al.An insight into the properties of Aegle marmelos pectin-chitosan cross-linked films[J]. International Journal of Biological Macromolecules,2013,52:77-84.
[2]Munarin F,Tanzi M C,Petrini P,et al.Advances in biomedical applications of pectin gels[J].International Journal of Biological Macromolecules,2012,51(4):681-689.
[3]Sahoo D,Sahoo S,Mohanty P,et al.Chitosan:a New Versatile Bio-polymer for Various Applications[J].Designed Monomers and Polymers,2009,12(5):377-404.
[4]Jindal M,Kumar V,Rana V,et al.An insight into the properties of Aegle marmelos pectin-chitosan cross-linked films[J]. International Journal of Biological Macromolecules,2013,52:77-84.
[5]Dutta R K,Sahu S.Development of diclofenac sodium loaded magnetic nanocarriers of pectin interacted with chitosan for targeted and sustained drug delivery[J].Colloids and Surfaces B:Biointerfaces,2012,97(1):19-26.
[6]Chen P H,Kuo T Y,Kuo J Y,et al.Novel chitosan-pectin composite membranes with enhanced strength,hydrophilicity and controllable disintegration[J].Carbohydrate Polymers,2010,82(4):1236-1242.
[7]Kamiya S,Nagae K,Hayashi K,et al.Development of a new evaluation method for gelatin film sheets[J].International Journal of Pharmaceutics,2014,461(1):30-33.
[8]Martelli M R,Barros T T,Moura M R D,et al.Effect of Chitosan Nanoparticles and Pectin Content on Mechanical Properties and Water Vapor Permeability of Banana Puree Films[J].Journal of Food Science,2013,78(1):98-104.
[9]Fan L,Sun Y,Xie W,et al.Oxidized Pectin Cross-Linked Carboxymethyl Chitosan:A New Class of Hydrogels[J].Journal of Biomaterials Science,Polymer Edition,2012,23(16):2119-2132.
[10]Mathew S,Abraham T E.Characterisation of ferulic acid incorporated starch-chitosan blend films[J].Food Hydrocolloids,2008,22(5):826-835.
Effect of Preparation Process on the Mechanical Properties of Pectin/Chitosan Composite Membrane
WANG Hongxia, DING Keyi, LIU Jun*
(College of Chemistry&Environmental Protection Engineering,Southwest University for Nationalities,Chengdu 610041,China)
Five kinds of process were applied to prepare pectin/chitosan (PEC/CS)composite membranes and the effect of membrane-forming conditions on the mechanical properties were explored,FT-IR,XRD and SEM were adopted to describe the structure of membrane.The results indicated that,the membrane prepared by dissolving the flocculent precipitate(formed by dissolving PEC/CS in the solution of acetic acid)with formic acid solution was smooth and transparent,and its tensile strength could reach 45.38 MPa,which was 1.42 times as that of gelatin membrane.The result of FT-IR analysis indicated that,a polyelectrolyte reaction happened between pectin and chitosan molecules through electrostatic and hydrogen bond interaction between-COOH and-NH2,and in this way,a composite material was formed.The result of XRD analysis showed that,the adding of pectin reduced the crystallinity of chitosan,a network structure was formed,and the mechanical property of the composite membrane was improved.The result of SEM analysis showed that,clear streaks could be observed in the surface of PEC/CS composite flocculent precipitate,andthis indicated the poly-reaction occurred between pectin and chitosan molecules.Based on these experiment results.
pectin,chitosan,composite membrane,mechanical property,mechanism
Q 539
A
1673—1689(2015)01—0068—06
2014-06-07
四川省科技创新苗子工程资助项目(2012CZ008);西南民族大学研究生创新科研重点项目(CX2013SZ14)。
*通信作者:刘 军(1966—),女,四川绵阳人,副教授,主要从事高分子化学研究。E-mail:liujun106@sohu.com
