高效液相色谱-串联质谱法同时测定塑料食品接触材料中20种邻苯二甲酸酯迁移量*
2015-01-05张子豪张海峰麦晓霞李全忠李丹刘莹峰蚁乐洲钟志光郑建国
张子豪,张海峰,麦晓霞,李全忠,李丹,刘莹峰,蚁乐洲,钟志光,郑建国
(广东出入境检验检疫局,广州 510623)
高效液相色谱-串联质谱法同时测定塑料食品接触材料中20种邻苯二甲酸酯迁移量*
张子豪,张海峰,麦晓霞,李全忠,李丹,刘莹峰,蚁乐洲,钟志光,郑建国
(广东出入境检验检疫局,广州 510623)
采用高效液相色谱-串联质谱(LC-MS/MS)技术建立了食品接触材料中20种邻苯二甲酸酯类迁移量的测定方法。样品分别采用欧盟(EU) No.10/2011法规中食品模拟液浸泡,橄榄油浸泡液用乙腈进行液-液萃取,水基浸泡液直接过滤,C18色谱柱(100 mm×2.1 mm,2.7 µm)分离,以0.1%甲酸溶液-甲醇溶液为流动相,梯度洗脱,采用多反应监控(MRM)模式进行分析检测。20种邻苯二甲酸酯类化合物质量浓度在1~500 ng/mL范围内与色谱峰面积呈线性关系。水溶液、3%乙酸食品模拟浸泡液、10%乙醇食品模拟浸泡液、20%乙醇食品模拟浸泡液、50%乙醇食品模拟浸泡液、橄榄油食品模拟浸泡液中方法定量限分别为0.20~9.81 ng/mL,0.19~9.76 ng/mL,0.25~12.3 ng/mL,0.21~10.8 ng/mL,0.19~11.7 ng/mL,0.45~20.3 ng/mL。样品加标回收率为85.8%~111.3%(3%乙酸浸泡液),79.4%~123.6%(橄榄油浸泡液),两种浸泡液中测定结果的相对标准偏差不大于8.48%(n=6)。该方法具有快速简便、灵敏度高及准确性好等特点,适用于塑料类食品接触材料中邻苯二甲酸酯类迁移量的检测。
食品接触材料;邻苯二甲酸酯;迁移量;液相色谱-串联质谱
邻苯二甲酸酯类化合物常用作增塑剂以提高塑料及其制品的柔韧性、透明度和耐用性[1],广泛用于塑料类产品中。大量研究表明,邻苯二甲酸酯是一类环境雌激素,会对人体激素产生影响,具有内分泌干扰作用,并具有致突变性和致癌性[2-4]。由于邻苯二甲酸酯与原材料并非共价结合而只是混合,很容易迁移出来,因此食品接触材料中的增塑剂很容易迁移到食品中去,从而使食品中也含有邻苯二甲酸酯。因此建立邻苯二甲酸酯迁移量的准确可靠的检测方法非常重要。
目前关于邻苯二甲酸酯类增塑剂的检测标准主要为气相色谱-质谱法[5-9],液相色谱法[10],液相色谱-质谱法[11]。近年来,随着液相色谱-串联质谱技术的快速发展,该技术已用于检测食品、化妆品[12]、食品包装[13-14]、香料[15]中多种邻苯二甲酸酯的含量,报道的检测对象多为食品。对于食品接触材料中邻苯二甲酸酯的前处理有冷冻粉碎、正己烷超声提取[14]等方法,对于食品接触材料,欧盟法规(Eu) No.10/2011严格控制使用的7种邻苯二甲酸酯与被我国卫生部列为优先控制污染物的17种邻苯二甲酸酯迁移量测定的相关报道较少。
笔者建立了利用液相色谱-串联质谱技术对食品接触材料中20种邻苯二甲酸酯类迁移量的测定方法,方法灵敏度高、准确可靠,可用于食品接触材料中邻苯二甲酸酯类化合物的迁移量分析。
1 实验部分
1.1 主要仪器与试剂
液相色谱仪:Agilent 1200型,配有G1312B二元混合泵,美国安捷伦科技公司;
三重四级杆串联质谱仪:Agilent 6410型,配有电喷雾离子源(ESI)和MassHunter软件数据处理系统,美国安捷伦科技公司;
涡旋振荡器:IKAMS2 Minishaker型,德国IKA公司;
超纯水机:Milli-Q型,美国Millipore公司;
邻苯二甲酸二甲酯(DMP,99.0%),邻苯二甲酸二乙酯(DEP,99.5%),邻苯二甲酸二烯丙酯(DAP,98.0%),邻苯二甲酸二丁酯(DBP,99.0%),邻苯二甲酸二异丁酯(DIBP,98.0 %),邻苯二甲酸二(2-甲氧基)乙酯(DMEP,98.0%),邻苯二甲酸二(2-乙氧基)乙酯(DEEP,99.4%),邻苯二甲酸二苯酯(DPhP,99.5 %),邻苯二甲酸苄基丁基酯(BBP,99.5%),邻苯二甲酸二(2-丁氧基)乙酯(DBEP,85.0%),邻苯二甲酸二戊酯(DPP,98.0%),邻苯二甲酸二环己酯(DCHP,99.5%),邻苯二甲酸二(4-甲基-2-戊基)酯(BMPP,99.3%),邻苯二甲酸二己酯(DHXP,98.0%),邻苯二甲酸(2-乙基己基)酯(DEHP,98.0%),邻苯二甲酸二辛酯(DNOP,99.5%),邻苯二甲酸二异辛酯(DIOP,99.4%),邻苯二甲酸二壬酯(DNP,99.0 %),邻苯二甲酸二异壬酯(DINP,99.0%),邻苯二甲酸二异癸酯(DIDP,99.0%):DPP,DCHP,DNP,BMPP购自美国xstandard公司,其它均购自德国Dr.E公司;
甲醇、乙腈:色谱纯,TEDIA company Inc,USA;
实验所用其它试剂均为色谱纯;
精制橄榄油;
实验用水为超纯水。
1.2 工作溶液的配制
称取各邻苯二甲酸酯标准品0.012 5 g,用甲醇溶解并定容至25 mL,各单独配制成质量浓度为500 μg/mL的邻苯二甲酸酯储备液。移取各邻苯二甲酸酯储备液2.0 mL到100 mL容量瓶,用甲醇定容,配制成质量浓度为10 μg/mL的邻苯二甲酸酯混合标准中间液。
水基食品模拟物标准工作溶液:准确移取以上邻苯二甲酸酯混合标准中间液,分别用迁移试验中选用的水基食品模拟物(蒸馏水、3%乙酸溶液、10%乙醇溶液、20%乙醇溶液、50%乙醇溶液)定容,得到相应介质中邻苯二甲酸酯质量浓度分别为1,10,20,50,100,200,500 ng/mL的标准工作溶液。
橄榄油基标准工作溶液:量取2.0 mL橄榄油于7个试管中,向其中加入以上邻苯二甲酸酯混合标准中间液,配制成质量浓度分别为1,10,20,50,100,200,500 ng/mL的邻苯二甲酸酯标准工作溶液。在以上7个试管中加入2.0 mL乙腈,旋涡混合器混匀5 min后静置分层,用注射器吸取上层乙腈溶液,经过滤后待上机测试。
1.3 样品处理
样品处理按照(Eu) No.10/2011的要求,每6 dm2食品接触材料用1 L食品模拟液进行浸泡。
对于水基食品模拟液(3%乙酸溶液、10%乙醇溶液、20%乙醇溶液、50%乙醇溶液):直接取浸泡液,用0.22μm针式过滤器过滤后上LC-MS/MS分析。
对于橄榄油浸泡液:取2 mL橄榄油浸泡液于离心管中,加入2 mL乙腈,涡旋振荡5 min,静置分层后,取上层乙腈溶液用0.22 μm针式过滤器过滤后上LC-MS/MS分析。
为减少试剂,耗材等引入的背景干扰,制备空白食品模拟浸泡液(空白橄榄油模拟液为经过萃取后的乙腈溶液),经0.22 μm针式过滤器过滤后上LC-MS/MS分析。
1.4 液相色谱-串联质谱条件
1.4.1 色谱条件
色 谱 柱:PoroShell 120 EC-C18色 谱 柱(100 mm×2.1 mm,2.7 µm,美国安捷伦科技公司);柱温:40℃;流动相:A为0.1%甲酸溶液,B为甲醇溶液;梯度洗脱程序:0~1 min 40% B,1~4 min 50% B,4~5 min 60% B,5~7 min 70%B,7~9 min 50%B,9~10 min 90% B,10~11 min 40% B,11~14 min 50% B,14~15 min 60% B,15~16 min 70% B,16~25 min 100% B,25~30 min 40% B;流速:0.3 mL/min;进样体积:2 μL。
1.4.2 质谱条件
电喷雾离子源(ESI),多反应监测正离子模式;干燥气温度:350℃;气体流量:10 L/min;雾化器压力:0.34 MPa(50 psi);毛细管电压:4 000 V;碰撞能量:1~51 eV;驻留时间:30 ms。
2 结果与讨论
2.1 质谱条件优化
将邻苯二甲酸酯标准溶液在ESI正离子模式下进行一级质谱扫描,结果表明20种化合物最强峰均为准分子离子峰[M+1]+,因此选择[M+1]+为母离子。再分别对各准分子离子峰进行子离子扫描,得到碎片离子信息。选取最大响应且干扰较少的碎片离子对作为定量、定性离子对。为了得到较好的灵敏度,分别对定性定量离子对、碎裂电压、碰撞能量等参数进行优化。优化后的参数见表1。

表1 20种邻苯二甲酸酯定量、定性离子对、碎裂电压和碰撞能量
2.2 色谱条件优化
分别考察Agilent SB-C3(100 mm×3.0 mm,1.8 μm),Poroshell 120 EC-C18(100 mm×2.1 mm,2.7 µm)和EclipseXDB C-18(150 mm×4.6 mm,3.5 µm) 3种实验室常用色谱柱,标准样品质量浓度为200 ng/mL。结果表明,用SB-C3色谱柱时,较长支链的邻苯二甲酸酯分离效果较差;用EclipseXDB C-18色谱柱时分离效果改善较好,但DMP,DMEP,DEP,DEEP,DIBP,DBP,DBP,DBEP的色谱峰分离效果不佳;用Poroshell 120 EC-C18色谱柱时,分离效果最好,在25 min内20种邻苯二甲酸酯可很好地分离,20种邻苯二甲酸酯混合标准溶液的MRM色谱图见图1。
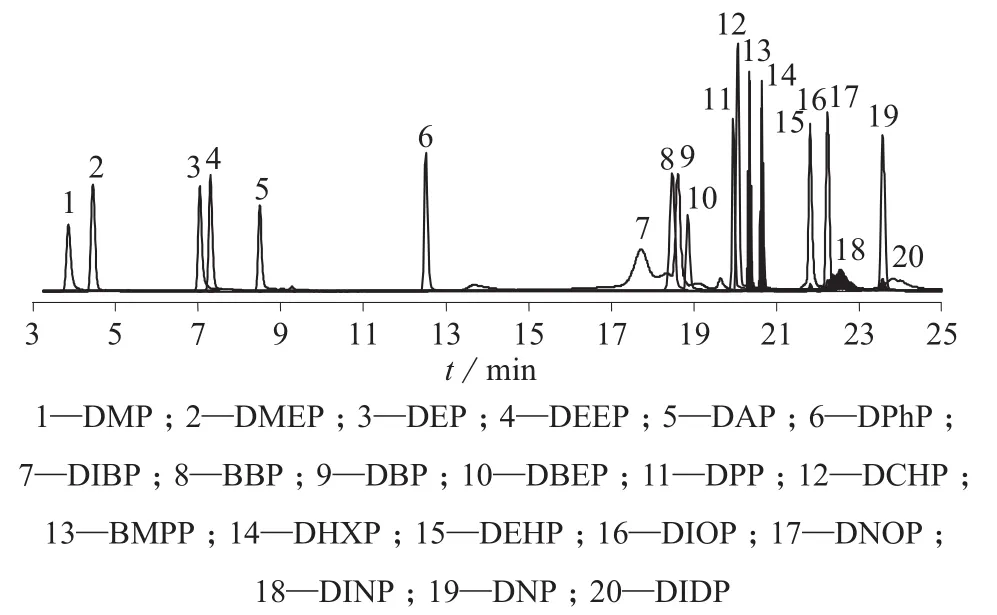
图1 Poroshell120 EC-C18色谱柱的邻苯二甲酸酯多反应监控色谱图
分别采用甲醇-0.1%甲酸水溶液、甲醇-10 mmoL乙酸铵水溶液(内含0.1%甲酸)、甲醇-水、乙腈-水体系作为流动相,对质量浓度均为500 ng/mL的标准溶液进行测定。结果表明,乙腈-水体系中,DMP与DMEP,DEP与DEEP分离效果不好。以上4种流动相系统中,目标物质的响应为乙腈-水体系最弱,甲醇-水体系次之,甲醇-0.1%甲酸溶液体系与甲醇-10 mmoL乙酸铵溶液(内含0.1%甲酸)体系最强且相当。以上结果的原因可能是待测物质均将准分子离子[M+1]1+作为母离子进行检测,酸性流动相给予待测物质富含质子的环境,增强了母离子的形成。最终选定酸性较强且配置简便的甲醇-0.1%甲酸溶液作为流动相。
2.3 橄榄油浸泡液中邻苯二甲酸酯萃取溶剂的选择
分别采用甲醇-水(1∶1)、乙腈-水(1∶1)、乙腈、甲醇四种萃取溶剂对橄榄油模拟液中的20种邻苯二甲酸酯进行萃取试验,结果见表2。表2结果表明,用乙腈进行萃取时,上层溶剂乙腈与橄榄油分层非常清晰,回收率也最高;而甲醇与橄榄油混合后分层不明显,其它两种萃取溶剂的回收率都较低。原因可能是邻苯二甲酸酯属于脂溶性物质,对水和甲醇这样强氢键溶剂的亲和力较差。根据试验结果,最终选定乙腈作为橄榄油模拟液样品中邻苯二甲酸酯的萃取剂。

表2 橄榄油模拟物中DEHP萃取溶液选择试验结果
2.4 方法的线性关系与定量限
以3%乙酸模拟液和橄榄油模拟液配制成1.2中浓度的标准工作溶液,以质量浓度为横坐标,邻苯二甲酸酯的色谱峰面积为纵坐标绘制标准工作曲线,20种邻苯二甲酸酯在1~500 ng/mL范围线性良好,相关系数为0.995 5~0.999 4。以10倍信噪比(S/N)作为最低定量限,各物质在6种模拟浸泡液中的定量限见表3。
由表3可知,各物质在蒸馏水浸泡液中方法定量限为0.20~9.81 ng/mL;3%乙酸食品浸泡液中方法定量限为0.19~9.76 ng/mL;10%乙醇食品浸泡液中方法定量限为0.25~12.3 ng/mL;20%乙醇食品浸泡液中方法定量限为0.21~10.8 ng/mL;50%乙醇食品浸泡液中方法定量限为0.19~11.7 ng/mL;橄榄油食品浸泡液中方法定量限为0.45~20.3 ng/mL。

表3 20种邻苯二甲酸酯在6种模拟浸泡液中的定量限
2.5 回收试验与精密度试验
分别以3%乙酸食品浸泡液和橄榄油浸泡液为例,将已知不含邻苯二甲酸酯的塑料分别用3%乙酸与橄榄油浸泡,得到3%乙酸和橄榄油基质空白。然后分别向其中定量添加2个不同水平的邻苯二甲酸酯类混合标准溶液,得到最终浓度分别为10 ng/mL和100 ng/mL的基质加标溶液。每个添加水平平行测试6次,结果见表4。由表4可知,20种邻苯二甲酸酯在3%乙酸基质加标液中回收率为85.8%~111.3%,测定结果的相对标准偏差RSD≤6.24%;在橄榄油基质加标液中回收率为79.4%~123.6%,测定结果的相对标准偏差RSD≤8.48%,均满足定量分析要求。

表4 3%乙酸和橄榄油基质加标回收试验与精密度试验结果(n=6)
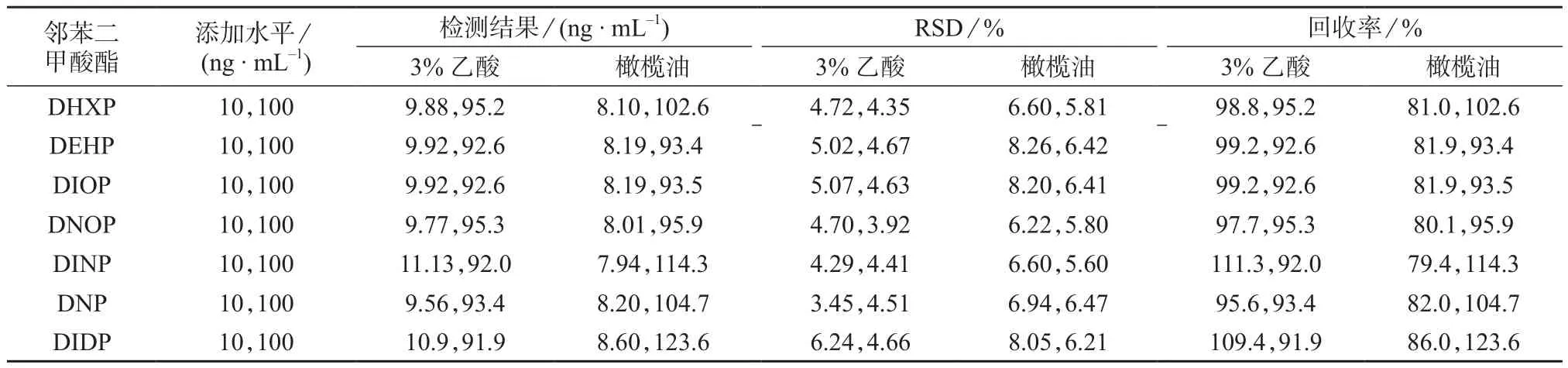
续表4
2.6 实际样品测试
分别对PE,CPP/DPP,PS,PVC等材质的24个食品接触材料样品进行测试,结果在3个PVC样品中检出DBP和DEHP。在3%乙酸浸泡模拟液中检出DBP含量为253~763 ng/mL、DEHP 为86.7~542 ng/mL;在橄榄油模拟液中检出DBP为216~635 ng/mL、DEHP为73.2~468 ng/mL;其余样品中均未检出邻苯二甲酸酯。某PVC样品用3%乙酸和橄榄油浸泡后的色谱图分别见图2和图3。
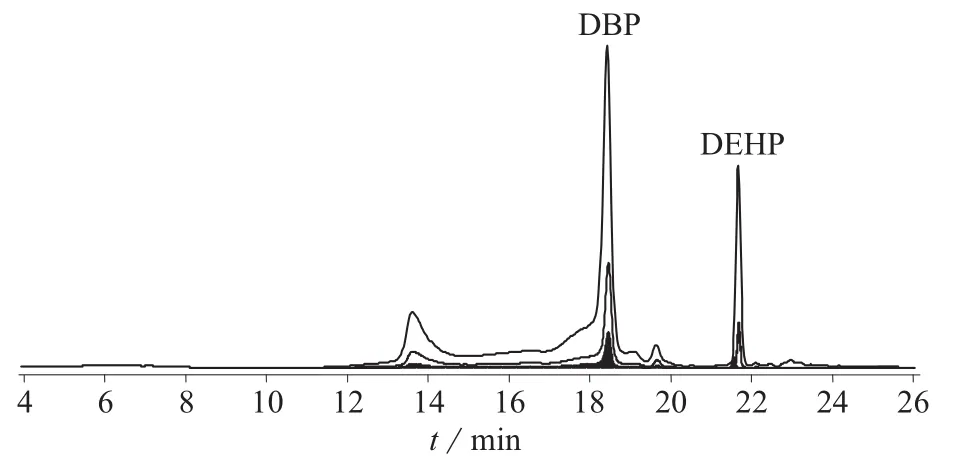
图2 某PVC样品的色谱图(3%乙酸水模拟液)

图3 某PVC样品的色谱图(橄榄油模拟液)
3 结语
采用高效液相色谱-串联质谱法同时测定食品接触材料中20种邻苯二甲酸酯迁移量。该法可有效地分离待测目标物,灵敏度高,精密度和准确度好,能够满足塑料材质食品接触材料中邻苯二甲酸酯迁移量的实际检测需要。
[1] SN/T 2037-2007 与食品接触的塑料成型品中邻苯二甲酸酯类增塑剂迁移量的测定气相色谱质谱联用法[S].
[2] 房丽萍,牛增元,蔡发,等.邻苯二甲酸酯类增塑剂分析方法进展[J].分析科学学报,2005,21(6): 687-691.
[3] Gomez-Hens A,Aguilarcm P. Social and economic interest in the control of phthalate acid esters[J]. Trends Anal Chem,2003,22(11): 847-857.
[4] Kambia K,Dine T,Gressier B. High-performance liquid chromatographic method for the determination of di(2-ethylhexyl) phthalate intotal parental nutrition and in plasma[J]. J Chromatogr B,2001,755: 297-303.
[5] 马康,汤福寿,何雅娟,等.食品包装材料中13种增塑剂的毛细管气相色谱法测定[J].分析测试学报,2011,30(3): 284-288.
[6] 刘俊,朱然,田延河,等.气相色谱-质谱法对食品包装材料中邻苯二甲酸酯类与己二酸酯类增塑剂的同时测定[J].分析测试学报,2010,29(9): 943-947.
[7] 谈金辉,蒋永祥,孟靖颖.食品包装用塑料制品中六种邻苯二甲酸酯类化合物的测定方法研究[J].分析试验室,2007,26(增刊): 133-135.
[8] Shen H Y. Simultaneous screening and determination eight phthalates in plastic products for food use by sonicationassisted extraction/GCMS methods[J]. Talanta,2005,66: 734-739.
[9] 刘丽,牟峻,杨左军,等.聚氯乙烯塑料中增塑剂的气相色谱/质谱法分析[J].分析化学,2002,30(3): 289-291.
[10] 孙海燕.3种脂溶性溶剂对PVC膜中邻苯二甲酸酯类增塑剂溶出量的测定[J].科技信息,2010,33: 15-16.
[11] 王芹,叶曦雯,牛增元,等.高效液相色谱-质谱法测定压敏胶及其制品中9种邻苯二甲酸酯[J].分析测试学报,2011,30(7): 720-726.
[12] 郑荣,许勇,于建,等.色谱-质谱联用技术测定化妆品中25种邻苯二甲酸酯[J].分析试验室,2014,33(7): 864-868.
[13] 王东辉,李懿睿,田玉平,等.食品包装用塑料中八种邻苯二甲酸酯的检测方法[J].氨基酸和生物资源,2010,34(3): 83-86.
[14] 杨荣静,卫碧文,高欢,等.高效液相色谱-串联质谱法检测食品接触材料中的17种邻苯二甲酸酯类增塑剂[J].环境化学,2012,31(6): 925-929.
[15] 张小涛,候宏卫,刘彤,等.高效液相色谱-串联质谱法同时测定烟用香精香料中16种邻苯二甲酸酯类化合物[J].分析科学学报,2013,29(6): 806-808.
Simultaneous Determination of the Migration of 20 Phthalates in Plastic Food Contact Materials by HPLC-MS-MS
Zhang Zihao, Zhang Haifeng, Mai Xiaoxia, Li Quanzhong, Li Dan, Liu Yingfeng, Yi Lezhou, Zhong Zhiguang, Zheng Jianguo
(Guangdong Entry-Exit Inspection and Quarantine Bureau, Guangzhou, 510623,China)
A high performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) method was developed for the determination of migration of 20 phthalates in food contact materials. Samples were soaked in different kinds of food simulants according to (EU) No.10/2011,the extractants from water-based simulants were directly filtered,while the extractant from olive oil simulant was extracted with acetonitrile. A C18column (100 mm×2.1 mm,2.7 µm) was used to separate the target ingredients,and a system of 0.1% formylic acid solution-methanol was used as the mobile phases with a procedure of gradient elution. The phthalates were analyzed by multiple reaction monitoring mode. The linear range was 1-500 ng/mL. The limits of quantification were 0.20-9.81 ng/mL in distilled water,0.19-9.76 ng/mL in 3% acetic acid,0.25-12.3 ng/mL in 10% alcohol,0.21-10.8 ng/mL in 20% alcohol,0.19-11.7 ng/mL in 50% alcohol,and 0.45-20.3 ng/mL in olive oil. The recoveries was 85.8%-111.3%(3% acetic acid) and 79.4%-123.6%(olive oil),and the relative standard deviations (RSDs) were not more than 8.48%(n=6). This method was simple,sensitive,accurate and precise,and appropriate for the determination of phthalates in food contact plastic materials.
food contact materials; phthalates; migration; HPLC-MS-MS
O657.7
:A
:1008-6145(2015)06-0006-05
10.3969/j.issn.1008-6145.2015.06.002
*国家质检总局科研项目(2015IK049,2013IK003);质检行业公益性科研专项(2012104020);广东检验检疫局科研项目(2014GDK52);广东省科技计划项目(2013B040402005)
联系人:张子豪;E-mail: zhang_ziho@126.com
2015-07-31
