参附注射液治疗急性胰腺炎的系统评价与Meta分析
2015-01-05张春漪逯阳张良登
张春漪逯 阳张良登
(1.北京密云县中医医院,北京 101500;2.北京国医药研究院,北京 100050;3.北京中医药大学东直门医院,北京 100700;4.中国中医科学院望京医院,北京 100102)
·文献分析·
参附注射液治疗急性胰腺炎的系统评价与Meta分析
张春漪1逯 阳2张良登3,4△
(1.北京密云县中医医院,北京 101500;2.北京国医药研究院,北京 100050;3.北京中医药大学东直门医院,北京 100700;4.中国中医科学院望京医院,北京 100102)
目的评价参附注射液治疗急性胰腺炎(AP)的疗效。方法检索10个中英文数据库,纳入参附注射液治疗AP随机对照试验(RCT)的文献,对其方法学及终点结局进行合成分析。结果纳入15个RCT共计975例AP患者,其方法学质量均为高偏倚风险。所有RCT试验组采用参附注射液结合西药及常规措施救治,对照组采用西药及常规措施救治,有5个RCT报告主要终点死亡率及手术率。对次要终点行Meta分析表明:试验组治疗后总有效率、血淀粉酶改善效果优于对照组。结论参附注射液治疗AP有效并且安全,但由于所纳入RCT方法学质量较低,建议开展更为严格的RCT以提供充分证据支持参附注射液治疗AP。
参附注射液 急性胰腺炎 Meta分析 中西医结合
急性胰腺炎(AP)是最常见的急腹症之一,20%发展为重症AP,病势凶险,死亡率高,严重危害人民健康[1]。中西医结合治疗AP疗效优于单纯西医治疗。胰腺微循环紊乱贯穿于AP病理病程,亦是AP发病始动因子之一。参附注射液源自参附汤,为人参、附子两味药的有效组分,研究表明其能通过抑制炎症、抗血栓形成、改善微循环及抗休克等作用而改善AP。应用参附注射液治疗AP临床广泛报道,但目前没有Meta分析与系统评价对参附注射液治疗AP疗效进行评价。本文在收集参附注射液治疗AP随机对照试验(RCT)数据基础上,对纳入RCT质量、安全性及疗效进行评价,为参附注射液治疗AP提供循证医学证据。
1 资料与方法
1.1 数据库与检索策略 外文数据库是SCI-E,MEDLINE,EMBASE,Clinical Trials.gov,CENTRAL,检索词是 “Shenfu injection”“Shen-Fu injection”“acute pancreatitis”“pancreatitis”“randomized controlled trial”“clinical trial”“randomized trial”。中文数据库是万方数据库、中国生物医学文献数据库、中国期刊全文数据库、中国临床试验注册中心、中文科技期刊全文数据库,检索词是“参附注射液”“急性胰腺炎”“胰腺炎”“随机对照试验”“临床试验”“中西医结合”。数据库检索时间是建库至2015年2月。
1.2 纳入标准 RCT对照组是西药及常规治疗,试验组在对照组基础上加用参附注射液。对半随机对照试验予以排除。结局指标评价包括主要终点(不良反应事件、死亡及手术率等),次要终点(血/尿淀粉酶、血常规、血糖、血钙、住院时间、症状缓解时间等)。
1.3 数据提取与质量评价 由作者张春漪、张良登分别独立实施数据检索并纳入,采用统一标准表格开展数据提取,包括提取纳入RCT的发表时间、作者、干预方法、样本量、报告结局等(见表1),同时通过第三方明确共识 (逯阳)。RCT方法学质量评价标准参照Cochrane相关标准[2],内容包括报告偏倚、选择偏倚、发表偏倚、实施偏倚、测量偏倚等方面,从而将RCT文献分为低偏倚风险和高偏倚风险两个类别。
1.4 数据合成 统计软件采用RevMan5.2。计量资料采用均数作为疗效分析统计量,计数资料采用相对危险度作为疗效分析统计量。统计分析RCT患者、疗程、干预措施及报告结局等以明确文献异质性。同时结合χ2检验、森林图、I2及P值判断异质性。如果存在异质性,应用随机效应模型分析;如果是同质性,则应用固定效应模型分析。
2 结 果
2.1 检索结果 采用PRISMA[3]流程开展RCT文献纳入。初检出临床试验文献478篇,均是中文文献。按照标准经多次筛选,提取63篇临床试验文献进入全文筛选,最终纳入15个RCT[4-11]进行定量与定性合成分析。见图1。
△通信作者(电子邮箱:zldeng3@163.com)
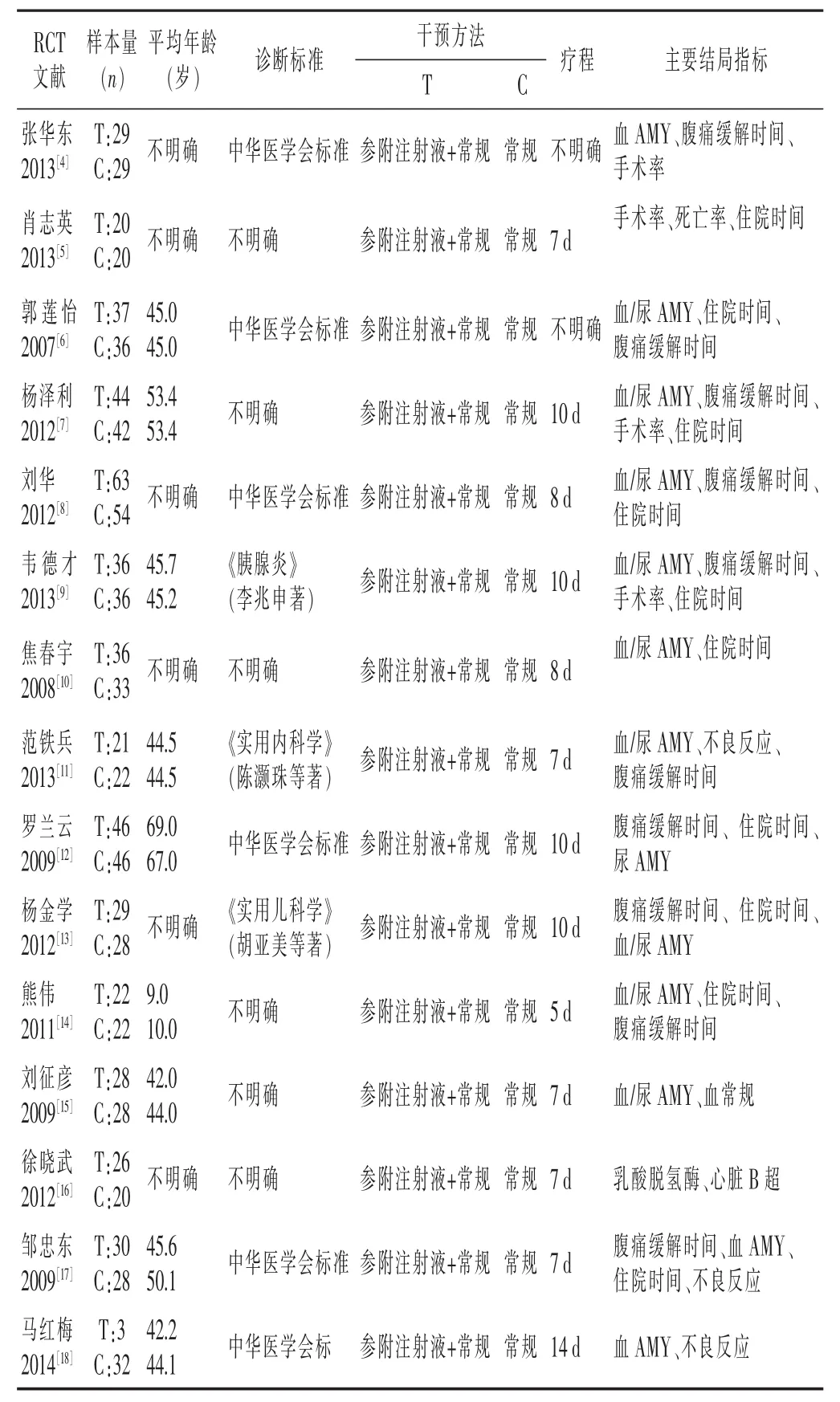
表1 RCT特点描述
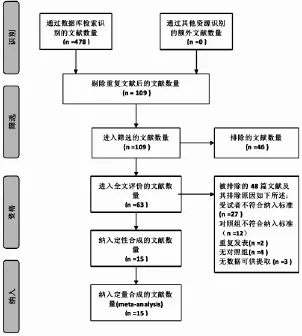
图1 PRISMA标准流程图
2.2 纳入RCT特点 纳入15个RCT合计975例AP受试者。纳入RCT样本量最大为117例,最小是40例,平均是65例,受试者年龄最小是9岁,最大是69岁。RCT对照组给予常规共识治疗,试验组则在对照组治疗基础上加用参附注射液,疗程5~14 d。次要终点包括血/尿淀粉酶、血钙、血糖、血常规、症状体征缓解时间、住院时间等。仅有5个RCT给出主要终点死亡率和手术率,试验组死亡、手术例数各为5例、7例,对照组死亡、手术例数各为14例、25例。只有3个RCT报道不良反应,1个RCT报道参附注射液试验组出现恶心、面部潮红不良反应,对照组出现恶心、面部潮红不良反应。
2.3 偏倚风险 纳入RCT所提供的方法学信息均十分有限,均为高偏倚风险RCT(见表2)。全部RCT报道基线一般资料各组之间有可比性,有10个RCT报道纳入标准,有5个RCT给出排除标准。所有RCT均报道随机分组,有4个RCT给出分配序列产生方法;均未报道盲法、随机隐藏、样本量估算方法等。
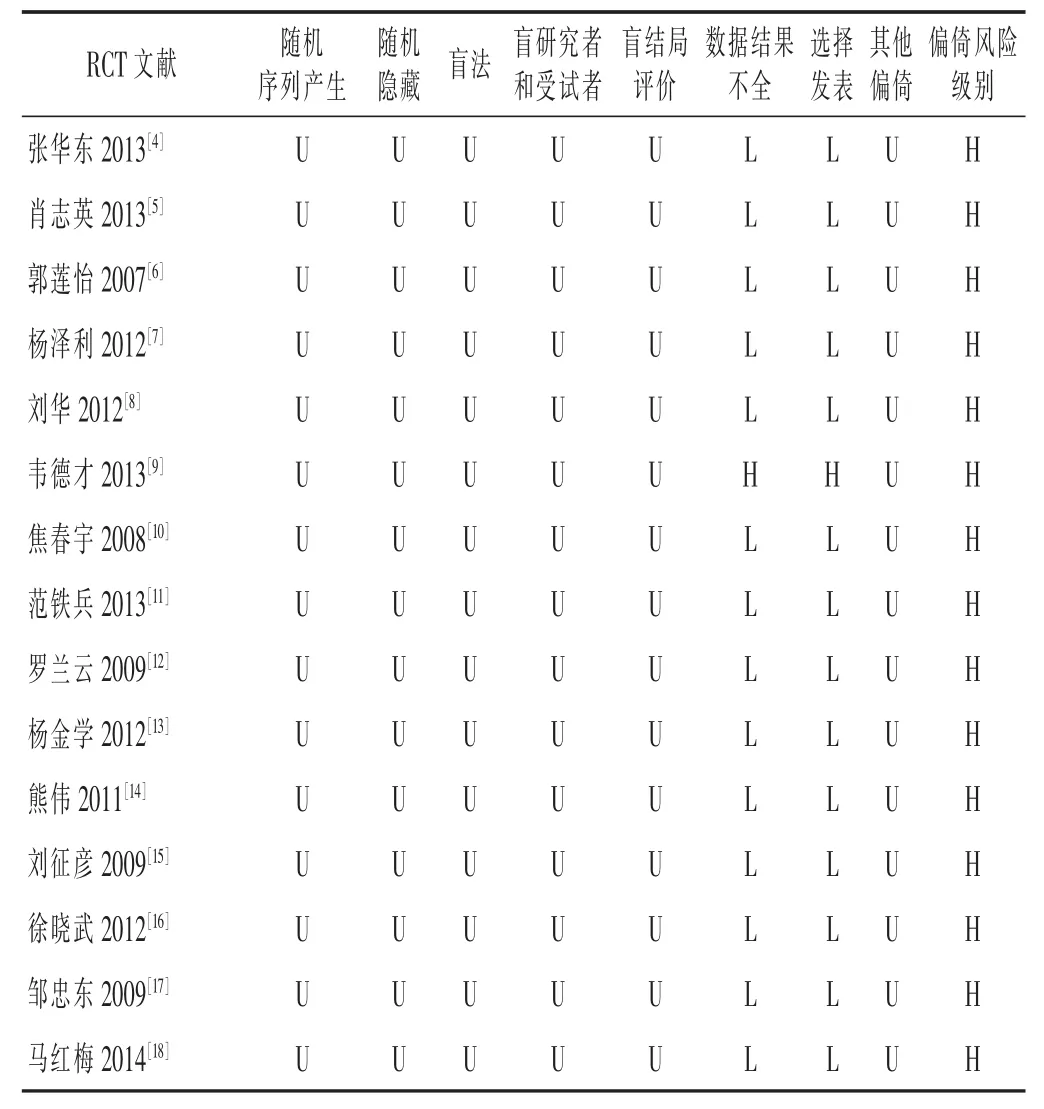
表2 RCT方法学质量评价
2.4 治疗结果 有10个RCT报道血淀粉酶,Meta分析提示参附注射液试验组治疗后血淀粉酶改善效果优于对照组(P<0.00001),如图2所示。有6个RCT报道尿淀粉酶,Meta分析提示试验组治疗后尿淀粉酶改善效果优于对照组(P<0.00001),如图3所示。有11个RCT报道平均住院时间,Meta分析提示试验组治疗后平均住院时间少于对照组(P<0.00001),如图4所示。有7个RCT报道总有效率,Meta分析提示试验组治疗后总有效率优于对照组(P<0.0001),如图4所示。行敏感性分析提示Meta分析结果均稳定,行漏斗图分析提示纳入RCT存在发表偏倚趋势。
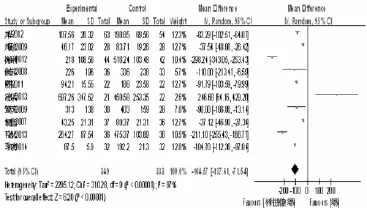
图2 两组血淀粉酶比较
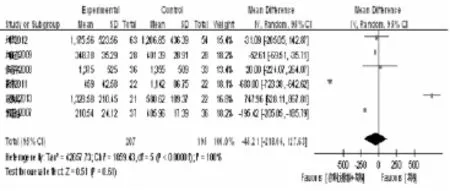
图3 两组尿淀粉酶比较

图4 两组平均住院时间比较
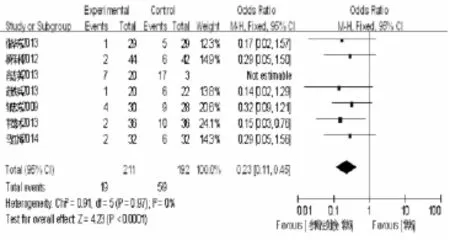
图5 两组总有效率比较
3 讨 论
AP是各种致病因素导致胰酶在胰腺内被激活后引起胰腺组织自身消化、水肿、出血甚至坏死的炎症反应病理综合征。参附注射液是现代中药有效组分配伍的产业范例,能改善微循环、抑制炎症反应,目前临床试验均报道参附注射液治疗AP有效与安全。本研究共有15个RCT合计975例AP受试者。单个RCT样本量最大117例,最小40例,平均为65例,患者年龄9~69岁。有2个RCT报告未发现不良反应;1个RCT发现轻度不良反应。有10个RCT报道参附注射液试验组治疗后血淀粉酶改善效果优于对照组,有6个RCT报道试验组治疗后尿淀粉酶改善效果优于对照组,有11个RCT报告试验组治疗后平均住院时间少于对照组,有7个RCT报道试验组治疗后总有效率优于对照组。所有RCT疗程5~14 d。有5个RCT报道主要终点死亡率及手术率,试验组死亡、手术例数各为5例、7例,对照组死亡、手术例数各为14例、25例。由于样本量偏小、缺乏远期随访数据、未充分评价主要终点与次要终点指标等原因,故对附注射液治疗AP的长期疗效尚无法达成共识。纳入RCT在方法学质量、临床试验方案设计、结果报告、结论分析等均为高偏倚风险级别,遵循循证医学与精准医学而言,目前仍缺乏充分证据支持推荐参附注射液用于治疗AP,建议开展多中心、大样本、双盲、随机化高质量临床对照试验,以提供参附注射液治疗AP循证证据,从而指导临床应用。
[1] Lei QC,Wang XY,Xia XF,et al.The role of omega-3 fatty acids in acute pancreatitis:A Meta-analysis of randomized controlled trials[J].Nutrients,2015,7(4):2261-2273.
[2] Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0[EB/OL].[2011-04]. http://www.cochrane-handbook.org/.
[3] Moher D,Liberati A,Tetzlaff J,et al.Preferred reporting items for systematic reviews and Meta-analyses:the PRISMA statement[J].Ann Intern Med,2009,151:264-269.
[4] 张华东,黄月琴.奥曲肽合用参附注射液及硫酸镁治疗急性胰腺炎的疗效观察[J].医学信息,2013,26(5):590.
[5] 肖志英,朱军华,何静,等.参附注射液对重症急性胰腺炎患者血浆IL-1、IL-6表达的影响[J].中国中医急症,2013,22(5):806-807.
[6] 郭莲怡,金旭鹏,李舒.参附注射液对重症急性胰腺炎患者血浆内皮素、一氧化氮浓度的影响[J].中国中医急症,2007,16(3):298-299.
[7] 杨泽利,姜鑫,王洪波,等.参附注射液联合奥曲肽治疗急性胰腺炎[J].中国中西医结合外科杂志,2012,18(4):352-354.
[8] 刘华,万荣,周姝,等.参附注射液在急性胰腺炎治疗中的应用[J].中国中医急症,2012,21(3):473-474.
[9] 韦德才,龚晓兵,周思栋.参附注射液治疗急性胰腺炎的临床观察[J].医药前沿,2013,12(21):33-34.
[10]焦春宇,和利稼,单孝军,等.参附注射液治疗急性胰腺炎的临床观察[J].中医药信息,2008,25(4):32-33.
[11]范铁兵,杨志旭.参附注射液治疗急性胰腺炎临床疗效观察[J].辽宁中医药大学学报,2013,15(5):185-187.
[12]罗兰云,王俭,郑波,等.参附注射液治疗老年急性胰腺炎临床观察[J].中国中医急症,2009,18(8):1269-1270.
[13]杨金学.参附注射液治疗小儿急性胰腺炎的临床观察[J].求医问药,2012,10(2):561-562.
[14]熊伟,郑波,陈峰.参附注射液治疗小儿急性胰腺炎临床研究[J].四川医学,2011,32(9):1362-1364.
[15]刘征彦,龙允杰,江儒文,等.参附注射液治疗重症急性胰腺炎伴全身炎症反应综合征患者的临床观察[J].中国民族民间医药,2009,18(z1):26-27.
[16]徐晓武,李利义,林海舵,等.参附注射液治疗重症急性胰腺炎并发心肌损伤临床观察[J].浙江中西医结合杂志,2012,22(9):701-702.
[17]邹忠东,张再重,王烈,等.参附注射液治疗重症急性胰腺炎的临床研究[J].中华胰腺病杂志,2009,9(5):291-293.
[18]马红梅,戴丐国,连建安,等.生长抑素联合参附注射液治疗胆源性急性胰腺炎的临床观察[J].中国药房,2014,25(4):343-345.
R576
A
1004-745X(2015)07-1200-04
10.3969/j.issn.1004-745X.2015.07.027
2015-03-29)
