苍术麸炒后茅术醇含量变化研究
2015-01-04黄占波楚冬海辽宁科技学院生物医药与化学工程学院
刘 彬 黄占波 楚冬海/辽宁科技学院生物医药与化学工程学院
苍术麸炒后茅术醇含量变化研究
刘 彬 黄占波 楚冬海/辽宁科技学院生物医药与化学工程学院
目的:采用气相色谱法测定苍术麸炒前后茅朮醇的含量,明确麸炒对苍术中该成分含量的影响。方法:色谱柱为HP-5石英弹性毛细管柱(30 m×0.32 mm×0.25 μm),氮气作为载气,采用氢火焰检测器,程序升温方式,分流进样(10∶1),进样口温度为220 ℃,检测器温度为250 ℃。
苍术;麸炒;茅朮醇;气相色谱
传统中药材苍术来源于菊科植物茅苍术Atractylodes lancea(Thunb.)DC.或北苍术Atractylodes chinensis(DC.)Koidz.的干燥根茎,具有燥湿健脾、祛风散寒等功效[1]。现代药理研究发现苍术具有抗胃溃疡、促进肝蛋白合成、改善脾虚、利尿等作用[2]。苍术的化学成分主要为倍半萜、聚乙烯炔类等成分组成的挥发油,以及氨基酸、倍半萜糖苷等水溶性成分和少量的糠醛[3-5];其中苍术挥发油是其主要的活性成分,茅术醇和β-桉叶醇含量较高。临床上目前应用的苍术多为麸炒苍术,苍术麸炒后的化学成分尤其是挥发油成分会发生明显变化,本实验采用气相色谱法测定全国十个地区的生苍术片及自行炮制的麸炒苍术片中茅朮醇的含量,评价苍术麸炒前后其挥发油中主要成分茅朮醇含量的差异[6],初步阐明麸炒该成分的的影响。
1.材料
1.1 仪器 Agilent 6820气相色谱仪及其配套设备,数据处理系统;HP-5(0.32 mm×30m)石英弹性毛细管柱;FID检测器;AR2140电子分析天平(上海奥豪斯公司);sartorius CP225D型电子天平( 十万分之一,德国sartorius公司);KH-300P型超声波清洗器(昆山禾创超声仪器有限公司)。
1.2 试剂和试药 β-桉叶油醇和茅术醇对照品均为自制,并经GC用归一化法测定,含量均大于98%。正十六醇(GC级,纯度大于99%)。苍术饮片分别购自浙江宁波,河北,内蒙古等地,经辽宁中医药大学李峰教授鉴定均为茅苍术[Atractylodes lancea (Thunb.) DC.]。麸炒品按照2010版《中华人民共和国药典》自制。色谱纯甲醇(天津市科密欧化学试剂有限公司);分析纯甲醇(天津市科密欧化学试剂有限公司)。
2.方法与结果
2.1 色谱条件 HP-5(0.32 mm×30m)石英弹性毛细管柱,进样口温度220℃,氢火焰检测器(FID)250℃,载气为N2气,进样量1μL,分流进样(10:1),柱流量1 mL·min-1;程序升温:柱初始温度为120℃(持续2min),以10℃·min-1升至166℃(持续8min),以20℃·min-1升至250℃(持续1min)。采用内标法,以正十六醇为内标物。见图1。
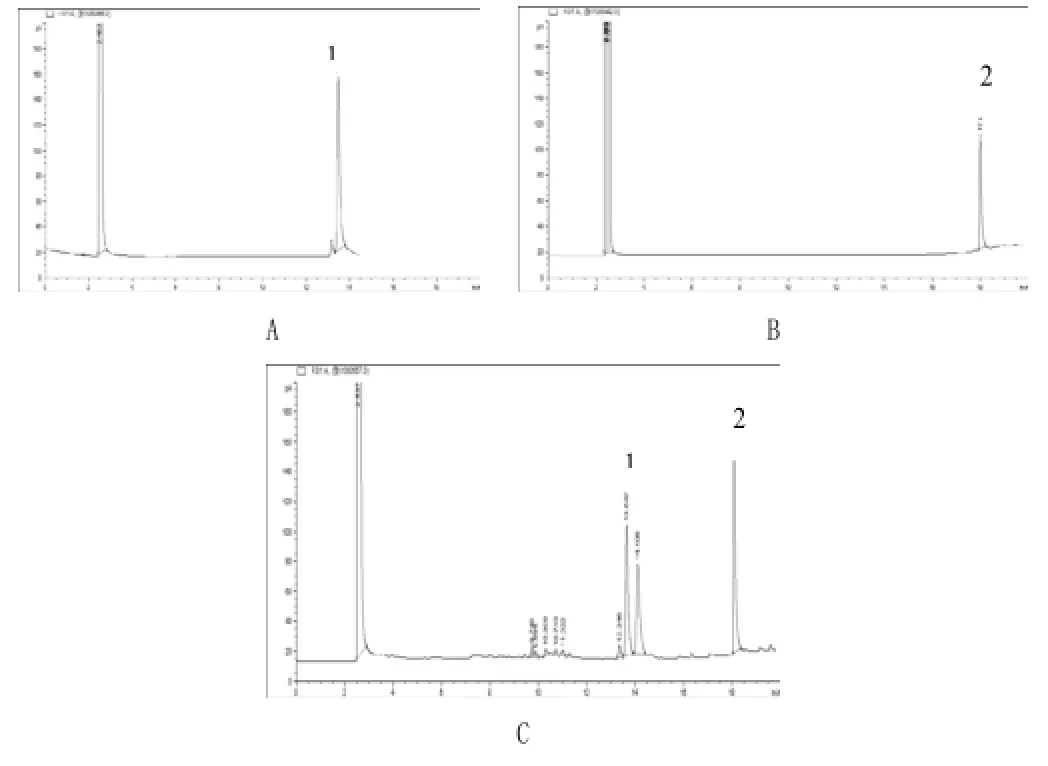
图1 气相色谱图图
A 对照品 B 内标 C 供试品
1.茅术醇;2. 正十六醇
2.2 对照品储备液的制备
称取茅术醇适量,加甲醇定容,制成1 mL含茅术醇10 mg的溶液。
2.3 内标溶液的制备
称取正十六醇适量,精密称定,制成每1 ml含15 mg正十六醇的甲醇溶液,作为内标溶液。
2.4 对照品溶液的制备
精密量取对照品储备液2 ml,内标1 mL,置于5mL容量瓶中,加甲醇稀释至刻度,摇匀,作为对照品溶液。
2.5 供试品溶液的制备
取苍术粉末(过60目筛),精密称取0.2g,置具塞锥形瓶中,精密加入甲醇,称重,放置12小时,超声处理(功率250 W,频率50kHz)30min,称重,加甲醇补足减失的重量,摇匀,滤过,置10mL量瓶中,加甲醇定容至刻度,作为供试品溶液。
2.6 线性范围考察
精密吸取对照品储备液0.3 mL,0.6 mL,0.9 mL,1.2 mL,1.5 mL,1.8 mL至5 mL量瓶中,加入内标溶液1mL,加甲醇定容至刻度,摇匀,备用。精密吸取1 μL,注入气相色谱仪中,按照“2.1”项下色谱条件,测定峰。以进样量为横坐标,以对照品与内标物的色谱峰面积之比为纵坐标,绘制标准曲线,回归方程为:Y=1.2134X+0.1879,r=0.9995。表明茅术醇进样量在0.6μg-3.6μg范围内线性关系良好。
2.7 校正因子的测定
吸取含正十六醇的对照品1 μL,按“2.1”项下的色谱条件进样6次,计算校正因子,结果平均校正因子为0.912,RSD为1.12%。
2.8 稳定性试验考察
取同一供试品溶液(浙江宁波)5μL,按“2.1”项下色谱条件,分别在0、4、8、12、24、48h时间,进样,测定色谱峰面积,计算,RSD为0.87%,结果表明,供试品溶液在48h内色谱峰面积比无明显变化。
2.9 精密度试验考察
精密吸取供试品溶液5μL(浙江宁波),按“2.1”项下色谱条件,连续进样6次,测定色谱峰面积,并将茅术醇峰面积与内标物色谱峰面积作比,RSD为0.98%,结果表明,本试验精密度试验符合规定。
2.10 重复性试验考察
精密称取本品0.2g(浙江宁波),按“2.1”项下色谱条件,测定,茅术醇的平均含量为21.2mg/g,RSD为2.87%,结果表明,本试验测定方法的重复性良好。
2.11 回收率试验考察
取已知含量的苍术(浙江宁波,茅术醇含量为21.2 mg/g)6份,每份0.1 g,精密称定,置锥形瓶中,加入茅术醇浓度为1.02 mg/mL的对照品溶液2 mL,测定,计算,结果茅术醇平均回收率为98.7%,RSD为2.3%,表明符合有关规定。
2.12 含量测定
按“2.1”项下色谱条件,测定10批来源于不同地区的的苍术片和相应的麸炒苍术片中茅术醇的含量,结果见表1 。
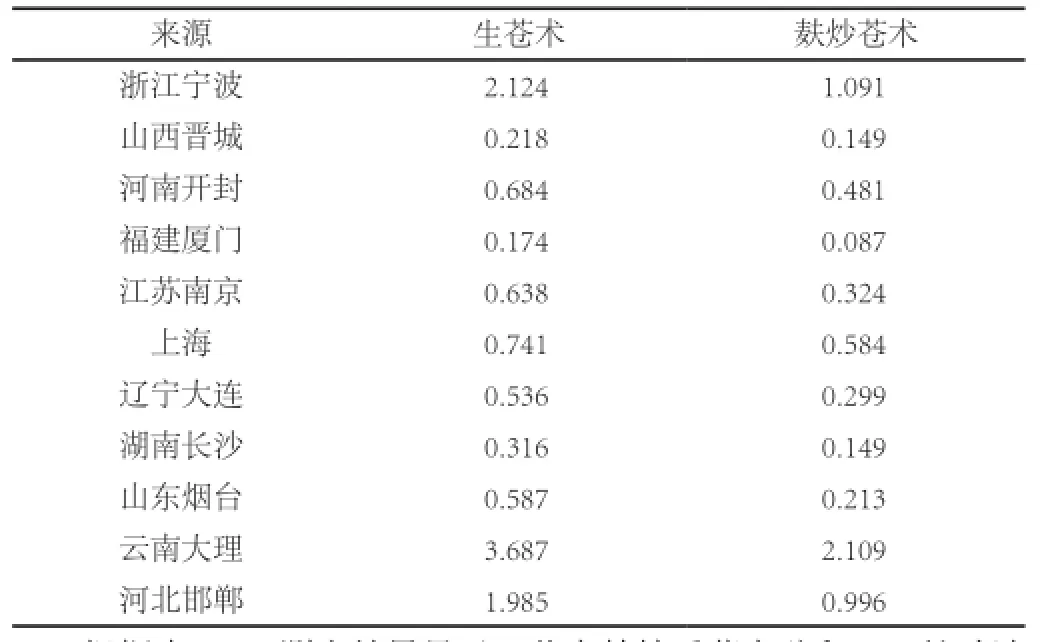
表1 不同来源生苍术和麸炒苍术中茅术醇的含量 (n=3)
根据表2-12测定结果显示,苍术麸炒后茅术醇和β-桉叶油醇的含量均呈现下降的趋势。
3.讨论
3.1 在确定供试品溶液的制备方法时,本实验先后考察了超声、回流和索氏提取等不同的提取方法,考察了甲醇、石油醚、环己烷等不同的提取溶剂,还考察了不同的提取时间和提取溶剂的容量,最终确定了本文的最佳提取方法。
3.2 由不同来源的苍术饮片的测定结果可知,来源于不同地区的苍术,茅术醇的含量相差较大,最高和最低含量相差达到20倍,说明苍术来源不同,质量不同。
3.3 通过比较生苍术和相对应的麸炒苍术中茅术醇的含量可知,苍术麸炒后该成分的含量明显降低,分析原因可能是在炮制过程中茅术醇作为挥发性成分受加热的影响,导致含量的降低。
[1] 国家药典委员会.中华人民共和国药典:一部[S]. 2010 年版.北京:中国医药科技出版社,2010:150.
[2] 刘国生,孙备,明亮,等.苍术挥发油与水溶性成分的主要药理作用比较[J]. 安徽医科大学学报,2003,38(2):124.
[3] 关颖丽: 苍术化学成分的现代研究进展[J]. 人参研究,2007,(1)28-33.
[4] 欧阳臻,江涛涛,缪亚东, 等. 苍术的化学成分、道地性和药理活性研究进展[J]. 时珍国医国药,2006,10(17):1936-1938.
[5] 李霞,王金辉,李铣,等: 北苍术化学成分的研究[J]. 沈阳药科大学学报,2002,9(3):178.
[6] 姚佳,刘玉强,才谦. GC 法测定不同来源苍术饮片中茅术醇和β-桉叶醇的含量[J]. 中国药房,2014,25(3):246-248.
刘彬(1978-),女(汉族),新疆人,本科,研究方向:制药工程。
楚冬海(1982-),男(汉族),山东人,研究生,研究方向:天然药物化学。
结果:测定了10个不同地区市售苍术片及自制的麸炒苍术片中茅朮醇的含量,发现麸炒苍术中该成分的含量低于生苍术。结论:麸炒导致苍术挥发性成分茅朮醇的含量下降。
辽宁省教育厅一般项目,编号:L2014502。
