CT血管造影术(CTA)后处理技术在肾癌分期中的临床应用
2014-12-28武汉大学人民医院放射科武汉441700
武汉大学人民医院放射科(武汉 441700)
毕 阳 谢宝君
随着CT技术的飞速发展,特别是CT血管造影术的广泛应用,我们可以更精确的了解肿瘤的空间位置、肿瘤与邻近器官的关系以及肿瘤的血供,为诊疗提供更精确的影像依据。本文通过总结我院57名肾细胞癌患者的术前影像特点,探讨CT血管造影在肾细胞癌分期中的临床应用的价值。
1 资料和方法
1.1 一般资料 回顾性分析2012年1月至2013年7月我院收治的57例肾细胞癌,术前均行CT血管造影检查,除3例因远处转移行穿刺活检外,余均行肾切除术。其中男性37例,女性20例,最小12岁,最大81岁,平均年龄51.8岁。均为单侧发病,左肾27例,右肾30例。临床表现其中肉眼或镜下血尿22例,腰痛12例,腹部可触及包块7例,同时出现血尿、疼痛及包块者5例,无临床症状体检偶然发现者11例。
1.2 检查方法 采用64排螺旋CT(GE,Lightspeed VCT),管电压120KV,管电流250MA,扫描层厚5mm,层间距5mm。扫描范围从肾上极至耻骨联合水平。增强扫描采用双管高压注射器经右前臂静脉团注优维显80ml(非离子型对比剂,浓度370mgI/100ml)。以每秒钟4ml的速度注射。所获得的图像以层厚0.625mm,层间距0.625mm重建后,在CTAW4.5工作站对原始横断位图像分别采用最大密度投影(MIP)、容积重组(VR)、MPR技术获得CTA图像。
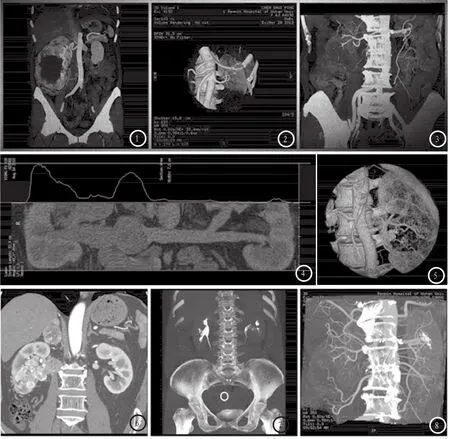
图1 右肾细胞癌。薄层MIP显示肿瘤边缘见粗大供血血管,部分分支受侵形态不规则,部分中断。图2左肾细胞癌。VR图像显示肿瘤周围血管受压,周围肾组织见明显压迹。图3右肾细胞癌。肿瘤供血动脉呈“鸟爪”样改变。图4右肾细胞癌。CPR图像显示右肾静脉及下腔静脉受侵病瘤栓形成。图5右肾细胞癌。MPR图像显示肿瘤侵犯肾盂肾盏及同侧肾上腺。图6左肾细胞癌。MIP图像显示左肾盂肾盏形态不规则,是肿瘤侵犯所致。图7右肾细胞癌。VR图像显示肿瘤下极见一肾外供血动脉,来源于肠系膜上动脉分支。图8左肾细胞癌。VR图像显示左肾见一条副肾动脉参与肿瘤供血。
1.3 图像分析 由两名腹部影像学研究方向的副主任医师对每名患者的术前肾脏CT血管造影图像进行综合评估,在两位医师都不了解患者手术病理组织学结果的情况下对图像回顾性分析,对肿瘤的分期参照2010年美国癌症联合会(AJCC)制定的肾细胞癌TNM分期标准[1]即:T1期 最大径≤7cm,肿瘤局限于肾脏;T2期 肿瘤最大径>7cm,局限于肾脏(T2a 7cm<最大径≤10cm,T2b 最大径>10cm);T3期 肿瘤侵及大静脉或肾上腺或膈肌组织但未超出Gerota筋膜(T3a 直接侵犯肾静脉及其分支或肾周脂肪但未超出Gerota筋膜,T3b 侵犯膈肌以下下腔静脉,T3c侵犯膈肌以上下腔静脉或侵犯下腔静脉壁);T4期 肿瘤超出Gerota包膜(包括侵犯同侧肾上腺);N1 单侧局域淋巴结转移;M1 远处转移。同时观察肿瘤的供血情况,肿瘤周围血管有无受侵,有无类似DSA的典型征象(如血池、肿瘤染色等)及肾动脉本身有无异常。
2 结 果
除3例因远处未行手术切除外,其余51例均接受单侧根治性肾切除术。肾细胞癌57例。肿瘤在右肾30例,左侧27例。在所有57例肾细胞癌的组织病理学评估,显示了以下的肿瘤细胞类型:肾透明细胞癌52例,肾乳头状癌3例,嫌色性肾细胞癌2例。平均肿瘤大小为6.9厘米(范围为0.5~12厘米)。T1和T2期共31例(占65%)肿瘤局限于肾内,无肾周脂肪浸润,肿瘤供血血管分支简单,其内见数目不多的稀疏血管影;T3期23例,其中同侧肾上腺受侵者3例,肾静脉或下腔静脉受侵并癌栓者10例;T4期2例;T3和T4期肿瘤内见丰富的血管树或血管网,分支复杂,血管走行迂曲而不规则,肿瘤边缘见血管包绕[2]。累及肾门及腹膜后淋巴结发现9例,其中N1期6例和N2期3例。远处转移者2例。手术病理学检查发现23例肿瘤T1期(占44%),T2期7例(占12%),T3期25例(占44%),和2例T4期(3%)。在评价淋巴结受累和远处转移中,6人N1期(10%),和3人N2期(5%),54人M0期(95%),和2人M1期(5%)。
CTA对肾细胞癌的T分期与手术病理的结果具有很好的一致性(κ=0.87),CTA准确评价了51例占总数的89%,在T分期中有6例被高估,原因主要是肾周筋膜的炎性反应性增厚,误认为是肿瘤侵犯所致;CTA在N分期中一致性稍差(κ=0.40),主要原因是因为把11例大于1cm的反应性的淋巴结增生误认为转移;CTA对肾细胞癌的远处转移评价有很好的一致性(κ=1.0),对扫描范围内转移灶可明显显示。
3 讨 论
3.1 CT血管造影术特点及基本方法 CT血管造影术(CTA)对肾细胞来讲常用的后处理技术有多平面重组(MPR)、最大密度投影(MIP)、容积再现(VR),这些后处理技术不仅有助于提供诊断信息,而且常常为手术方案的制定提供极其重要的解剖信息。MPR中的曲面重组(CPR)可以将弯曲的血管在一个横断面上显示,可多角度、任意方向旋转,避免了血管重叠给观察带来的不便,更好显示血管的解剖关系;MIP是三维数据叠加起来的图像,在了解肿瘤供血血管与周围组织关系方面明显较DSA有优势;VR可明显显示肿瘤的空间位置及其与肾盂肾盏关系。
3.2 CTA在肾细胞癌分期及临床价值 肾细胞癌起源于肾实质,主要来自近球小管,占成人所有肾脏恶性肿瘤的90%[2]。肾癌大多发生于一侧,原发于两侧的不到2%[3-5]。肾癌分为不同的病理类型,常见有透明细胞癌、乳头状细胞癌、嫌色细胞癌,所占的比例分别为70%~80%、10%~15%和5%~11%[6-14]。Gandhi D等研究认为肿瘤恶性程度越高,其分化程度越低,新生血管越多,肿瘤血管内皮细胞越不完整,通透性明显增加,癌细胞就越容易进出血管形成远处转移[15]。本组CTA探讨中也发现高分期肾癌(T3、T4期)与低分期肾癌(T1、T2期)相比,前者肿瘤内有丰富的血管网,分支复杂,血管走行迂曲而不规则,邻近肾动脉有明显受侵征象(图1);低级别肾癌(T1、T2期)其内走行血管稀疏,邻近血管分支仅见受压改变(图2),较大肿瘤周围见“鹰爪”征(图3)。CTA为肾癌分期提供有效依据,对于T1、T2来讲,分期主要是依据肿瘤的大小,CTA图像可清楚显示肿瘤的大小、位置、边界;对于T3期来说用CPR(图4)可准确了解肾静脉及下腔静脉癌栓情况(如癌栓范围、位置及长度),为外科手术路径选择提供有效依据;通过不同方位的MIP图像可准确显示同侧肾上腺以及Gerota筋膜有无受侵,受侵表现为同侧肾上腺与肿瘤分解不清(图5),Gerota筋膜不规则增厚,边缘毛糙,甚至穿破包膜向外生长;肿瘤对集合系统的破坏,单纯横断位不能明确显示肿瘤对肾集合系统破坏程度,VR可以明确肿瘤的空间位置及在分泌期肾盂肾盏有无受侵(图6)。CTA对肿大淋巴结是不是肿瘤所致特异性不高。对肿瘤远处转移有较高敏感性。
根治性肾切除长期以来都认为是肾癌治疗的唯一有效方法,但随着新的技术及手术方法的应用,如肾癌保留肾单位手术及肾动脉化疗栓塞术的推广,B超及DSA不能满足临床需要,而肾脏CTA可精确提供肾血管的解剖细节及空间关系。有学者研究表明肾癌与肝癌的血供一样,呈现多样化表现,即除肾动脉来源的供血外,常出现多渠道的血供[16,17],这就是行CTA检查的另外一个重要目的,了解肿瘤供血血管来源及肾动脉有无变异、基础病(如动脉硬化、胡桃夹综合征),在本组研究中发现肾外供血2例(图7),副肾动脉3例(图8),部分病例有轻度肾动脉狭窄,通过这些情况的反应,使临床更加准确的了解患者情况。关于肾外动脉供血的发生,杜端明[18]等认为肿瘤是否突破肾包膜与肾外营养性供血动脉的形成密切相关,是肾外供血动脉形成的主要影响因素。因此,了解有无肾外供血动脉对肾癌的分期也有重要指导意义。
CTA还可以精确显示肾静脉的病变及变异。肾静脉的变异最常见的是多肾静脉,多表现为肾静脉在汇入下腔静脉前可分成两条,15%~30%患者可以见到。另一类常见的变异是环绕肾静脉,约17%的患者可以见到[19],表现为左肾静脉分成腹侧支和背侧支两支包绕腹主动脉,也有部分变异的肾静脉在进入下腔静脉前在肾门区分为两条[20]。在环绕肾静脉存在时,通常肾上腺静脉、性腺静脉会参加主动脉前方及后方的分支。约3%的患者会看到一种少见的的静脉异常即完全主动脉后肾静脉,表现为单支左肾静走行于主动脉后方并汇流入下腔静脉的下腰段。明确这些血管变异,可以明确静脉癌栓的扩散路径、癌栓的范围及位置,更有利于手术方式的选择。
如前所述,肾脏CTA既可以清晰显示肾肿瘤与供血血管、邻近血管及周围组织解剖关系,也可以准确的显示正常和异常解剖,临床医师可以做出更为合理的治疗计划,提高手术安全性。
1.Edge S B.Byrd D R.Compton C C,etal.AJCCCancer Staging Manua[M].7th ed.New York:Springer,2010:480-488.
2.Jemal A,Murray T,Samuels A,et al.Cancer Statistics[J].CA Cancer J Clin,2003,53:5-26.
3.黄怀钱。多层螺旋CT在肾癌诊断中的应用-附42例分析[J].中国CT和MRI杂志.2006.4(2):53-55.
4.赵 艳,王成林,袁知东,等.肾脏小肾癌的影像学特征[J].罕少疾病杂志,2007,14(5):47-49.
5.周华亭,柳美玲.囊性肾癌的CT诊断[J].中国中西医结合影像学杂志,2011,9(1):76-79.
6.Bostwick DG,Eble JN.Diagnosis and classification of renal cell carci-noma[J].Urol Clin North Am,1999,26:628-633.
7.Bosnib SM.Risk and prognosis in renal neoplasm:a pathologist's pro-spective[J].Urol Clin North Am,1999,26:645-659.
8.Soyer P,Dufresne A,Klein I,et al.Renal cell carcinoma of clear type:correlation of CT features with tumor size,architectural p a t t e r n s,and pathologic staging[J].E u r Radiol,1997,7:224-229.
9.del Vecchio MT,Lazzi S,Bruni A,et al.DNA ploidy pattern in papil-lary renal cell carcinoma.Correlation with clinicopathologicl parameters and survival[J].Pathol Res Pract,1998,194:326-332.
10.Velickovic M,Delahunt B,Storkel S,et al.VHL and FHIT locus loss of heterozygosity is common in all renal cancer morphotypes but differs in pattern and prognostic significance[J].Cancer Res,2001,61:4816-4818.
11.Crotty TB,Farrow GM,Lieber MM.Chromophobe cell renal carcino-ma:clinicop athological features of50cases[J].J Urol,1995,154:965-966.
12.Thoenes W,Storkel S,Rumpelt HJ,et al.Chromophobe cell renal car-cinoma and its variants-a report on32cases[J].J Pathol,1988,155:278-286.
13.Akhtar M,Kadar H,Linjawi T,et al.Chromophobe cell carcinoma of the kidney:a clinicopathologic study of21cases[J].Am J Surg Pathol,1995,19:1246-1255.
14.Megumi Y,Nishimua K.Chromophobe cell renal carcinoma[J].Urol Int,1998,61:172-173.
15.Gandhi D.Ih,effner EG.Carlos RC,et al.Computed Tomography perfusion of squamous Cell Carcinoma of the Upper Aerodigestive Tract:INitial[J],J Comput Assist Tomogr,2003,27 (5):688-692.
16.Sprayregen S.Parasitic blood supply of neoplasms.Mechanisms and significance[J].Radiology,1973,106(3):530-535.
17.Brindle MJ.Alternative vascular channels in renal cell carcinoma[J].Clin Radiol,1972,23(3):322-329.
18.杜端明,佟小强,宋 莉,邹英华。肾恶性肿瘤血供特点及临床意义[J]。中国介入影像与治疗学2007,4(1):13.
19.Andrew H,Andrew S,Paul D,et a1.Assessment of 100 Live Potential Renal Donors for Laparoscopic Nephrectomy with Multi-Detector Row Helical CT[J].Radiology 2005;237:975-979.
20.谭婉嫦,张应和,陆巧葱,等。3D DCE MRA诊断肾静脉主干变异[J].中国CT和MRI杂志.2008.6(4):65-67.
