纳米氧化锌光催化降解甲基橙的研究
2014-12-23朱良俊崔玉民苗慧尹虎陶栋梁
朱良俊,崔玉民,苗慧,尹虎,陶栋梁
(1.阜阳师范学院 化学化工学院,安徽 阜阳 236041;2.安徽环境污染物降解与监测省级实验室,安徽 阜阳 236041)
自1976 年Cary J H 等[1]报道在紫外光照射下使用纳米TiO2把难降解的有机化合物多氯联苯脱氯后,无机半导体纳米材料的光催化氧化降解技术在环境污染治理领域的研究引起了众多研究者的重视。多年来,许多科研工作者在探索光催化氧化降解过程的机理、提高材料的光催化活性和开发新型光催化剂等方面进行了大量的研究工作[2-9]。ZnO是一种重要的宽禁带直接带隙(Eg=3.37 eV)半导体材料,具有纤锌矿结构。ZnO 在室温下具有较大的激子束缚能(60 meV),其能量远高于GaN 的激子束缚能(21 ~25 meV)[10-12],并以其独特的光电性能得到了广泛的应用。纳米ZnO 呈现出普通ZnO 所不具备的特殊性能,例如无毒、非迁移性、荧光性、压电性、吸收和散射紫外线等能力[13],这对于提高光电器件[14]、紫外激光器性能[15]及光催化剂效率[16]都具有重要作用。
纳米氧化锌的制备方法有很多,如固相法、均匀沉淀法、直接沉淀法、溶胶-凝胶、激光诱导、化学气相沉淀法、气相合成和电弧等离子体等。本文采用加热煅烧硝酸锌和聚乙烯吡咯烷酮复合物的方法制备纳米ZnO 粉体,以甲基橙的溶液为研究对象,研究了纳米ZnO 催化剂的用量、光照时间及pH 值对光催化性能的影响。
1 实验部分
1.1 试剂与仪器
Zn(NO3)2·6H2O、聚乙烯吡咯烷酮、甲基橙均为分析纯。
TU-1901 双光束紫外可见分光光度计;XPA 系列多功能光化学反应仪;UV-1100 紫外可见分光光度计;FA1104N 电子天平;2.5-10 箱式电阻炉;TGL-16G 台式高速离心机;SX-4-13 实验电炉;JEOL JSM-6700F 场发射扫描电子显微镜。
1.2 实验方法
1.2.1 纳米ZnO 粉体的制备 称量硝酸锌10 g,聚乙烯吡咯烷酮5 g 于烧杯;加入100 mL 蒸馏水搅拌均匀,将所得混合溶液放入80 ℃的恒温水浴中,搅拌保温蒸发8 h;待所得浓缩溶液冷却后倒进坩埚,然后再放入烘箱中干燥10 h,烘箱温度保持在100 ℃;最后,将干燥后的样品放入温度为500 ℃马弗炉中煅烧4 h 得到纳米ZnO 粉体。
1.2.2 光催化实验方法 分别称量10,15,20 mg由甲基橙固体配制1 000 mL 溶液作为降解对象。在避光罩内安装一支300 W 的紫外灯,固定紫外灯至甲基橙溶液液面的高度为8 cm。在100 mL 的试管中加入50 mL 甲基橙溶液,再加入一定量的纳米ZnO 粉体,进行磁力搅拌,并定时取样,然后测其吸光度A。
1.2.3 分析测定方法 采用分光光度法进行分析,先用紫外可见分光光度计对甲基橙进行全波段(190 ~700 nm)扫描,确定甲基橙的最大吸收波长(464 nm),再用UV-1100 紫外可见分光光度计在此波长下测定取样离心后上清液的吸光度。由Lambert-Beer 定律可知:A =bcε,式中b 的单位为cm;c为质量浓度(g/L);ε 为质量吸光系数,L/g·cm,降解效果以试样脱色率来比较,甲基橙溶液的脱色率按照下面的公式进行计算:
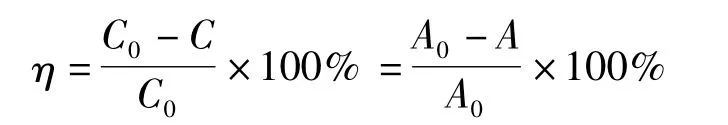
式中 η——甲基橙溶液的脱色率,%;
C0——甲基橙溶液的初始浓度,g/L;
C——甲基橙溶液的最终浓度,g/L;
A0——甲基橙溶液的初始吸光度;
A——甲基橙溶液的最终吸光度。
2 结果与讨论
2.1 扫描电镜分析
扫描电镜分析见图1。

图1 纳米氧化锌的扫描电镜照片Fig.1 SEM image of nanometer ZnO
由图1 可知,所制备的氧化锌颗粒是均匀分散的纳米颗粒,粒径在30 nm 左右。
2.2 催化剂ZnO 用量对甲基橙脱色率的影响
在光催化氧化反应中,催化剂的用量是非常重要的因素。在50 mL 质量浓度为10 mg/L 的甲基橙溶液(pH 值未调)中,改变光催化剂ZnO 的加入量,比较60 min 后甲基橙溶液的脱色率,其结果见图2。
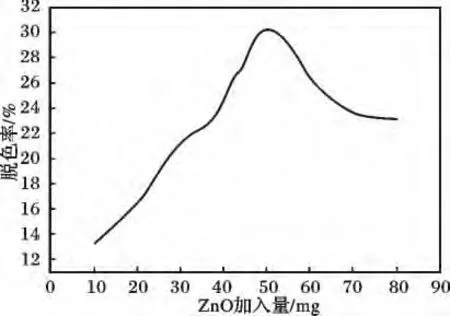
图2 ZnO 用量对甲基橙脱色率的影响Fig.2 The effect of amount of ZnO on the decolorization rate of MO(methyl orange)
由图2 可知,随着光催化剂ZnO 用量的增加,甲基橙溶液的脱色率逐渐增加。但是当催化剂的加入量增加到一定量,即50 mg 时,甲基橙溶液的脱色率最大(30.3%)。当超过50 mg 时,甲基橙溶液的脱色率反而逐渐下降。这说明ZnO 加入量并不是越多越好。如果催化剂投加量过低,溶液中活性物降低,催化降解效率相应降低;如果催化剂投加量过高,颗粒对太阳光散射损失光能,催化降解效率也相应降低。因此只有适当投加催化剂的用量才能得到最佳的效果。无论从处理效率还是从处理成本上考虑,催化剂的用量都有一个最佳值。从本实验综合考虑,确定催化剂的最佳投入量为1 g/L。
2.3 光照时间对甲基橙脱色率的影响
在其他反应条件固定不变的情况下,在50 mL甲基橙溶液中投加50 mg 光催化剂ZnO,比较不同时间甲基橙的脱色率,见图3。
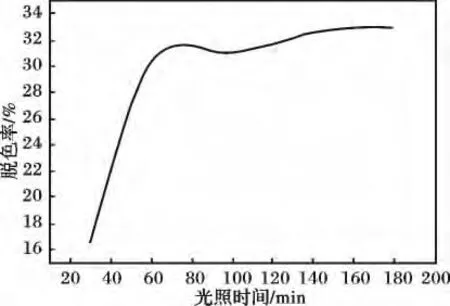
图3 光照时间对甲基橙脱色率的影响Fig.3 The effect of illumination time on the decolorization rate of MO
由图3 可知,随光照时间的延长,甲基橙溶液的脱色率增加,但是,当光照时间延长到150 min 时,甲基橙溶液的脱色率最大(32.9%),继续延长光照时间,溶液的脱色率不再有明显的提高。
2.4 pH 值对甲基橙脱色率的影响
将50 mL 浓度为10 mg/L 的甲基橙溶液分别用HCl 和NaOH 调节pH 值,在不同的pH 值下进行光催化反应,光照60 min 后计算脱色率,pH 值对甲基橙溶液脱色率的影响,结果见图4。
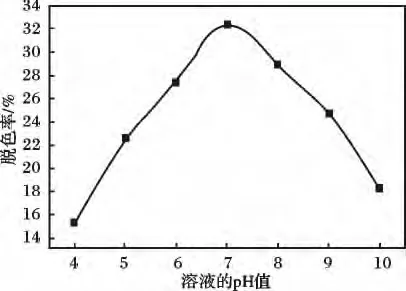
图4 pH 值对甲基橙脱色率的影响Fig.4 The effect of pH value on the decolorization rate of MO
由图4 可知,pH 值在7 左右时,即中性条件下甲基橙溶液的脱色率明显高于酸性或者碱性条件下的脱色率,最大脱色率32.4%。其原因可能是ZnO是两性氧化物,在碱性或者酸性条件都容易发生酸碱反应,不利于其光催化反应的进行。
3 结论
本文采用加热煅烧以硝酸锌、聚乙烯吡咯烷酮为原料的复合物,成功制备出对甲基橙溶液具有良好脱色性能的纳米ZnO 光催化剂。并考察了催化剂用量、光照时间及pH 值对光催化性能的影响。其结果表明,光催化剂ZnO 的投加量适当才能得到最佳效果,最佳投加量是1 g/L;光照时间在150 min已经达到饱和催化状态;光催化反应宜在中性条件下进行。
[1] Carey J H,Lawrence J,Tosine H M. Photochlorination of PCBs in the presence of TiO2in aqueous suspensions[J].Bull Environ Contam Toxicol,1976,16:697-700.
[2] Keiichi Tanaka,Mario F V Capule,Teruaki Hisanaga.Effect of crystallinity of TiO2on its photocatalytic action[J].Chemical Physics Letters,1991,187(l/2):73-76.
[3] Chen L C,Chou T C.Photodecolorization of methyl orange using silver ion modified TiO2as photocatalyst[J].Industrial & Engineering Chemistry Research,1994,33(6):1436-1443.
[4] Choi W,Hoffmann R. Kinetics and mechanism of CCh photo reductive degradation on TiO2:The role of trichloromethyl radical and dichlorocrbene[J].Journal of Physical Chemistry,1996,100(6):2161-2169.
[5] Paz Y,Heller A. Photo-oxidatively self-cleaning transparent titanium dioxide films on soda lime glass:The deleterious effect of sodium contamination and its prevention[J].Journal of Materials Research,1997,12(10):2759-2766.
[6] Machida M,Norimoto K,Watanabe T,et al.The effect of SiO2addition in superhydrophilic property of TiO2photocatalyst[J].Journal of Materials Science,1999,34(11):2569-2574.
[7] Toshiya W,Shigemichi F,Masahiro M,et al.Photocatalytic activity and photo-induced wettability conversion of TiO2thin film prepared by sol-gel process on a soda-lime glass[J]. Journal of Sol-Gel Science and Technology,2000,19(1/2/3):71-76.
[8] Mitsunobu I,Masayoshi H,Hiromi K,et al. Cobalt iondoped TiO2photocatalyst response to visible light[J].Journal of Colloid and Interface Science,2000,224(1):202-204.
[9] Tetsu Tatsuma,Shuichi S,Yoshihisa O,et al. TiO2-WO3photoelectro chemical anticorrosion system with an energy storage ability[J]. Chemistry of Materials,2001,13(9):2838-2842.
[10] 李新华,徐家跃. 半导体ZnO 单晶生长的技术进展[J].功能材料,2005,36(5):652-654.
[11] 夏昌奎,黄剑锋,曹丽云,等.微波水热法制备ZnO 纳米晶[J].人工晶体学报,2008,37(4):833-838.
[12]Zhou Q.Preparation process of ZnO nano belts selfassem bling generated via polymer[J].Inor Chem Trans,2006,22:1675-1678.
[13]Pal U,Santiago P.Controlling the morphology of ZnO nano structures in a low temperature hydrothermal process[J].J Phys Chem B,2005,109(32):15317-15321.
[14]Tak Y J,Yong K J.Controlled growth of well aligned ZnO nanorod array using a novel solution method[J]. J Phys Chem B,2005,109:19263-19269.
[15]吴莉莉.纳米氧化锌的制备及其光学性能研究[D].济南:山东大学,2005.
[16]Li M,Riley D J.Templated electrosynthesis of zinc oxide nanorods[J].Chem Mater,2006,18:2233-2237.
