乳胶增强免疫比浊法测定髓过氧化物酶试剂盒性能验证评价
2014-12-16高小文孙安平陈建华乔永峰孔花娟李玲贤李雄海陕西省汉中市中心医院检验科723000
高小文,孙安平,陈建华,乔永峰,孔花娟,李玲贤,陈 皎,郑 荣,李雄海(陕西省汉中市中心医院检验科 723000)
血浆髓过氧化物酶(MPO)为一种血红素蛋白,主要来源于多形核中性粒细胞,单核细胞、巨噬细胞中亦存在。当受到炎症刺激、白细胞激活并脱颗粒时,多形核中性粒细胞释放MPO[1]。近年来随着研究的深入,认为MPO水平与急性冠脉综合征的近期预后有明显的相关性,是急性冠脉综合征发生的危险因素。MPO测定的方法国内外主要是酶联免疫吸附试验,自动化程度低,误差大,北京九强公司在国家863计划支持下研发的乳胶增强免疫比浊法试剂盒,实现了在全自动生化分析仪的检测,分析精确度和准确度都大大提高。在临床应用和课题研究中为了评价该方法试剂盒的性能指标,本文参照美国临床实验室标准化委员会(NCCLS)的评价方案,结合国内专家对性能验证的系统设计要求[2-4],进行了准确度验证实验(回收试验)、精密度验证实验、临床可报告范围及干扰试验的性能验证,现将评价结果首次报道如下。
1 材料与方法
1.1 材料贝克曼AU2700全自动生化分析仪及北京九强生物技术有限公司研发生产的MPO乳胶增强免疫比浊法试剂盒(批号:13-0412);MPO的校准品为人血清基质(量值溯源至FDA方法,批号:13-0412),5个浓度水平分别是87、141、349、652、1 172ng/mL;质控品为液体,开启即用,(批号:13-0412),人血清基质,2个浓度水平(低值/高值)。
1.2 标本来源于心血管内科住院患者早上空腹肝素钠抗凝血标本。肝素钠采样管由湖南浏阳市医用仪具厂生产,采集的血样1h内分离血浆,室温22℃,标本要求无黄疸和肉眼脂血。
1.3 方法
1.3.1 准确度验证实验(回收试验)[2]:取435.8、471.9、1122 ng/mL 3个已知不同高浓度MPO的肝素钠抗凝新鲜血浆,加入到121.4、211.1、384.6ng/mL 3个已知不同低浓度MPO的新鲜血浆中,加入比例10份低浓度与1份高浓度新鲜血浆混匀,每个连续测3次,取均值计算回收率,回收率在90%~110%,结果为可接受[5]。
1.3.2 精密度验证实验[6-7]:依照EP15-A方案,选两个浓度水平的质控品,用相同试剂每个每天重复测3次,连续5天,测得15个数据,计算实验室变异系数CV%,小于厂家变异系数CV<10%的要求,结果为可接受。
1.3.3 分析测量范围(AMR)验证实验[8]按照EP6-A2文件要求,选择MPO浓度163ng/mL和1 084ng/mL高低血浆各1份,将2份血浆按3∶1、1∶1、1∶3的比例混合,同时将163ng/mL稀释1倍,配制成82ng/mL,产生6个不同理论水平的混合血浆(82,163,393,624,854,1084),分别重复测定3次,取均值作为实测值,以理论值和实测均值作回归分析,计算相关系数r,回归方程Y=aX+b,按a=1.0±0.05、r≥0.97为验证合格标准,说明在82~1084ng/mL浓度范围内线性关系良好。
1.3.4 干扰试验
1.3.4.1 溶血的干扰 先测血浆的MPO值,然后人为造成溶血,离心后测血浆中血红蛋白g/L含量,选取5个不同血红蛋白浓度的血浆,再次测其MPO值两次,取均值逐一计算干扰偏差。
1.3.4.2 抗坏血酸的干扰 在定值233ng/mL的MPO血浆中分别加入100、50、25、12.5、6.3g/L浓度的抗坏血酸(按9∶1的比例),混匀静置5min,每个重复测2次,取均值逐一计算干扰偏差%。
1.3.4.3 三酰甘油的干扰 同样在定值233ng/mL的MPO血浆中分别加入13.33、6.83、3.46、1.78、0.88mmol/L浓度的三酰甘油(按9∶1的比例),混匀静置5min,每个重复测2次,取均值逐一计算干扰偏差%。
1.4 统计学方法采用microsoft office Excel统计分析。
2 结 果
2.1 准确度验证实验(回收试验) 3个新鲜配制的高中低值混合血浆的回收率分别见下表1,结果说明回收率在95.7%~108.3%之间,均在90%~110%回收率要求的可接受范围内。见表1。

表1 MPO 准确度验证实验(回收试验)数据统计分析
2.2 精密度验证实验依照EP-15方案,选两个浓度水平的质控品,用相同试剂每个每天重复测3次,连续5d,测得15个数据,计算出实验室精密度CV为8.9%小于厂家变异系数CV<10%的要求。
2.3 分析测量范围(AMR)验证实验将6个不同水平的混合血浆测定后,把测定值(Y)和理论值(X)进行线性回归分析,计算相关系数r=0.997,线性回归方程为Y=1.033 X-25.092。同时各点与回归直线的分布关系见图1,说明在82~1 084ng/mL浓度范围内线性关系良好。
2.4 干扰试验
2.4.1 溶血的干扰 5个不同血红蛋白浓度溶血的血浆,对测定MPO的干扰,计算干扰偏差结果见表2,数据显示不同程度的标本溶血均对测定MPO造成严重干扰。
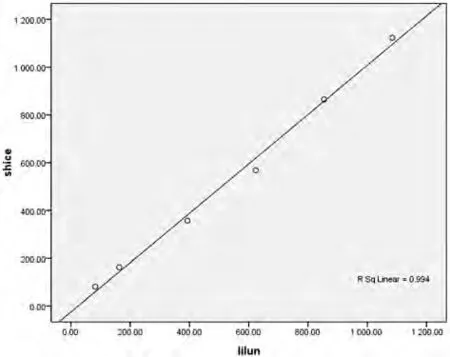
图1 线性回归分析各点与回归直线的分布关系图
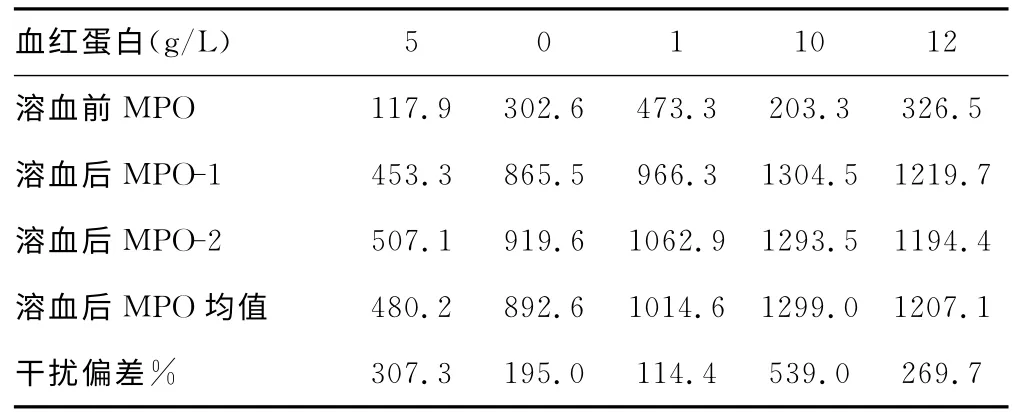
表2 不同溶血程度对MPO测定的干扰分析偏差
2.4.2 抗坏血酸的干扰 在233ng/mL定值血浆中加入配比稀释浓度下的抗坏血酸后,对测定MPO的干扰偏差结果见表3,结果显示抗坏血酸对测定MPO偏差小于10%,最高达6.5%。
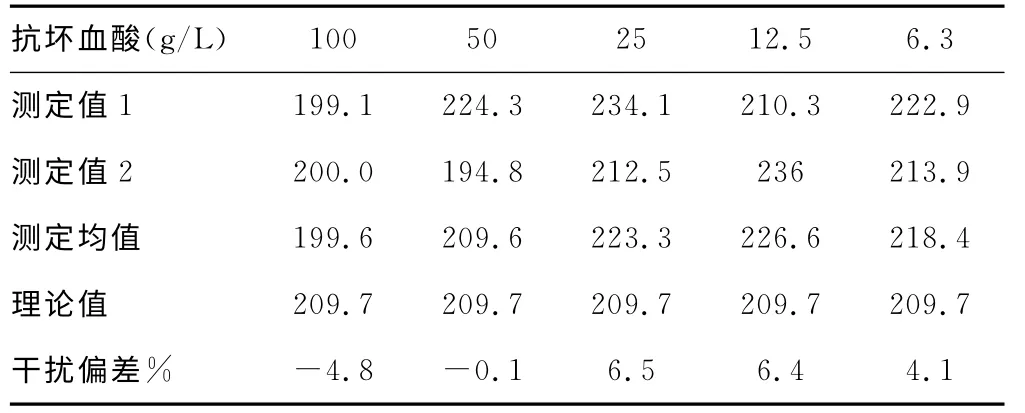
表3 配比稀释浓度下抗坏血酸对MPO测定的干扰分析偏差表
2.4.3 三酰甘油的干扰 在233ng/mL定值血浆中加入配比稀释浓度下的三酰甘油后,对测定MPO的干扰偏差结果见表4,数据显示三酰甘油浓度在3.46mmol/L以上会造成大于10%的负偏差。
3 讨 论
临床实验室在正式使用选购的商品试剂盒之前对厂家声称的相关指标要进行验证,以保证所选用的试剂盒达到临床实验室要求,这也是ISO 15189在其“检验程序”一节中明确要求“使用经确认的程序,性能适合其预期用途”,要求临床实验室在选择测定项目的试剂盒之前,须在临床和顾客需要基础上确定其(最低)性能。我国“医疗机构临床实验室管理办法”也做出了这样的要求,保证所选用的试剂盒达到临床实验室要求的临床性能、分析性能和经济性能等各方面的要求.确保能提供更准确反映患者真实病情的信息,指导临床医生的诊断。但这并不是说需要对厂家声明的全部分析性能进行验证。CLIA′88就明确提出临床实验室可只对3项主要分析性能进行验证,即准确度、精密度和分析测量范围(AMR)[9]。本文依据以上标准和要求,首次对MPO试剂盒进行了主要分析性能的验证。
准确度验证实验,一般可采用与参考方法比较[10]、应用参考物质[11]、回收实验、检测配套定值质控品,与质控说明书标示的靶值范围比较[12]以及与室间质评结果比较等方式进行。目前该项目国际上未发布参考方法,也没有有证的参考物质,定值质控品因厂家采取的检测系统与本次的检测系统不同,结果存在一定的偏差,而不能简单比较,另外,因为是新研制的项目,卫生部临检中心也没有开展此项目的室间质评。同时,免疫比浊法因各厂家制备的抗体特异性差异,造成不同厂家、不同批号间有一定的误差,本文根据实际情况采取了新鲜样本间的回收实验,结果比较理想,回收率在95.7%~108.3%之间,符合定量试验回收率(100±10)%的范围,今后如有参考方法和有证参考物质,可以对该方法的准确度进行更好的验证。
精密度是表示测定结果中随机误差大小程度的指标,是定量试验重要的评价指标,其CV值越小,重复性越好。良好的重复性是进行其他方法学验证实验的前提,精密度的验证,EP15-A2精密度方案提供了评估的详细方法[7],此方案比其他学者[9]采用的要简单易行,耗时短,临床应用和报道的也多。本文验证的实验室精密度CV为8.9%小于厂家变异系数CV<10%的要求。
分析测量范围(AMR)验证,目的是验证检测系统的最高检测值和高低检测值之间是否呈线性关系,实验室应为每个系统建立各自的线性参数,不应直接引用厂家提供的线性范围。CLSI EP6-A2提供了对线性验证的指导文件,常规实验室对商品试剂盒的线性验证,一般只取5种浓度标本,多次重复测定,再使用一些判断标准即可。本文按推荐标准用6种系列浓度的新鲜血浆对试剂盒的线性进行评价,结果相关系数r=0.997,线性回归方程为Y=1.033 X-25.092。AMR与定标范围(87~1 172ng/mL)一致,略低于厂家提供的线性范围25~1 300ng/mL;说明线性良好。
另外,本文选取了临床常见的溶血、抗坏血酸、三酰甘油做干扰试验,发现不同程度的标本溶血均对测定MPO造成严重干扰。抗坏血酸偏差最高达6.5%,基本无干扰,三酰甘油浓度在3.46mmol/L以上会造成大于10%的负偏差,说明该方法对三酰甘油的抗干扰能力有限,这也是免疫比浊法共有的问题,因此,临床在测定MPO时,应避免标本溶血和乳糜血,减少分析前的测量误差。
综上所述京九强公司研制的乳胶增强散射比浊法测定MPO,在AU2700全自动生化分析仪上的主要分析性能验证结果符合临床检验的质量要求。各实验室对检测系统的性能进行有效地评估,有助于提高检测结果的准确性和可靠性。同时国内自建检测系统较多,在性能验证时应根据实际情况系统和合理地选择、设计每一种定量检测项目的验证方案。
[1]Leckie MJ,Gomma AH,Purcell IF,et al.Automated quantitation of peripheral blood neutrophil activation in patients with myocardial ischaemia[J].Int J Cardiol,2004,95(2/3):307-313.
[2]王治国.临床检验方法确认与性能验证[M].北京:人民卫生出版社,2009:131-284.
[3]毕波,吕元.定量检测方法学性能验证的系统设计[J].中华检验医学杂志,2007,30(2):143-145.
[4]徐淑贞,陈明涛,姚轶敏.浅谈医学实验室检测系统的性能验证[J].中医药管理杂志,2011,19(12):1154-1155.
[5]张葵.定量检测系统方法学性能验证实验的基本方法[J].临床检验杂志,2009,27(5):321-323.
[6]杨志钊,缪丽韶,杨山虹,等.利用CLSI EP15-A指南验证精密度和准确度[J].国际检验医学杂志,2010,31(3):231-232,237.
[7]王薇,王治国,李少男.临床实验室对厂家声明的精密度和真实度的性能验证要求[J].检验医学,2010,25(12):1001-1005.
[8]吴文清,黄志基.罗氏电化学发光检测系统乙型肝炎表面抗原定量检测方法学评价及性能验证[J].检验医学与临床,2013,10(11):1407-1408.
[9]U.S.department of health and human services.42CFR part 493:Medicare,Medicaid and CIIA programs;laboratory requirements relating to quality systems and certain personnel qualifications;final rule[J].Fed Regist,2003,68(40):3640-3714.
[10]杨曙梅,浦江,张芹,等.两种商品定量试剂盒分析性能的验证试验[J].检验医学与临床,2013,10(3):301-302.
[11]莫扬.按照CLSI EP15-A指南验证BN Prospec特定蛋白仪测定免疫球蛋白的精密度和正确度[J].现代检验医学杂志,2012,27(1):129.
[12]官燕飞,彭建明,刘树沅,等.STA-R凝血分析仪检测D-二聚体的性能验证[J].国际检验医学杂志,2013,34(14):1875-1877.
