粉碎粒度对毛木耳吸附特性影响的研究
2014-12-16岳凤丽安东于克学李新胜井瑞洁姜桂传
岳凤丽,安东,于克学,*,李新胜,井瑞洁,姜桂传
(1.山东农业工程学院,山东济南250100;2.中华全国供销合作总社济南果品研究院,山东济南250014)
毛木耳(Auricularia polytricha)又名粗木耳[1],属担子菌纲、木耳目、木耳科、木耳属,是热带和亚热带地区主要栽培的食用菌之一。与黑木耳相比,虽是同属不同的种类,但其耳片较黑木耳大、厚,且背面长有较长的绒毛,质地较粗韧,硬脆耐嚼;氨基酸组成、营养成分及功效与黑木耳基本相似,富含多糖、胶质、蛋白质、维生素和多种矿物质元素,具有益气强身、活血止血、降低人体血液凝块、缓和冠状动脉硬化、防止血栓形成、清除肠胃中积食、纤维素之功能。由于毛木耳抗逆性强,适应性广,生产技术容易掌握,因此,近年来在山东、河南、浙江、福建等地栽培面积不断扩大。2013年,仅山东省鱼台县年产毛木耳就达 6000万公斤。随着生活水平的提高,人们在食品安全、健康方面的意识逐步增强,过量的油脂摄入、农田土壤中重金属以及食用水源的污染等因素[2-3],促使慢性非传染疾病发病率提高,影响着人体健康。如何通过食物本身除去影响人体健康的脂肪、重金属等有害成分已成为营养学、食品科学及预防医学等学科研究的课题之一[4]。毛木耳子实体中的胶质成分,是一种天然的生物吸附剂,近几年来的研究,揭示了毛木耳胶质具有吸附铜离子的功能[5-9],但尚未见到不同粒度的毛木耳粉体吸附水分、油脂及重金属镉离子的报道。本研究通过不同粉碎处理,探讨不同粒度毛木耳粉体吸附能力的影响[10-13],旨在为合理开发利用毛木耳资源,乃至工业化生产提供参考。
1 材料与方法
1.1 材料与试剂
毛木耳:产于济宁鱼台县毛木耳种植基地,清理除杂后,按试验要求进行不同粒度的粉碎以备用。
主要试剂:重金属离子标准品:北京中标华威科技有限公司。
1.2 仪器与设备
6B-1型贝利微粉机:济南贝利粉体技术工程有限公司;RXH-B1型热风循环烘箱:上海一恒科技有限公司;A3-F型原子吸收分光光度计:北京普析通用公司。
1.3 毛木耳粉体的制备
取毛木耳子实体原料清洗除杂,烘干,含水量≤13%。在0℃~4℃条件下将处理的毛木耳置于超微粉碎机中超微粉碎,按粉碎时间不同,分别过筛得到40目、100目、300目3个粉体样品,并以未处理的毛木耳子实体原料作为对照样品。
1.4 毛木耳吸附水分能力的测定
称取毛木耳粉体样品及对照样品各(2±0.01)g,分别置于离心管中,加入50 g的去离子水并搅拌1 min,静置30 min后,以 1000 r/min离心5 min,去余水,称重,计算每克样品的吸水质量。每组重复处理3次。
1.5 毛木耳吸附油脂能力的测定
称取毛木耳粉体样品及对照样品各(5±0.01)g,分别置于离心管中,加大豆油20 mL并搅拌1 min,静置30 min后,以 1000 r/min离心5 min,称重,计算每克样品的吸油体积。每组重复处理3次。
1.6 毛木耳吸附重金属含量的测定
1.6.1 重金属溶液的配制
以Cd2+离子溶液的配制为例。用移液器分别精确吸取 Cd2+离子溶液标准品(浓度为 1 mg/mL)5、4、3、2 mL和1 mL,加入500 mL容量瓶中,用新配2%硝酸溶液定容,配制成浓度为分别为 2、4、6、8、10 μg/mL 的Cd2+离子标准溶液,以备用。
2.6.2 重金属吸附试验
称取毛木耳粉体样品及对照样品各(2±0.01)g,放入装有 100 mL 浓度分别为 2、4、6、8、10 μg/mL 重金属溶液的三角锥瓶中,用恒温振荡器在150 r/min和25℃的条件下振荡吸附5 h,振荡后溶液用定量滤纸过滤,收集滤液,用FAAS法测定吸附前后溶液重金属含量,每组重复处理3次。注:检测方法参照GB/T 5009.15-2003。
1.7 吸附量计算公式

式中:m1、m2、m3为加入毛木耳粉体样品的质量;C1为吸附前溶液中重金属离子浓度,(μg/mL);C2为吸附后溶液中重金属离子浓度,(μg/mL)。
2 结果与分析
2.1 毛木耳粉体吸附水分能力
不同毛木耳粉体样品饱和吸附水分能力见图1。
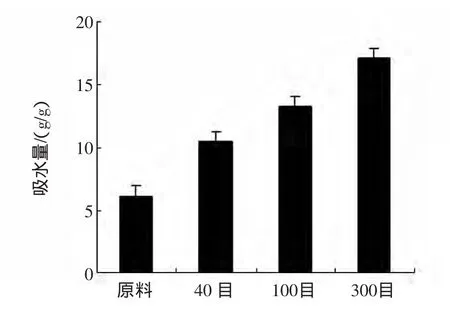
图1 不同目数毛木耳样品对水分吸附Fig.1 Adsorpted water of Auricularia polytricha samples at different mesh
由图1所示,随着粉体目数的增加,毛木耳粉体饱和吸水量显著增大,当粉碎目数达到300目时,饱和吸水量为17.12 g/g,与对照组(6.13 g/g)相比,吸附水分能力提高179.3%。这说明,毛木耳经过粉碎处理后,随着粉体比表面积增大,更多的亲水基团暴露出来,对水分吸附能力显著增强。
2.2 毛木耳粉体吸附油脂能力
不同毛木耳样品油脂能力见图2。
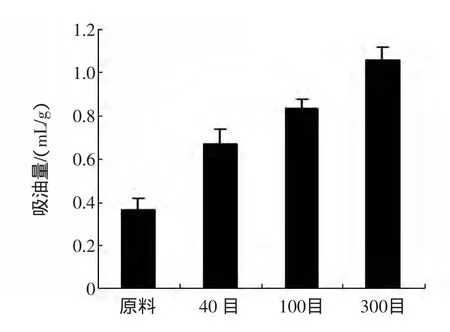
图2 不同目数毛木耳样品对油脂吸附Fig.2 Adsorpted oil of Auricularia polytricha samples at different mesh
由图2所示,随着粉碎目数的增加,毛木耳吸附油脂﹙具体油脂名称﹚的能力逐渐增强。在粉碎目数达到300目时,饱和吸油量为1.06 mL/g,与对照组(0.37 mL/g)相比,吸附油脂能力提高186.5%。经过粉碎后,吸附能力有了显著提高,但由于毛木耳子实体中亲油基团较少,因而对油脂的吸附能力表现一般,不及吸附水的量大。
2.3 毛木耳粉体吸附Cd2+离子能力
毛木耳样品对Cd2+离子的吸附能力见图3。
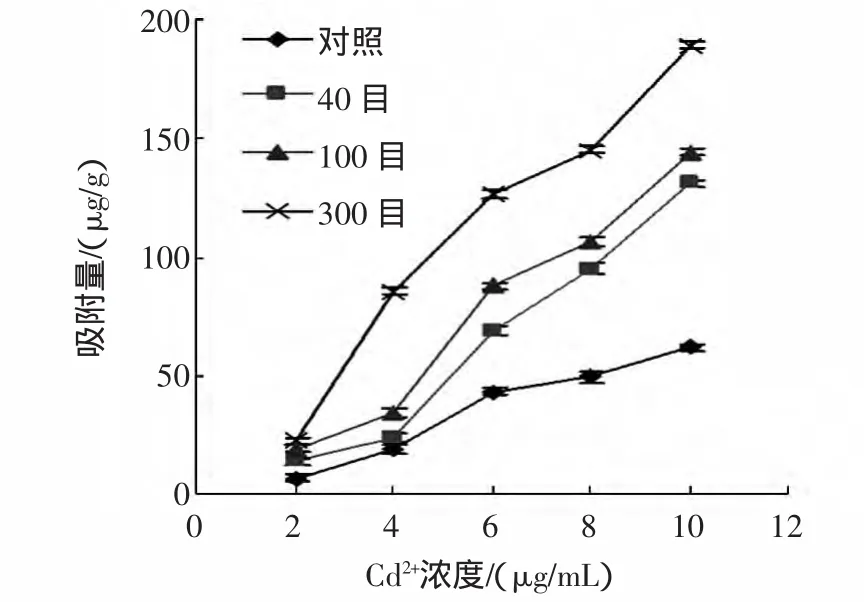
图3 不同目数毛木耳样品对金属离子Cd2+吸附Fig.3 Adsorpted metal ion Cd2+of Auricularia polytricha samples at different mesh
从图3可以看出,随着溶液中Cd2+离子浓度的增加,四组样品的吸附量均呈现增加趋势。且粉碎目数越大,吸附量越大。在Cd2+离子浓度达到10μg/mL时,此时 40、100、300 目样品的吸附量分别为:115.25、126.55、165.80 μg/g,与对照组的吸附量 55.23 μg/g相比,吸附能力分别提高了108.7%、129.1%及200.2%。这表明,粉碎处理能够增大毛木耳的比表面积,使其暴露更多的吸附基团,显著增强其吸附Cd2+离子的能力。
2.4 毛木耳粉体吸附Pb2+离子能力
毛木耳样品对Pb2+离子的吸附能力见图4。

图4 不同目数毛木耳样品对金属离子Pb2+吸附Fig.4 Adsorpted metal ion Pb2+of Auricularia polytricha samples at different mesh
从图4可以看出,随着溶液中离子Pb2+浓度的增加,四组样品的吸附量同样均呈现增加趋势。且粉碎目数越大,吸附量也越大。在Pb2+离子浓度达到10 μg/mL时,此时40、100、300目样品的吸附量分别为:110.02、144.13、196.08μg/g,与对照组的吸附量85.95μg/g相比,吸附能力分别提高了28.0%、67.7%及128.1%。这同样说明,粉碎处理能够增强毛木耳吸附Pb2+离子的能力。对比样品吸附Cb2+离子的能力,可以发现吸附Pb2+离子能力提高幅度小于吸附Cb2+离子,是由于Pb2+离子溶液的量浓度最小,其包含的离子数量少所致。
3 结论
通过粉碎处理得到不同目数的毛木耳粉体样品,以未粉碎毛木耳样品为对照,发现粉碎处理对毛木耳吸附能力的影响显著。总体趋势为,粉碎目数越大,表面积越大,毛木耳的吸附能力越强。在吸附水分方面,300目毛木耳样品饱和吸水量达到17.12 g/g,与对照组(6.13 g/g)相比,吸附能力提高179.3%;在吸附油脂方面,300目毛木耳样品饱和吸油量为1.06 mL/g,与对照组(0.37 mL/g)相比,吸附油脂能力提高186.5%;在吸附重金属离子方面,在Cd2+离子浓度达到10 μg/mL时,40、100、300 目样品的吸附量分别为 115.25、126.55、165.80 μg/g,与对照组的吸附量 55.23 μg/g 相比,吸附能力分别提高了108.7%、129.1%及200.2%,在Pb2+离子浓度达到 10 μg/mL 时,40、100、300 目样品的吸附量分别为:110.02、144.13、196.08 μg/g,与对照组的吸附量85.95 μg/g相比,吸附能力分别提高了28.0%、67.7%及128.1%。
通过粉碎处理后,粉体粒度越小,表面积越大,毛木耳吸附水、油脂及重金属能力得到提高,提示食用毛木耳时粉体好于子实体,且食用子实体时咀嚼越细,毛木耳清除肠胃积食、纤维、油脂及重金属等功能越强。随着子实体粒度减小,目数增加,提示细胞的破壁率逐渐增加,一系列功效成分也逐渐的释放出来,在食用后更容易被人体吸收,提升了毛木耳自身的营养价值。基于本研究理论基础之上,充分利用毛木耳自身物料的特性,开展毛木耳粉体加工产品的研发,无论对于开发利用毛木耳资源还是益于人体健康发展,都具有重要的现实意义。
[1] 张丹,郑有良.毛木耳的研究进展[J].西南农业学报,2004,17(5):668-673
[2] 张洪玲,吴海琐,王连军.生物吸附重金属的研究进展[J].污染防治技术,2003,16(4):53-56
[3]王翠苹,徐伟昌.生物吸附剂在含重金属的废水处理的研究进展[J].南华大学学报,2002,16(3):46-50
[4] 张丹,高健伟,殷义高,等.毛木耳对铜的生物吸附影响因子研究[J].生态环境,2006,15(2):295-298
[5]KAPPOOR A,VIRARAGHAYAN T.Fungal biosorption―an alternative treatment option for heavy metal bearing wastewaters:a review[J].Bioresource Technology,1995,53(3):195-206
[6] 陈灿,王建龙.重金属离子的生物吸附容量与离子性质之间的关系[J].环境科学,2007,28(8):1732-1737
[7] GALLIE,DII MARIO F,RAPANA P,et al.Copper biosorption by Auricularia polytricha[J].Letter in Applied Microbiology,2003,37(2):133-137
[8] FERRAZ A L,TEIXERIA J A.The use of flocculating brewer’s yeast for Cr(Ⅲ)and Pb(Ⅱ)removal from residual wastewaters[J].Bioprocess Engineering,1999(21):431-437
[9] Kok K H,Karim MIA,Ariff A.Bioremoval of cadmium,leadand zinc using non-living biomass of Aspergillus flavus[J].Pak JBiol Sci,2002,4(7):849-853
[10]刘月英,傅锦坤,陈平,等.巨大芽孢杆菌D01吸附金(Au3+)的研究[J].微生物学报,2000,40(4):425-429
[11]高健伟,张丹,陈红,等.蕈菌菌丝体死粒胞对水溶液中微量铅离子的吸附[J].工业用水与废水,2006,37(4):23-26
[12]林荣根,周俊良,黄朋林.螺旋藻吸附水溶液中铜离子的研究[J].海洋环境科学,1998,17(2):8-11
[13]Gupta S,Kumar D,Gaur J P.Kinetic and isotherm modeling of lead(Ⅱ)sorption onto some waste plant materials[J].ChemEng J,2009,148(2/3):226-233
