在体单向灌流法研究厄贝沙坦的大鼠肠吸收
2014-12-13师云才蒋曙光周建平周湘颖
师云才,蒋曙光,周建平,袁 静,周湘颖
(1.中国药科大学,江苏 南京 211198;2.University of Liverpool,UK)
厄贝沙坦是一种血管紧张素Ⅱ受体的拮抗剂,主要用于治疗轻中度的高血压,其不良反应较少、耐受性较高,疗效好。厄贝沙坦不仅能有效的降低血压[1-3],还有保护患者器官、防止器官损伤的作用[4-7]。本研究参考有关文献[8-11],应用大鼠在体肠灌流模型考察厄贝沙坦在大鼠各肠段的吸收情况,及浓度和溶液pH值对药物吸收的影响,为进一步研究其药代动力学、药效学及厄贝沙坦相关制剂的研发奠定基础。
1 材料与仪器
1.1 药品与试剂 Krebs-Ringer缓冲液(自行配制,1 000 mL 内含有 NaCl 7.80 g、KCl 0.35 g、CaCl20.37 g、NaHCO31.37 g、NaH2PO4·2H2O 0.416 g、MgCl2·6H2O 42.7 mg、葡萄糖 1.40 g),乌拉坦(20%),乐氏生理盐水(自行配制,1 000 mL中有NaCl 9.0 g,NaHCO30.2 g,KCl 0.42 g,CaCl20.24 g),酚红,厄贝沙坦原料药,甲醇,乙腈,其余试剂均为分析纯。
1.2 仪器 依利特P1201型高效液相色谱仪(依利特 P1201二元泵,UV1201紫外-可见检测器,EC2006色谱数据处理工作站),HL-2恒流泵(上海沪西分析仪器厂有限公司),752型紫外可见分光光度计(上海舜宇恒平),恒温水浴锅HH-2(上海特成机械设备有限公司),雷磁PHS-25数显型 pH计(上海精科),ACCULAB型电子天平(北京赛多利斯)。
1.3 实验动物 健康雄性 SD大鼠,(250±20)g,江苏大学scxk(苏)2013-0011。
2 实验方法与结果
2.1 溶液的制备 含酚红的Krebs-Ringer液:精密称量 CaCl20.37 g,葡萄糖 1.4 g,加少量蒸馏水使其完全溶解,再精密称取 NaCl 7.8 g、KCl 0.35 g、NaHCO31.37 g、NaH2PO4·2H2O 0.416 g、MgCl2·6H2O 0.0427 g,加蒸馏水使其完全溶解,加酚红20 mg溶解,稀释后与上述溶液混合并定容至1 000 mL。
药物灌流液:分别精密称取50、100、150 mg厄贝沙坦原料药,含酚红的Krebs-Ringer液溶解并稀释至 1 000 mL,即得 50、100、150 mg·L-1的药物灌流液。
空白肠灌流液:取含酚红的Krebs-Ringer液,按照“2.2”节大鼠在体肠灌流实验方法进行实验,得空白肠灌流液。
2.2 大鼠在体肠灌流实验方法 取体重为(250±20)g的大鼠,禁食12 h,不禁水。腹腔注射20%乌拉坦进行麻醉(1 g·kg-1),将大鼠固定在手术台上,红外灯保温。手术剪沿腹中白线打开腹腔,依次小心的分离出十二指肠、空肠、回肠和结肠。十二指肠为幽门下约2 cm处开始向下数约10 cm;空肠为幽门下约15 cm处,向下数约10 cm;回肠为盲肠上约2 cm处向上数约10 cm;结肠为盲肠后端紧邻盲肠开始向下量取,尽可能多取。分别于肠段两端切口插管,小心缝合结扎,用37°C乐氏生理盐水冲洗,排出肠段内容物,然后泵入空气排去生理盐水。取37°C的供试药液先以1.0 mL·min-1的流速灌流,使药液充满肠段,保持10 min。再以0.2 mL·min-1的速度灌流,平衡30 min后开始接受灌流液,以15 min作为一个时间段,共收集4个时间段的灌流液。实验过程中用浸有生理盐水的脱脂棉覆盖伤口处,并不时滴加生理盐水保湿。移液管精密移取0.5 mL接受液,检测酚红浓度,剩余的接受液用0.45 μm滤膜过滤,取续滤液,进样检测药物浓度。
2.3 厄贝沙坦的含量测定
2.3.1 色谱条件 色谱柱:Hedera ODS-2色谱柱(5 μm,4.6 mm ×150 mm),流动相:pH 3.2 磷酸盐缓冲液—乙腈(55∶45),流速 1.0 mL·min-1,进样量25 μL,检测波长245 nm,柱温30℃。
2.3.2 方法专属性考察 分别取空白肠灌流液、厄贝沙坦标准溶液,含药灌流液分别进样测定,考察方法专属性。色谱图见图1,由图1可知,空白灌流液对药物的测定没有干扰。
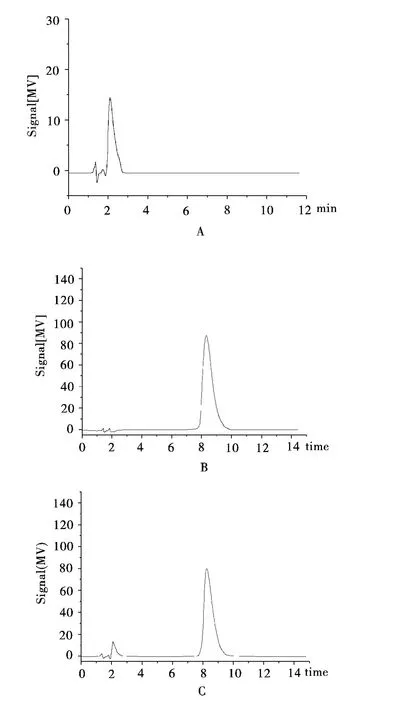
图1 高效液相色谱图
2.3.3 药物标准曲线的制备 分别精密配制浓度分别为 20、40、60、80、100、120、140 mg·L-1的厄贝沙坦K-R溶液,0.45 μm滤膜过滤,取续滤液进样25 μL,得峰面积。以药物浓度C对峰面积A进行线性回归,得药物标准曲线:Y=38.324X -124.86,R2=0.998(n=7),线性范围为 20 ~140 mg·L-1,最低定量 10 mg·L-1。
分别精确配制 40、80、120 mg·L-1的药物 K-R溶液,考察标曲回收率及精密度(n=5)。结果回收率均在98.5%到101%之间,日内RSD和日间RSD均在4%以内,说明本方法回收率较高,精密度较好。
2.3.4 药物在K-R溶液及空白肠灌流液中的稳定性 分别用K-R液和空白肠灌流液配制50、100、150 mg·L-1的厄贝沙坦原料药溶液,37℃水浴中放置,分别于0、2、4 h取样,检测药物含量。结果3个药物浓度的溶液在各时间点测得的峰面积基本相同,RSD均在3%以内,表明厄贝沙坦在K-R液及空白肠灌流液中较为稳定。
2.4 酚红标准曲线的制备 分别精密配制浓度为5、10、15、20、30、40、60 mg·L-1的酚红 K-R 溶液,各精密移取1 mL置于10 mL容量瓶,加NaOH溶液(1 mol·L-1)2 mL,K-R 液稀释至刻度,摇匀后在558 nm可见光下测定各浓度溶液的吸光度,以酚红浓度C对溶液吸光度A线性回归,得酚红标准曲线:Y=0.0151X+0.0436,R2=0.999 8(n=8),线性范围为5 ~60 mg·L-1。
分别精确配制10、10、60 mg·L-1的酚红 K-R 溶液,考察标曲回收率及精密度(n=5)。结果回收率均在98%到100.5%之间,日内RSD和日间RSD均在5%以内,说明本方法回收率较高,精密度较好。
2.5 数据处理方法 酚红法校正灌流液体积变化,校正公式为:
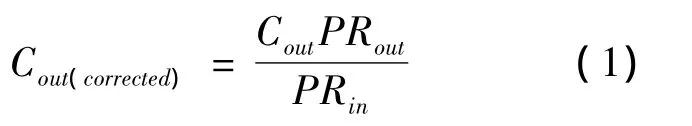
Cout(corrected)为流出液校正后的药物浓度,Cout为实际测得的药物浓度,PRout为流出液中酚红的浓度,PRin为灌流液入口处酚红的浓度。
药物有效渗透系数(Peff)和吸收速率常数(Ka)分别用公式(2)、(3)计算得到:
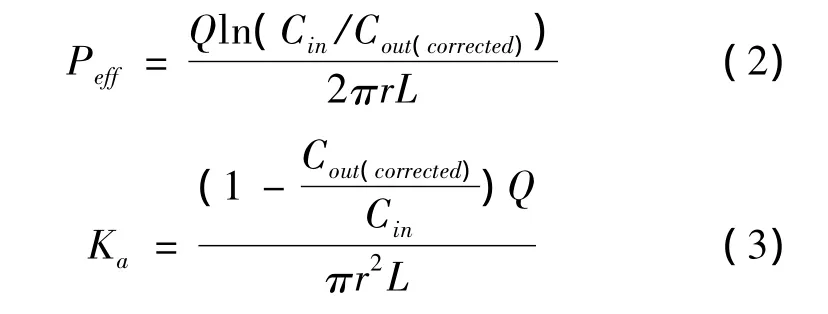
Cin为灌流液入口处药物浓度,Q为灌流液流速,本实验为 0.02 mL·min-1,r为在体实验肠段的肠道半径,L为在体实验肠段的长度。
经公式(1)、(2)和(3)计算得到不同浓度、不同pH值以及不同肠段Ka和Peff,使用SPSS19.0软件LSD检验法进行单因素方差分析,以P<0.05时认为差异有统计学意义。
2.6 厄贝沙坦肠吸收影响因素的考察
2.6.1 肠段及浓度对厄贝沙坦肠吸收的影响 取50、100、150 mg·L-1的药物灌流液,按照“2.2”节的试验方法对大鼠的十二指肠、空肠、回肠和结肠同时进行单肠灌流实验,按照“2.4”节数据处理方法对测定的数据进行处理,结果见表1和图2,结果显示厄贝沙坦在各肠段吸收较好,为全肠道吸收药物。

表1 不同浓度的厄贝沙坦溶液在不同肠段的吸收速率常数
经方差分析,当灌流液中药物浓度为50、100 mg·L-1时,十二指肠的吸收速率常数Ka与空肠、回肠以及结肠的Ka差异有显著性,空肠、回肠和结肠之间的Ka差异无显著性;当灌流液中药物浓度为150 mg·L-1时四肠段的Ka均差异无显著性。十二指肠50 和 100 mg·L-1的 Ka都与 150 mg·L-1的 Ka差异有显著性,空肠、回肠和结肠三个浓度间均差异无显著性。方差分析结果显示厄贝沙坦在空肠、回肠和结肠的吸收以被动扩散为主,而在十二指肠中的吸收是以被动扩散和主动转运相结合的方式进行。

图2 不同浓度的厄贝沙坦溶液在不同肠段的有效渗透系数
2.6.2 灌流液pH值对药物吸收的影响 按照本节“2.1”药物灌流液配制方法制备 100 mg·L-1的厄贝沙坦肠灌流液,用NaOH、HCl分别调节pH值,得 pH 值分别为6.0、6.8、7.4 的药物灌流液,分别按照“2.2”大鼠在体单向肠灌流的实验方法进行实验,考察不同pH值的灌流液中药物的吸收情况。结果见表2和图3,经方差分析,各肠段中,不同pH值灌流液之间的Ka和Peff差异无显著性,表明灌流液pH值对药物的吸收没有影响。

表2 不同pH值灌流液的药物吸收速率常数

图3 不同pH值灌流液的药物有效渗透系数
3 讨论
本研究采用在体单向肠灌流法考察药物厄贝沙坦在大鼠十二指肠、空肠、回肠和结肠四个肠段的吸收速率常数Ka和有效渗透系数Peff,以及浓度和pH值对药物吸收的影响,在体单向肠灌流法与离体法相比能够更加真实地反映出药物在大鼠肠道的吸收情况,与循环肠灌流法相比,其吸收速率稳定,实验对大鼠肠壁造成损伤较小,与人体相关性较好。本研究的结果显示厄贝沙坦为全肠道吸收的药物,且以十二指肠为主要吸收肠段,肠道pH对药物的吸收没有影响。
考虑到厄贝沙坦为生物药剂学分类系统Ⅱ类药物[12],本研究也证明了厄贝沙坦在肠道有较好的吸收,因此在制备厄贝沙坦药物制剂时,可以通过提高厄贝沙坦的溶解度来提高药物的生物利用度,增强药物的治疗效果。
[1] 吕留强,赵 立,李晓波,等.厄贝沙坦氢氯噻嗪对原发性高血压伴早期肾损害尿微量白蛋白和N-乙酰-β-D-氨基葡萄糖苷酶的影响[J].实用心脑肺血管病杂志,2012,20(1):34 -36.
[2] 卢金萍,陈 玲,李 夏,等.厄贝沙坦在老年肥胖高血压患者中的疗效[J].临床心血管病杂志,2012,27(11):841 -843.
[3] 潘宏华,边平达.厄贝沙坦联合氨氯地平或氢氯噻嗪在老年高血压患者中的疗效[J].中国临床药理学杂志,2013,29(4):246-248.
[4] Substudy TM.Irbesartan in patients with atrial fibrillation[J].N Engl J Med,2011,364(10):928 -938.
[5] Ros-Ruiz S,Aranda-Lara P,Fernández JC,et al.High doses of irbesartan offer long-term kidney protection in cases of established diabetic nephropathy[J].Nefrologia,2012,32(2):132.
[6] 王 用,邢玉龙.胺碘酮联合厄贝沙坦治疗阵发性房颤疗效观察[J].安徽医药,2013,17(3):492 -493.
[7] Hadi NR,Alamran FG,Mohammad BI,et al.Irbesartan Ameliorates Myocardial Ischaemia/Reperfusion Injury in Rats Via Down Regulation of Apoptosis and the Inflammatory Pathways[J].Journal of the American College of Cardiology,2013,62(18):C58 - C59.
[8] 沈 杰,杜望春,宋钟娟.替米沙坦的大鼠肠吸收特性及联用药物对其吸收的影响[J].中国医院药学杂志,2012,32(22):1805-1808.
[9] 王亚男,甄毅岚,李晓亮,等.牡荆素与牡荆素鼠李糖苷大鼠在体肠吸收对比研究[J].安徽医药,2013,17(10):1660 -1663.
[10] Luo Z,Liu Y,Zhao B,et al.Ex vivo and in situ approaches used to study intestinal absorption[J].Journal of pharmacological and toxicological methods,2013,68(2):208 -216.
[11] 彭俊杰,蔺聪聪,李 江,等.氟比洛芬的大鼠在体肠吸收动力学研究[J].药学学报,2013,48(3):423 -427.
[12] Ganapuram BR,Alle M,Dadigala R,et al.Development,evaluation and characterization of surface solid dispersion for solubility and dispersion enhancement of irbesartan[J].Journal of Pharmacy Research,2013,7(6):472 -477.
