民族药岩白菜的化学成分研究*
2014-12-01石晓丽毛泽伟左爱学饶高雄
石晓丽,毛泽伟,左爱学,饶高雄
(云南中医学院药学院,云南昆明 650500)
岩白菜为虎耳草科岩白菜属多年生草本植物,主要分布云南、四川、西藏等地,具有抗菌、消炎、化痰止咳等功效,中医临床广泛用于治疗腹泻、痢疾、食欲不振、肺结核咳嗽、气管炎咳嗽、风湿疼痛等[1-2]。文献报道[3],岩白菜主要含香豆素、黄酮等成分。从岩白菜中已经发现了一些具有显著生物活性的物质,如岩白菜素(Bergenin)具有镇咳化痰作用[4],熊果苷(Arbutin)具有抗菌消炎作用[5]等。为了进一步探索岩白菜的化学成分,比较不同产地岩白菜药材化学成分的异同,我们对产自云南大理岩白菜的化学成分进行了研究。
1 实验仪器与材料
YANACO显微熔点仪测定;Bio-Rad FTS-135红外光谱仪,KBr压片;岛津UV-2450紫外光谱仪;Bruker AM-400核磁共振波谱仪,TMS为内标。柱色谱硅胶及薄层色谱硅胶板均为青岛海洋化工厂生产,葡聚糖凝胶LH-20为Pharmacia公司生产;乙醇、丙酮、环己烷等试剂用工业或化学纯溶剂;薄层色谱显色剂用10%硫酸乙醇溶液或5%磷钼酸乙醇溶液。
岩白菜药材于2010年采自云南大理,植物标本经中国科学院昆明植物研究所标本馆鉴定为虎耳草科岩白菜属岩白菜(Bergenia pururascens(Hook.f.et Thoms.)Engl.)。
2 提取与分离
岩白菜块根1.5kg,粉碎过60目筛网,以95%乙醇回流提取3次,每次加5L溶剂,回流2h,合并提取液,减压回收乙醇得浸膏500g。乙醇浸膏加1L水分散,依次用环己烷、乙酸乙酯和正丁醇萃取,分别得到环己烷部分(Fr-A,10g)、乙酸乙酯部分(Fr-B,143g)和正丁醇部分(Fr-C,123g)。
Fr-A部分以20g硅胶拌样后用200g硅胶柱层析,用环己烷-乙酸乙酯溶剂系统梯度洗脱(10:0~10:10),主要斑点流份再经多次硅胶柱色谱分离纯化,得到化合物 2(500mg)。
Fr-B部分有结晶析出,重结晶后,得到化合物1(29g);残留滤液 114g用硅胶柱色谱,用氯仿-甲醇溶剂系统梯度洗脱(50:1~10:1),洗脱液经薄层色谱检查后合并成8个流份,再经多次硅胶柱色谱分离,氯仿-丙酮(80:10~60:40)洗脱,并辅以十八烷基键合相RP-18[以甲醇-水溶剂系统梯度洗脱]分离,最后用LH-20纯化,甲醇洗脱得到化合物3(3.78g)、4(43mg)、7(69mg)、8(369mg)、9(2.08g)。
Fr-C部分用MCI树脂柱色谱分段,用水-甲醇溶剂系统梯度洗脱,水洗脱去糖和水溶性色素,含醇溶剂部分经薄层色谱检查后合并成2个流份,各流份再经多次硅胶柱色谱分离,氯仿-甲醇(80:10~70:30)洗脱,并辅以十八烷基键合相RP-18多次分离,以甲醇-水溶剂系统梯度洗脱,最后用LH-20纯化,甲醇洗脱得到化合物 1 (5.1g)、3(2.69g)、5(534mg)、6(632mg)。
3 研究结果
从大理产岩白菜药材中分离得到9个单体化合物,通过理化性质和光谱测试,分别鉴定岩白菜素(Bergenin,1)、齐墩果酸(Oleanic acid,2)、熊果苷(Arbutin,3)、阿夫儿茶精(Afzelechin,4)、11-O-没食子酰岩白菜素(11-O-galloyl bergenin,5)、没食子酸(Gallic acid,6)、Breynioside A(7)、Diethyl disulfoxide(8)、(+)-儿茶素((+)-Catechin,9)。
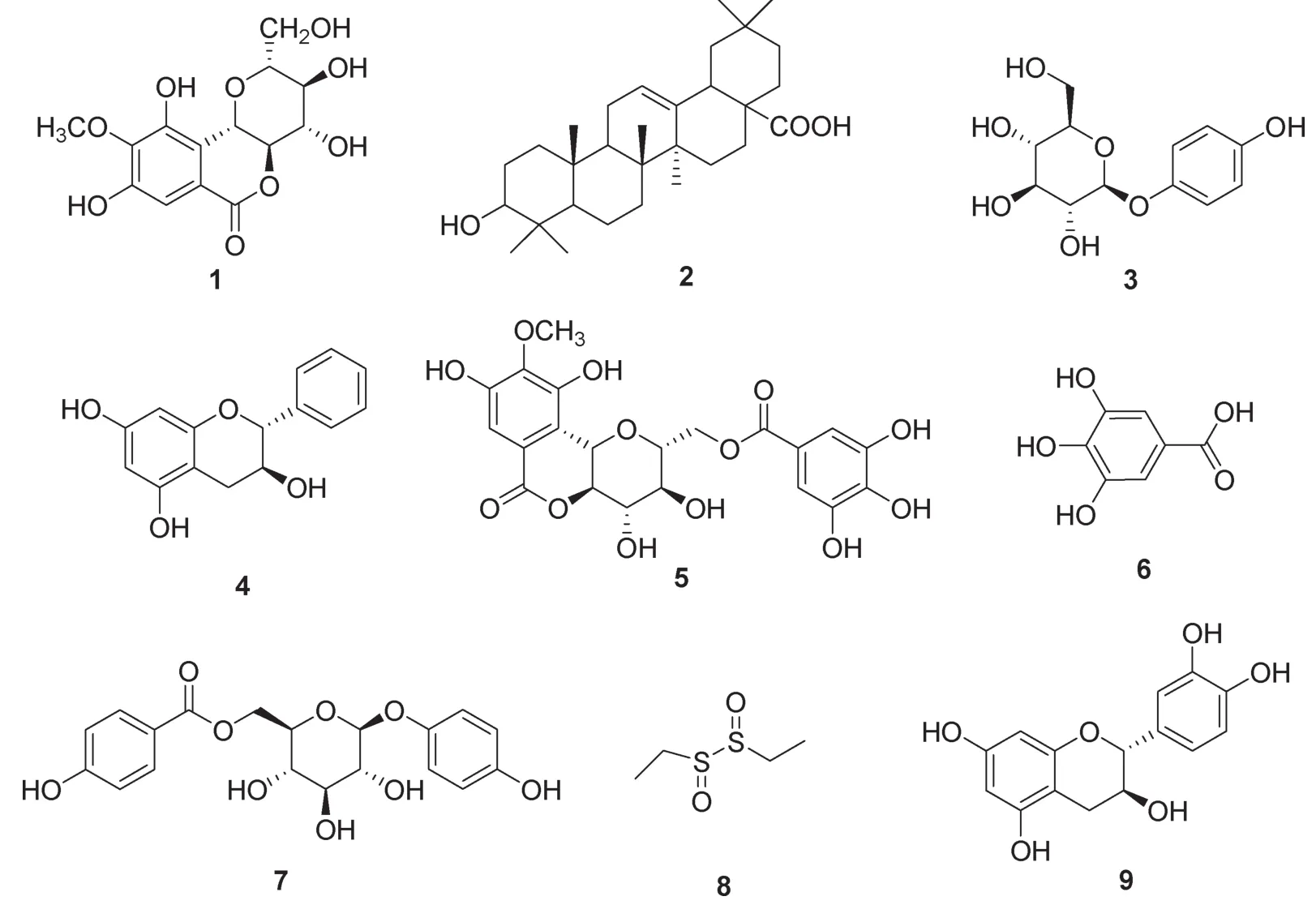
结构鉴定
化合物 1:白色粉末;mp.133.0~133.4℃;IR(KBr)cm-1:3392 cm-1,3246 cm-1,1703 cm-1,1610 cm-1,1462 cm-1,1338 cm-1,1087 cm-1;1H-NMR(500 MHz,DMSO)δ:3.17(1H,m,H-2),3.19(1H,m,H-3),3.63 (1H,m,H-3),4.00(1H,t,J=9.9 Hz,H-4a),7.08(1H,s,H-7),4.94(1H,d,J=10.5 Hz,H-10b),3.80(1H,d,J=11.4 Hz,H-11),3.54(1H,t,J=10.0 Hz,H-11),5.43 (1H,d,J=4.3 Hz,3-OH),5.64(1H,d,J=4.5 Hz,4-OH),3.63 (3H,s,9-OCH3),9.78(1H,s,8-OH),8.43(1H,s,10-OH),4.96(1H,d,J=10.5 Hz,11-OH);13C-NMR(125 MHz,DMSO)δ:82.5(d,C-1),71.5(d,C-2),74.5(d,C-3),80.5(d,C-4),164.2(s,C-5),118.9(s,C-6),110.2(d,C-6a),151.7(s,C-7),141.3(s,C-8),148.8(s,C-9),116.8(s,C-10),72.9(d,C-10a),61.8(t,C-10b),60.6(q,C-9-OCH3)。其 1H-NMR 和 13C-NMR数据与文献[6]报道的基本一致,鉴定为岩白菜素(Bergenin)。
化合物2:白色针状(丙酮);紫色斑点(10%硫酸乙醇),mp.285~288℃;与齐墩果酸标准品对照,在TLC中Rf值和显色行为一致,且混合熔点不下降,确定为齐墩果酸(Oleanic acid)。
化合物 3:白色粉末;mp.161.5~162 ℃;IR(KBr)cm-1:3329 cm-1,1647 cm-1,1512 cm-1,1450 cm-1,827 cm-1,1217 cm-1;1H-NMR (500 MHz,CD3OD)δ:6.96(1H,d,J=10.0 HZ,H-2),6.69(1H,d,J=10.0 HZ,H-3),6.69(1H,d,J=10.0 HZ,H-5),6.96(1H,d,J=10.0 HZ,H-6),4.73 (1H,d,J=7.2 HZ,H-1′),3.38(1H,m,H-2′),3.42(1H,m,H-3′),3.38(1H,m,H-4′),3.42(1H,m,H-5′),3.44(1H,dd,J=11.9,3.9 HZ,H-6′),3.8(1H,d,J=11.9 HZ,H-6′);13C-NMR(125 MHz,CD3OD)δ:153.8(s,C-1),119.3(d,C-2),116.6(d,C-3),152.4(s,C-4),116.6(d,C-5),119.3(d,C-6),103.6(d,C-1′),74.9(d,C-2′),78(d,C-3′),71.4(d,C-4′),77.9(d,C-5′),62.3(t,C-6′)。其1H-NMR和13C-NMR数据[7]与文献报道基本一致,鉴定为熊果苷(Arbutin)。
化合物 4:白色粉末;mp.190.0~190.5℃;IR(KBr)cm-1:3379 cm-1,1618 cm-1,1512 cm-1,1460 cm-1,1138 cm-1,1032 cm-1,1082 cm-1;1H-NMR(500 MHz,CD3OD):δH 4.60 (1H,d,J=7.85 Hz,H-2),4.00(1H,m,H-3),2.90(1H,dd,J=16.1,5.5 Hz,H-4),2.52(1H,dd,J=16.1,8.5 HZ,H-4),5.84(1H,d,J=2.3 Hz,H-6),5.93 (1H,d,J=2.3 Hz,H-8),7.22(1H,d,J=10.5 Hz,H-2),6.80(1H,d,J=10.5 Hz,H-3′),6.80(1H,d,J=10.5 Hz,H-5′),7.22(1H,d,J=10.5 Hz,H-6′);13C-NMR(125 MHz,CD3OD)δ:82.9(d,C-2),68.8(d,C-3),28.9(t,C-4),157(s,C-5),96.3(d,C-6),157.6(s,C-7),96.4(d,C-8),157.9(s,C-9),100.9(s,C-10),131.5(s,C-1′),129.6(d,C-2′),116(d,C-3′),158.4(s,C-4′),116(d,C-5′),129.6(d,C-6′)。其1H-NMR和13C-NMR数据与文献[8]报道基本一致,鉴定为阿夫儿茶精(Afzelechin)。
化合物 5:白色粉末;mp.217.0~218.0℃;IR(KBr)cm-1:3412 cm-1,1699 cm-1,1616 cm-1,1458 cm-1;1H-NMR(500 MHz,CD3OD)δ:3.94(1H,m,H-2),3.54(1H,t,J=8.9 Hz,H-3),3.84(1H,t,J=8.9 Hz,H-4),4.12(1H,t,J=10.2 Hz,H-4a),7.08(1H,s,H-7),5.03(1H,d,J=10.4 Hz,H-10b),4.82(1H,d,J=12.3,2.0 Hz,H-11),4.40 (1H,m,H-11),3.88(3H,s,H-9-OCH3),7.10(1H,s,H-2′),7.10(1H,s,H-6′);13C-NMR(125 MHz,CD3OD)δ:80.7(d,C-2),71.8(d,C-3),75.4(d,C-4),81.3(d,C-4a),165.7(s,C-6),119.4(s,C-6a),110.2(d,C-7),152.4(s,C-8),142.2(s,C-9),149.3(s,C-10),117(s,C-10a),74.4(d,C-10b),64.6(t,C-11),61(q,C-9-OCH3),121(s,C-1′),110.2(d,C-2′),146.5(s,C-3′),140(s,C-4′),146.5(s,C-5′),110.2(d,C-6′),168.1(s,C-7′)。其1H-NMR和13C-NMR数据与文献[9]报道的基本一致,鉴定为11-O-没食子酰岩白菜(11-O-dalloyl Bergenin)。
化合物 6:白色粉末;mp.236.2~237.0℃;IR(KBr)cm-1:3462 cm-1,1654 cm-1,1263 cm-1,1612 cm-1,1444 cm-1;1H-NMR (500 MHz,CD3OD)δ:7.05(1H,s,H-2),7.05(1H,s,H-6);13C-NMR(125 MHz,CD3OD)δ:121.9(s,C-1),110.3(d,C-2),146.4(s,C-3),139.6(s,C-4),146.4(s,C-5),110.3(d,C-6),170.4(s,1-COOH)。其1H-NMR和13C-NMR数据与文献[10]报道基本一致,鉴定为没食子酸(Gallic acid)。
化合物 7:白色粉末;mp.228.8~229.6℃;IR(KBr)cm-1:3406 cm-1,1699 cm-1,1606 cm-1,1510 cm-1,1070 cm-1;1H-NMR (500 MHz,CD3OD)δ:6.94(1H,d,J=10.0 Hz,H-2)、6.61(1H,d,J=10.0 Hz,H-3),6.61(1H,d,J=10.0 Hz,H-5),6.94(1H,d,J=10.0 Hz,H-6),4.72 (1H,d,J=7.4 Hz,H-1′),3.48-3.41(3H,m,H-2′),3.48-3.41(3H,m,H-3′),3.48-3.41(3H,m,H-4′),3.75(1H,ddd,J=10.0 Hz,7.5,2.0 Hz,H-5′),4.36(1H,dd,J=11.8,2.1 Hz,H-6′),4.67(1H,dd,J=11.8,2.1 Hz,H-6′),7.89(1H,d,J=10.5 Hz,H-2′′),6.94(1H,d,J=10.0 Hz,H-3′′),6.94(1H,d,J=10.0 Hz,H-5′′),7.89(1H,d,J=10.5 Hz,H-6′′);13C-NMR (125 MHz,CD3OD)δ:152.2(s,C-1),119.5(d,C-2),116.5(d,C-3),153.9(d,C-4),116.5(d,C-5),119.5(d,C-6),103.6(d,C-1′),74.9(d,C-2′),77.9(d,C-3′),72(d,C-4′),75.5(d,C-5′),65(t,C-6′),122.1(s,C-1′′),132.9(d,C-2′′),116.2(d,C-3′′),163.6(s,C-4′′),116.2(d,C-5′′),132.9(d,C-6′′),167.9(s,C-7′′)。其1H-NMR和13C-NMR数据与文献[11]报道基本一致,鉴定为Breynioside A。
化合物8:无色针状结晶;mp.136.2~136.8℃;IR(KBr)cm-1:2935 cm-1,2748 cm-1,2677 cm-1,2490 cm-1,1473 cm-1,1035 cm-1;1H-NMR (500 MHz,CD3OD)δ:1.32 (3H,t,J=7.0 Hz,H-1),3.22(3H,dd,J=7.3,14.5 Hz,H-2),3.22(3H,dd,J=7.3,14.5 Hz,H-5),1.32(3H,t,J=7.0 Hz,H-6);13C-NMR(125 MHz,CD3OD)δ:9.2(q,C-1),47.8(t,C-2),47.8(t,C-3),9.2(q,C-4)。其1H-NMR 和13C-NMR 数据与文献[12]报道基本一致,鉴定为Diethyl disulfoxide。
化合物 9:白色粉末;mp.150.6~151.0℃;IR(KBr)cm-1:3390 cm-1,1618 cm-1,1519cm-1,1460 cm-1,1145 cm-1,1107 cm-1,1030 cm-1;1H-NMR(500 MHz,CD3OD)δ:4.56 (1H,d,J=7.5 Hz,H-2),3.96(1H,m,H-3),2.85 (1H,dd,J=16.1,5.5 Hz,H-4),2.51(1H,dd,J=16.1,8.2 Hz,H-4),5.85(1H,d,J=2.3 Hz,H-6),5.92(1H,d,J=2.3 Hz,H-8),6.83(1H,d,J=2.5 Hz,H-2′),6.75(1H,d,J=10.0 Hz,H-5′),6.70(1H,dd,J=10.0,2.0 Hz,H-6′);C-NMR(125 MHz,CD3OD)δ:82.8(d,C-2),68.8(d,C-3),28.5(t,C-4),100.8(s,C-4a),157.6(s,C-5),96.2(d,C-6),156.9(s,C-7),95.5(d,C-8),157.8(s,C-9),132.2(s,C-1′),116.1(d,C-2′),146.2(s,C-3′),146.2(s,C-4′),115.2(d,C-5′),120(d,C-6′)。其1H-NMR 和13C-NMR数据与文献[13]报道基本一致,鉴定为(+)-儿茶素((+)-Catechin)。
4 结果与讨论
从云南大理产岩白菜药材中分离得到9个成分,分别鉴定为岩白菜素(1)、齐墩果酸(2)、熊果苷(3)、阿夫儿茶精(4)、11-O-没食子酰岩白菜素(5)、没食子酸(6)、Breynioside A(7)、Diethyl disulfoxide(8)、(+)-儿茶素(9)。其中,化合物 4、7、8是首次从该种植物中分离得到,化合物8为首次从该属植物中分离得到。研究结果丰富了我们对于岩白菜药材物质基础认识,也为从内在物质基础的角度评价岩白菜药材质量控制指标提供了分析比较的线索和依据。
值得注意的是化合物8是含硫化合物,此类成分在自然界分布极少,以前只在木棉科的著名热带水果榴莲(Durio zibethinus Murr.)中分离得到过[14]。此外,一系列和岩白菜素结构类似的化合物的发现,为进一步筛选和寻找抗支气管炎的天然活性成分具有一定的意义。
[1]南京中医药大学.中药大辞典[M].上海:上海科学技术出版社,2006:1986-1987.
[2]中华人民共和国卫生部药典委员会.中华人民共和国药典2010版(第一增补本)[M].北京:中国医药科技出版社,2012:4.
[3]王碧霞,赵欢,黎云祥.岩白菜属植物研究的新进展[J].光谱实验室,2012,29(1):367-370.
[4]董成梅,杨丽川,邹澄,等.岩白菜素的研究进展[J].昆明医学院学报,2012(1):150-154.
[5]王 佩,赖瑛,吴锡铭.熊果苷抗炎作用的研究[J].中华中医药学刊,2008,26(9):1933-1935.
[6]尉耀元.秦岭岩白菜的化学成分研究[J].中国实验方剂学杂志,2012,18(9):154-156.
[7]黄开毅,何乐,王大成,等.西藏胡黄连的化学成分研究[J].中国药学杂志,2008,43(18):1382-1385.
[8]陶华明,朱全红,刘永红,等.草麻黄根的黄酮类成分研究[J].中草药,2011,42(9):1678-1682.
[9]池翠云,王 峰,雷 婷,等.瑶药四方藤成分研究[J].中药材,2010,33(10):1566-1568.
[10]崔莹.盘龙七化学成分研究(Ⅱ)[J].中草药,2012,43(9):1704-1707.
[11]H.Morikawa,R.Kasai,H.Otsuka,et al.Terpenic and phenolic glycosides from leaves of Breynia officinalis hemsl[J].Chem.Pharm.Bull.,2004,52(9):1086.
[12]C.Pouchert.The Aldrich Library of 13C and 1H FT-NMR Spectra[M].Wiley,1993.
[13]张思巨,王怡微,刘 丽,等.锁阳化学成分研究[J].中国药学杂志,2012,42(13):975-977.
[14]R.Nf,A.Velluz.Sulphur Compounds and some Uncommon Esters in Durian(Durio zibethinus Murr.)[J].Flavour and fragrance journal,1996,11(5):295-303.
