美国移植协会《实体器官移植感染疾病诊疗指南》2013年第3版介绍(续二)实体器官移植中供体来源的感染
2014-11-23隋明星
手术技术、免疫抑制药物和预防性抗菌药物的发展已明显减少了器官移植后的发病率和病死率。因此,目前移植被认为是终末期器官衰竭患者的最佳治疗方案。尽管取得了这些进展,突发性供者来源感染仍然是移植后的一种罕见并发症。一旦发生,其病死率往往较高。本章节主要讨论供者来源感染疾病的流行病学特点、降低风险的策略和筛查方法。
1 定 义
大多数供者来源疾病的传播都是可预测的,包括巨细胞病毒(CMV)和乙型肝炎病毒(HBV)在内的疾病,都可以预测其发生;如果知道了供者的病原体,并且通过病毒监测提前治疗或预防,可以最大程度减少疾病的传播。而无法预测的疾病传播,如锥虫病、人类免疫缺陷病毒(HIV)、丙型肝炎病毒(HCV)、淋巴细胞性脉络丛脑膜炎病毒(LCVM)、结核分枝杆菌、多药耐药(MDR)细菌,狂犬病毒和西尼罗河病毒(WNV),目前常规的筛查方法很难发现这些病原体,在供者捐献时也不能明确其是否存在。在一些疾病传播的病例中,供者在死亡时其临床疾病尚未明确。有时虽经过筛查,但并未针对相关病原体。尽管大部分疾病传播与尸体供者器官捐献有关,最近发生的HIV和HCV感染说明活体移植的受者也可能有感染风险。
目前,对于供者来源的感染性疾病的定义(表1)国际上已达成了共识。
2 流行病学
目前有几个系统可以评估供者来源感染性疾病传播的流行病学特征,如法国的Agence de la Biome'decine、美国器官获取和移植网络(OPTN)下的疾病传播咨询委员会、意大利DRIN系统、西班牙的跟踪疾病传播研究设施(RESITRA)。
尽管可能发生漏诊和漏报,仍可以得出以下结论:来源于供者的感染性疾病发病率约占尸体供者器官移植的0.2%;值得注意的是,RESITRA的数据稍高(1.7%)。发生感染传播时一般伴有明显的发病率和病死率;在病情不严重的情况下,可能发生漏诊和漏报。此外感染传播发病率的差异可能与疫苗接种、移植器官类型和免疫抑制剂有关。
3 减少风险
虽然不可能完全消除实体器官移植中疾病传播的风险,但仍有一些减少风险的方法可供使用。基本上这些方法可以分为以下几类:① 对供者的医疗、社会史的危险分层;② 对供者和供者器官进行全面的临床评价;③ 实验室筛选感染的供者。

表1 供体来源的感染性疾病的定义
3.1 供者风险评估
通过全面回顾供者的医疗史和社会史对其进行危险分层,并通过培养和其他检测方法对供者情况进行详细筛查,如血清学和核酸检验〔NAT,有时也被称为多重聚合酶链反应(PCR)或病毒负荷试验〕。阳性结果的判断要依赖于疾病传播的风险与受者对风险耐受,以及受者的医疗状况间的匹配情况。然而,一些培养或者检测结果要在器官移植之后才能知晓(如分枝杆菌培养常需要8周),器官获取和移植中心应该据此做出相应的信息记录和受者治疗计划。此外,由熟悉供者的人提供供者社会史。注意供者旅行史,尤其是地方性感染风险(如组织胞浆菌、芽生菌、球孢子菌、南美锥虫、线虫和肺结核等)。如果有明确的地方性感染暴露,需要采取额外的供者筛查手段或者受者预防措施。美国组织库协会目前制定了统一的供者健康问卷,以期规范地从亲友中获得医疗史和社会史。需要认识到,信息提供人员不可能知道所有供者的危险因素,故需要评估他们的了解程度。回顾性分析供者医疗史,搜集其社会史可用于确定受者感染HIV、HBV和HCV的风险(表2)。应该告知接收髙危供者器官的受者上述风险以及其他选择,在移植后检查有无这些感染。血清和(或)核酸检测后,与特定行为相关的残留感染风险见表3。
目前,有两种方法对器官供者风险分层:在美国,供者被分为髙风险或不确定的感染性疾病传播风险;而欧洲的分层梯度更多。美国的系统主要关注HIV、HBV、HCV、行为危险因素(见表2)、血液稀释和供者社会史不充分,并据此判定血行传播疾病高风险,其他受者则不会进一步分类。2002年,意大利国家移植中心(CNT)最早提出了器官移植供者感染传播风险分层,被欧洲广泛应用以评价供者的安全性和可接受性。CNT/欧洲风险分类系统的规定如下:① 不可接受的风险因素包括绝对禁忌证,除非是用于个别的没有其他治疗措施来挽救生命的移植手术;② 增高但可接受的风险包括供者的评估过程中发现感染性病原体,但是受者的健康状况和临床病情严重程度需要移植;③ 中等风险(指择期移植的标准)包括以下情况:即使存在感染性疾病,允许移植给患同种疾病或有血清学保护的受者;患菌血症和(或)细菌性脑膜炎的供者经过至少24~48小时的针对性抗菌药物治疗后也可以使用;④ 不可评估的风险包括评估过程无法对感染性疾病的风险进行适当地评估;⑤ 标准风险指评估过程中未发现感染性疾病。

表2 供者可增加传播HIV、HBV和HCV风险的行为
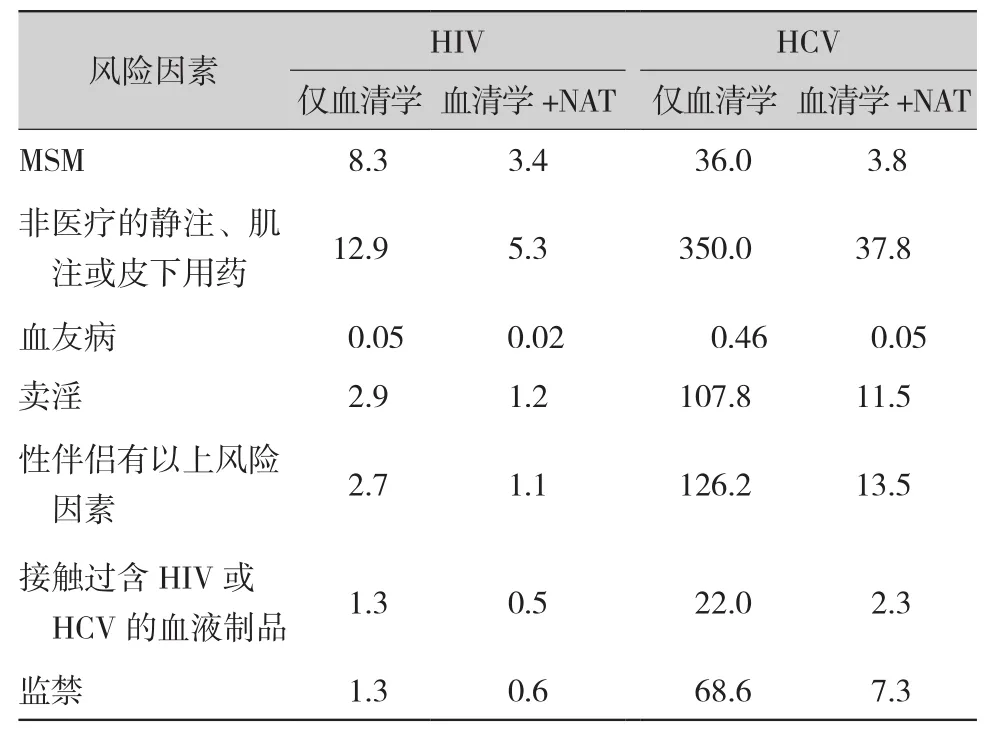
表3 每10 000个高风险供者中未诊断HIV和HCV的剩余风险因素
这两个系统均建议,如果供者中有明确的风险,那受者要签署特定的知情同意书。
3.2 体格检査
器官获取团队和手术医师均应对供者进行全面体格检査,同时评价器官和血管。体检应着重查看感染体征,包括脓肿、溃疡、生殖器或肛门外伤和淋巴结肿大等,除此之外还要明确最近是否有吸毒情况。体检也应该评估其他潜在疾病的体征,如肝硬化或其他感染或恶性肿瘤的表现。移植外科医师应该确保没有肠内容物溢出、没有明显的脓液或感染的器官或血管,包括淋巴结肿大。
3.3 供者血清学和核酸检测
病毒感染后,在血液中最先检测到的是病毒而不是针对该病毒的抗体,这叫血清学窗口。患者产生针对感染病毒的抗体后,才能通过血清学试验检测到感染。由于存在窗口期,仅使用血清学检测会导致一些供者感染被漏诊。HIV的窗口期为22天左右,但有时长达6个月。因此,供者在潜伏期内的血清学检测可能是阴性。使用核酸检测可以将HIV的窗口期减少到5.6~10.2天〔如NAT检测时间为4~15天,而非酶联免疫吸附试验(ELISA)方法〕 。美国最近在开展一种第4代HIV抗体-抗原结合-血清诊断试验,可能将窗口期减少到1~2周;值得注意的是,这项检测未被批准用于筛选供者,而其在尸体供者中的有效性数据很有限。最新的数据显示,血清学筛查潜在供者HIV的漏诊率约为1/50 000,而筛査高风险供者的漏诊率为1/11 000。乙型肝炎表面抗原(HBsAg)ELISA检测的窗口期为38.3~49.7天,NAT的窗口期为20.4~25.7天。HBV的NAT测试可以检测HBsAg阴性、HBcAg阳性的患者是否有病毒复制。HCV的ELISA试剂盒的窗口期为38.0~94.0天,通过NAT的窗口期为6.1~8.7天。最新数据显示,血清学筛査潜在供者HCV的漏诊率约为1/5 000,而筛查高风险供者的漏诊率为1/1 000。第4代HCV抗体筛査试剂在美国以外地区可以使用,但在美国尚未批准使用;与现有的方法相比,其窗口期更短。
这些数据表明,NAT可以用来检测常规血清学筛查漏诊的感染,然而许多专家建议只在OPTN分级为髙风险的人群中使用NAT,因为考虑到假阳性结果会使未受感染的器官被丢弃。最近有报道称成功移植了NAT确诊或可疑阳性结果的供者器官。此外,有报道称有很大部分的供者器官HIV、HBV和HCV血清学检测阳性但NAT阴性。这样的供体器官可以在特定的移植受者或完全知情同意的受者中使用(如感染过HBV或接种过疫苗的受者)。应当指出的是,目前美国法律不允许使用HIV感染的器官。如果有明确的证据表明结果可能是假阳性(即血清学阳性但NAT阴性,没有HIV感染的危险因素),可以考虑使用这些器官,只要患者及移植中心完全了解这些测试结果。
最近国际上开始关注筛査供者的其他感染性疾病如肺结核、南美锥虫病和WNV感染。筛查供者结核感染非常有挑战性,相关支持数据也很有限。目前结核菌素纯蛋白衍生物(PPD)试验并没有广泛应用,因为没有足够的时间去等待其产生反应结果;此外供者在脑死亡或使用激素时可能也不会产生反应。目前正在研究γ-干扰素(IFN-γ)释放试验是否可行,因此也没有广泛应用于供者筛查。应检测伴结核风险的供者(去过中至高度流行国家、无家可归、药物滥用、或监禁)有无活动性肺结核;活动性结核的器官不应使用。目前专家推荐有针对性地筛査出生于墨西哥、中美洲和南美洲的供者有无潜在的克氏锥虫感染。应当指出的是,大多数现有的供者筛查试验有很髙的假阳性率,并且建议对所有的阳性结果进行确诊试验。这种确诊试验通常不能及时执行,但是可以指导移植后的干预策略。克氏锥虫感染的、或检测阳性的供者来源的肝脏和肾脏在受者知情的情况下可以考虑使用,因为其相对感染率较低;但是心脏则不能使用,因为其感染率较高。WNV是目前可经供者器官感染但无法检测的一种病毒。现有数据表明,如果对供者进行筛选,应该利用血清核酸检测病毒,不建议此时行尿WNV核酸检测和血清学检测。如果供者来自病毒小范围传播的地区,WNV核酸检测通常会产生假阳性结果,故而仅当地有活动性病毒流行时才考虑检测;建议与当地血库合作以决定是否检测。
3.4 特殊情况
3.4.1 供者血液样本稀释
大量失血后大量静脉补充血液制品或胶体和晶体液会导致血液稀释,致使检测结果不可靠。美国食品和药物管理局(FDA)发布了如何评估组织供者血液稀释的指南,这些指南可以估算器官供者的血液稀释程度。目前OPTN将血液稀释的供者划入高风险感染组,因此应该谨慎解释其血清学筛查结果的意义,并告知受者有关供者的血液稀释状况和此条件下感染性疾病假阴性的风险。
3.4.2 新生儿的检测
一般情况下,母亲抗体可能会传递给婴儿并持续6~15个月。在解释抗体检测结果时应考虑这一点。一些人主张检测婴儿尿中的CMV以验证有无感染。
3.4.3 活体供者
最近一例活体供者来源的HIV感染的报道提示我们需要在临近获取器官时进行检测。目前指南建议,活体供者应该检测HIV、HBV和HCV。其他检测可在手术前28天进行,最好是14天。这些晚期测试应包括HIV、HCV的核酸检测和HBsAg检测,从而直接检测供者是否携带病毒。最后,应向供者宣教如何在从检査到手术这段时间内避免感染。
3.4.4 在获取器官时供者伴有感染
是否使用这些活动性感染或潜在性感染的器官要根据受者移植的紧迫性、是否有其他代替的器官和受者意愿来决定。应仔细评估供者和供者的感染,包括药敏测试、使用的抗菌方案和治疗是否有效。具体的指南可能有助于决定供者是否合格以及指导术后降低感染风险的策略。一般来说,伴有任何活动性细菌或真菌感染的供者或受者应该马上接受治疗,最好能在移植手术前治愈;如果器官携带有可能感染给受者的病原体则不能移植。
3.5 菌血症供者
据估计,在获取器官时,5%的器官捐献者有菌血症。这类疾病传播涉及的细菌对通常使用的围手术期抗菌药物不敏感,发生感染后常伴有明显的移植物丢失,患病率和病死率上升。虽然供者的菌血症和细菌感染造成了受者可能感染的风险,但由于器官日益紧缺还是要慎重考虑弃用器官。供者传播疾病的风险与引起感染的细菌种类有关,凝固酶阴性葡萄球菌为革兰阳性菌中感染风险低且相对毒性较小的细菌。相比较而言,革兰阴性杆菌的感染风险更大、预后更差。
目前最关心的是不断增加的更具挑战性的MDR细菌,如耐甲氧西林金黄色葡萄球菌(MRSA)、耐万古霉素肠球菌(VRE)和MDR革兰阴性杆菌。产碳青霉烯酶的革兰阴性菌尤其严重,通常广泛耐药并且只对极少数的药物有效。对这些高度耐药细菌的评估和降低风险措施的报道很少。开放和快速的机构和部门间沟通、根据药敏试验的预防性抗菌药物和细致的感染控制措施是移植后减少供者来源细菌感染危害的合理措施。需要进一步明确MDR革兰阴性菌感染的供者器官何时可以安全使用,前瞻性地明确供者是否有亚临床感染以及移植后如何优化供者来源感染的治疗方案。
新近数据表明,在某些情况下可以使用伴菌血症的供者器官。一般来说,建议感染的供者接受至少24~48小时抗菌药物治疗,最好有良好疗效(白细胞计数、血流动力学得到改善,发热消退)。此外建议受者接受针对性抗菌药物治疗7~14天。
3.6 细菌性脑膜炎供者
有大量的数据表明,患细菌性脑膜炎的供者可以安全用于器官捐献。记录细菌性脑膜炎是必要的,因为曾有报道在怀疑但未确诊的细菌性脑膜炎供者中出现感染和恶性疾病的传播。伴有脑膜炎奈瑟菌、肺炎链球菌、流感嗜血杆菌或大肠杆菌引起的细菌性脑膜炎的供者,其器官如肾脏、肝脏和胸腔内器官都曾成功移植。一般来说,在移植前供者需要进行抗菌药物治疗24~48小时,最好有临床改善的证据。受者在移植后通常接受7~14天的针对性抗菌药物治疗。由高毒性细菌或细胞内病原体如李斯特菌引起的脑膜炎在很多移植中心仍然被认为是移植的禁忌。
3.7 确定或怀疑脑炎感染的受者
脑炎特别是不明原因伴发烧的脑炎,常与传播疾病相关。有报道称供者患脑炎时曾致受者出现狂犬病、寄生虫、淋巴瘤和白血病。因此,死于脑炎的供者器官应该避免使用。这条原则有2个例外,即明确的细菌性脑膜炎(见上文)和福氏耐格里阿米巴脑膜脑炎供者。阿米巴虫感染通常仅限于中枢神经系统,即使有中枢神经系统外寄生虫感染的分子学证据,也没有曾发生感染的报道。如果供者有明确的福氏耐格里阿米巴脑膜脑炎,感染风险很小,只要告知受者风险和密切监测就可以使用。
3.8 评估疑似患供者来源感染的受者
尽管供者来源的感染很罕见(估计占总移植的比例<0.2%),但考虑到供者是移植后感染或恶性肿瘤来源是很重要的,并且要向当地器官获取组织(OPO)或国家机关如美国的器官共享联合网络(UNOS)立即报告。不幸的是,受者可能在同一家医院内或很多家医院接受不同团队的治疗,这可能影响识别感染源于何处。另外,最近的几例报告表明,患者在移植术后不同时期会有不同的临床症状;来源于同一供者的器官导致所有受者感染应该考虑供体来源的感染,但通常无法进行相应的调查。OPO应该有相应的机制来迅速评估接收同一供体来源器官、组织和血管的其他受者的状态,并迅速上报给OPTN。明确的移植后早期感染应该马上审查供者的标本培养结果,考虑供者来源的感染。
常见的并发症如伤口或手术部位感染、移植排斥反应、吻合口瘘、血管损害、药物毒性、肺炎或艰难梭菌结肠炎等必须评估、治疗。如果考虑是供者来源的,则应立即报告给国家移植权威部门、当地OPO和当地公共卫生部门。应尽早报告,以提醒接受同一供者器官的其他受者进行评估并采取降低风险的措施;要强调不应在明确感染之后才报告。作为评估的一部分,应联系相关实验室保留任何残留的血液、血清、脑脊液和供者组织(如血管)以方便调査,确保它们被保存而不能随便处理掉。
最后,移植团队需要协同合作来为有供者感染传播风险的受者进行评估和治疗。这应包括一个明确的计划确定负责随访(如随访培养或PCR/血清学检测)和治疗的相关人员。一般来说,当确诊供者发生感染,受者应该接受适当的针对病原体的抗菌药物治疗,疗程与受者自身感染时需要的治疗时间一致。此外,目前建议所有接受有感染HIV、HBV和HCV风险供体器官的受者在术后接受检测。虽然对检测的最佳时间有争议,但是用于直接检测病毒的方法很重要(如HIV和HCV核酸检测和HBsAg检测),因为患者常常不发生血清转换,不能仅依赖于血清学检测。
4 未来的研究
由于供者来源的感染是一个相对较新的课题,所以需要更多的研究。关键是需要更多的国家建立器官警戒和监控系统来进一步确定供者来源感染的流行病学情况。这包括对有地域限制的感染的评估,在监控下则可能不会导致其传播。另外,只有在获得全球数据的情况下才能评估特定的病原体和降低风险策略。器官供者和受者的前瞻性研究,类似于输血医学所进行的逆转录病毒供体流行病学研究(REDS),需要更全面地确定其真实的供者疾病传播的风险和流行病学情况。需要评估现有的诊断和筛选方法,用于对潜在供者的危险分层。最后,需要登记上报特定潜在的供者传播的感染(如美洲锥虫、脑炎或菌血症),并告知是否可以安全使用供体器官以及降低风险策略以有效防止疾病传播。
(未完待续)
