高效液相色谱-四级杆/线性离子阱质谱法筛查兽药中非法添加物的研究
2014-11-23陈慧华应永飞陆春波林仙军朱聪英
周 炜,陈慧华,应永飞,陆春波,林仙军,朱聪英
(浙江省畜产品质量安全检测中心,杭州310020)
2013年3月,本实验室收到某品牌兽药样品若干,经调查这些兽药明显具有标签外药物的生理/药理学作用,即可明显促进育肥猪采食、提高出肉率,但具体是其中哪种药及具体成分不明。为配合相关行政执法部门严厉打击畜产品质量安全犯罪、超范围滥用兽药等违法行为,保障畜产品质量安全,急需对其中非法添加的未知成分进行筛查与确证。
目前,国际上多用核磁法和飞行时间质谱法等技术对某种未知成分进行定性分析[1-2]。但这些技术对仪器的要求,限制了其应用与推广。自20世纪50年代开始,基于常规四级杆质谱发展而来的四级杆/线性离子阱质谱技术日趋成熟[3-4],已广泛应用于检验检测领域。针对离子阱可进行选择性离子富集与裂解功能而研发的增强子离子扫描(Enhanced Product Ion Scan,EPI)技术,可根据可疑目标化合物的质荷比、裂解规律等参数,自动与已建谱库中的化合物进行匹配分析,从而实现对复杂基质中目标化合物的确证与测定[5-6]。然而,迄今为止,利用四极杆/线性离子阱质谱对未知物进行筛查的方法鲜有报道。本研究旨在以如何确证上述兽药中非法添加氯丙那林的过程为例,初步探讨了四级杆/线性离子阱质谱在兽药非法添加物筛查中的运用。
1 材料与方法
1.1 材料
1.1.1 仪器 Agilent 1290N高效液相色谱仪(美国Agilent公司);AB 5500 Q-Trap质谱仪(美国AB公司),配电喷雾离子源(ESI);电子天平(瑞士Mettler,精度十万分之一);离心机(德国Sigma公司)。
1.1.2 试剂与药品 试验用甲醇、乙腈、醋酸铅均为分析纯,甲酸及作为流动相的甲醇均为色谱纯,水为超纯水。氯丙那林(Clorprenaline,CLN)标准品购自Witega公司。所检阳性样品(包含:水性溶剂注射液、非水性溶剂注射液和中兽药散剂等三种剂型)及相应阴性对照样品均来自公安和农业行政执法部门。
1.1.3 EPI谱库 本实验室已对激素类、镇定剂/抑郁药类、脱羧酶抑制剂类、中枢神经兴奋剂类、抗病毒类等五大类药物进行了EPI谱库建立,谱库中“瘦肉精”类药物包括:马喷特罗、溴代克伦特罗、克伦塞罗、克伦异磅特罗、克伦潘特、羟甲基克伦特罗、Clenhexerol、马布特罗、妥布特罗、溴布特罗、氯丙那林、喷布特罗、西布特罗、特布他林、非诺特罗、克伦普罗、西马特罗、莱克多巴胺、齐帕特罗、班布特罗、沙丁胺醇、丙卡特罗、克伦特罗、福莫特罗(阿福特罗)、苯乙醇胺A等25种药物。
1.2 方法
1.2.1 样品前处理 结合目标化合物的生物学功用,推测其极有可能属于“瘦肉精”类化合物。由于“瘦肉精”类化合物多易溶于水,故本试验均采用水溶性目标化合物处理方法。
水性溶剂注射液:量取供试品适量,用0.2%甲酸水稀释依次成100倍、104倍和106倍稀释液,按浓度从低到高过膜上机,直至检测浓度适宜为止。
非水性溶剂注射液与中兽药散剂:取相应供试品适量(非水性溶剂注射液:5.0 mL;中兽药散剂:5.0 g)于50 mL离心管中,加入20 mL 0.2%甲酸水,水浴超声提取30 min,期间每5 min振摇1次。12000 r/min离心10 min,取上清液适量,用0.2%甲酸水稀释依次成100倍、104倍和106倍稀释液,按浓度从低到高过膜上机,直至检测浓度适宜为止。
1.2.2 靶目标分子筛查方法 为得到目标化合物的分子质量数信息,本研究采用Q3全扫描方式,通过比较样品与阴性对照的差异,获取靶目标化合物的分子质量。
质谱条件:采集模式为蠕动泵进样,ESI+模式Q3全扫描;泵流速为5 μL/min;离子源电压5500 V;辅助加热气温度550℃;气帘气流速40 L/h;离子源气流流速雾化气(Gas1)15 L/h、辅助气(Gas2)20 L/h;DP(Declustering Potential,去簇电压)50 eV;碰撞室入口电压(Entrance Potential,EP)10 eV;碰撞室出口电压(Collision Cell Exit Potential,CXP)10 eV;扫描速率200 Da/s。
1.2.3 靶目标分子质谱参数优化 为得到质荷比为214.2 Da的靶目标分子准确质量数及MRM(Multiple Reaction Monitoring)模式下的质谱参数,本试验先用0.2%甲酸水/甲醇/乙腈(50∶25∶25,V/V)对Q3全扫描上机液进行了10倍稀释,并依次优化了DP、EP、母离子质荷比、两特征子离子的碰撞能量(Collision Energy,CE)、CXP与子离子质荷比等参数。
1.2.4 靶目标分子的色谱分离 在筛查得到靶目标分子母离子质荷比后,初步验证了其属于“瘦肉精”类物质的推测,适用未知物筛查ESI+模式下的通用色谱条件进行分离。色谱条件:色谱柱:Waters Atlantis dC18 柱(3.0 mm ×150 mm,粒径3 μm);流动相及流速见表1;柱温:30℃;进样量:5 μL。

表1 通用流动相和流速
根据靶目标分子的保留时间与洗脱特性,对流动相组成进行了适当优化,以得到最佳色谱条件。优化后的流动相见表2。
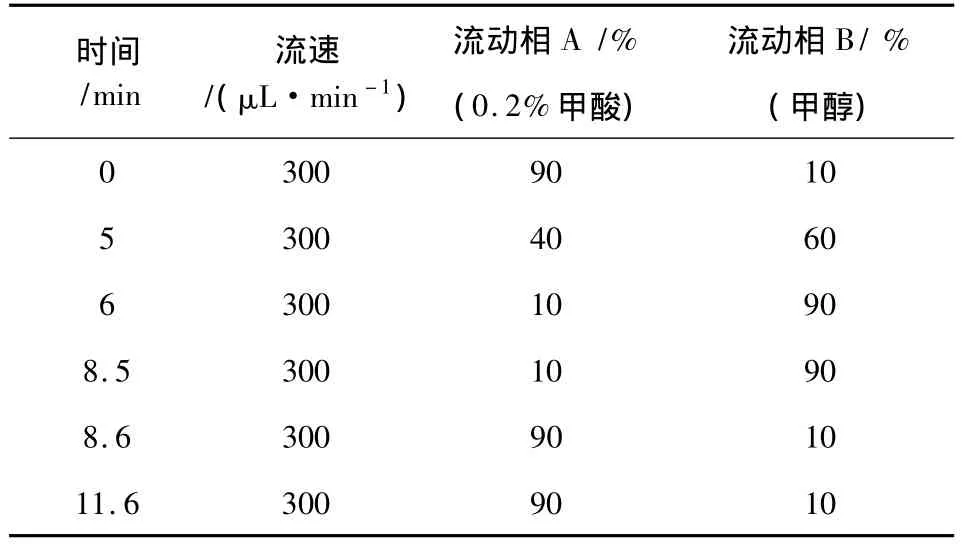
表2 流动相组成和流速
1.2.5 靶目标分子的定性确证方法 在优化了色谱条件后,本试验用仪器自带的“MRM-IDA(Information Dependent Acquistion)-EPI”(多反应监测触发增强子离子扫描)技术进行了谱库匹配检索,以进一步作定性确证。
质谱条件:MRM条件电喷雾离子源;正离子扫描;多反应监测;离子源电压:5500 V;碰撞气能量:高;辅助加热气温度:550℃;气帘气流速:40 L/h;离子源气流流速:Gas1为50 L/h,Gas2为35 L/h。目标化合物MRM参数见表3。
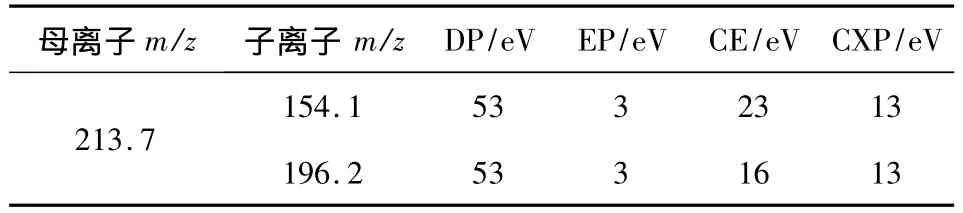
表3 多反应监测条件
IDA条件[5-6]:进行IDA监测时允许质量数偏离范围为±250 mDa;启用动态背景扣除(MRM响应值超出5000 cps,选择1个最强离子触发IDAEPI);当MRM到达已建库化合物的保留时间且响应值超出6000 cps,强制1个最强离子触发IDA-EPI。
EPI条件:扫描速率10000 Da/s;进行 EPI时CE为35、(35±15)eV(即最终所获得的EPI谱图为20、35、50 eV三个水平的碰撞能量下的叠加图)。
2 结果与分析
2.1 靶目标分子量筛查 本试验通过阴性对照的方法,寻找样品谱图中除阴性对照样品峰外的特征离子峰,对靶目标母离子质荷比进行筛查。由于四极杆质谱中Q1部分,对质量数的定量不能满足试验要求,因而采用Q2不进行碰撞裂解的Q3全扫描。扫描结果如图1、图2所示,所检“扶正解毒散”样品色谱图中在214.2 Da处有明显特征离子峰,与氯丙那林母离子质荷比(213.7 Da)相近。

图1 阴性对照样品Q3扫描图
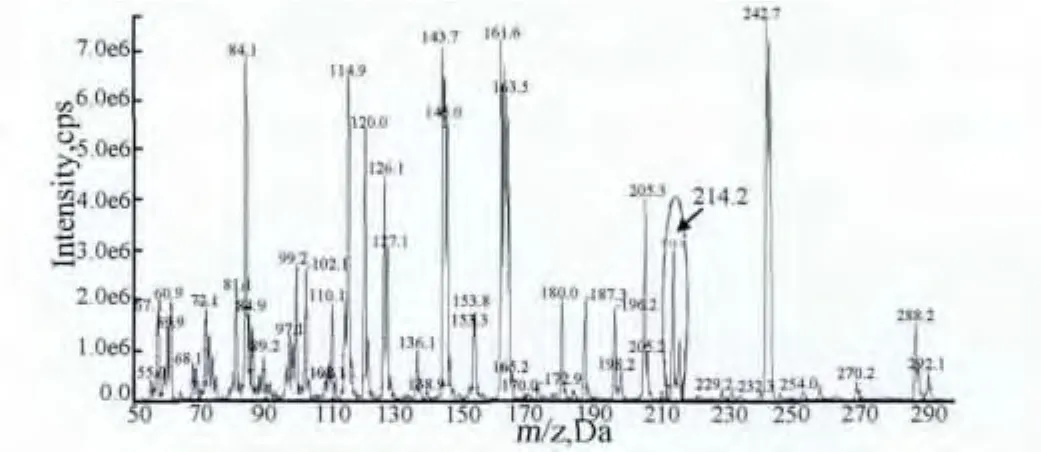
图2 样品Q3扫描图
2.2 靶目标分子的色谱分离 为保障高通量定性分析的可比性,本实验室对雌激素类、同化激素、镇定剂/抑郁药类、受体激动剂类、抗病毒类等均用ESI+离子源模式进行电离的药物,建立了通用流动相条件,以便于直接进行MRM-IDA-EPI谱库检索。在初步得到验证结果后,再对流动相条件进行进一步优化,然后在该流动相条件下对靶目标分子与标准物的谱图进行匹配度查询。通用模式下靶目标化合物的离子流图见图3,优化流动相及稀释倍数后的靶目标化合物的离子流图见图4。如图4所示,经优化条件后,靶目标化合物与基质得到了良好分离。
2.3 靶目标分子的定性确证 如图5、图6所示,在优化色谱条件后,靶目标化合物的保留时间(6.92 min)与氯丙那林对照品的保留时间(6.93 min)一致,均有质荷比为 154.1 Da、119.0 Da、91.0 Da 和76.9 Da特征碎片离子,且这四个特征碎片离子的峰度比也高度一致。从图7中可以看出,EPI谱库检索匹配度为93.2,远大于80的判定标准[7-8]。根据欧盟2002/657/EC决议要求,共获得7个识别点[7],远高于欧盟96/23/EC指令附录I的A组的物质(β-兴奋剂)确认要求(4个识别点)[9]。基于如上结果,该靶目标化合物可定性为氯丙那林。
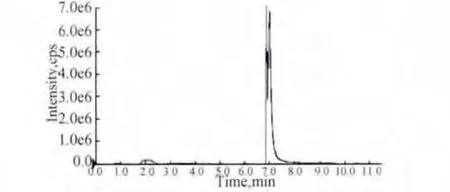
图3 通用模式下的总离子流图

图4 优化参数后的总离子流及CLN提取离子流图
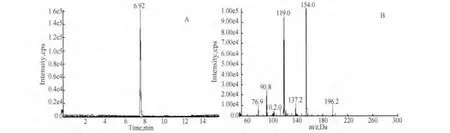
图5 靶目标化合物的MRM谱图(图A)和EPI谱图(图B)
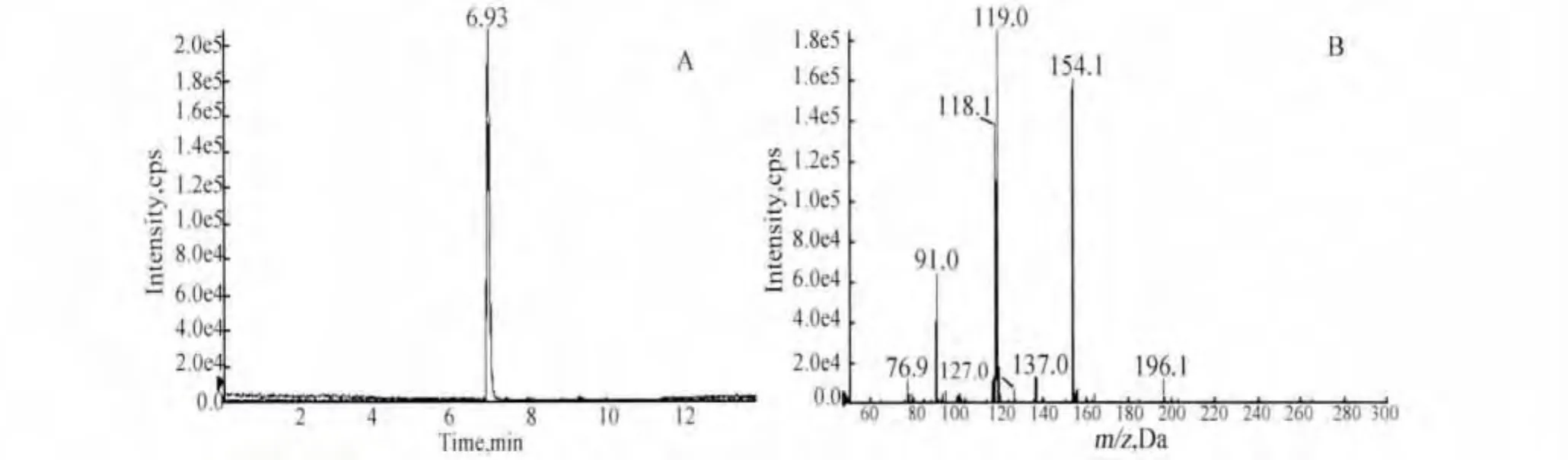
图6 氯丙那林标准品的MRM谱图(图A)与EPI谱图(图B)

图7 靶目标化合物与氯丙那林标准品的EPI谱图匹配度结果图
3 讨论
本研究以定性确证某品牌兽药中非法添加有氯丙那林的过程为例,建立了一整套利用高效液相色谱串联四级杆/线性离子阱质谱对兽药中非法添加物进行定性确证的方法,即:先从基质中提取目标化合物,利用Q3全扫描得到其分子质量数,随后对其HPLC、MRM参数进行优化,最后利用EPI谱库检索进行定性确证。
利用四级杆/线性离子阱进行未知物筛查与验证,过程可分为Target Scan和Non-target Scan两种方式进行。Target Scan是基于已知目标化合物可能的生理/药理学作用一类筛查方法,主要通过数据库比对、类似物分析两种方法进行。Non-target Scan是针对完全未知物的一类筛查方法[3],目前主要通过特征离子的质量与结构,结合这些结构潜在的生理、药理学作用、经济价值等情况进行。
本研究建立了一整套从兽药中筛查并确证非法添加物的Target Scan方法。对于已建立谱库的非法添加物或超标签范围使用的化学成分,可利用此方法对兽药、饲料及畜产品开展针对性筛查。同时,这一方法对于这些药物的同系物或类似物的筛查也具有一定指导性意义。就Non-target Scan方法而言,还需要在样品前处理过程中引入有机溶剂提取处理,在Q3全扫描和MRM方法建立时引入ESI-模式等处理方法以拓宽筛查范围。此外,无论是Target Scan,还是Non-target Scan,寻找合适的阴性对照物、探明靶目标化合物可能的生理/药理学作用对于畜产品及相关投入品中未知物的筛查均有着至关重要的意义。
由于四级杆/线性离子阱质谱仍属低分辩质谱,无法获得飞行时间质谱等高分辩质谱分析时所能得到的离子精确质量数和高通量同时扫描[1],因而目前还只能依赖标准物质及谱库的建立,而谱库的建立又需要长期的积累与维护。
[1]胡 莉,雷绍荣,郭灵安,等.液相色谱-离子阱-飞行时间质谱法定性分析未知着色剂[J].分析化学,2013,41(1):110-114.
[2]王象泰.离子阱研究的进展[J].厦门大学学报(自然科学版),1993,32:23-27.
[3]Timothy R Croley,Kevin D White,John H Callahan,et al.The chromatographic role in high resolution mass spectrometry for non-targeted analysis[J].J Am Soc Mass Spectrom,2012,(23):1569-1578.
[4]Raymond E March,John F Todd.Quadrupole ion trap mass spectrometry[M].New York:Wiley-Inter-science,2005:346.
[5]张鸿伟,蔡 雪,林黎明,等.液相色谱-四极杆/离子阱质谱同时确证和测定肌肉中16种同化甾体激素残留[J].色谱,2012,30(10):991-1001.
[6]方慧文,周 原,卢跃鹏,等.高效液相色谱-线性离子阱串联质谱技术用于白酒中甜蜜素测定的确证分析[J].色谱,2012,30(3):252-255.
[7]欧洲共同体委员会.2002/657/EC号决议[S].2002.
[8]张鸿伟,简慧敏,林黎明,等.液相色谱-四极杆/离子阱质谱快速测定蜂蜜中痕量硝基咪唑类药物及其代谢物残留[J].分析测试学报,2012,31(7):763-770.
[9]欧洲共同体委员会.96/23/EC号决议[S].1996.
