烟酸黄藤素注射液安全性试验研究
2014-11-23陆荣宝银慧慧覃振华姜源明甘渝群孙建华
赵 武,刘 伟,孟 菲,陆荣宝,银慧慧,覃振华,姜源明,甘渝群,孙建华*
(1.广西壮族自治区兽医研究所,广西畜禽疫苗新技术重点实验室,南宁530001;2.广西动物卫生监督所,南宁530001;3.广西康普动物保健品股份有限公司,南宁530001)
黄藤素(Fibriuretinin)是我国自行研制的纯天然植物药,临床用于治疗生殖系统炎症、外科感染、菌痢、肠炎、呼吸道以及泌尿道感染、眼结膜炎等[1]。天然黄藤素主要从防已科植物黄藤的干燥藤茎中提取获得,是一种季胺盐异喹啉类生物碱,主要成分为巴马汀(Palmatine)盐酸盐;盐酸巴马汀易溶于热水,但冷水中溶解度低,其水溶液制剂在低温环境易结晶析出,物理性状不稳定,不利于注射液、口服溶液剂等制剂的开发利用。为此,经过溶解性试验和制剂稳定性试验,筛选出性质稳定、毒性低、对动物机体无危害的烟酸作助剂,并成功制备3%烟酸黄藤素注射液。黄藤素以植物提取物形式入药,其药理毒理基础研究相对比较薄弱,系统性研究鲜有资料报道;相反,时有黄藤素致过敏性休克、药疹、腹痛、大便潜血、唾液腺肿大、肺水肿等临床不良反应报道[2]。本研究通过溶血性试验、肌肉刺激性试验、口服和腹腔注射急性毒性试验对烟酸黄藤素注射液安全性和毒性进行了评价,为进一步进行临床试验和临床应用提供药理毒理依据。
1 材料与方法
1.1 材料
1.1.1 药物 烟酸黄藤素注射液由广西兽医研究所兽药新技术研发中心与广西康普动物保健品股份有限公司联合制备,批号20130806,含量规格3%,性状为黄色澄明液体。
1.1.2 试验动物 新西兰大耳白兔2只,雌雄各1 只,体重2.0 ~2.5 kg;昆明种小鼠,4 周龄,130 只,雌雄各半,体重18~22 g,其中30只用于预实验,100只用于正式试验,购自广西医科大学实验动物中心,实验动物生产许可证号:SCXK桂2009-0002。
1.2 方法
1.2.1 溶血与凝集试验[3]
1.2.1.1 红细胞混悬液制备 取兔耳静脉血约20 mL,置于装有玻璃珠的灭菌玻璃瓶内,轻轻摇动玻璃瓶约20 min,除去纤维蛋白,取出血液,加等量生理盐水混匀,纱布过滤,滤液1500 r/min离心10 min,吸去上清液;沉淀的红细胞再加生理盐水清洗,离心。如此重复3~5次至上清液无色透明。最后一次3000 r/min离心沉淀10 min,按红细胞容积加生理盐水配成2%的红细胞混悬液。
1.2.1.2 测定方法 取干燥无菌试管7只,1至6号试管分别加入烟酸黄藤素注射液 0.5、0.4、0.3、0.2、0.1、0 mL,生理盐水 2.0、2.1、2.2、2.3、2.4、2.5 mL;7号试管加入蒸馏水2.5 mL,摇匀,然后向1至7号试管分别加入2.5 mL 2%红细胞混悬液,摇匀,置于 37 ℃恒温箱中,分别于 0.5、1、2、3 h 观察是否有溶血及凝血现象发生。
1.2.2 肌肉刺激性试验 参照文献[3]方法,新西兰兔2只,剪去两腿外侧被毛,2.5%碘酊和75%的乙醇消毒后,每只兔左、右腿股四头肌内分别注射3%烟酸黄藤素注射液1 mL,注射后48 h处死动物,解剖取出两侧股四头肌,纵向切开,观察注射局部刺激反应,取局部组织标本进行病理组织学检查。按以下标准换算相应的反应级:0级为无明显变化;1级为轻度充血,范围在0.5 cm×1.0 cm以下;2级为中度充血,范围在0.5 cm×1.0 cm以上;3级为重度充血,伴有肌肉变性;4级为出现坏死,有褐色变性;5级为出现广泛性坏死。计算出4块股四头肌反应级的总和。
1.2.3 小鼠急性毒性试验[4]
1.2.3.1 口服试验 50只小鼠,雌雄各半,随机分为5组,每组10只(雌雄各5只),正常给水及广西医科大学提供的小鼠混合饲料,观察3 d,饮水、采食、精神状态均正常。根据预试验结果,灌服4200 mg/kg,小鼠100%死亡,灌服 2000 mg/kg,小鼠0%死亡。按相邻组间距比值1.2计算5组给药剂量为:2000、2400、2880、3456、4147 mg/kg;按剂量用灌胃针灌服。观察小鼠饮水、采食和行为变化,以及死亡情况,剖检观察死亡小鼠脏器病理变化。连续观察7 d,并作记录。
1.2.3.2 腹腔注射试验 50只小鼠,雌雄各半,随机分为5组,每组10只(雌雄各5只),正常给水及广西医科大学提供的小鼠混合饲料,观察3 d,饮水、采食、精神状态均正常。根据预试验结果,腹腔注射剂量300 mg/kg,小鼠100%死亡,腹腔注射剂量75 mg/kg,小鼠0%死亡。按相邻组间距比值1.4 计算 5 组给药剂量为:75、105、147、206、288 mg/kg;按剂量腹腔注射。观察小鼠饮水、采食和行为变化,以及死亡情况,剖检观察死亡小鼠脏器病理变化。连续观察7 d,并作记录。
2 结果
2.1 溶血与凝集试验结果 在观察时间内,1~6号管未见溶血和红细胞凝聚现象,第7管溶液呈红色透明,有溶血现象。结果表明烟酸黄藤素注射液0.1~0.5 mL在3 h内对兔红细胞不产生溶血和凝聚作用。
2.2 肌肉刺激性试验结果 肉眼观察发现,1号兔左侧股四头肌轻度充血,其范围小于0.5 cm×1 cm,右侧股四头肌无明显变化;2号兔左右两侧股四头肌均轻度充血,其范围小于0.5 cm×1 cm。根据刺激反应中反应级的分值计为分3,结果见表1。镜检见肌纤维组织横纹清晰,结构基本完整,部分区域见局灶性出血,未见炎细胞浸润以及肌纤维的变性坏死。

表1 肌肉刺激反应分级结果
2.3 小鼠急性毒性试验结果
2.3.1 口服试验结果 经食管灌入烟酸黄藤素注射液30 min后,部分小鼠开始出现药物反应,第3组至第5组小鼠活跃程度不如第1组,采食量比第1组明显减少,但饮水量增加,部分昆明小鼠表现出兴奋不安,痉挛,缩成一团,呼吸困难,昏迷,4 h后开始出现死亡。到第7 d,存活小鼠采食、饮水正常,活动自如。死亡小鼠剖检,外形未见异常,剖检发现,肺脏轻微充血,支气管淤血,粘液较多;胃粘膜充血、水肿,肠系膜充血;脾脏肿大,边缘钝圆,肝脏表面呈暗紫红色,切面呈暗红色,质地变软;心脏充盈,轻微水肿。用改良寇氏法计算得出LD50为 2866 mg/kg,LD5095% 可信限为 2455~3346 mg/kg(表2)。
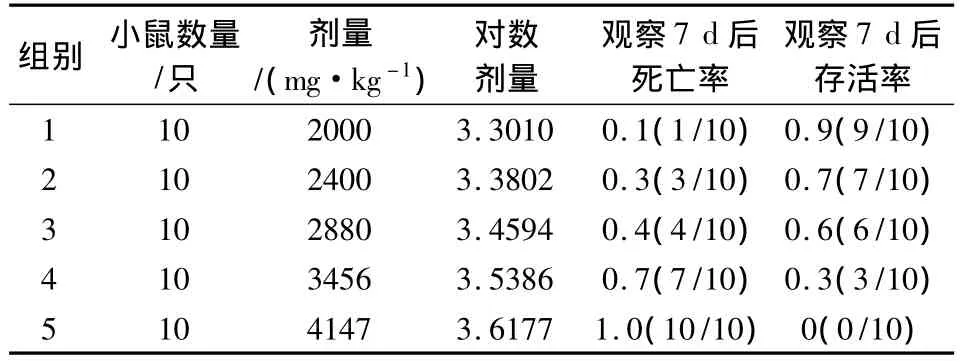
表2 小鼠口服急性毒性试验结果
2.3.2 腹腔注射试验结果 各组小鼠按剂量注射烟酸黄藤素注射液后,部分小鼠10 min开始出现药物反应,第3组至第5组小鼠活跃程度不如第1组,饮水量增加,部分小鼠躬腰缩背,卷缩起来,活动减少,痉挛,呼吸困难,昏迷,约30 min后第5组开始出现死亡。到第7 d,存活小鼠采食、饮水正常,活动自如。死亡小鼠剖检,外形未见异常,剖检发现,肺脏轻微充血,支气管淤血,粘液较多;肠系膜充血;脾脏肿大,边缘钝圆,肝脏表面呈暗紫红色,切面呈暗红色,质地变软;心脏充盈,轻微水肿;输尿管有白色尿酸盐沉积。用改良寇氏法计算得出LD50为 153 mg/kg,LD5095%可信限为 117~199 mg/kg(表3)。
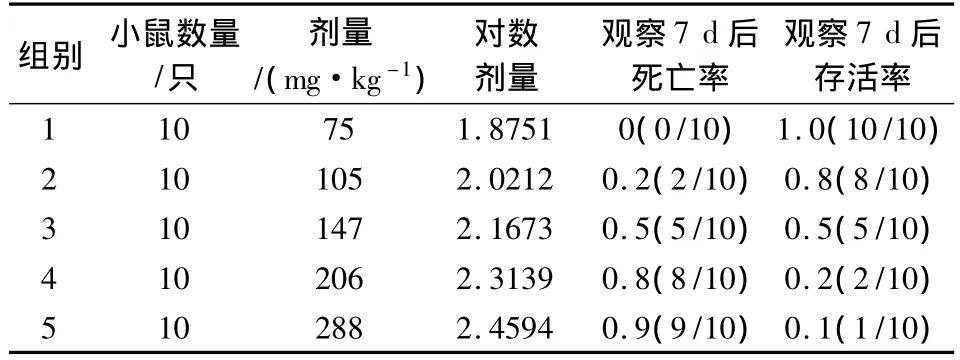
表3 小鼠腹腔注射急性毒性试验结果
3 讨论
为了制备有效药物浓度更高、物理性状稳定性更好、临床使用更为方便的黄藤素注射液,本研究筛选性质稳定、毒性低、对动物机体无危害的烟酸作助溶剂,成功制备3%烟酸黄藤素注射液。本试验对烟酸黄藤素注射液的溶血性、肌肉刺激性和急性毒性进行了试验。在溶血与凝集试验中,烟酸黄藤素注射液0.1~0.5 mL在3 h内对兔红细胞不产生溶血和凝聚作用,说明烟酸黄藤素注射液符合注射液溶血与凝集试验标准,与李群力等[5]发现黄藤素葡萄糖注射液在体外对家兔红细胞不产生溶血及凝集作用的研究结果相一致。在肌肉刺激性试验中,2只试验兔4块股四头肌反应级总和为3,按照2只试验兔4块股四头肌反应级之和小于10时,则认为供试品的局部刺激试验符合规定的标准判断,3%烟酸黄藤素注射液局部刺激反应轻微,肌肉刺激试验符合规定。在小鼠口服和腹腔注射急性毒性试验中,按照Karber法计算出LD50分别为2866 mg/kg、153 mg/kg;杨荣等[6]研究结果表明,黄藤素注射液Beagle犬静脉给药近似致死剂量接近50 mg/kg,本试验烟酸黄藤素注射液腹腔注射小鼠近似致死剂量接近75 mg/kg,考虑静脉注射和腹腔注射给药途径的差异,说明烟酸黄藤素注射液与黄藤素注射液比较毒性未明显增强。按照LD50在1 mg/kg以下者为极毒,1~50 mg/kg为剧毒,50~500 mg/kg为中等毒,500~5000 mg/kg为低毒,5001~15000 mg/kg为实际无毒,>15000 mg/kg为无毒标准判断,烟酸黄藤素口服给药属低毒性药物,注射给药属中等毒性药物。以上试验对烟酸黄藤素注射液安全性和毒性进行了综合评价,为进一步进行临床治疗试验提供了药理毒理学基本依据。
黄藤素是我国自行研制的纯天然植物药,1977年首次收载于《中华人民共和国药典》[7],现收载于《中华人民共和国药典》2010年版一部“植物油脂和提取物”部分[4],《兽药国家标准(化学药品、中药卷)第一册》也收载了兽用黄藤素注射液质量标准[8],黄藤素在医学、兽医临床均具有应用基础。但是,黄藤素以植物提取物形式入药,其药理毒理基础研究相对比较薄弱,系统性研究鲜有资料报道;相反,时有黄藤素致过敏性休克、药疹、腹痛、大便潜血、唾液腺肿大、肺水肿等临床不良反应报道[2]。因此,在开发黄藤素相关制剂的同时,应加强黄藤素药理毒理学基础研究,为临床应用提供更为全面的科学依据。
[1]国家药典委员会.中华人民共和国药典2010年版一部[S].
[2]杨小良,谢丽莎,龚志强.黄藤素的研究综述[J].中国医药指南,2009,7(17):42-44.
[3]国家食品药品监督管理局.[Z]GPT4-1.中药、天然药物刺激性和溶血性研究的技术指导原则[S].2005.
[4]农业部兽药评审中心.兽药研究技术指导原则汇编(2006-2011年)[S].2013.北京:化学工业出版社,2012:84-87.
[5]李群力,陈 菲.黄藤素葡萄糖注射液安全性实验研究[J].中草药,2007,38:252-253.
[6]杨 荣,陆 瑛,张 玲,等.黄藤素注射液Beagle犬静脉给药毒性观察[J].四川生理科学杂志,2005,27(1):48.
[7]国家药典委员会.中华人民共和国药典1997年版一部[S].
[8]中国兽药典委员会.兽药国家标准(化学药品、中药卷)第一册[M].北京:中国农业出版社,2013:41.
