高效毛细管电泳法分析附子多糖中单糖组分
2014-11-08付昆,叶强
付 昆,叶 强
(1.四川省成都市第三人民医院,四川 成都 610031;2.成都中医药大学,四川 成都 611137)
目前,多糖中单糖组成的分析主要采用纸层析、液相色谱、气相色谱等方法,样品用量大、试验条件严格,毛细管电泳技术(CE)具有样品用量少、时间短、灵敏度高、分离效果明显的特点[1],主要用于寡糖的分析。多糖的高效毛细管电泳(HPCE)研究目前尚处于探索阶段[2],由于单糖在水溶液中解离能力极差,在强碱条件下才能带上电荷。使用含硼砂的缓冲液会让单糖在较低的pH条件下带上足够的负电荷。不同的单糖在相同介质条件下与硼砂的络合物具有有效淌度的差异,足以被毛细管电泳分辨。单糖的紫外吸收很弱,采用α-萘胺为衍生试剂使其带上可被检测的基团[3]。将多糖水解成单糖,再经过和标准单糖相同的处理。用毛细管电泳分析出其所含单糖的谱图,与标准单糖的谱图对照,即可得出多糖中单糖的种类与含量。本试验中应用高效毛细管电泳对附子多糖中单糖组成及其含量进行测定,并确定HPCE试验条件。
1 仪器与试药
P/MDQ型高效毛细管电泳仪(美国Beckman公司);32Karasoft操作软件;石英毛细管柱(50 μm × 75 cm,Beckman)。半乳糖、木糖、甘露糖、葡萄糖、鼠李糖、阿拉伯糖(国药集团化学试剂公司);乙醇、丙酮、正丁醇、氯仿、α-萘胺、硼氰化氢钠、硼砂等其他试剂均为分析纯;所用水均为去离子水;附子药材(四川省中药饮片有限责任公司,批号为110701)。
2 方法与结果
2.1 多糖样品制备
2.1.1 提取
干燥附子100 g粉碎后,用8倍量95%的乙醇回流提取2次,每次2 h,抽滤后所得残渣干燥,加入8倍量水于90℃提取2次,每次15 h,水提液减压浓缩至200 mL。冷却后用95%的乙醇调节终浓度为80%,密封保存。次日用适量的无水乙醇、丙酮和石油醚依次抽洗,干燥后得浅褐色附子粗多糖。
2.1.2 纯化
除蛋白:多糖25 g溶于50 mL水中,将10 mL的sevage液(氯仿∶正丁醇=4∶1)加入粗多糖液中,剧烈震荡10 min后,以4 000 r/min的速率离心10 min。除去水相与有机相间的蛋白,将上层水相反复操作6次。
脱色:除蛋白后的多糖溶液调节pH为8~9,加入10%的H2O2250 mL置4℃冰箱中放置24 h。
透析:透析袋用50%的乙醇蒸制1 h,接着依次用0.01 mol/L的NaHCO3、0.001 mol/L的EDAE和蒸馏水洗涤。将脱色2 d后的多糖溶液装入处理好的透析袋中,先用自来水流水透析2 d,然后用流动的蒸馏水透析2 d。
醇沉:将透析过的多糖液经70℃减压浓缩至25 mL,待自然冷却后加入95%的乙醇调节终浓度为80%,次日按上述方法处理得精制后的多糖。
2.2 电泳条件及缓冲液
运行缓冲液为 50,75,100 mmol/L 硼砂溶液。pH:9.5,10,10.5;柱温:25℃;电压:20 kV;检测波长:214 nm;进样气压:0.5psi;进样时间:15 s。清洗液:0.1 mol/L HCL 溶液;0.1 mol/L NaOH 溶液;重蒸水。
2.3 单糖标准品的α-萘胺衍生化[4]
称取 α-萘胺 143.2 mg和 NaBH3CN 35 mg,溶于450 mL无水甲醇中,再加入41 mL冰乙酸,置冰箱中待用。取各种单糖用重蒸水配成质量浓度为10 g/L的水溶液,各取200 mL,加40 mL衍生试剂置安瓿管中封管,80℃恒温2 h衍生化。然后各加入三氯甲烷和重蒸水1 mL,反复离心萃取3次,取上层水相过滤后定容至5 mL,分别制成各单糖及混合单糖衍生溶液冷藏备测。
2.4 多糖水解样品制备
取生附子多糖10 mg,加入2 mol/L H2SO41 mL,封管100℃恒温水解8 h,冷却后用碳酸钡完全中和(pH=7),放置过夜,过滤后取200 mL,按2.3项下方法进行衍生化。
2.5 标准品及样品测定
取衍生化的标准品及样品溶液按2.2项下所示条件测定迁移时间和峰面积,分别平行做3份,每份测3次。根据各吸收峰的峰面积计算各单糖组成的相对比例。
2.6 结果与分析
硼砂浓度及pH的选定:用硼砂做缓冲液,单糖混合物的分离度随pH增加而增大,其最佳分离条件为pH=10.5,6种单糖的混合物完全分离。增加缓冲液中的硼砂浓度,能有效地增加分离度,但单糖的出峰时间亦有所延长。试验用50 mmol/L时分离效果不好,在75 mmol/L时分离效果较好,100 mmol/L时电流较小,分离效果不好。结果最终确定硼砂缓冲液浓度为75 mmol/L,pH=10.5。
标准单糖谱图:将6个单糖标准品电泳分析,得出各个单糖的出峰时间,与混合单糖标准品谱图对照,得出每个标准单糖的电泳迁移时间。混合单糖标准品出现6个明显的峰,得到了有效分离。混合单糖中鼠李糖、木糖、葡萄糖、甘露糖、阿拉伯糖、半乳糖的迁移时间分别为 20.638,24.134,28.665,29.275,31.102,39.927 min。电泳谱图见图1(其中峰1为衍生试剂α-萘胺)。
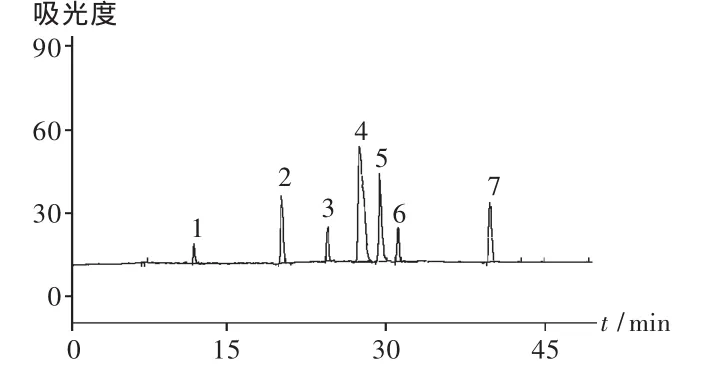
图1 混合单糖毛细管电泳图
多糖样品分析:将附子多糖作出的谱图与标准混合单糖谱图对照(见图2),根据其出峰时间的对应关系,可确定附子多糖由葡萄糖和半乳糖组成,其比例为 Glc ∶Gal=16.55 ∶28.72。单糖组成有鼠李糖、木糖、葡萄糖、甘露糖、阿位伯糖、半乳糖,葡萄糖和半乳糖的迁移时间分别为28.285 min和39.254 min,相对峰面积分别为16.55%和28.72%。
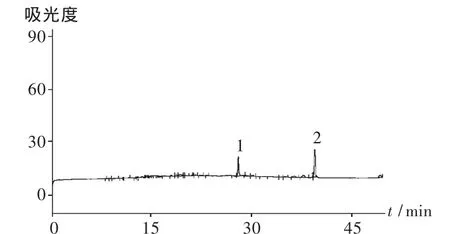
图2 附子多糖中单糖毛细管电泳图
3 讨论
本试验中利用HPCE法检测附子多糖单糖组成,取得了较好的分离效果,且操作简单、精度高,可发展为检测多糖中单糖组成的一种常用方法[5]。用α-萘胺将糖衍生化,使糖分子的还原端与其反应成为Schiff's碱,再利用NaBH3CN还原成仲胺[6],引入了可供检测的基团使糖形成硼酸盐络合物,带上了固有电荷。试验中发现,影响HPCE分离效果的主要因素是缓冲液的pH,增加的缓冲液pH可以使糖类的分离度相应地增加,但出峰时间相应延长;增加缓冲液浓度,电流变大,峰信号强度增强,选择75 mmol/L的硼砂溶液分离效果良好。试验结果表明,附子多糖主要由葡萄糖和半乳糖组成,其比例为Glc∶Gal=16.55∶28.72。
[3]贾国惠.糖类的高效毛细管电泳分析[J].中国医院药学杂志,2003,23(8):492-493.
[4]耿 越,王暖波.花粉多糖组分的高效毛细管电泳分析[J].山东科学,2001,14(4):10-13.
[5]Nicola V,Francesca M.Separation of capsular polysaccharide K4 and defructosylated K4 derived disaccharides by fluorophore-assisted carbohydrate electrophoresis(FACE)[J].Carbohydrate Polymers,2005,61(3):327-333.
[6]张剑波,田庚元.糖类的高效毛细管电泳[J].有机化学,1998,18(3):88-96.
