Zr/ZSM-5-SBA-15的制备及其氧化脱硫动力学研究
2014-10-17李智超李会鹏蔡天凤
李智超,李会鹏,赵 华,蔡天凤
(辽宁石油化工大学石油化工学院,辽宁抚顺 113001)
出于保护环境的目的,许多国家制定了越来越严格的标准和燃油限制条例,因此,燃料油的深度脱硫受到了广泛的关注和重视[1-3]。日本、欧洲以及美国等已经将含硫量限制在15 mg/L。近些年来,氧化脱硫、吸附脱硫和萃取脱硫等新的脱硫方法受到了越来越广泛的关注。氧化-萃取脱硫由于温和的反应条件和高脱硫率被认为是有望在近期内获得重大突破的超深度脱硫技术。
反应动力学是研究化学反应速率以及各种因素对化学反应速率影响的学科。活化能是表示化学反应受温度影响的一个重要的指标,活化能越大,反应进行越困难;反应活性越低,活化能越大,反应进行得越容易,反应活性越高[4]。因此,反应动力学的研究有着潜在的应用价值。
1 实验部分
1.1 材料与仪器
ZSM-5;SBA-15、ZSM-5-SBA-15[5]均为自制;四水硫酸锆、四乙基溴化铵、H2O2(30%)、噻吩、二甲亚砜、磷钼酸、甲酸、二甲苯、苯、正己烷均为分析纯。
DF-101S集热式恒温加热磁力搅拌器;JJ-1精密增力电动搅拌器;DD10A数字温度显示仪;601电热鼓风干燥箱;HANGPING JA5003电子天平;WK-2D微库仑仪;ASAP2400型物理吸附仪。
1.2 催化剂制备
以ZrSO4为活性组分,ZSM-5、SBA-15和ZSM-5-SBA-15为载体,采用等体积浸渍法制备催化剂,于500℃焙烧5 h,制得催化剂。
1.3 氧化脱硫
以模拟油为原料,H2O2为氧化剂,四乙基溴化铵为相转移催化剂,在恒温水浴锅中进行加热和搅拌。其脱硫反应条件为:模拟油30 mL,70℃下反应120 min,剂油比(催化剂与模拟油的质量比)为1∶40,V(H2O2)∶V(油)=0.02,四乙基溴化铵 0.08 g。
1.4 N2 吸附-脱附
样品在测定前经过300℃抽真空活化4 h以上,然后将样品瓶置于液氮罐中进行吸附-脱附实验。
1.5 动力学实验
三口烧瓶中加入模拟油和H2O2,以Zr/ZSM-5-SBA-15为催化剂,并加入一定量的相转移催化剂,剂油比(催化剂与模拟油的质量比)为1∶40,V(H2O2)∶V(油)=0.02,反应时间为 120 min,考察反应温度为40,50,60,70,80 ℃时不同反应时间下的脱硫率。根据不同反应时间下的含硫量作图,计算得出不同反应温度下的n及lnk值。根据lnk值与温度的倒数来作图,计算可得表观活化能。
2 结果与讨论
2.1 催化剂的N2吸附-脱附等温线
图 1为 Zr/SBA-15、Zr/ZSM-5和 Zr/ZSM-5-SBA-15催化剂的N2吸附-脱附等温线。
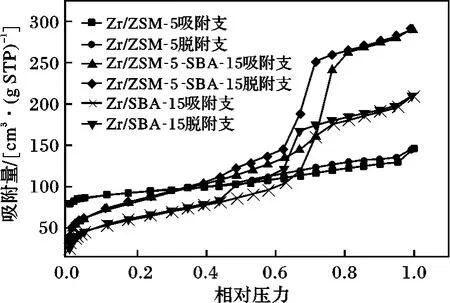
图1 改性ZSM-5-SBA-15的N2吸附-脱附等温线Fig.1 N2 adsorption-desorption isotherms of ZSM-5-SBA-15
由图1可知,Zr/SBA-15和 Zr/ZSM-5-SBA-15的N2吸附-脱附等温线都有一个明显的滞后环,按BDDT分类均属于Ⅳ型[6]。它们在低压段,吸附量随p/po的增加而平缓增加,且Zr/ZSM-5-SBA-15比Zr/SBA-15有较陡峭的起势,表明样品中有比较发达的微孔存在。N2分子以单层到多层吸附于孔的内表面;Zr/SBA-15的脱附支与吸附支在 p/po<0.43时完全重合,且 Zr/ZSM-5-SBA-15在 p/po<0.4时完全重合,与纯的分子筛材料相比,明显降低。一般来说,重合点的位置可以明确表明孔径的大小:p/po越高介孔分子筛的孔径越大。所以Zr/ZSM-5-SBA-15比Zr/SBA-15的孔径更大一些。在较高的p/po区,N2分子由于毛细管凝聚填满孔,吸附量随p/po的增加急剧增大;脱附支与吸附支不重合,形成一个典型的滞后环,这表明催化剂中包含介孔孔道。
Zr/ZSM-5的N2吸附-脱附等温线以一个平台为特征,在较低相对压力时吸附量迅速增加,然后趋于恒定的数值(即极限吸附量)。极限吸附量有时表示单分子层饱和吸附量,对于微孔吸附剂可能是将微孔填充满的量。按BDDT分类均属于I型[6],是典型的微孔固体的吸附。
2.2 催化剂的制备条件对脱硫率的影响
2.2.1 焙烧温度对脱硫率的影响 模拟油30 mL,反应温度70℃,剂油比(催化剂与模拟油的质量比)为1 ∶40,反应时间120 min,V(H2O2)∶V(油)=0.02,Zr负载量(质量分数)为20%,四乙基溴化铵为0.08 g,考察催化剂的焙烧温度对脱硫率的影响,结果见图2。

图2 Zr/ZSM-5-SBA-15催化剂焙烧温度对脱硫率的影响Fig.2 The influence of Zr/ZSM-5-SBA-15 catalyst calcination temperature on desulfurization rate
由图2可知,随着焙烧温度的增加,脱硫率先增加后下降,焙烧温度500℃时,脱硫率达到最大值。这主要是因为催化剂的焙烧过程也是其活化的过程,焙烧温度过高或过低,都会使催化剂活性降低。①随着焙烧温度的升高,四水硫酸锆的结晶水会逐渐失去,从而使催化剂的活性中心逐渐凸显出来,使催化剂的脱硫活性提高;②焙烧温度过高时,四水硫酸锆失水过度,导致活性组分在载体表面的聚集和迁移,当温度过高时,甚至还可能发生热分解,因此使它的活性中心减少,脱硫率降低。对Zr/ZSM-5-SBA-15分子筛来说,过高的焙烧温度也会使其在高温下发生一些副反应,降低了对含硫物质的催化性能。所以,最佳焙烧温度确定为500℃。
2.2.2 焙烧时间对脱硫率的影响 模拟油30 mL,反应温度70℃,剂油比(催化剂与模拟油的质量比)为1 ∶40,反应时间120 min,V(H2O2)∶V(油)=0.02,Zr负载量(质量分数)为20%,四乙基溴化铵0.08 g,考察催化剂的焙烧时间对脱硫率的影响,结果见图3。
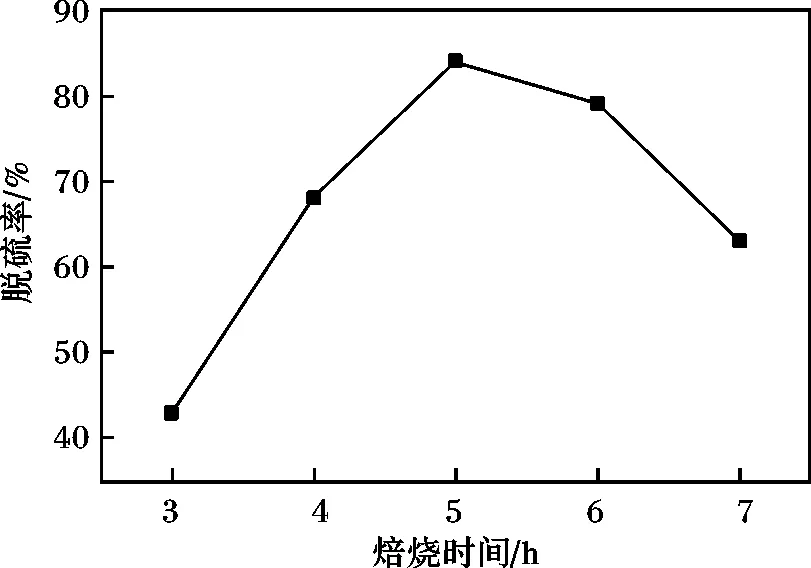
图3 Zr/ZSM-5-SBA-15催化剂焙烧时间对脱硫率的影响Fig.3 The influence of Zr/ZSM-5-SBA-15 catalyst calcination time on desulfurization rate
由图3可知,催化剂随着焙烧时间的增加,脱硫率先增加后下降。当焙烧温度为500℃,焙烧时间5 h,脱硫率达到最大值。这主要是因为在同一焙烧温度下,随着焙烧时间的增加,金属氧化物的结晶度降低,更容易在载体上分散,形成更多的活性中心。然而再增加焙烧时间时,由于金属原子热运动造成了金属原子向载体表面发生迁移,导致金属粒子在长时间的焙烧条件下相互间又发生了聚集,因此活性降低。所以,最佳的焙烧时间是5 h。
2.2.3 Zr负载量对脱硫率的影响 模拟油30 mL,反应温度70℃,反应时间120 min,剂油比(催化剂与模拟油的质量比)为1∶40,V(H2O2)∶V(油)=0.02,四乙基溴化铵0.08 g,考察 Zr负载量的脱硫效果,结果见图4。

图4 锆的不同负载量对脱硫率的影响Fig.4 The influence of different Zr loading on desulfurization rate
由图4可知,当焙烧温度为500℃,焙烧时间5 h时,随着Zr负载量的增加,脱硫率先增加后下降,负载量20%时,脱硫率达到最大值。这主要是因为过量的硫酸锆可能会阻塞孔道,导致催化剂的比表面积下降,导致催化剂的活性中心数量下降,使催化剂的氧化吸附能力下降。
2.3 动力学分析
2.3.1 建立动力学模型 氧化脱硫反应式可表示为:

其催化氧化脱硫反应的反应速率方程可表示为:

由于反应原料中氧化剂H2O2过量,所以可将看为常数(设 k1=),上式可转化为:

根据反应方程(2),不同时间不同温度下的脱硫率可以得到脱硫反应级数n,速率常数k1。
阿伦尼乌斯方程可以体现反应温度对反应速率的影响

对上式等号两边同时取对数得:

以lnk1对1/T作图,进行直线拟合,依拟合后的直线方程的斜率可求得表观活化能Eα,依直线截距可得指前因子k0。
2.3.2 动力学计算 根据公式计算,得出不同反应温度下的n及lnk,见表1。

表1 不同温度下反应表观动力学参数Table1 Reaction kinetic parameters under different temperature
由不同温度下的反应级数求得脱硫反应的平均反应级数为1.13,说明此反应为一级反应。
用1/T对lnk作图,并对其进行直线拟合,结果见图5。
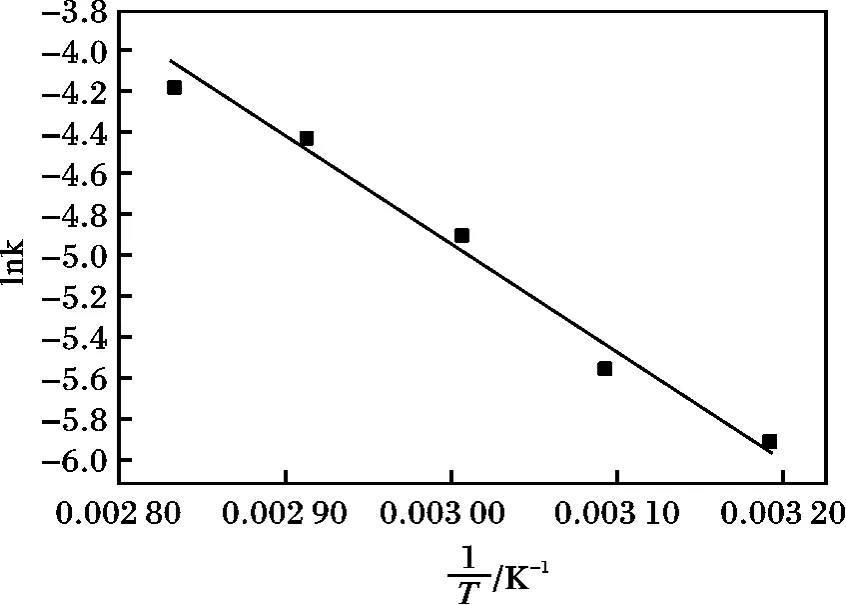
图5 反应活化能Fig.5 The activation energy of the reaction
由图5可得拟合直线方程为:y=-5 320.11x+11.02,其R2=0.96,说明拟合后的直线与实验点相关性较好。依拟合后的直线方程斜率知-Ea/R=-5 320.11,Ea=5 320.11 × R=5 320.11 ×8.31=44.23 kJ/mol,即催化氧化脱硫实验的表观活化能为44.23 kJ/mol。加氢脱硫反应的表观活化能一般为 100 ~200 kJ/mol[4],与加氢反应相比,催化氧化脱硫反应的活性更高,更具有应用价值。
3 结论
(1)催化剂Zr/ZSM-5-SBA-15的最佳制备条件为:以ZSM-5-SBA-15为载体,以ZrSO4为活性组分,500℃焙烧5 h。
(2)氧化脱硫反应的平均反应级数为1.13,说明此反应为一级反应。
(3)催化氧化脱硫实验的表观活化能为44.23 kJ/mol。催化氧化脱硫反应的活性更高,更具有应用价值。
[1] 赵丽娜.大气硫污染与脱硫技术研究现状[J].中国化工贸易,2011(7):231-236.
[2] 李志东.H2O2氧化燃料油的脱硫研究[J].科技创新与应用,2013(1):16.
[3] 唐彬,吕振荣.常减压装置汽油腐蚀指标不合格原因分析[J].炼油与化工,2010(6):31-33.
[4] 郁青春,张世超,王新东,等.CeO2/γ-Al2O3脱硫剂的制备及脱硫动力学研究[J].洁净煤技术,2007,13(3):74-77.
[5] 蔡天凤,李会鹏,赵华.Zr-ZSM-5/SBA-15催化氧化-萃取模拟油脱硫性能研究[J].石油化工高等学校学报,2013,26(2):29-33,39.
[6] 格雷格.吸附,比表面与孔隙率[M].北京:化学工业出版社,1989:304-305.
