纳米二氧化钛光催化降解染料废水动力学研究
2014-10-17张建斌田海锋左国防雷新有唐惠安
张建斌,田海锋,查 飞,左国防,雷新有,唐惠安
(1.天水师范学院生命科学与化学学院,甘肃天水 741001;2.天水师范学院新型分子材料设计与功能重点实验室,甘肃天水 741001;3.西北师范大学化学化工学院,甘肃兰州 730070)
染料生产企业由于废水浓度高、污染物复杂、排污量大等因素而受到广泛关注。加强对染料生产企业废水的处理,对保护环境、维持生态平衡、缓解水资源匮乏等有着重要的作用。目前较成熟的处理方法包括生物降解法、吸附法、混凝法、化学氧化法等[1-4]。
光催化氧化技术能有效降解染料、多环芳烃、表面活性剂、农药、氰化物等生物难降解的有机物,且具有高效节能等优点。20世纪80年代,利用TiO2光催化降解水、气环境中的污染物逐渐成为环境领域研究的热点之一[5-6]。其中,锐钛型TiO2因其高活性、高稳定性、无毒、廉价、抗光腐蚀等优点,逐渐成为理想的光催化剂。然而,由于光催化反应体系复杂,一些反应机理与动力学行为等问题尚需解决,使得这项新型污染控制技术的实用化难以大范围推广[7-10]。进一步研究其反应机理和动力学有利于改进光催化反应器的设计,可为这项新型技术的实用化奠定理论基础。
1 实验部分
1.1 试剂与仪器
TiO2、pH缓冲剂、盐酸、氢氧化钠均为分析纯;实验用废水主要来源于生产3120耐晒艳红BBC和3168B艳红RGS等染料工艺,其主要成分为4B酸(3-甲基-6-氨基苯磺酸),2B 酸(5-甲基-4-氨基-4-氯苯磺酸),CLT 酸(2-氨基-4-甲基-5-氯苯磺酸),2,3-酸(3-羟基-2-萘甲酸),吐氏酸(2-氨基-1-萘磺酸)等,废水pH 为6.8。
PHS-3C精密pH计;721-可见分光光度计;BLGHX-IV型光化学反应仪;紫外灯(254 nm);791-磁力加热搅拌器等。
1.2 实验方法
取一定浓度的染料废水50 mL,加入一定量纳米TiO2,混合均匀,置于光化学反应仪中,开启曝气搅拌装置,同时开启光源,开始计时,进行光催化氧化处理;每隔10 min取样,离心,取上清液3 mL,测其吸光度。
实验基准条件:纳米TiO2用量为2.0 g/L,染料初始质量浓度为54.8 g/L,pH 为6.8,室温,反应时间为60 min。在此基准条件下,考察了各参数变化对染料废水光催化氧化降解效果的影响,分析其动力学特性。
2 结果与讨论
2.1 染料废水浓度与吸光度的标准曲线
分别移取浓度为54.8 g/L的原废水溶液7.50,5.00,2.50,1.25,0.50 mL 于比色管中,稀释至10.00 mL,在波长480 nm处测量吸光度A,然后以A对浓度c(g/L)作图,根据图拟合得直线方程:A=0.015 8c- 0.059 6,R2=0.994 9。
2.2 光催化反应动力学特征
光催化降解反应的动力学模型较多,其中Langmuir-Hinshelwood(L-H)模型得到广泛认同,其方程式为[11-12]:

式中,r为反应物的总反应速率;c为反应物的浓度;t为反应时间;k为表观反应速率常数;K为表观吸附常数。
(1)当反应物的浓度很低时,反应动力学表现为一级反应:
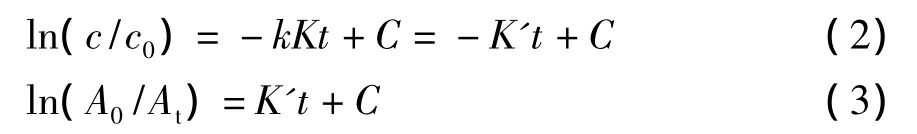
式中,K'=kK,为拟一级反应动力学常数,C为常数,A为吸光度。
(2)当反应物浓度很高时,反应动力学表现为零级反应:

若将TiO2光降解该染料废水的反应以零级反应来处理,反应速率的控制因素则主要是光照时间、光照强度以及光利用率等,与反应物初始浓度c0无关[13-14]。根据式(4),对染料吸光度A和光照时间t进行线性拟合。拟合直线见图1,拟合结果见表1。

图1 废水吸光度与光照时间的关系曲线Fig.1 Relationship curve of light application time and the absorbance of dyeing wastewater

表1 零级反应动力学拟合结果Table1 Result following zero-order reaction kinetics law

表2 一级反应动力学拟合结果Table2 Result following first-order reaction kinetics law
若将该反应以一级反应来处理,根据式(3),对ln(A0/At)和光照时间t线性拟合,拟合直线见图2,拟合结果见表2。
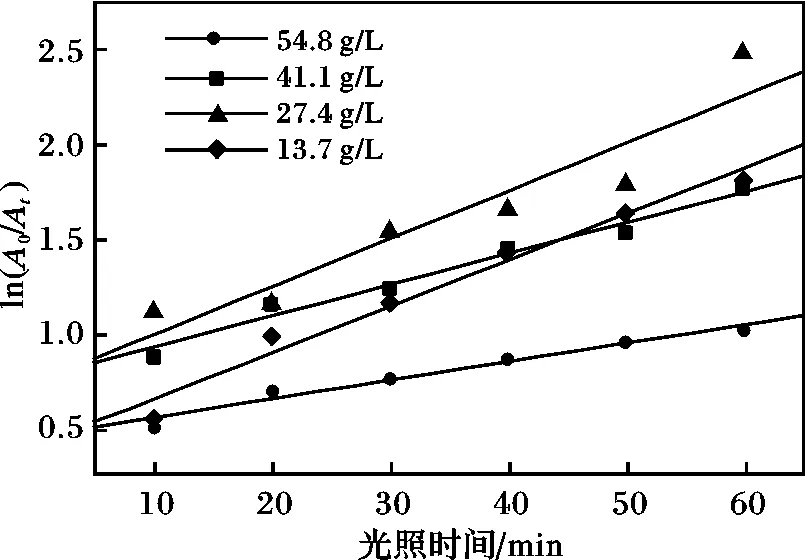
图2 ln(A0/At)与光照时间的关系曲线Fig.2 Relationship curve of light application time and the value of ln(A0/At)
比较表1和表2线性拟合方差R2值,可见采用一级反应动力学方程的模拟结果与实验数据吻合较好,表明TiO2光催化降解该染料废水的反应遵循一级反应动力学规律,反应速率主要受反应物浓度控制。
2.3 光催化氧化动力学规律
2.3.1 TiO2用量的影响 废水的起始浓度为54.8 g/L,pH 值为 6.8,改变 TiO2的添加量,光催化反应60 min,取样分析并按一级动力学方程拟合,结果见图3。

图3 ln(A0/A t)与TiO2投加量的关系曲线Fig.3 Relationship curve of TiO2 dosage on the value of ln(A0/A t)
由图3可知,当TiO2的投加量由0.5 g/L增至2.0 g/L时,废水降解的反应动力学常数K'逐渐升高,说明增大TiO2投加量有利于该染料废水的催化降解;但是当TiO2投加量超过2.0 g/L时,降解速率反而下降。这是因为当增加TiO2的用量时,催化剂表面吸附的染料分子数量增多,染料分子与催化剂颗粒表面的接触加强,电子-空穴对数量增多,反应体系中的催化活性点位增加,反应速率因而提高;然而,催化剂加量过大则会导致催化剂自身聚集,使体系浊度提高、反应体系对光的吸收减弱,从而引起反应速率下降[15-17]。本实验选择TiO2的添加量为2.0 g/L。
2.3.2 pH的影响 废水的起始浓度为54.8 g/L,TiO2的投加量为2.0 g/L,将活性艳红溶液由自然pH为6.8条件下,分别调整为3.0和8.0进行光催化降解反应,每隔10 min取样离心后取其清液测吸光度值A,并按一级动力学进行拟合,结果见图4。

图4 pH值对反应速率常数的影响Fig.4 Influence of pH on the value of ln(A0/A t)
由图4可知,当溶液的pH值为3.0时,催化剂对染料废水的处理效果最好,其一级反应动力学常数 K'为 0.009 8 min-1,是原液 pH 值为 6.8 时的1.36 倍;pH 增至 8.0 时,K'则降为 0.001 2 min-1。这表明降低染料废水pH值有利于其光催化降解。然而,实际生产中考虑到酸性废水脱酸成本较高,因而,应根据实际条件综合评价,以选择适宜的光催化pH值。
2.3.3 底物浓度的影响
2.3.3.1 底物浓度对反应速率的影响 由图2可知,当二氧化钛的投加量为2.0 g/L,pH为6.8时,改变废水的起始浓度,取样分析并按一级动力学方程拟合,结果表明,降解速率随废水起始浓度的增大而减小,当废水的起始浓度由13.7 g/L增加到54.8 g/L时,一 级 反 应 动 力 学 常 数 K'由 0.024 3 min-1降至0.009 8 min-1。这是因为当染料浓度过高时,透光率下降,光的利用率随之降低,从而使反应速率下降。在实际生产中,应从工艺的经济性角度出发,综合考虑选择适宜的反应废水起始浓度。
2.3.3.2 表观吸附常数K 将 L-H公式(1)进行变换后得到:

对1/r-1/c进行线性拟合,得到L-H动力学曲线(见图5),其中斜率为1/kK,截距为1/k。
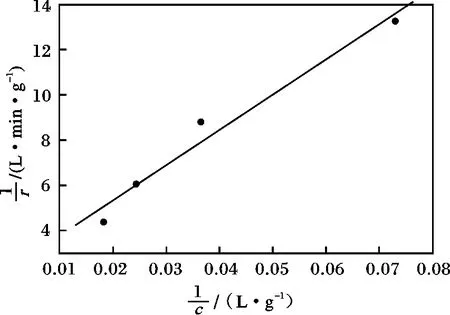
图5 L-H动力学曲线Fig.5 Kinetic curve according with Langmuir-Hinshelwood model
由图5可知,TiO2光催化降解该染料废水为表面反应,符合L-H动力学模型,其线性方程为1/r=156.37/c+2.18,R2=0.969 4,反应速率常数 k 为0.458 7 g/(L·min),表观吸附常数 K=1.39 ×10-2L/g。
3 结论
(1)采用纳米二氧化钛为催化剂,对生产3120耐晒艳红BBC和3168B艳红RGS等染料废水进行了光催化降解研究。结果表明,TiO2光催化降解该染料废水的反应为一级反应,反应规律可以用Langmuir-Hinshelwood动力学方程描述,反应速率常数k=0.458 7 g/(L·min),表观吸附常数 K=1.39 ×10-2L/g,一级反应动力学常数K'随废水起始浓度的增加而减小。
(2)溶液pH值是该降解反应速率的重要的影响因素之一,随反应体系pH值的降低,一级反应动力学常数K'增大;在一定范围内增大TiO2的添加量可以有效提高降解速率,然而催化剂过多对染料降解反而不利,适宜的投加量为2.0 g/L。
[1] Chen T,Gao B Y,Yue Q Y.Effect of dosing method and pH on color removal performance and floc-aggregation of polyferric chloride-polyamine dual-coagulant in synthetic dyeing wastewater treatment[J].Colloids and Surfaces A:Physicochemical and Engineering Spects,2010,355(1/2/3):121-129.
[2] Liu S,Wang Qun H,Ma H Z,et al.Effect of micro-bubbles on coagulation flotation process of dyeing wastewater[J].Separation and Purification Technology,2010,71(3):337-346.
[3] Zhang Lihong,Hu Chenhui,Cheng Liyuan,et al.S-doped HTiNbO5nanosheets:A novel efficient visiblelight photocatalyst[J].Chinese Journal of Catalysis,2013,34(11):2089-2097.
[4] 高玉梅,宋慧君,王非,等.复合高铁酸盐片剂的制备及对印染废水的处理研究[J].郑州大学学报:理学版,2012,44(1):107-110.
[5] 刘志强,李先国,冯丽娟.二氧化钛薄膜的改性技术研究进展[J].表面技术,2006,35(1):9-11.
[6] Senthilkumaar S,Porkodi K,Gomathi R,et al.Solegel derived silver doped nanocrystalline titania catalysed photodegradation of methylene blue from aqueous solution[J].Dyes and Pigments,2006,69(1/2):22-30.
[7] Amrit P T,Anoop V,Jotshi CK,et al.Photocatalytic degradation of direct Yellow12 dye using UV/TiO2in a shallow pond slurry reactor[J].Dyes and Pigments,2006,68(1):53-60.
[8] 陈芳,杨水金.二氧化钛光催化降解活性染料废水的研究进展[J].应用化工,2005,34(1):9-11.
[9] Tang WZ,Huang CP.Photo catalyzed oxidation pathways of 2,4-dichlorophenol by CdSin basic and acidic aqueous solutions[J].Water Research,1995,29(2):745-756.
[10]徐瑞银,王殿芳,王禹,等.用于染料废水光降解处理的催化剂及其作用机制[J].北京石油化工学院院报,2004,12(2):26-30.
[11]景晓辉,丁欣宇,喻红梅,等.纳米TiO2光催化氧化降解甲基橙动力学研究[J].印染助剂,2009,26(2):28-31.
[12]尹晓红,孙长江,辛峰,等.水溶液中TiO2对4BS染料的吸附及光催化降解动力学[J].化学工程与工艺,2008,24(4):375-379.
[13]吴辉,党炜,李成芳,等.TiO2光催化氧化亚甲基蓝的动力学研究[J].化学与生物工程,2009,26(6):36-39.
[14]张晶晶,王立敏.PMo/TiO2光催化降解甲基橙反应条件优化及动力学研究[J].精细石油化工进展,2009,10(1):23-26.
[15]贾陈忠,王焰新,张彩香,等.UV-TiO2光催化氧化降解双酚A的动力学研究[J].环境污染与防治,2009,31(11):48-52.
[16]于秀娟,王永强,孙德智,等.光催化氧化苯甲酸的动力学分析[J].哈尔滨工业大学学报,2008,40(6):861-864.
[17]姜聚慧,吕华,席国喜,等.TiO2光催化降解活性艳兰KN-R的动力学研究[J].河南师范大学学报:自然科学版,2008,36(5):93-96.
