复方当归姜汁搽剂的质量标准研究
2014-09-26潘遐陶兰萍刘汉斌
潘遐,陶兰萍,刘汉斌
(1.定西市药品检验检测中心,甘肃 定西 743000; 2.定西市第一人民医院,甘肃 定西 743000)
复方当归姜汁搽剂的质量标准研究
潘遐1*,陶兰萍1,刘汉斌2
(1.定西市药品检验检测中心,甘肃 定西 743000; 2.定西市第一人民医院,甘肃 定西 743000)
目的:建立复方当归姜汁搽剂的质量标准。方法:采用TLC鉴别制剂中当归、制何首乌;采用HPLC同时定量测定制剂中阿魏酸和二苯乙烯苷。结果:TLC能定性检出当归、制何首乌,斑点清晰,且阴性对照无干扰;阿魏酸在0.131~0.789 μg与峰面积线性关系良好(r=0.999 9),平均回收率为97.29%,RSD=0.85%;二苯乙烯苷在0.292~1.750 μg与峰面积线性关系良好(r=0.999 9),平均回收率为98.48%,RSD=1.22%。结论:所建立的定性、定量检测方法操作简便,结果准确可靠、重现性好,能有效地控制复方当归姜汁搽剂的质量。
复方当归姜汁搽剂;质量标准;薄层色谱法;高效液相色谱法;阿魏酸;二苯乙烯苷
复方当归姜汁搽剂是由甘肃省定西市第一人民医院“复方当归姜汁搽剂”课题组在民间验方组方基础上,整理改进验方剂型,采用当归、制何首乌等4味中药经提取、加工、精制研发而成。用于治疗脂溢性脱发[1],具有很好的推广应用前景。方中当归补血活血,制何首乌补益精血养须发,两药合用共为君药[2]。当归中主要成分为有机酸、丰富的氨基酸等,其中阿魏酸是较早被分离出来的主要成分之一;何首乌中主要成分为二苯乙烯苷、蒽醌类和磷脂[3]。为了有效控制复方当归姜汁搽剂质量,课题组研究采用薄层色谱法对方中当归、制何首乌进行定性鉴别,并采用高效液相色谱法同时测定本制剂中阿魏酸和二苯乙烯苷的质量浓度。
1 仪器与试药
1.1 仪器
LC-20A型高效液相色谱仪(日本岛津公司,包括LC-20AT型泵、SIL-20A型自动进样器、CTO-10ASvp型柱温箱、SPD-20A型紫外检测器、ELSD-LTⅡ型蒸发光散射检测器、CBM-20A型控制器、DGU-20A5型脱气机);U-3900H型紫外可见分光光度仪(日本日立公司);AUW220D型电子分析天平(日本岛津公司)。
1.2 试药
当归对照药材(批号:120927-200613)、何首乌对照药材(批号:120934-201009)、阿魏酸对照品(批号:110773-201012)、二苯乙烯苷对照品(批号:110844-201109)、藁本内酯对照品(批号:111737-201204),均购自中国食品药品检定研究院;薄层用硅胶G板(青岛海洋化工有限公司)。乙腈、甲醇为色谱纯;其他所用试剂为分析纯;水为屈臣氏蒸馏水。
复方当归姜汁搽剂(定西市第一人民医院“复方当归姜汁搽剂”课题组自制,批号:20110922,20110924,20110926)。
2 方法与结果
2.1 薄层色谱鉴别
2.1.1 当归的薄层色谱鉴别[2-5]取本品10 mL,置分液漏斗中,加水10 mL,加乙醚30 mL振摇提取,分取乙醚液,置水浴上,蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液。取当归对照药材0.5 g,加乙醇20 mL,超声处理10 min,滤过,滤液蒸干,残渣加乙醇1 mL溶解,作为对照药材溶液。另取阿魏酸对照品、藁本内酯对照品,加甲醇分别制成1 mg·mL-1的溶液,作为对照品溶液。取不含当归的其他处方量饮片,按制备工艺制成缺当归的阴性制剂样品,按供试品溶液制备方法制备,作为缺当归的阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录ⅥB)试验,吸取上述5种溶液各5 μL,分别点于同一硅胶G薄层板上,以正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点,而阴性对照无此斑点。见图1。
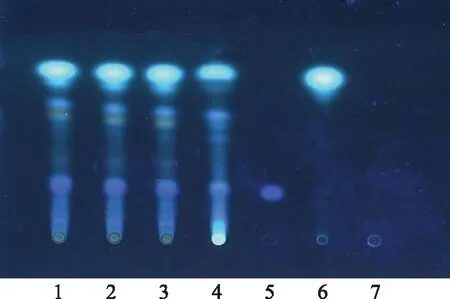
1~3.供试品 4.当归对照药材 5.阿魏酸对照品 6.藁本内酯对照品 7.缺当归的阴性对照品图1 复方当归姜汁搽剂中当归TLC图
2.1.2 何首乌薄层色谱鉴别[2-3]取本品10 mL,置水浴上,蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液。取何首乌对照药材,加乙醇10 mL,加热回流1 h,滤过,滤液浓缩至1 mL,作为对照药材溶液。取不含制何首乌的其他处方量饮片,按制备工艺制成缺制何首乌的阴性制剂样品,按供试品溶液制备方法制备,作为缺制何首乌的阴性对照溶液。照薄层色谱法(《中国药典》2010年版一部附录ⅥB)试验,吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(4∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。 供试品色谱中,在与对照药材色谱相应的位置上,显相同的黄色斑点,而阴性对照无此斑点。见图2。

1~3.供试品 4.何首乌对照药材 5.缺何首乌阴性对照品图2 复方当归姜汁搽剂中何首乌TLC图
2.2 定量测定[6-7]
2.2.1 色谱条件 phenomenexC18色谱柱(250 mm×4.6 mm,5 μm),流动相:乙腈-0.085%磷酸溶液(15∶85);检测波长:316 nm;体积流量:1.0 mL·min-1;柱温:35 ℃。理论板数按阿魏酸峰计算应不低于5 000,按二苯乙烯苷峰计算应不低于2 000。
2.2.2 对照品溶液的制备 精密称取阿魏酸对照品和二苯乙烯苷对照品适量,加70%甲醇制成阿魏酸和二苯乙烯苷质量浓度分别为65.736 μg·mL-1,145.838 μg·mL-1的混合溶液,作为混合对照品溶液。
2.2.3 供试品溶液的制备 精密量取本品溶液5 mL,置10 mL容量瓶中,加70%甲醇定容至刻度,即得供试品溶液。
2.2.4 阴性对照溶液的制备 按本品处方及制备工艺分别制备缺当归及缺制何首乌的阴性样品,照2.2.3项供试品溶液制备方法处理,即得缺当归及缺制何首乌的阴性对照溶液。
2.2.5 专属性试验 分别精密吸取混合对照品溶液、供试品溶液和阴性对照溶液各10 μL,注入液相色谱仪,按2.2.1项色谱条件进行色谱分离,记录色谱图,结果表明,在上述色谱条件下,供试品溶液中其他成分与阿魏酸、二苯乙烯苷分离良好,阴性对照色谱图中阿魏酸峰和二苯乙烯苷峰处未检测到峰,对测定结果无干扰。见图3。

A.阿魏酸和二苯乙烯苷混合对照品 B.供试品 C.缺当归的阴性对照品 D.缺何首乌的阴性对照品图3 复方当归姜汁搽剂及对照品HPLC图
2.2.6 线性关系考察 分别精密吸取上述混合对照品溶液2,4,6,8,10,12 μL,注入液相色谱仪,按2.2.1项色谱条件测定阿魏酸和二苯乙烯苷的峰面积值。以进样量为横坐标(X),峰面积分值为纵坐标(Y),绘制标准曲线,分别得阿魏酸回归方程:Y=365 546X,r=0.999 9(n=6);二苯乙烯苷回归方程:Y=303 100X,r=0.999 9(n=6)。结果表明阿魏酸在0.131~0.789 μg、二苯乙烯苷在0.292~1.750 μg与峰面积呈良好线性关系。
2.2.7 精密度试验 取2.2.2项下对照品溶液,按照2.2.1项下方法进行测定,重复进样6次,阿魏酸和二苯乙烯苷峰面积的RSD分别为0.105%和0.115%(n=6),表明方法精密度良好。
2.2.8 稳定性试验 取供试品溶液(20110922)分别于0,1,2,3,5,12,24 h各进样10 μL,记录每次进样的峰面积。结果阿魏酸和二苯乙烯苷的RSD分别为0.921%和0.779%,表明供试品溶液在24 h内稳定。
2.2.9 重复性试验 取同一批样品(20110922),照2.2.3项下方法制备供试品溶液,照2.2.1项下条件测定,重复进样6次,测得阿魏酸和二苯乙烯苷的平均质量浓度分别为0.060 mg·mL-1和0.141 mg·mL-1,RSD分别为0.874%和0.614%(n=6),表明重复性良好。
2.2.10 加样回收率试验 精密量取已知含量的同一批样品(20110922)3 mL,置10 mL量瓶中,共6份,另精密加入2.2.2项下的混合对照品溶液(阿魏酸和二苯乙烯苷质量浓度分别为65.736 μg·mL-1,145.838 μg·mL-1)3 mL,加70%甲醇定容至刻度。按2.2.1项下条件测定,计算回收率,结果见表1、2。
2.2.11 样品测定 取3批复方当归姜汁搽剂样品,按2.2.3制备成样品溶液,照2.2.1项下条件测定阿魏酸、二苯乙烯苷的质量浓度,结果见表3。

表1 复方当归姜汁搽剂中阿魏酸加样回收率测定
注:阿魏酸对照品加入量均为0.197 mg

表2 复方当归姜汁搽剂中二苯乙烯苷加样回收率测定
注:二苯乙烯苷对照品加入量均为0.438 mg

表3 复方当归姜汁搽剂中阿魏酸、二苯乙烯苷的测定(n=3)
3 讨论
3.1 展开剂选择
参照《中国药典》[2]与其他文献[4],使用正己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)展开剂进行当归的薄层鉴别,结果在供试品色谱中,在与对照品和对照药材色谱相应的位置,均显相同颜色的斑点,阴性对照均无干扰。
3.2 波长选择
通过紫外扫描可知,阿魏酸在316 nm处有最大吸收,二苯乙烯苷在320 nm处有最大吸收。结合HPLC将混合对照品在不同波长进行测定,发现在316 nm波长处阿魏酸、二苯乙烯苷的理论塔板数最大,分别为21 596、18 574,且分离度最大为5.804。综合考虑,故选择316 nm作为检测波长。
3.3 流动相的选择
参照《中国药典》[2],通过改变流动相比例能达到同时分离两种成分的目的,最后确定最佳配比乙腈-0.085%磷酸(15∶85)为流动相。分离效果较好,色谱图形对称且尖锐,拖尾因子分别为1.026、1.033,重复性强。
3.4 方法评价
实验所建立的定性、定量检测方法操作简便,结果准确可靠、重现性好,能有效地控制复方当归姜汁搽剂的质量。
[1] 龙倡达,张桂林,李绍兴,等.中药归乌合剂治疗斑秃疗效观察[J].中华皮肤科杂志,2000,33(2):130.
[2] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:124,164.
[3] 肖培根,新编中药志[M].第一卷.北京:化学工业出版社,2001:425,518.
[4] 华永丽,郭延生,杨洪申,等.酒当归饮片质量标准研究[J].中成药,2010,32(10):1724-1729.
[5] 胡杰,冯丽莉,崔福德.当归川芎中阿魏酸提取的研究[J].时珍国医国药,2004,15(11):732-733.
[6] 班翊,刘其礼,金悠,等.二苯乙烯苷的稳定性研究[J].中草药,2004,35(11):1235-1237.
[7] 张纯,杨少麟,袁海龙,等.高效液相色谱法测定何首乌中二苯乙烯甙的含量及其稳定性考察[J].中国中药杂志,1999,24(6):357-359.
QualityStandadforDangguiGingerLiniment
PAN Xia1,*,TAO Lanping1,LIU Hanbin2
(1.TheTestingCenterforDrugofDingxiCity,Gansu743000,China; 2.TheFirstPeople’sHospitalofDingxiCity,Gansu743000,China)
Objective:To establish the quality standard for Danggui Ginger Liniment.Methods:Angelica sinensis radix and Polygoni multiflori preparata radix identified by TLC,the contents of ferulic acid and stilbene glycoside were determined by HPLC.Results:The relevant spots on TLC plates were clear without any interference by the blank reference;The content of ferulic acid showed a good linearity in the range of 0.131~0.789 μg(r=0.999 9).The average recovery rate was 97.29%,RSD was 0.85%,the content of stilbene glycoside showed a good linearity in the range of 0.292-1.750 μg (r=0.999 9).The average recovery rate was 98.48%,RSD was 1.22%.Conclusion:Established qualitative and quantitative methods were simple,accurate,reliable and reproducible,and can be effectively used as the quality standard of Danggui Ginger Liniment.
Danggui Ginger Liniment;Quality standard;TLC;HPLC;Ferulic acid;Stilbene
10.13313/j.issn.1673-4890.2014.08.012
2014-01-14)
*
潘遐,主管药师,研究方向:中成药、中药材检测分析;E-mail:panxia0932@163.com
glycoside
