哌嗪的氨基酸缀合物的合成、表征及抑菌活性研究
2014-09-18付晓磊赵春晖崔洪光杨君微张翼轩赵龙铉
付晓磊,赵春晖,崔洪光,杨君微,张翼轩,赵龙铉,,*
(1. 辽宁师范大学 化学化工学院,辽宁 大连 116029;2. 辽宁师范大学 生物技术与分子药物研发辽宁省重点实验室,辽宁大连 116029;3. 大连大学 环境与化学工程学院,辽宁 大连 116622)
0 引言
哌嗪环是药物研发中常用的碱性基团,易形成氢键或离子键,能有效调节药物的脂水分配系数和酸碱平衡常数,将其引入分子,能有效地增加分子的碱性和水溶性,进而显示出更好的生物活性[1]。由于取代基的基团、位置及连接方式的不同,哌嗪类化合物显示出了广泛的药理活性[2],如抗菌、抗氧化、抗肿瘤、治疗阿尔茨海默病等[3-6]。在合成药物方面,主要有吡酮酸(俗称喹诺酮)类抗生素[7],利福霉素类抗生素[8],驱肠虫药等[9]。
氨基酸具有良好的生物相容性和亲和性,无免疫源性,对人体无不良反应。将其引入药物分子进行偶联,不但可以促进细胞对药物的吸收,增强药物的溶解度,而且有利于降低药物的毒性。Ruchi[10]等通过哌嗪双取代物与O,O-二乙基氯代磷酸盐反应得到相应的哌嗪双取代衍生物,其中的 1,4-二(4-氯苯烯基)哌嗪二缩氨基硫脲和 1,4-二(4-甲基苯烯基)哌嗪二缩氨基硫脲有明显的抗真菌活性。Robert[11]等研究发现,一些哌嗪的双取代醇类、酮类、烷基类化合物对疟疾有显著的抑制作用。胡国强等[12]设计并合成了一系列的双取代哌嗪衍生物,发现其有良好的抗菌活性。
因此,根据药物设计原理中的拼合原理,我们设计合成了一系列哌嗪的氨基酸双取代化合物,然后对目标产物进行了野生型大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus)抑菌活性测试。合成路线如图1所示。
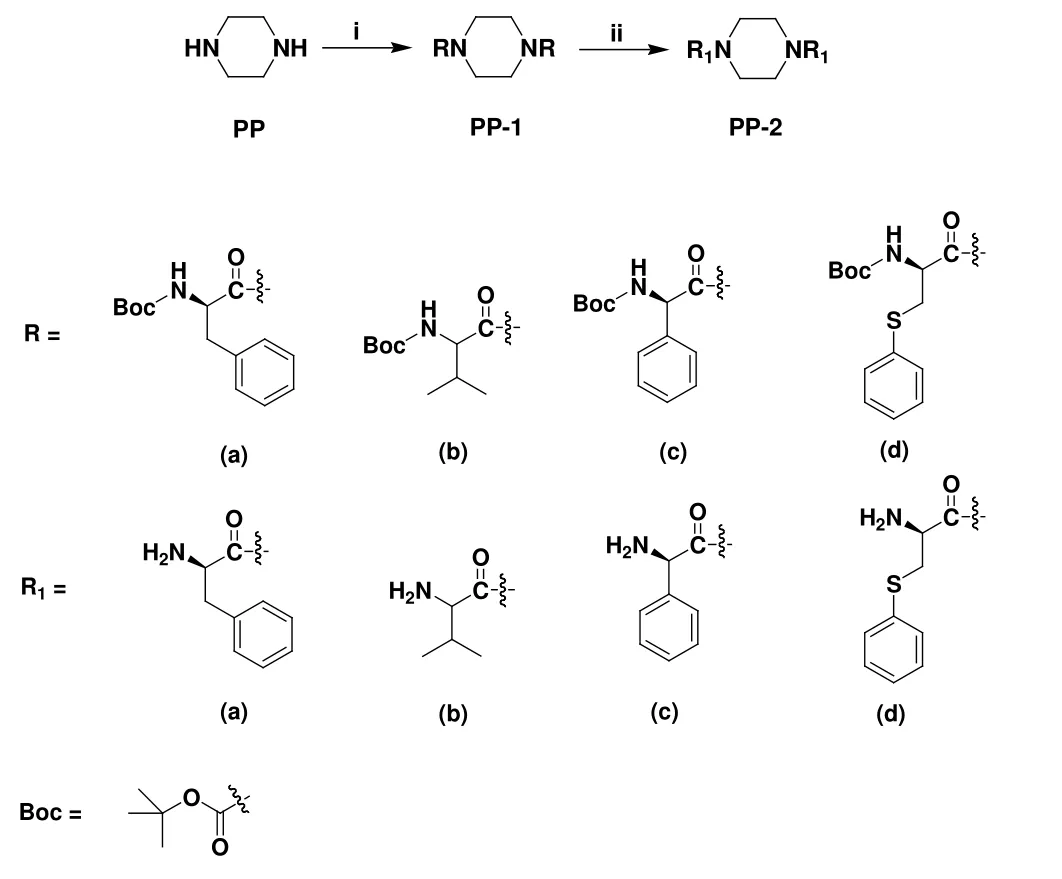
图1 哌嗪的氨基酸缀合物的合成路线
1 实验部分
1.1 仪器和试剂
WGH-30双光束红外分光光度计,KBr压片;BRUKER-500MHz核磁共振仪,CDCl3为溶剂;X-5显微熔点测定仪(控温型),温度未经校正;Multiskan Ascent酶标仪。所用的试剂均为国产分析纯或化学纯。
菌种:野生型大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus)。
1.2 PP-1a的合成和表征
在 100 mL圆底烧瓶中,将 PP(50 mg, 0.58 mmol)、Boc-Phe-OH(327 mg, 1.28 mmol)、DMAP(142 mg, 1.16 mmol)的 CH2Cl2(7 mL)溶液液冷却到 0℃,把 EDCI(223 mg,1.16 mmol)的 CH2Cl2(3 mL)溶液在搅拌下逐滴加入反应瓶中,滴加完毕后再在0℃条件下搅拌5 min,室温下搅拌5 h,反应完毕后,用水和CH2Cl2对反应混合物进行萃取,并用饱和NaCl溶液洗涤,有机相用无水硫酸镁干燥,过滤,减压蒸馏除去溶剂得粗产品,再用乙酸乙酯/石油醚(3:2, V:V)作洗脱剂进行加压柱层析,分离得白色固体PP-1a: 1,4-双-(N-叔丁氧羰基苯丙氨酰基)哌嗪。产量:236 mg,产率:70%,熔点:215.2~217.7 ℃; IR(KBr): 3445,3275, 2969, 1701, 1631, 1536, 1442, 1297, 1223, 1162 cm-1;1H NMR (500MHz, CDCl3):δ7.29-7.15(m, 10H,10×Ph-H), 5.34-5.31(m, 2H, 2×-NH-), 4.78-4.73(m, 1H,-COCHNH-), 4.69-4.64(m, 1H, -COCHNH-), 3.55(d,J=10.3 Hz 1H, piperazine CH), 3.29(brs, 1H, piperazine CH), 3.19(brs, 1H, piperazine CH), 3.10(d,J=9.7 Hz 1H, piperazine CH), 3.01-2.96(m, 2H, piperazine CH2),2.90-2.85(m, 2H, Ph-CH2-), 2.74-2.73(m, 2H,piperazine CH2), 1.46(s, 9H, (CH3)3CO-), 1.45(s, 9H,(CH3)3CO-)。
1.3 PP-1b的合成和表征
按照合成PP-1a的实验方法由化合物PP(50 mg,0.58 mmol)和 Boc-Val-OH(278 mg,1.28 mmol)反应得到了白色固体PP-1b: 1,4-双-(N-叔丁氧羰基缬氨酰基)哌嗪。产量:234 mg,产率:83.2%,熔点:>300℃;IR(KBr): 3438, 3323, 2975, 1701, 1638, 1516, 1442,1237, 1169 cm-1;1H NMR(500 MHz, CDCl3):δ5.25(d,J=9.2 Hz, 2H, 2×-NH-), 4.42(d,J=5.8 Hz, 2H,2×-COCH NH-), 3.89-3.37(m, 8H, 4×piperazine CH2),1.96-1.90(m, 2H, 2×(CH3)2CH-), 1.44(s, 18H, 2×(CH3)3CO-), 0.95(d,J=6.1Hz, 6H, (CH3)2CH-), 0.90(d,J=6.8Hz, 6H, (CH3)2CH-)。
1.4 PP-1c的合成和表征
按照合成PP-1a的实验方法由化合物PP(50 mg,0.58 mmol)和 Boc-D-Phg-OH(322 mg,1.28 mmol)反应得到了白色固体PP-1c: 1,4-双-(N-叔丁氧羰基苯甘氨酰基)哌嗪。产量:240 mg,产率:75%,熔点:115.3~117.9 ℃; IR(KBr): 3426, 3305, 2915, 1712,1550, 1436, 1285, 1249, 1120 cm-1;1H NMR(500MHz,CDCl3):δ7.34-7.30(m, 10H, 10×Ph-H), 5.90(d,J=6.5 Hz 2H, 2×Ph-CH-NH-), 5.52(d,J=6.5 Hz 1H, Ph-CHNH-), 5.38(d,J=6.5 Hz 1H, Ph-CH-NH-), 3.99(d,J=9.8 Hz 1H, piperazine CH), 3.54(brs, 1H, piperazine CH),3.43(brs, 1H, piperazine CH), 3.17-3.13(m, 4H,2×piperazine CH2), 2.56(d,J=9.8 Hz 1H, piperazine CH), 1.39(s, 18H, 2×(CH3)3CO-)。
1.5 PP-1d的合成和表征
按照合成PP-1a的实验方法由化合物PP(50 mg,0.58 mmol)和 Boc-PDC(380 mg,1.28 mmol)反应得到了白色固体PP-1d: 1,4-双-(N-叔丁氧羰基苯硫丙氨酰基)哌嗪。产量:340 mg,产率:90.9%,熔点:57.1~59.9 ℃; IR(KBr): 3445, 3298, 2945, 1706, 1649,1576, 1474, 1260, 1115 cm-1;1H NMR(400 MHz,CDCl3):δ7.40-7.20(m, 10H, 10×Ph-H), 5.39-5.36(m,2H, 2×-NH-), 4.78-4.74(m, 2H, 2×-CH-NH-), 3.47-3.13(m, 12H, 2×-S-CH2- and 4×piperazine CH2), 1.44(s,9H, (CH3)3CO-), 1.43(s, 9H, (CH3)3CO-)。
1.6 PP-2a的合成和表征
在冰浴搅拌条件下,将 TFA(0.38 mL)逐滴加入到 PP-1a(100 mg,0.17 mmol)的 CH2Cl2(3 mL)溶液中,室温下反应2 h。反应完毕后,减压蒸馏除去溶剂,剩余液体用氨水调节pH至碱性,用水和CH2Cl2对反应混合物进行萃取,有机相用无水硫酸镁干燥,过滤,减压蒸馏除去溶剂得粗产品,再用甲醇/二氯甲烷(1:10, V:V)作洗脱剂进行加压柱层析,分离得白色固体PP-2a: 1,4-双-(苯丙氨酰基)哌嗪。产量:52 mg,产率:80%,熔点:112.5~113.4℃; IR(KBr): 3525, 3393,2948, 1715, 1540, 1430, 1268, 1156 cm-1;1H NMR(500 MHz, DMSO-d6):δ7.28-7.15(m, 10H, 2×Ph-), 3.92-3.88(m, 2H, 2×NH2-CH-), 3.44-3.13(m, 8H, 4×piperazine CH2), 3.05-2.94(m, 4H, 2×Ph-CH2-), 2.80-2.69(m, 4H, 2×NH2-)。
1.7 PP-2b的合成和表征
按照合成PP-2a的实验方法由化合物PP-1b(100 mg, 0.21 mmol)反应得到了白色固体PP-2b: 1,4-双-(缬氨酰基)哌嗪。产量:50 mg,产率:84.7%,熔点:110.2~112.0 ℃; IR(KBr): 3526, 3331, 2950, 1685,1237, 1146cm-1;1H NMR(400MHz, CDCl3):δ3.82-3.46(m, 10H, 2×-COCHNH2, 4×piperazine CH2), 1.92-1.84(m, 2H, 2×(CH3)2CH-), 1.29(brs, 2H, 2×NH2-),1.00(d,J=6.8Hz, 6H, (CH3)2CH-), 0.93(d,J=6.4Hz, 6H,(CH3)2CH-)。
1.8 PP-2c的合成和表征
按照合成PP-2a的实验方法由化合物PP-1c(100 mg,0.21 mmol)反应得到了白色固体PP-2c: 1,4-双-(苯甘氨酰基)哌嗪。产量:51 mg,产率:80.6%,熔点:104.7~106.7 ℃; IR(KBr): 3513, 3343, 2926, 1638,1515, 1448, 1223, 1189 cm-1;1HNMR (400 MHz,CD3OD):δ7.39-7.34(m, 10H, 10×Ph-H), 4.98-4.80(m,2H, 2×Ph-CH-), 3.75(d,J=12.0 Hz 1H, piperazine CH),3.53-3.48(m, 2H, piperazine CH2), 3.37-3.35(m, 1H,piperazine CH), 3.20-3.13(m, 2H, piperazine CH2),3.06-3.03(m, 1H, piperazine CH), 2.84(d,J=12.0 Hz 1H,piperazine CH)。
1.9 PP-2d的合成和表征
按照合成PP-2a的实验方法由化合物PP-1d(150 mg, 0.23 mmol)反应得到了白色油状固体 PP-2d:1,4-双-(苯硫丙氨酰基)哌嗪。产量:72 mg,产率:70.5%; IR(KBr): 3580, 3364, 2903, 1713, 1524, 1496,1256, 1102 cm-1;1HNMR(500 MHz, DMSO-d6):δ7.36-7.17(m, 10H, 10×Ph-H), 3.79(brs, 2H, 2×NH2-CH-), 3.48-3.34(m, 8H, 4×piperazine CH2), 3.16(dd,J=13.3 Hz, 7.2Hz, 2H, Ph-S-CH2-), 3.02(dd,J=13.3 Hz,7.2 Hz, 2H, Ph-S-CH2-), 2.01(brs, 4H, 2×NH2-)。
2 哌嗪的氨基酸缀合物的抑菌活性测试
2.1 菌种培养
分别取3 L的野生型大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus)接种于两支含有3 mL LB液体培养基的试管中,过夜活化。取活化后的菌液各5 L,分别加入两支含有5 mL的LB液体培养基中,摇2 h20 min,使用血球计数板记录两种菌数,用LB液体培养基稀释到1×106CFU/mL备用。
2.2 抑菌实验
(1) 化合物的配制:将化合物用 DMSO 溶解为10 mg/mL,再用LB液体培养基稀释成为1.5 mg/mL。
(2) TTC的称取:快速称取TTC于棕色试剂瓶中,用ddH2O溶解为4%浓度的溶液,使用0.22 L的滤膜滤菌,再用无菌LB液体培养基稀释成0.5%的溶液(避光保存)。
(3) 抗菌实验:取出96孔板,向第B-G行均加入50 L LB液体培养基;向A、B行加50 L化合物,每种化合物两个平行;用排枪从 B-G行梯度稀释,使得A-G的浓度依次为0.75 mg/mL,0.375 mg/mL,0.188 mg/mL,0.094 mg/mL,0.047 mg/mL,0.023 mg/mL,0.012 mg/mL。向所有孔中加入 50 L菌液(1×106CFU/mL ),混匀后每孔加入10 L 0.5%TTC;其中需做Amp阳性对照及不加抗菌肽的阴性对照。
(4) 过夜孵育:将加完样的 96孔板放于酶标仪上震动1 min,使各孔溶液混匀,放入37 ℃培养箱孵育14 h。用肉眼观察孔内颜色变化(有菌生长则呈现红色,无菌生长则无颜色变化),并使用酶标仪在OD492时测量MIC值。
2.3 实验结果
我们通过对所合成的目标化合物进行抑菌活性测试,得到化合物在浓度范围0.012~0.75 mg/mL时对E. coli和S. a的抑制作用曲线,如图2、图3所示。根据抑菌作用曲线,总结 8个哌嗪氨基酸缀合物对E. coli和S. a的抑菌效果,如表1所示。

图2 化合物在浓度范围0.012-0.75时对E. coli的抑制作用
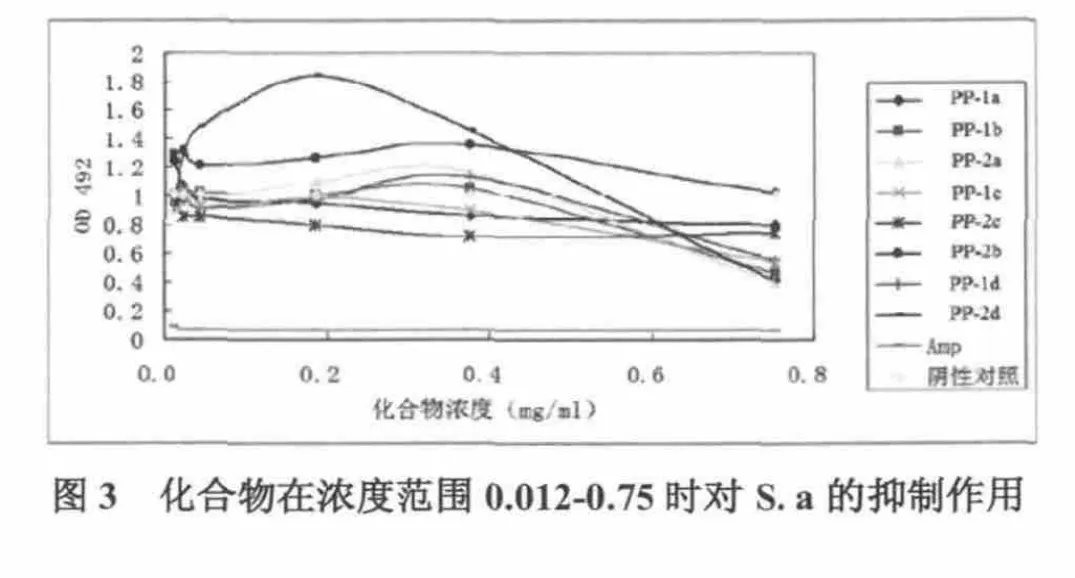
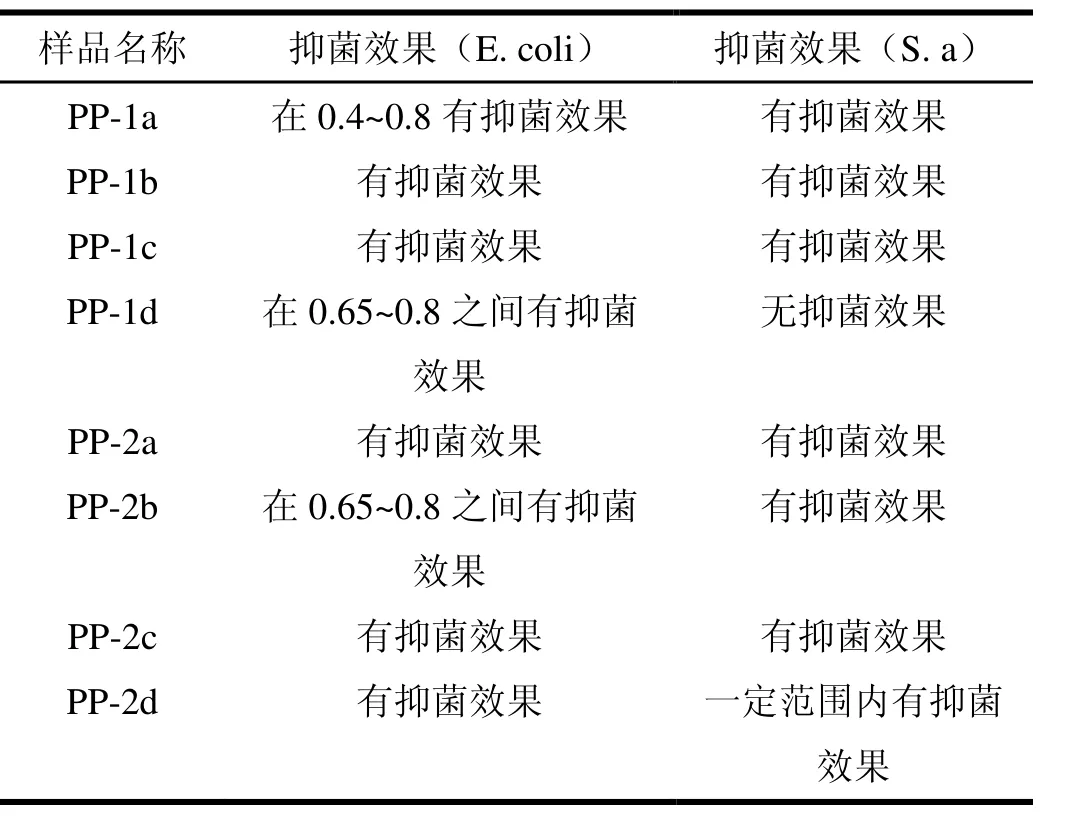
表1 化合物在浓度范围0.012~0.75 mg/mL时对E. coli、S. a的抑制作用
3 结果与讨论
我们做了以下工作:(1)首先以哌嗪为起始原料,在哌嗪N-1和N-4位导入氨基被保护的氨基酸,(2)在CH2Cl2溶剂中、在TFA作用下,打掉氨基的Boc保护基,得到8个哌嗪的氨基酸缀合物。
从以上图、表中可以看出,化合物PP-1b、PP-2a、PP-1c、PP-2c、PP-2d对E. coli具有抑菌效果,并且抑菌作用随化合物浓度的升高而增强;PP-1a在0.4~0.8 mg/mL具有抑菌效果,作用效果较弱;PP-2b、PP-1d在0.65~0.8 mg/mL具有抑菌效果,作用效果较弱。化合物 PP-1a、PP-2a、PP-1b、PP-2b、PP-1c、PP-2c、PP-2d对S. a具有一定的抑菌效果并且抑菌作用随化合物浓度的升高增强;PP-1d在 0.012~0.75 mg/mL浓度间不具有抑菌效果。
4 结论
本文以哌嗪为起始原料,在DMAP为催化剂、EDCI为脱水剂条件下,与一系列氨基被保护的氨基酸进行偶联,再在三氟乙酸条件下脱去Boc保护基,共设计合成了8种未见报道的哌嗪氨基酸缀合物,利用IR和1H NMR波谱技术对其结构进行了表征。然后对目标产物进行了野生型大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus)抑菌活性测试。结果表明化合物 PP-1a、PP-2a、PP-1b、PP-2b、PP-1c、PP-2c、PP-2d对Staphylococcus aureus具有一定的抑菌效果并且抑菌作用随化合物浓度的升高增强。
[1]甘淋玲, 卢一卉, 周合成. 哌嗪化合物作为酶抑制剂的研究进展[J]. 中国生化药物杂志,, 2009, 30(2): 127-130.
[2]农娟, 农克良, 郑广进. 哌嗪类化合物的研究进展[J]. 化工技术与开发, 2012, 41(2): 24-27.
[3]SOLOMON V R, HU C, LEE H. Design and synthesis of anti-breast cancer agents from 4-piperazinylquinoline: A hybird pharmacoghore approach[J]. Bioorg. Med. Chem.,2010, 18(4): 1563-1572.
[4]KIMURA M, MASUDA T, YAMADA K, et al. Antioxidative activitives of novel diphenylalkyl piperazine derivatives with high affinities for the dopamine transporter [J]. Bioorg. Med.Chem. Lett., 2004, 14(16): 4287-4290.
[5]SHAPIRO L A, OFFORD S J, ORDWAY G A. The effect of chronic treatment with a novel aryl-piperazine antipsychotic on monoamine receptors in rat brain [J]. Brain Research,1995, 677(2): 250-256.
[6]YANG C, XU G, LI J, et al. Benzothiophenes containing a piperazine side chain as selective ligands for the estrogen receptor and their bioactivities in vivo[J]. Bioorg. Med. Chem.Lett., 2005, 15(5): 1505-1507.
[7]SHAH PM. Re: C. Schellhorn: Classification of quinolones by V. andriole [J]. Infection, 1998, 26(4): 255.
[8]王文祥, 刘洪杰. 哌嗪的合成与应用[J]. 河南化工,1995(7): 28-30.
[9]贺以乐. 哌嗪的合成应用及市场趋势[J]. 化工中间体,2002, 10: 3-5.
[10]CHANDRA R, PANDEY O P, SENGUPTA S K.Organophosphorus derivatives containing piperazine dithiosemicarbazones as chemotherapeutants against fungal pathogens of sugarcane[J]. J Agric. Food Chem., 2005, 53(6):2181-2184.
[11]LUTZ R E, SHEARER N H. Antimalarials some piperazine derivatives[J]. J Org. Chem., 1947, 12(6): 771-775.
[12]胡国强, 许秋菊, 张中泉, 等. 1,4-双[(5-芳基-1,3,4-噁二唑-2-)亚甲基]哌嗪的合成及其抗菌活性[J]. 中国药物化学杂志, 2004, 14(2): 76-79.
