人参首乌胶囊制备工艺的研究
2014-09-18魏宇峰周国儿
魏宇峰,周国儿
(舟山医院 药剂科,浙江 舟山 316000)
人参首乌胶囊制备工艺的研究
魏宇峰,周国儿
(舟山医院 药剂科,浙江 舟山 316000)
目的优选人参首乌胶囊回流制备工艺。比较回流提取、渗漉提取对人参首乌胶囊有效成分的影响。方法按正交实验设计,高效液相色谱法(high performance liquid chromatography,HPLC)测定人参皂苷Rg1、二苯乙烯苷含量,以人参皂苷Rg1和二苯乙烯苷综合转移率(1∶1)为指标,分别考察了乙醇浓度(%)、乙醇用量(倍)、提取时间、提取次数(次)对回流提取的影响;比较了回流提取与渗漉提取的优劣。结果最优提取方法为8倍50%乙醇加热回流提取1次,每次1.5 h。结论该制备方法简便、可行、稳定性高,为工业生产提供依据。
人参皂苷Rg1;二苯乙烯苷;正交实验;高效液相色谱法;超声提取;回流提取
1.2 方法
1.2.1 HPLC测定人参皂苷Rg1的含量 按处方比例,精密称取红参药材粉末(过二号筛)12 g、制何首乌药材粉末18 g,按照文献方法进行测定[5]。色谱柱:岛津SPD-20AC18(4.0mm×200mm,5μm)柱,柱温 35℃;流动相:乙腈:0.05%磷酸溶液(19∶81);流速为 1.2 mL/min;检测波长为 203 nm;进样量20μL。得到对照品、供试品和阴性图。
1.2.2 HPLC测定二苯乙烯苷的含量 按处方比例,精密称取红参药材粉末(过二号筛)12 g、制何首乌药材粉末18 g,按照药典方法制备溶液进行含量测定[1]。色谱柱:岛津 SPD-20AC18(4.0mm×200mm,5μm)柱,柱温25℃;流动相:乙腈∶水(20∶80);流速为 1 mL/min;检测波长为 320 nm;进样量20μL。得到对照品、供试品和阴性图。
1.2.3 回流提取实验 根据回流提取的预实验结果,以乙醇浓度A(%)、乙醇用量B(倍)、提取时间C、提取次数D(次)为影响因素,以人参皂苷Rg1和二苯乙烯苷转移率(%)为综合指标,进行 L9(34)正交实验设计(见表1)。
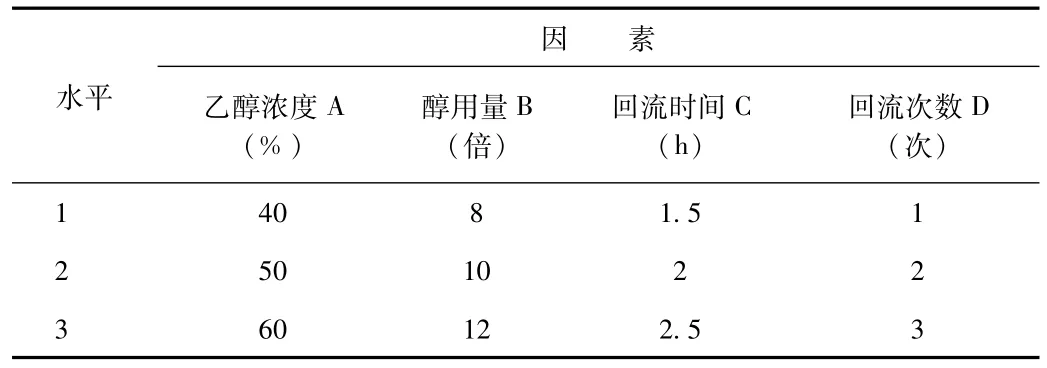
表1 回流提取实验因素水平Tab.1 The orthogonal factor level of refluxing
1.2.4 验证实验 按处方比例,精密称取红参药材粉末(过二号筛)12 g、制何首乌药材粉末18 g,按照2.1、2.2项下制备,进样检测,记录回流提取转移率。按照药典中记录渗漉法制备,进样检测,记录转移率,结果与回流提取转移率做比较。
2 结果
2.1 HPLC测定人参皂苷Rg1的含量 按照2.1项下方法制备得到人参皂苷Rg1对照品、供试品和阴性如图1~3所示。结果表明阴性无干扰,分离度良好。

图1 人参皂苷Rg1对照品HPLC图谱Fig.1 The control article of Ginsenoside Rg1

图2 供试品HPLC图谱Fig.2 The sample of Ginsenoside Rg1
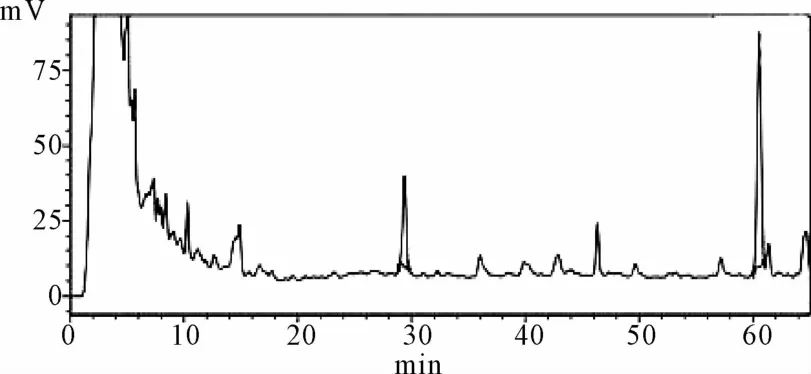
图3 阴性样品HPLC图谱Fig.3 The negative of Ginsenoside Rg1
2.2 HPLC测定二苯乙烯苷的含量 按照2.2项下方法制备样品进样,得到对照品、供试品和阴性如图4~6所示。

图4 二苯乙烯苷对照品HPLC图谱Fig.4 The control article of Stilbene glycoside
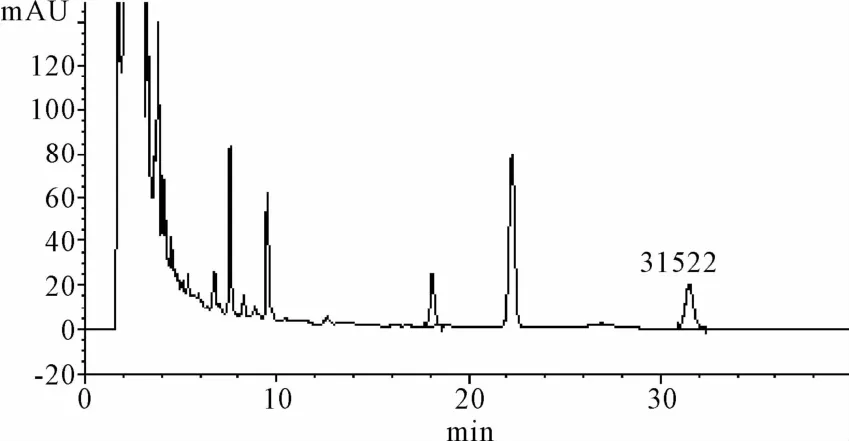
图5 二苯乙烯苷供试品HPLC图谱Fig.5 The sample of Stilbene glycoside
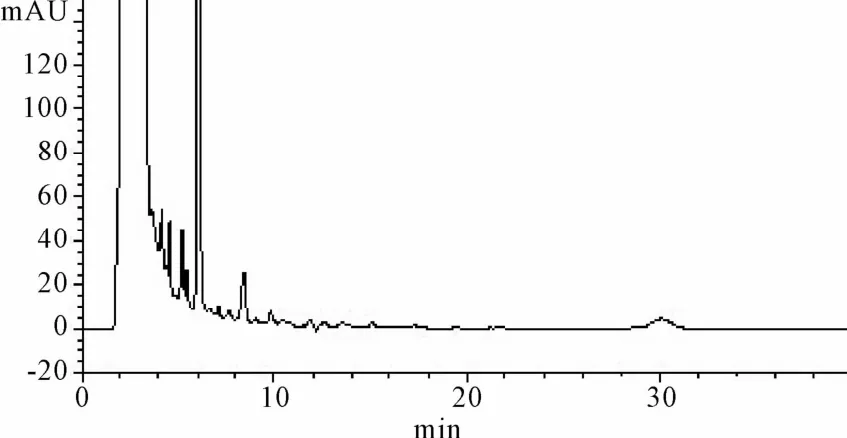
图6 二苯乙烯苷阴性样品HPLC图谱Fig.6 The negative of Stilbene glycoside
2.3 回流提取实验 回流提取正交实验结果如表2-3所示。

表2 回流提取实验结果Tab.2 The orthogonal experimental results of refluxing
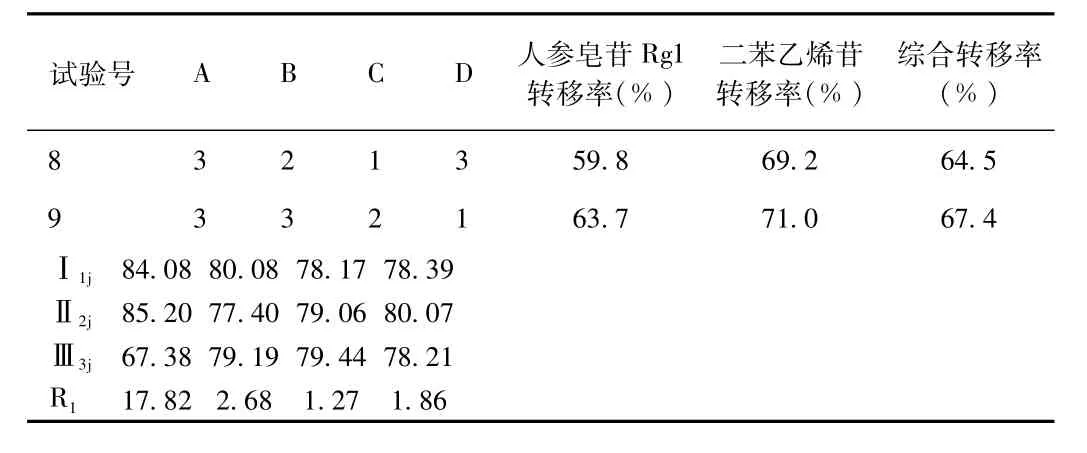
续表
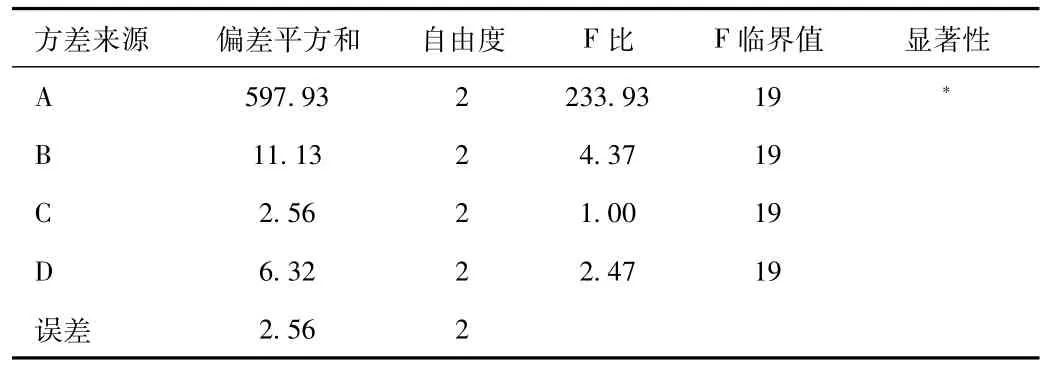
表3 回流提取方差分析表Tab.3 The analysis of variance table of refluxing
由表2、3的结果可见,同样以人参皂苷Rg1和二苯乙烯苷综合转移率(%)为评价指标,乙醇浓度A对提取(P>0.05),B、C、D(P<0.05),说明A对含量有显著性影响,根据直观分析得最佳提取工艺为A2B1C3D2,由于B、C对提取工艺并非主要因素,综合考虑成本和效益,最终确定最佳提取条件为A2B1C1D1,即8倍50%乙醇加热回流提取1次,每次1.5 h。
2.4 验证实验 渗漉提取和回流提取结果如表4所示。
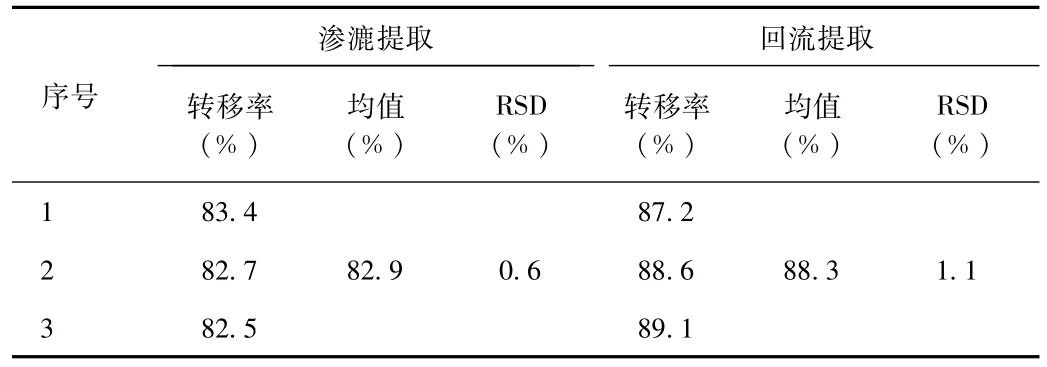
表4 验证实验Tab.4 The verification experiment
由表可知,回流提取的人参皂苷Rg1和二苯乙烯苷转移率(%)明显高于渗漉提取,并且对于工业生产而言,渗漉提取时间较长,因此,人参首乌胶囊最优提取方法为:8倍50%乙醇加热回流提取1次,每次1.5 h。
2.5 实验小结 本实验综合运用了正交实验设计、综合加权法、HPLC法,以人参皂苷Rg1和二苯乙烯苷综合转移率(人参皂苷Rg1转移率:二苯乙烯苷转移率=1∶1)为指标,分别考察了乙醇浓度(%)、乙醇用量(倍)、提取时间、提取D(次)对回流提取的影响。结果表明,最优回流提取法为8倍50%乙醇加热回流提取1次,每次1.5 h。
实验中比较了回流提取和传统的渗漉提取法,最终的实验证明回流提取明显优于渗漉提取,并且提取周期短,更加适合工业大生产。
3 讨论
人参主要含有人参皂苷、人参多糖、人参蛋白等成分。其中,人参皂苷为主要活性物质,很多文献均以人参皂苷的含量作为判断人参质量和疗效的主要指标[5-9]。人参皂皂主要含有人参皂苷Rg1、Re等,其中,由于人参皂苷Re不稳定,测定过程中发生降解[10-11],人参皂苷Rg1含量高,性质稳定,并且药典中也以其作为定量成分。因此,本实验中选择了人参皂苷Rg1的含量作为指标判断提取方法的优劣。
综合加权评分法是将多指标试验的结果,根据各项试验指标在整个试验中的重要性,确定出其所占的权重,将多指标的实验结果化为单指标的实验结果[12]。它更适应多指标的评价。2010版药典中记载的人参首乌胶囊为渗漉法,渗漉法适用于有效成分遇热不稳定或含大量淀粉、树胶、果胶、粘液质的中药,但常温下需不断向粉碎中药材中添加新鲜溶剂,消耗溶剂量大、费时、操作麻烦,而回流提取省溶剂,操作简单,可以有效的缩短制备时间,进而降低成本[13-15]。
[1]中国药典一部[S].北京:中国医药科技出版社,2010:439.
[2]李芳,雷建林,张抗怀.HPLC法测定愈伤灵胶囊中人参皂苷Rg1的含量[J].西北药学杂志,2006,21(6):246-247.
[3]王哲华.HPLC法测定人参首乌精的含量[J].牡丹江医学院学报,2003,24(2):27-29.
[4]李玉芳,和玄华.何首乌现代研究进展[J].中成药,1997,19(5):37-38.
[5]易运辉.人参首乌胶囊中人参皂苷Rg1的含量测定[J].中国实用医药,2008,3(25):40-41.
[6]吉丽娜,冯伟红,王智民,等.HPLC-DAD测定人参首乌胶囊中8种人参皂苷类成分[J].中国中药杂志,2013,38(17):2798-2802.
[7]李静,林晓,高辉.HPLC-ELSD法测定阿胶补血口服液中黄芪甲苷的含量[J].齐鲁药事,2011,30(5):269-270.
[8]丘明明.HPLC-ELSD法测定三七血伤宁胶囊中三七皂苷R1、人参皂苷 Rg1和 Rb1的含量[J].药物分析杂志,2010,30(4):629-932.
[9]闫天午,宋承吉,杜秀娟,等.人参首乌精中人参皂甙含量测定[J].中成药,1993,15(11):14-15.
[10]周迎春,赵怀清,梁宁,等.高效液相色谱法同时测定三七总皂苷中人参皂苷Rg1,Re,Rb1与三七皂苷R1含量[J].沈阳药科大学学报,2003,20(1):27-31.
[11]潘桂湘,高秀梅,张伯礼.HPLC测定复方丹参方中三七皂苷类成分的含量[J].中药新药与临床药理,2003,14(2):112-114.
[12]陶菊春,吴建民.综合加权评分法的综合权重确定新探[J].系统工程理论与实践,2001,8(8):43-48.
[13]谭朝阳,尤昭玲,袁宏佳.三七渗漉提取工艺的研究[J].中国中药信息杂志,2010,17(4):51-52.
[14]王生瑶.连续逆流提取工艺的设备及其应用[J].应用能源技术,2007(2):18-20.
[15]黄伟,孙蓉,张作平.益母草不同炮制品的小鼠急性毒性实验研究[J].中国药物警戒,2010,7(2):65-69.
(编校:李璐璐)
Study on the preparation process of Radix Ginseng Capsules
WEIYu-feng,ZHOU Guo-er
(Department of Pharmacy,Zhoushan Hospital,Zhoushan 316000,China)
ObjectiveTo screen and optimize the preparation process of Radix Ginseng Capsules.This paper compares the reflux extraction and effects of infiltration percolation extraction to the renshenshouwu capsules.MethodsBased on the Orthogonal test,the content of ginsenosides Rg1 and Stilbene glycoside weremeasured by HPLC.The transferring rates of ginsenosides Rg1 and Stilbene glycoside(1:1)were regarded as the index to evaluate extracting conditions,such as the ethanol concentration(%),consumption of alcohol(times),extraction time and extraction times(times).ResultsThe optimum extract conditions of ginsenosides Rg1 and Stilbene glycoside are:with 8 times volume of50%concentration ethanol as the extract liquid,to refluxing extract1 times,1.5 h every time.ConclusionThe preparation method is simple,practical,high stability and provides the basis for industrial production.
Ginsenosides Rg1;Stilbene glycoside;orthogonal experiment;high performance liquid chromatography;ultrasonic extraction;reflux extraction
R283.6
A
1005-1678(2014)04-0169-03
人参首乌胶囊收录于2010版《中国药典》[1],由红参、制何首乌二味中药组成,临床主要用于气血两虚所致的须发早白、健忘失眠、食欲不振、体疲乏力等。现在药理学研究表明,红参主要含人参皂苷Rg1[2-3],具有强心、增强免疫力等功效;何首乌主要成分二苯乙烯苷类化合物具有抗衰老、提高免疫功能、防治动脉硬化及保肝等作用[4]。传统的人参首乌胶囊采用30%乙醇渗漉提取。由于渗漉提取法时间较长,溶剂消耗量大,成本高,因此,在本实验中以人参皂苷Rg1、二苯乙烯苷为指标,比较回流和超声两种提取方法,旨在为人参首乌胶囊的工业生产提供依据。
1 材料与方法
1.1 材料与仪器 高效液相色谱仪(LC-20A,日本岛津公司);电子分析天平(A200s,德国Sartorius公司);人参皂苷 Rg1对照品(中国食品药品检定研究院,批号:110703-2012029);二苯乙烯苷对照品(中国食品药品检定研究院,批号:0773-9210);乙醇、乙腈(色谱纯,J&K SCIENTIFIC LTD);乙醇、磷酸(分析纯,重庆川东化工集团有限公司);红参为五加科植物人参PanaxginsengC.A.Mey.的栽培品(习称圆参)经蒸制后的干燥根;何首乌为蓼科植物何首乌Polygonum multi florum Thunb.的干燥根块,制何首乌为其炮制品。
国家自然科学基金(20112015)
魏宇峰,女,本科,副主任药师,研究方向:妇科临床药学及药物分析,E-mail:weiyufeng622722@126.com。
