响应曲面法优化鸡冠中透明质酸提取工艺条件
2014-09-14郭瑞琳许丹丹宋天雪
郭瑞琳,王 鑫,孟 颖,魏 静,许丹丹,宋天雪
(哈尔滨商业大学 食品工程学院省高校食品科学与工程重点实验室, 哈尔滨 150076)
透明质酸(Hyaluronic acid ,HA)是由N乙酰葡糖胺与D葡糖醛酸组成的黏多糖,是由肝间质细胞的储脂细胞合成、并通过肝内皮细胞特异的透明质酸酶水解的多聚长链化合物[1-2].透明质酸分子在空间上呈刚性无规则卷曲的螺旋柱状结构,由于其流体力学特点使透明质酸有高度黏弹性,良好的可塑性保湿性以及生物相容性,因此透明质酸既可以作为化妆品原料又可用于制作功能性食品,在美容手术及医药领域同样发挥着重要作用,有着良好的发展前景[3-6].在人体和动物的机体组织及细胞基质中,透明质酸结合着胶原、纤黏连蛋白,显示出多种重要的生理功能,例如对细胞运动、增殖、分化和稳定细胞与组织的表现型等,均有重要作用[7].基于其特殊的保水性,可以维持自身千倍的水分子,使透明质酸拥有良好的保湿性,在皮肤的真皮和表皮之间发挥着特殊的生理作用,防止胶原蛋白失水硬化,从而使肌肤维持柔嫩,延缓衰老,除此之外,透明质酸还可以供给肌肤营养,加速受伤肌肤的愈合速度.透明质酸还可以清除体内由于紫外线照射产生的氧自由基,从而减慢机体衰老进程,防止产生炎症,增强机体免疫力[8-9].近年来国内外对透明质酸保健食品进行了深入研究,发现透明质酸分子质量不同对机体吸收能力也不同,机体对大分子质量的透明质酸消化和吸收效果较差,食用降解后的小分子会在机体内合成为大分子质量的透明质酸,进而发挥其重要作用[10-11].
1 材料与方法
1.1 材料与仪器
鸡冠 市售,标准透明质酸 上海源叶生物科技有限公司,丙酮 天津市天新精细化工开发中心,正丁醇 天津市福晨化工试剂厂,氯仿 天津市天新精细化工开发中心,无水乙醇 天津市天力化学试剂有限公司,氯化钠 天津市北方医化学试剂厂.
TU-1900 紫外可见分光光度计 北京普析通用仪器有限责任公司;FZ102微型植物粉碎机、R-205 旋转蒸发器 上海申胜生物技术有限公司; SHZ-D(Ⅲ)循环水式真空泵 巩义市予华仪器有限责任公司.
1.2 实验方法
1.2.1 浸泡
称取20 g新鲜鸡冠5份,用乙醇溶液浸泡鸡冠至变硬并置于干燥箱中干燥,干燥后用植物型粉碎机将其粉碎.向粉碎的鸡冠粉末加入6倍的去离子水于烧杯中,搅拌后静置浸泡过夜.
1.2.2 除脂肪、蛋白
10%的固体氯化钠加入滤液中,玻璃棒搅拌至氯化钠完全溶解,加入等体积的氯仿、正丁醇溶液(氯仿∶正丁醇为4∶1)于分液漏斗中,搅拌3 h,取上层水相待用.以透明质酸得率作为检测指标选择最佳预处理溶液.
1.2.3 HA的单因素条件选择
1)乙醇体积分数单因素实验
量取5份预处理溶液,每份40 mL.将预处理的溶液按料液比1∶2 (g/mL)浸于80 %、85 %、90 %、95 %和100 %的乙醇溶液中,干燥24 h后沉淀物为HA粗品,计算HA得率,确定最佳乙醇体积分数.
2)料液比单因素实验
量取5份预处理溶液,每份40 mL.将预处理的溶液按料液比1∶1、2∶3、1∶2、2∶5和1∶3 (g/mL)加入90 %乙醇溶液中,干燥24 h后沉淀物为HA粗品,计算HA得率,确定最佳乙醇体积分数.
3)静置时间单因素实验
量取5份预处理溶液,每份40 mL.将预处理的溶液按料液比1∶2 (g/mL)加入90 %乙醇中,二者混合分别静置沉淀22、24、26、28、30 h,干燥后沉淀物即为HA粗品.计算HA得率,确定最佳乙醇体积分数.
1.2.4 HA最佳工艺条件的选择
对乙醇浸泡鸡冠实验进行响应面设计,选取以下三因素为优化自变量,根据Box-BenhnKen的中心组合试验设计原理,综合单因素结果,设计三元二次回归正交旋转组合的响应面分析试验.见表1.
表1因素水平表

因素代码编码水平编码值真实值-101时间/ hx1 X1242628料液比/ (g·mL-1)x2 X22∶32∶42∶5 乙醇体积分数/ %x3 X3859095
注:编码值与真实值之间的关系为:x1=(X1-3)/1;x2=(X2-1.3)/0.1;x3=(X3-6)/1.
1.2.5 定性定量分析实验
1)HA得率的测定

其中:W为HA得率,%;m为HA粗品量,g;M为鸡冠干粉,g.
2) 验证实验
量取20 mL滤液,以乙醇作为提取溶剂,根据响应曲面法优化鸡冠中HA提取的最优工艺条件,进行3次平行实验.
3) HA 定性分析试验
通过UV在OD值190~400 nm范围内扫描HA标准品及提取物,根据吸收峰来确定最大吸收波长,进而比较HA标品与样品图谱的出峰位置及峰形是否一致.
2 结果与讨论
2.1 提取HA单因素结果与分析
2.1.1 乙醇体积分数单因素的选择结果与分析
由图1可知,随着乙醇体积分数的增加HA得率有所增加,当乙醇体积分数为90%时,HA得率达到最高点,继续提高乙醇体积分数,HA得率呈现缓慢下降的趋势.由于HA具有高水溶性,乙醇具有价格低廉、无毒无害,并且有较好的吸水性,所以使用乙醇对其进行沉淀,随着乙醇体积分数的增大其吸水性增强,HA的得率增高,但乙醇体积分数达到90%时吸水达到饱和,所以随着乙醇体积分数大于90% HA的得率逐渐降低.因此,确定最佳提取乙醇体积分数为90%.
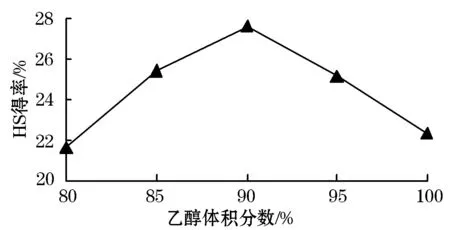
图1 乙醇体积分数对HA得率的影响
2.1.2 料液比单因素的选择结果与分析
由图2可知,料液比较小时HA的产量增加并不明显,但是随着料液比的增加HA的得率有了明显的增高,这是由于随着固相与液相比例加大时二者的接触面积增大,使反应充分固相内物质得到有效释放,且由于物料充足反应速度也大大提高,此时的实验结果也最为明显即为图中料液比为2∶1点所示,HA得率达到最高值.随后,随着料液比的继续增大HA的得率反而随之减少,出现这种现象的原因是由于随着液相高于固相过多导致反应产生的HA被多余的乙醇浸泡抑制了反应的进行,反应速率及产量都受到影响.随着料液比增大HA得率出现严重下滑趋势.可见再增加更多的乙醇并没有提高HA的得率反而析出多余的杂质影响试验准确性并增加了试验成本.因此,确定最佳提取料液比为1∶2.
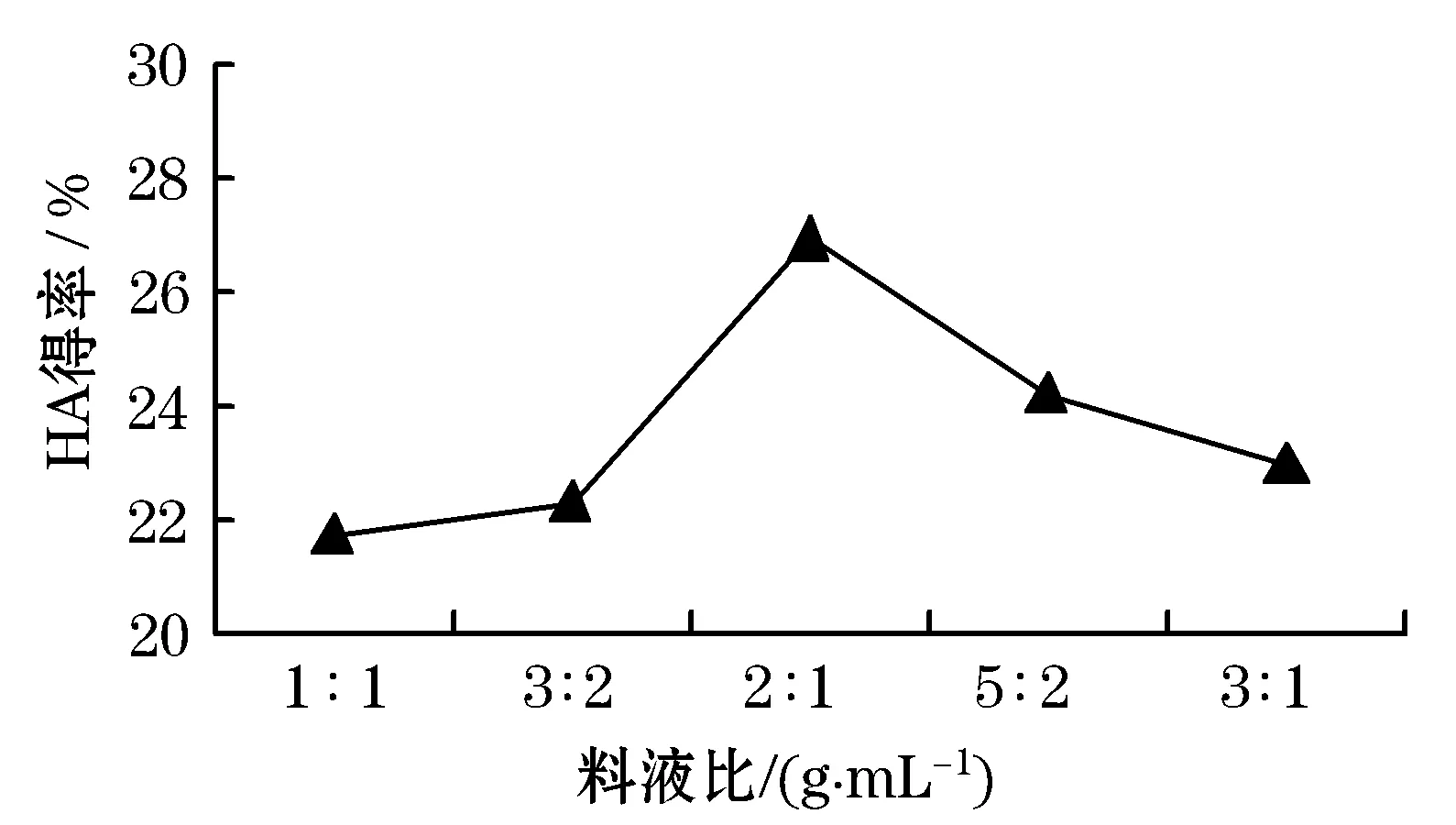
图2 料液比对HA得率的影响
2.1.3 沉淀时间单因素的选择结果与分析
由图3可知,随着反应时间的延长HA得率不断增大.由于随着反应时间增加,溶质在溶剂中得到充分溶解,使反应完全,当溶出的物质达到一定体积分数时反应趋于平衡,如果继续增加反应时间则会使析出物质被溶解,导致HA得率下降.当反应时间较短时,HA产量呈现明显上升趋势;随着反应时间的增加,HA产量上升趋势逐渐减小,在沉淀时间26 h时HA产量达到最高点,若继续延长时间,HA提取产量不在上升,并且呈下降趋势.由此看出,静置时间是影响HA得率的重要因素之一.但需要注意的是静置时间过长也可能使HA的结构发生变化,生物活性遭到到破坏,其中的有效成分不再被溶解,与此同时杂质溶出的量也随之增多,使实验误差增大.因此,当沉淀时间26 h,沉淀效果最佳.

图3 时间对HA得率的影响
2.2 响应曲面优化透明质酸提取工艺条件结果与分析
响应曲面二次多项式回归模型设计及试验结果见表2.
表2试验结果表
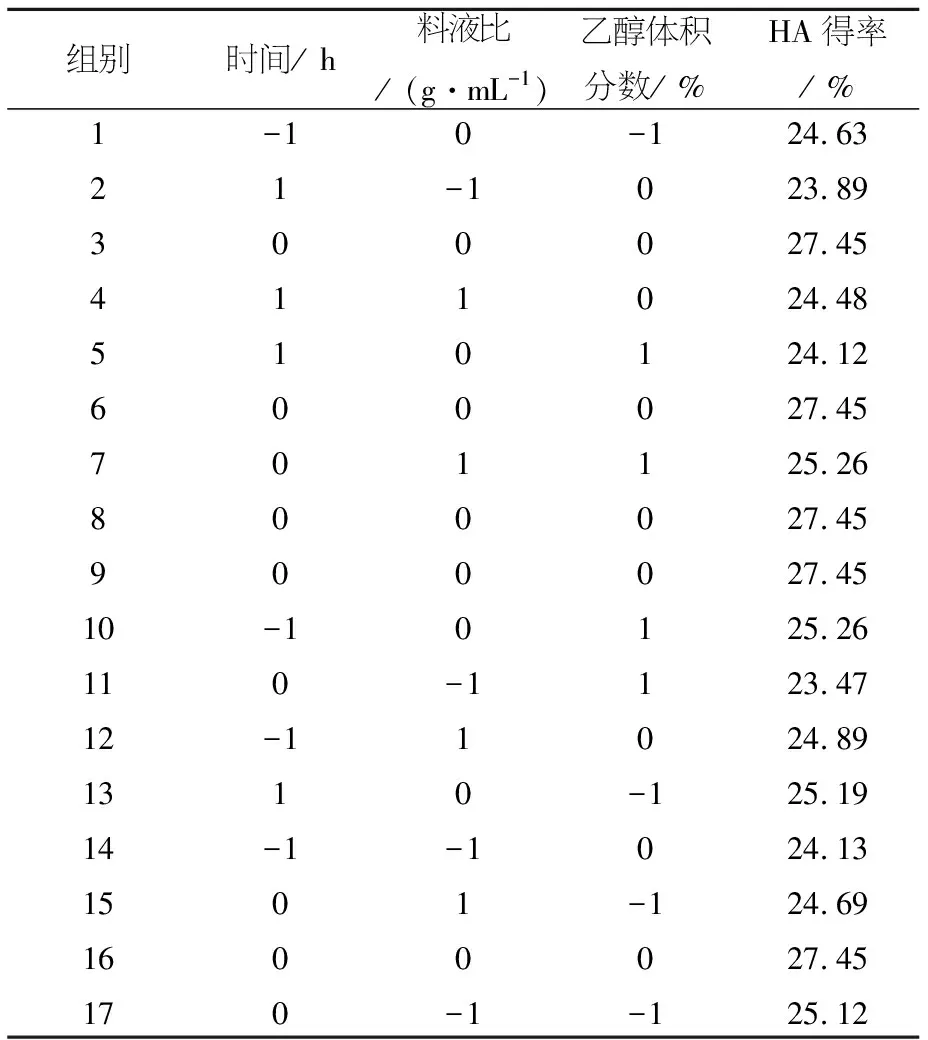
组别时间/ h料液比/ (g·mL-1)乙醇体积分数/ %HA得率/ %1234567891011121314151617-1 1 0110000 -10-11-10000 -10 1001000-110-110-1-1 0001 0100110-10-10-124.6323.8927.4524.4824.1227.4525.2627.4527.4525.2623.4724.8925.1924.1324.6927.4525.12
乙醇浸泡法提取鸡冠中HA的试验结果见表3.利用Design Expert 7.1.3软件对表的试验数据进行优化,获得乙醇沉淀法提取鸡冠中HA得率对提取时间(x1)、料液比(x2)和乙醇体积分数(x3)的二次多项方程为:
Y=27.45-0.15x1+0.34x2-0.19x3-0.043x1x2-0.43x1x3-0.56x2x3-1.47x12-1.63x22-1.18x32
其中:Y为鸡冠中HA的提取率;x1为提取时间,min;x2为料液比, g/mL;x3为乙醇体积分数,%.
由表3可知,本试验所建立的模型非常显著(P<0.000 1).该模型中仅有变异约为0.09%不能通过此模型来解释;相关系数为R=0.9984,该模型拟合程度非常好,试验产生的误差小,该模型是适用的.
表3模型方差分析表
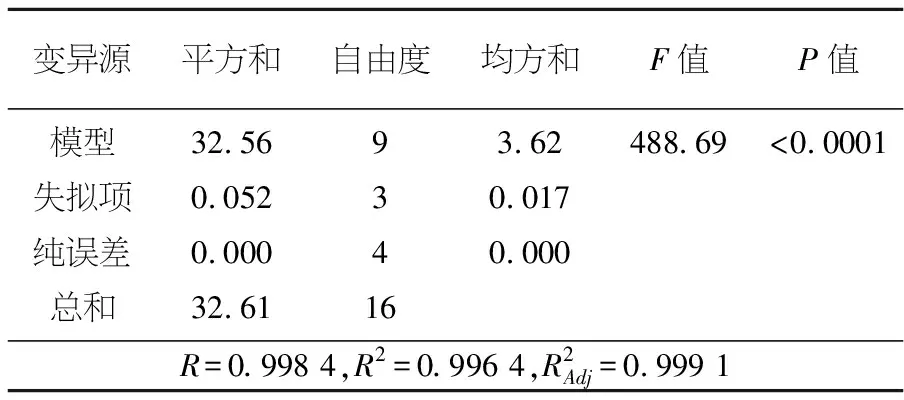
变异源平方和自由度均方和F值P值模型失拟项纯误差总和32.560.0520.00032.61934163.620.0170.000488.69<0.0001R=0.998 4,R2=0.996 4,R2Adj=0.999 1
表4回归方程系数显著性检验表
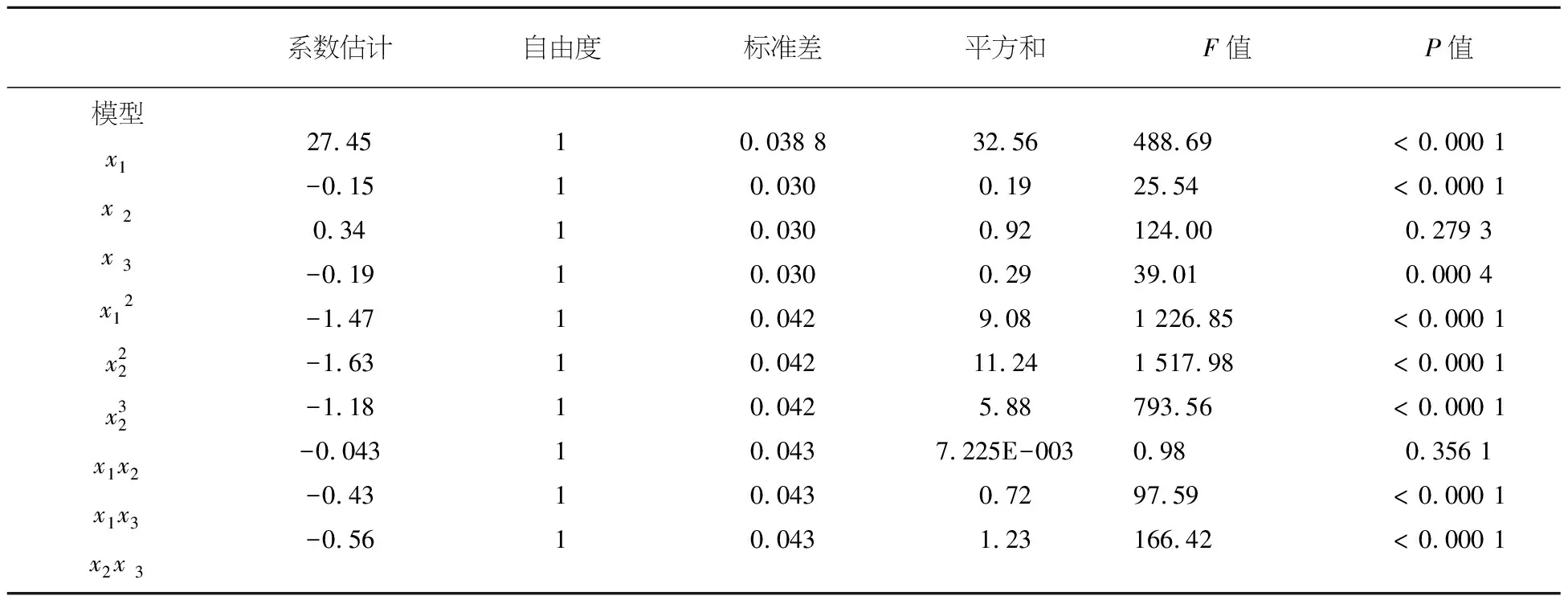
系数估计自由度标准差平方和F值P值模型x1x 2x 3x12x22x32x1x2x1x3x2x 327.45-0.150.34-0.19-1.47-1.63-1.18-0.043-0.43-0.5611111111110.038 80.0300.0300.0300.0420.0420.0420.0430.0430.04332.560.190.920.299.0811.245.887.225E-0030.721.23488.6925.54124.0039.011 226.851 517.98793.560.9897.59166.42< 0.000 1< 0.000 10.279 30.000 4< 0.000 1< 0.000 1< 0.000 10.356 1< 0.000 1< 0.000 1
2.2.1 料液比和乙醇体积分数及其交互作用对提取透明质酸的结果与分析
由图4等高线图可明显地看出,提取时间为最佳值25.71 h.乙醇提取体积分数和料液比两个因素的交互作用比较显著.在实验水平范围内,乙醇体积分数对HA产量的影响很大,随着乙醇体积分数的增大,HA产量迅速增加,乙醇体积分数基本在85%~95%范围内,HA产量可达到本次实验中的最大值.料液比对HA产量也有很大的影响,但随着料液比的增加,HA产量先增大后降低.观察二者的等高线图可以看出两个因素的交互作用极显著.在本次实验水平范围内,料液比和乙醇体积分数的值分别在2∶3 ~9∶5 (g/mL)和87%~90%的范围内,HA的得率达到试验最大值.
2.2.2 料液比和时间及其交互作用对提取透明质酸的结果与分析
由图5可以直观地看出,乙醇体积分数为最佳89.93%时,观察等高线图,提取时间与料液比两个因素之间的交互效果不显著.在本次试验水平范围内,提取时间对HA的得率影响不明显,在22~30 h之间随着滤液和乙醇体积分数两者之间料液比的增加,得率并没有明显的改变,当提取时间较短时,HA的得率随着时间的增加而增大,当时间超过26 h时,HA的得率随着提取时间的增加并没有明显提高.料液比和时间处于实验水平的中心点位置附近时,即料液比为1∶2 (g/mL)和时间约为26 h,HA得率最高.当二者的水平过高或过低时,都会使HA得率下降.由等高线的形状可直观地看出此两因素的交互作用不显著(P>0.05).
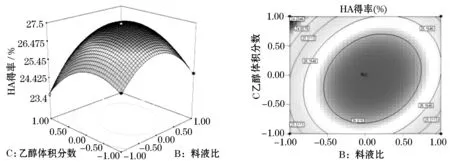
图4 料液比、乙醇体积分数及其交互作用对提取透明质酸的响应曲面和等高线图
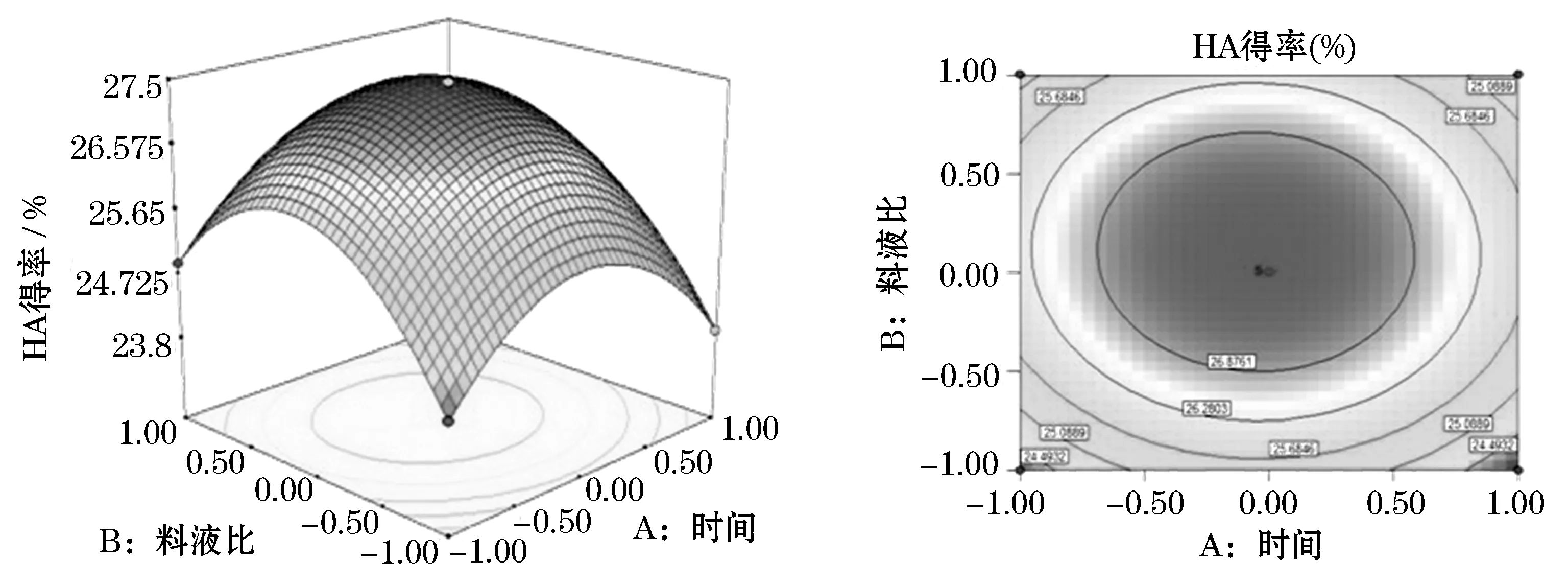
图5 料液比、时间及其交互作用对提取透明质酸的响应曲面和等高线图
2.2.3 提取时间和乙醇提取体积分数及其交互作用对提取透明质酸的结果与分析
从图6等高线图可以直观的看出,料液比为最佳100∶177 (g/mL)时,提取HA时间与乙醇提取体积分数两个因素之间的相互交互作用显著,在试验水平范围内,乙醇体积分数对HA的得率影响较大,随着乙醇体积分数的增加HA的得率增大;提取时间较短时,HA得率随时间的延长而增大,但当提取时间超过26 h时,HA得率随时间的延长而减小的幅度明显.在试验水平范围内,乙醇体积分数和提取时间的值分别在87%~92%和24~26 h的范围内,此时HA的得率达到试验最大值.
通过响应曲面分析,该模型确定提取HA的最佳工艺条件:提取时间为25.71 h、乙醇体积分数89.93%、料液比100∶177 (g/mL).
2.3 验证实验结果分析
从综合实际角度考虑,采用优化后的工艺提取HA,即提取时间为25.70 h、乙醇体积分数90.00%、料液比100∶177 (g/mL),该工艺制备透明质酸得率为27.31%.
2.4 紫外光谱检测结果分析
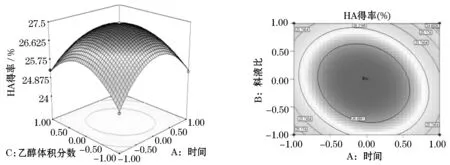
图6 提取时间、乙醇体积分数及其交互作用对提取透明质酸的响应曲面和等高线图
通过UV检测确定标准HA在198 nm吸收波长处有稳定的吸收峰.由图7可知,确定HA最大的吸收波长为198 nm.在最大吸收峰198 nm处检测HA样品与HA标品的最大出峰位置及峰形是一致的,可确定该提取物质为HA.

图7 透明质酸紫外光谱扫描图
3 结 语
以市售新鲜鸡冠为原料研究了HA提取的最佳提取方法.分别选用了丙酮和乙醇预处理提取HA,以HA得率为评价指标,采用响应曲面法优化提取工艺.确定乙醇处理的HA得率更高为24.85%,选择乙醇为预处理溶剂,通过响应曲面法分析,优化HA提取工艺,确定条件为:提取时间为25.70 h、乙醇体积分数90.00%、料液比100∶177 (g/mL),该工艺制备透明质酸得率为27.31%,通过定性试验确定从新鲜鸡冠中提取出的物质与HA标准品的波长及峰值相同.最大吸收波长为198 nm,确定鸡冠中提取物质为HA.
参考文献:
[1] 马云宝,何启志. 透明质酸的临床应用及研究进展[J].国外医学:放射医学核医学分册, 1995, 19(2): 66-68.
[2] MIYAZAKI T, YOMOTA C, OKADA S. Ultrasonic depolymerization of hyaluronic acid [J].Polymer Degradation and Stability, 2001, 74(1): 77-85.
[3] 潘红梅. 透明质酸的研究现状综述[J].四川食品与发酵, 2003, 39(116): 5-9.
[4] GURA E, HIICKEL M. Specific degradation of rheological hyaluronic acid and its properties[J].Polymer Degradation and Stability, 1998: 297-302.
[5] KANG S W, BADA L P, KANG C S,etal. Articular cartilage regeneration with micro fracture and hyaluronic acid[J].Biotechnology Letters, 2008, 30(3): 435-439.
[6] 刘 彤. 透明质酸及其在化妆品中的应用[J].广州化工, 2009, 37(8): 71-73.
[7] 路宏朝, 张 涛, 段晓强. 水稻中透明质酸提取工艺的初步研究[J].食品科技, 2010, 35(8): 226-228.
[8] 代 琼, 杨文鸽, 陈小芳. 鱿鱼眼透明质酸及其降解产物的抗氧化和保湿作用[J].食品科学, 2012, 33(1): 35-38.
[9] QI H M, ZHAO T T, ZHANG Q B,etal. Antioxidant activity of different molecular weight sulfated polysaccharides from Ulva pertusa Kjellm (Chlorophyta)[J].Journal of Applied Physiology, 2005, 17(6): 527-534.
[10] 卢佳芳. 鱿鱼眼中透明质酸的提取、降解及其生物活性研究[D].宁波: 宁波大学, 2010.
[11] 褚银玲,吴 春,代丽君.响应面法优化超声辅助提到紫洋葱花色苷[J].哈尔滨商业大学学报:自然科学版,2013,29(5):548-552.
