利拉鲁肽调节2型糖尿病的代谢紊乱
2014-09-12张建中赵文成王丽芬吉林大学中日联谊医院新民院区内分泌科吉林长春130021
李 洋,张建中,赵文成,门 岚,马 媛,张 颖,王丽芬 (吉林大学中日联谊医院新民院区内分泌科,吉林 长春 130021)
近年来,胰高血糖素样肽-1(Glucagon-like peptide-1,GLP-1)被认为是在2型糖尿病患者中起主要作用的一种肠促胰素,当随机血糖水平超过正常范围时可以调节胰岛素和胰高血糖素的分泌[1]。利拉鲁肽是一种GLP-1类似物,与人GLP-1具有97%的序列同源性,现在临床上已经将利拉鲁肽作为治疗2型糖尿病患者的一种新型降糖药物。本文主要对采用生活方式干预加胰岛素联合治疗血糖控制不达标的2型糖尿病住院患者进行研究,观察其联合使用利拉鲁肽后的治疗效果。
1 资料与方法
1.1 一般资料:前瞻性研究2011年11月~2012年3月间及出院后经过生活方式干预加胰岛素治疗血糖控制仍不达标,住院后联合应用利拉鲁肽的2型糖尿病患者30例作为治疗组,男18例,女12例,平均年龄(44.80±11.59)岁,糖尿病病程平均(5.54±5.45)年。同期住院未联合应用利拉鲁肽的2型糖尿病患者30例作为对照组,男19例,女11例,平均年龄(48.8±9.27)岁,糖尿病病程平均(6.01±3.73)年。以上患者均符合1999年WHO糖尿病诊断标准,无严重的心、肝、肾等重要脏器病变。
1.2 治疗方法:所有入选患者均采用生活方式干预加胰岛素联合治疗,血糖水平控制未达标,在原胰岛素基础上加用利拉鲁肽的作为治疗组,未加用利拉鲁肽的作为对照组。治疗组利拉鲁肽0.6 mg早餐前皮下注射,1周后改为1.2 mg早餐前皮下注射。对所有患者进行全天血糖监测,根据血糖监测结果调整胰岛素用量。
1.3 观察项目:观察所有选定对象治疗前、治疗后3个月空腹血糖、餐后2 h血糖、糖化血红蛋白、体重指数、血压、血脂、胰岛素用量、不良反应等临床指标,出院后每3个月随访一次。
1.4 统计学方法:采用SPSS13.0软件进行统计学处理,计量数据统计采用均数±标准差s)表示,组内比较采用配对t检验,计数数据统计采用构成比或率表示,比较采用χ2检验,P<0.05有统计学意义。
2 结果
治疗前对照组与治疗组的患者例数、年龄、糖尿病病程、空腹血糖、餐后2 h血糖、糖化血红蛋白、体重指数、血压、血脂、胰岛素用量差异均无统计学意义(P>0.05)。见表1。
表1 对照组与治疗组入选患者基本情况比较(n=30s)
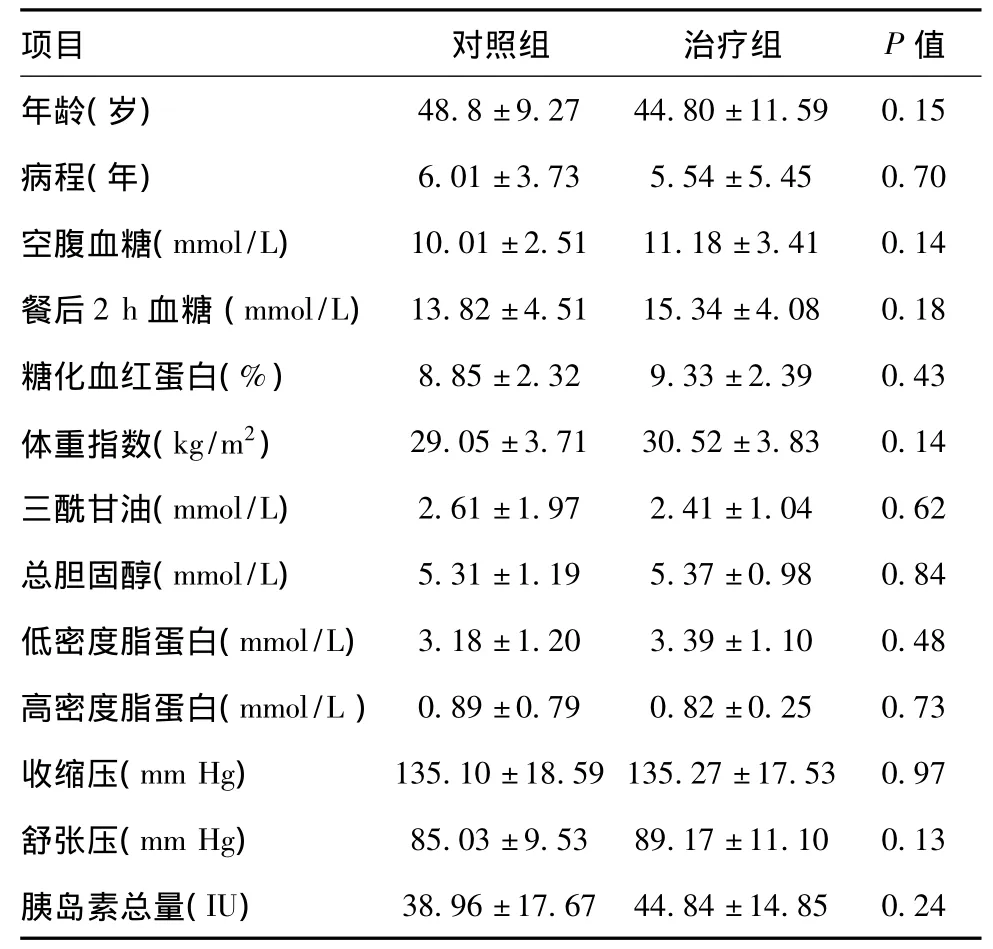
表1 对照组与治疗组入选患者基本情况比较(n=30s)
注:1 mmHg=0.1333 kPa
项目 对照组 治疗组 P值48.8±9.27 44.80±11.59 0.15病程(年) 6.01±3.73 5.54±5.45 0.70空腹血糖(mmol/L) 10.01±2.51 11.18±3.41 0.14餐后2 h血糖 (mmol/L) 13.82±4.51 15.34±4.08 0.18糖化血红蛋白(%) 8.85±2.32 9.33±2.39 0.43体重指数(kg/m2) 29.05±3.71 30.52±3.83 0.14三酰甘油(mmol/L) 2.61±1.97 2.41±1.04 0.62总胆固醇(mmol/L) 5.31±1.19 5.37±0.98 0.84低密度脂蛋白(mmol/L) 3.18±1.20 3.39±1.10 0.48高密度脂蛋白(mmol/L) 0.89±0.79 0.82±0.25 0.73收缩压(mm Hg) 135.10±18.59 135.27±17.53 0.97舒张压(mm Hg) 85.03±9.53 89.17±11.10 0.13胰岛素总量(IU)年龄(岁)38.96±17.67 44.84±14.85 0.24
组内比较对照组在治疗后,空腹血糖、餐后2 h血糖、糖化血红蛋白、收缩压、舒张压较治疗前下降,但体重指数较治疗前升高,差异有统计学意义(P<0.05);治疗组在治疗后,空腹血糖、餐后2 h血糖、糖化血红蛋白、体重指数、总胆固醇、低密度脂蛋白、收缩压、舒张压、胰岛素总量较治疗前下降,高密度脂蛋白较治疗前升高,差异有统计学意义(P<0.05)。两组间比较治疗后餐后2 h血糖、糖化血红蛋白、体重指数、胰岛素总量治疗组较对照组下降,高密度脂蛋白治疗组较对照组升高,差异有统计学意义(P<0.05)。见表2。治疗组30例患者中甚至还有8例完全停用胰岛素。
表2 治疗前后患者各种临床指标结果比较(n=30±s)

表2 治疗前后患者各种临床指标结果比较(n=30±s)
注:与同组治疗前比较,①P<0.05;与对照组治疗后比较,②P<0.05;1 mm Hg=0.1333 kPa
组别 项目 治疗前 治疗后对照组 空腹血糖(mmol/L) 10.01±2.57 6.96±1.55①餐后2 h血糖(mmol/L) 13.82±4.51 9.91±2.19①糖化血红蛋白(%) 8.85±2.32 8.06±0.98①体重指数(kg/m2) 29.05±3.71 29.44±3.44①三酰甘油(mmol/L) 2.61±1.97 2.40±1.58总胆固醇 (mmol/L) 5.31±1.19 5.08±1.17低密度脂蛋白(mmol/L) 3.18±1.20 2.98±1.27高密度脂蛋白(mmol/L) 0.89±0.79 0.93±0.61收缩压(mm Hg) 135.10±18.59 126.85±7.92①舒张压(mm Hg) 85.03±9.53 80.67±5.95①胰岛素总量(IU) 38.96±17.67 37.30±18.43治疗组 空腹血糖(mmol/L) 11.18±3.41 7.11±1.97①餐后2 h血糖(mmol/L) 15.34±4.08 8.35±2.32①②糖化血红蛋白(%) 9.33±2.39 7.50±1.11①②体重指数(kg/m2) 30.52±3.83 27.71±2.93①②三酰甘油(mmol/L) 2.41±1.04 2.57±1.59总胆固醇(mmol/L) 5.37±0.98 5.08±1.06①低密度脂蛋白(mmol/L) 3.39±1.10 3.03±1.14①高密度脂蛋白(mmol/L) 0.82±0.25 1.02±0.28①②收缩压(mm Hg) 135.27±17.53 125.33±9.43①舒张压(mm Hg) 89.17±11.10 78.50±6.90①胰岛素总量(IU) 44.84±14.85 26.79±15.41①②
治疗组中3例患者在治疗早期有恶心、腹泻等胃肠道不良反应,可耐受,低血糖发生率较对照组明显下降。
3 讨论
肠促胰素水平的降低被认为是2型糖尿病的主要病理生理缺陷之一,目前传统的糖尿病治疗方法尚无对该问题的解决。近年来研究发现它是由GLP-1和糖依赖性胰岛素释放肽(Gastric inhibitory polypeptide,GIP)两种激素组成,其中GLP-1在2型糖尿病中起着更为主要的作用[2]。胰高血糖素原基因在胰岛α细胞中的主要产物是胰高血糖素,而在肠黏膜L细胞中经酶类作用则生成GLP-1。GLP-1入血后易被二肽基肽酶4分解,利拉鲁肽作为一种GLP-1类似物,酶稳定性更高,血浆半衰期较长。
本组研究可见联合应用利拉鲁肽的治疗组在治疗后进行组内及组间对比,餐后2 h血糖、糖化血红蛋白、胰岛素总量均呈下降趋势(P<0.05)。空腹血糖仅于进行组内比较时有统计学意义(P<0.05),组间比较无统计学意义(P>0.05)。可见利拉鲁肽能够有效降低2型糖尿病血糖水平,尤其以降低餐后血糖水平明显。正常人群于进食后开始分泌GLP-1,其与GLP-1受体相结合后通过cAMP/PKA途径增加L-型电压门控钙离子通道的钙离子内流和内质网钙离子释放而活化钙调蛋白,最终增强胰岛素出胞作用,促进胰岛素分泌,发挥葡萄糖浓度依赖性降糖作用[3]。GLP-1的这种特性使其在联合胰岛素等其他药物治疗过程中并不增加低血糖风险,同时可减少外源性胰岛素的使用量,治疗组30例患者中甚至还有8例完全停用胰岛素。Lind等对4个瑞典治疗中心中使用胰岛素后联合应用GLP-1类似物的2型糖尿病患者65例进行研究[4],糖化血红蛋白由平均8.9%减少至7.9%(P<0.001),胰岛素总量由91.1 U下降至52.2 U(P<0.001),同时低血糖风险低。
胰岛素抵抗和肥胖同样也是导致2型糖尿病发展的潜在重要因素。有研究表明GLP-1类似物无论是单独使用还是联合其他降糖药物时都具有抑制胰高血糖素的分泌、延缓胃排空、调节摄食中枢,减轻饥饿感,增加饱腹感及减轻体重的作用[5]。本组研究中,治疗组体重指数较治疗前下降明显,组内与组间差异均有统计学意义(P<0.05)。而对照组体重指数反而较治疗前升高,差异有统计学意义(P<0.05)。Buse JB等对295例2型糖尿病患者进行研究表明GLP-1类似物治疗能够有效改善体重[6],通常可减少2~4 kg,而应用胰岛素治疗时体重通常可增加1~3 kg。Dushay等对非糖尿病的肥胖女性人群短期使用GLP-1类似物同样可以有效减轻体重,减小腰围[7]。也就是说无论在糖尿病或非糖尿病的肥胖人群中均可有效减轻体重,Vilsboll T等进行的荟萃分析亦得出这一结论[8]。
近年来人们对GLP-1研究的继续开展,除具控制血糖、减轻体重、降低血压、调节血脂等间接心血管保护作用外,可能还直接作用于心血管系统,发挥保护作用[9]。本结果显示,治疗组总胆固醇、低密度脂蛋白、收缩压、舒张压治疗后比治疗前降低(P<0.05),但与对照组进行组间对比差异无统计学意义(P>0.05);高密度脂蛋白较治疗前升高,同时较对照组亦升高(P<0.05);三酰甘油反而较治疗前升高,但差异无统计学意义(P>0.05)。Buse JB等研究表明GLP-1类似物治疗30周后血压及血脂得到有效改善[6],延长治疗至52周,收缩压、总胆固醇及低密度脂蛋白均得到进一步降低。不过,目前国内外对GLP-1能否降低脂质的讨论尚未达成共识,但通过观察可以肯定GLP-1能降低冠心病的发病率[10]。
治疗早期3例患者出现恶心、腹泻等胃肠道不良反应,但程度轻,耐受性好,且随着用药时间延长,不良反应逐步减轻。利拉鲁肽作为GLP-1类似物为2型糖尿病患者提供了新的治疗手段,但其长期临床益处及安全性仍有待进一步考证。
[1]Drucker DJ.Enhancing incretin action for the treatment of type 2 diabetes[J].Diabetes Care,2003,26(10):2929.
[2]Holst JJ,Vilsboll T,Deacon CF.The incretin system and its role in type 2 diabetes mellitus[J].Mol Cell Endocrinol,2009,297(1):127.
[3]Doyle ME,Egan JM.Mechanisms of Action of GLP -1 in the Pancreas[J].Pharmacol Ther,2007,113(3):546.
[4]Lind M,Jendle J,Lager I.Glucagon - like peptide 1(GLP-1)analogue combined with insulin reduces HbA1c and weight with low risk of hypoglycemia and high treatment satisfaction[J].Prim Care Diabetes,2012,6(1):41.
[5]Madsbad S.Liraglutide Effect and Action in Diabetes(LEAD?)trial[J].Expert Rev Endocrinol Metabol,2009,4(2):119.
[6]Buse JB,Drucker DJ,Porter LE.DURATION -1:Exenatide Once Weekly Produces Sustained Glycemic Control and Weight Loss Over 52 Weeks[J].Diabetes Care,2010,33(6):1255.
[7]Dushay J,Gao C,Maratos- Flier E.Short- term exenatide treatment leads to significant weight loss in a subset of obese women without diabetes[J].Diabetes Care,2012,35(1):4.
[8]Vilsboll T,Christensen M,Junder AE.Effects of glucagon -like peptide-1 receptor agonists on weight loss:systematic review and meta - analyses of randomised controlled trials[J].BMJ,2012,344:1.
[9]Forst T,Weber MM,Pfützner A.Cardiovascular Benefits of GLP-1-BasedTherapies in Patients with Diabetes Mellitus Type 2:Effects on Endothelial and Vascular Dysfunction beyond Glycemic Control[J].Exp Diabetes Res,2012,2012:1.
[10]Wen XD,Tang W,Liu ZM.Glucagon-like peptide-1 alleviating peripheral neuropathy in diabetic patients:advance in mechanism[J].Academic Journal of Second Military Medical University,2011,32(3):329.
