高效液相色谱法测定不同加工工艺天麻中天麻素和天麻苷元含量
2014-09-11沈肖晶金传山许凤清李保明
沈肖晶,金传山,许凤清,李保明,胡 雨
(1.安徽中医药大学药学院,安徽 合肥 230012;2.安徽道地中药材品质提升协同创新中心,安徽 合肥 230012;3.安徽协和成药业饮片有限公司,安徽 亳州 236800)
高效液相色谱法测定不同加工工艺天麻中天麻素和天麻苷元含量
沈肖晶1,2,金传山1,2,许凤清1,2,李保明3,胡 雨1,2
(1.安徽中医药大学药学院,安徽 合肥 230012;2.安徽道地中药材品质提升协同创新中心,安徽 合肥 230012;3.安徽协和成药业饮片有限公司,安徽 亳州 236800)
目的建立高效液相色谱法同时测定天麻中天麻素及天麻苷元含量的方法,优选不同产地的天麻加工工艺。方法采用高效液相色谱法测定天麻素和天麻苷元含量,色谱柱为Spursil C18-EP(250 mm×4.6 mm),流动相为甲醇-0.1%磷酸水(5∶95),检测波长220 nm,柱温40 ℃,流速1 mL/min。结果隔水蒸30 min、清水煮15 min、0.2%矾水煮15 min、煮后直接切片是4种较佳的加工工艺,所制得的天麻饮片中天麻素和天麻苷元含量依次降低。结论隔水蒸30 min所制得的天麻饮片中天麻素及天麻苷元含量最高,优于其他处理方法。
天麻;天麻素;天麻苷元;加工工艺;高效液相色谱法
天麻为兰科植物天麻GastradiaelataBl.的干燥块茎,是我国传统的常用名贵中药材,被历版《中华人民共和国药典》所收录,亦为安徽的大宗药材之一。天麻有“治风之神药”之称,具有平肝熄风止痉的作用,主要用于头痛眩晕、小儿惊风、破伤风、肢体麻木、癫痫抽搐等症[1]。目前,天麻传统产地加工方法主要有隔水蒸法、水煮法与矾煮法等,多依据药农经验进行加工,其质量参差不齐。
天麻素(对羟基苯甲醇-β-D-吡喃葡萄糖苷)具有镇静催眠、镇痛、抗癫痫等作用[2],一直被公认为是天麻的有效成分和质量控制的主要指标成分。现代药理研究表明,天麻中天麻素、天麻苷元(对羟基苯甲醇)等成分具有抗惊厥、镇痛、镇静、提高记忆力等生物活性[3]。而早期研究多仅仅选择天麻素作为质量评价指标[4-5],鲜见同时测定天麻素及天麻苷元以比较天麻加工工艺的文献[6]。故本实验采用高效液相色谱技术,建立同时测定天麻中天麻素及天麻苷元的方法,同时比较隔水蒸法、清水煮法、矾水煮法等不同参数条件下的加工方法对这两种成分的影响,为天麻加工工艺研究提供基础。
1 仪器与试药
1.1 仪器 Shimadzu LC-20AT型高效液相色谱仪(含LC-20AT泵、SPD20M检测器、天津东康DT-230A型柱温箱、LC-Solution工作站);Spursil C18-EP色谱柱:美国迪马公司;AT系列溶剂过滤器、AS3120型超声清洗仪:天津Autoscience公司;MS105/0.01 mg电子天平:上海梅特勒托利多公司;CP225D型十万分之一电子天平:德国Sartorius公司;202-2型电热恒温干燥箱:上海实验仪器有限公司;LK-400B型粉碎机:浙江温岭创新药材器械厂;2SHB-Ⅲ循环水式多用真空泵:河南郑州长城工贸有限公司;HH-S2系列恒温水浴锅:江苏金坛环宇科学仪器厂。
1.2 试药 天麻素标准品:中国药品生物制品检定所,批号 110807-200205;天麻苷元对照品:纯度98%,Adamas试剂公司;甲醇:色谱纯,天津市四友精细化学品有限公司生产,批号 401321;磷酸:分析纯,天津市永大化学试剂有限公司生产,批号 20100313;纯净水:杭州娃哈哈有限公司生产,批号 121530;天麻鲜品:2013年12月采于安徽省安庆市岳西县石关乡马畈村,经安徽中医药大学药学院金传山教授鉴定为天麻G.elataBl.的干燥块茎。
2 方法
2.1 色谱条件 采用Spursil C18-EP色谱柱(250 mm×4.6 mm),流动相为甲醇-0.1%磷酸水(5∶95),检测波长为220 nm,流速1 mL/min,柱温为40 ℃,进样量为20 μL。该条件下天麻素与天麻苷元分离度良好,见图1、图2。
2.2 对照品溶液的制备 精密称取80 ℃减压干燥1 h的天麻素对照品9.95 mg、天麻苷元对照品2.74 mg,流动相定容至25 mL容量瓶,混匀过0.22 μm滤膜,取续滤液,即得。
2.3 供试品溶液的制备 精密称取各样品粉末(24目)1 g,溶于70%甲醇,定容至25 mL容量瓶,超声20 min,取出放冷后精密移取10 mL,置洁净干燥蒸发皿中水浴浓缩至近干,残渣溶于流动相,定容至10 mL容量瓶,摇匀,过0.45 μm滤膜,取续滤液,即得。
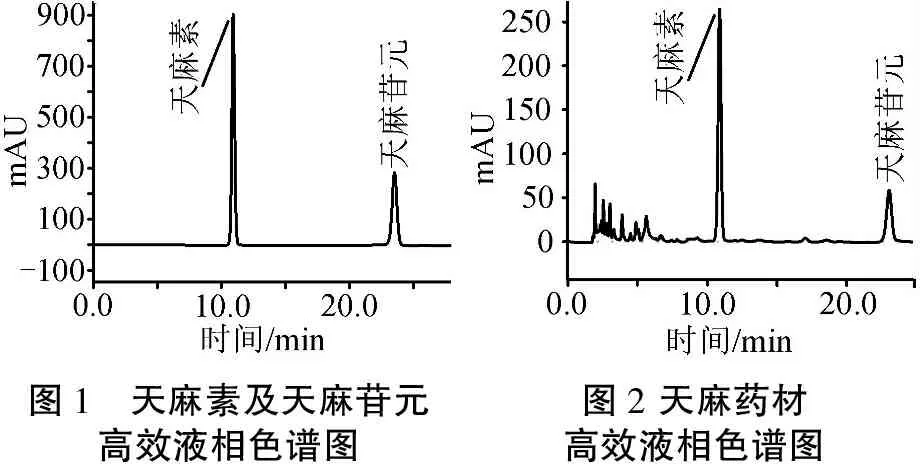
图1 天麻素及天麻苷元高效液相色谱图图2天麻药材高效液相色谱图
2.4 线性关系考察 精密移取天麻素与天麻苷元混合对照品溶液,按“2.2”项下方法制备,分别取0.05、0.2、0.5、1、2、3、5 mL混合对照品溶液,流动相定容至5 mL容量瓶中,按照“2.1”项下色谱条件进行测定。以对照品浓度(x)为横坐标,峰面积(y)为纵坐标,得天麻素线性方程为y=3.6×107x+122 715,r=0.999 8,线性范围为0.020 0~1.990 0 mg;天麻苷元线性方程为y=7.1×107x-70 748,r=0.999 3,线性范围为0.005 5~0.548 0 mg。在此范围内天麻素及天麻苷元线性关系良好。
2.5 精密度试验 取天麻素和天麻苷元混合对照溶液,按“2.1”项下操作,连续重复进样5次,测定天麻素、天麻苷元含量,天麻素和天麻苷元含量的RSD分别为0.16%、0.33%,符合定量分析要求。
2.6 重复性试验 称取样品粉末,按“2.3”项下方法制备供试品溶液,按上述色谱条件进样,测定样品中天麻素和天麻苷元含量,天麻素和天麻苷元含量的RSD分别为1.02%、1.19%,符合定量分析要求。
2.7 稳定性试验 称取样品粉末,按“2.3”项下方法制备供试品溶液,分别于0、2、4、8、12、24 h进样,测定样品中天麻素和天麻苷元含量,天麻素和天麻苷元含量的RSD分别为0.88%、0.92%,说明供试品在24 h内质量稳定。
2.8 加样回收试验 精密称取已知含量的样品粉末6份,每份0.5 g,加入适量的天麻素和天麻苷元对照品溶液,按“2.3”项下方法制备,测定天麻素和天麻苷元含量。天麻素和天麻苷元平均回收率分别为100.98%、104.28%,RSD分别为1.62%、1.72%,说明该方法回收率良好。见表1。
3 不同工艺加工的天麻中天麻素和天麻苷元含量测定
3.1 样品加工方法 将新鲜天麻样品洗净,大小分级,选取100~150 g天麻,分别进行如下加工。
3.1.1 隔水蒸法:取适量天麻置蒸笼上隔水蒸,圆气后开始计时,分别蒸10、15、20、30 min,取出置烘箱中50 ℃烘干。
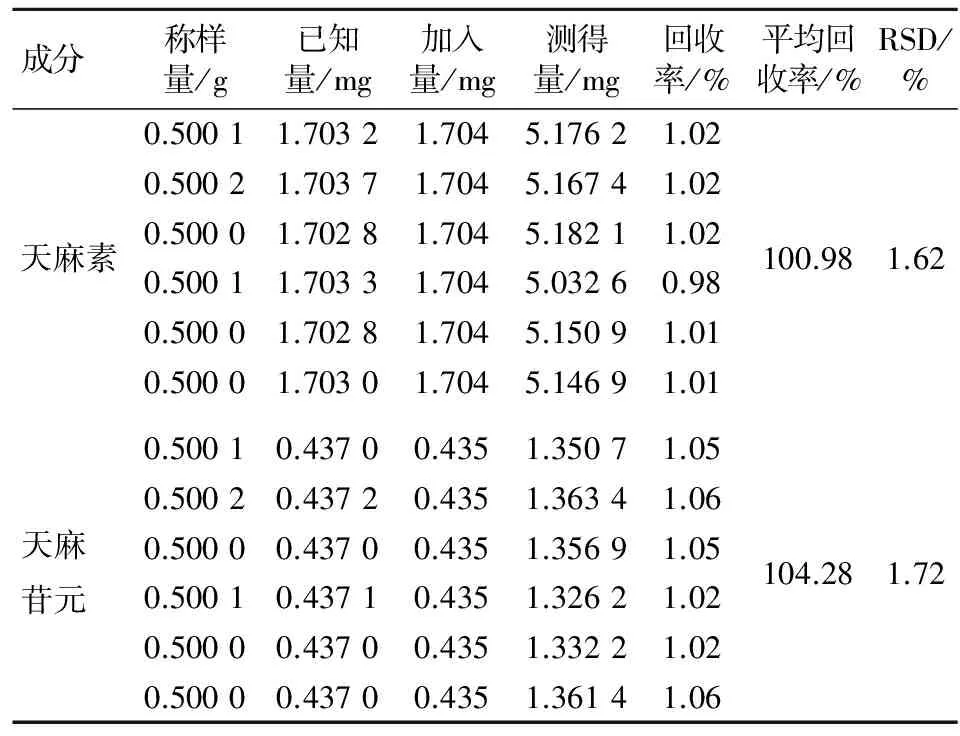
表1 天麻素、天麻苷元加样回收率
3.1.2 清水煮法:取适量天麻置清水中,清水淹没天麻,保持微沸,分别煮制10、15、20、25、30 min,捞出沥干表面水分,置烘箱中50 ℃烘干。
3.1.3 矾水煮法:分别配制浓度为0.2%、0.5%、1%、2%、4%的白矾溶液,取适量天麻置白矾溶液中,溶液浸没天麻,保持微沸15 min,捞出沥干表面水分,置烘箱中50 ℃烘干。
3.1.4 直接切片:分别对天麻水煮15 min后切片、新鲜天麻切片后水煮10 min、新鲜天麻切片后隔水蒸10 min、新鲜天麻切片后4%矾水煮20 min。
3.2 供试品测定 取不同加工工艺的天麻样品,编号,干燥,粉碎,取过24目不过60目的粉末,精密称取1 g,按照“2.3”项下方法制备,在“2.1”项色谱条件下测定,分别计算样品中天麻素和天麻苷元含量,结果见表2。
4 讨论
本实验中考察了纯甲醇超声法、70%甲醇超声法和50%乙醇热回流法[7-8]等样品制备方法,对于同一样品,70%甲醇超声法提取率约为回流法的80%,纯甲醇超声提取率约为回流法的25%。虽然提取率不及回流法,但超声法具有省时、简便、易操作的优点,故选用70%甲醇超声法制备样品。
综合样品含量测定结果,经过不同工艺处理的天麻中天麻素及天麻苷元含量差别较大,天麻素含量最高达0.82%,最低只有0.19%;天麻苷元含量最高达0.12%,最低仅为0.01%。从样品中天麻素及天麻苷元的含量来看,隔水蒸法要高于清水煮法,与大多文献报道一致,且隔水蒸30 min的天麻素含量明显高于其他,是否30 min为蒸制的最佳时间有待于进一步研究。

表2 各样品中天麻素与天麻苷元含量(n=3)
结合表2实验结果优选各工艺最佳参数,隔水蒸30 min、清水煮15 min、0.2%矾煮15 min、煮后直接切这4种工艺所制得的天麻饮片中天麻素及天麻苷元含量较高,具体工艺参数有待进一步研究。不同工艺炮制前后含量变化差别较大,直接切的样品含量下降较显著,隔水蒸的样品含量上升较明显。从含量变化趋势来看,隔水蒸法较稳定,清水煮法变化不成规律,较容易受水量、温度、时间的影响。
本实验比较了不同浓度白矾溶液煮制天麻的成分差异,结果显示在一定范围内,矾水浓度越高,天麻素含量越低;而天麻苷元变化不成规律,但与清水煮的天麻比较,其天麻苷元含量明显升高,其中2%矾水煮制天麻中天麻苷元含量最高,这一规律是否成立有待深入研究。实验中发现,0.1%矾水煮制天麻的色泽较差,且存储时较易被虫蛀,存储时间远低于0.2%及以上浓度矾水煮制的样品,故本实验中未考察0.1%矾水煮制的样品。
综上所述,不同加工工艺所制得的天麻中天麻素及天麻苷元含量存在差异,隔水蒸30 min、清水煮15 min、0.2%矾水煮15 min、煮后直接切片是4种较佳的加工工艺,所制得的天麻饮片中天麻素和天麻苷元含量依次降低。本研究可为天麻产地加工工艺的规范化研究与参数的进一步优选提供依据。
[1]高学敏.中药学[M].北京:中国中医药出版社,2002:478-480.
[2]洪全,陈淼,李雪萍.天麻药理研究进展[J].中国实用医药,2010,5(11):249-250.
[3]吴刚,秦民坚,康继川,等.不同产地天麻质量评价[J].现代中药研究与实践,2007,21(1):40-43.
[4]秦俊哲,张洁,周涵.不同炮制方法对天麻素含量的影响[J].中药材,2006,29(12):1285-1288.
[5]李德勋,陈桂,肖顺经,等.正交试验法优选鲜天麻的蒸制干燥工艺[J].现代中药研究与实践,2006,20(2):56-57.
[6]任守利,刘塔斯,林丽美,等.HPLC测定不同商品规格天麻中天麻苷与天麻苷元的含量[J].中国实验方剂学杂志,2011,17(15):55-58.
[7]李瑞洲,刘守金.天麻采集加工方法考察[J].安徽中医学院学报,2000,19(6):44-45.
[8]李德勋,肖顺经.天麻的传统加工工艺调查和质量考察[J].现代中药研究与实践,2004,18(4):12-13.
SimultaneousDeterminationofGastrodinandp-HydroxybenzylAlcoholinGastrodiaelataProcessedwithDifferentMethodsbyHigh-performanceLiquidChromatography
SHENXiao-jing1,2,JINChuan-shan1,2,XUFeng-qing1,2,LIBao-ming3,HUYu1,2
(1.SchoolofPharmacy,AnhuiUniversityofChineseMedicine,AnhuiHefei230012,China; 2.SynergeticInnovationCenterofAnhuiAuthenticChineseMedicineQualityImprovement,AnhuiHefei230012,China; 3.AnhuiXiehechengCo.,Ltd.,AnhuiBozhou236800,China)
ObjectiveTo establish a method for simultaneous determination of gastrodin and p-hydroxybenzyl alcohol inGastrodiaelataby high-performance liquid chromatography (HPLC) and to optimize the processing ofGastrodiaelatafrom different habitats.MethodsHPLC was performed on a Spursil C18-EP column (250 mm × 4.6 mm) with a mobile phase of methanol-0.1% phosphoric acid (5∶95) at a detection wavelength of 220 nm, a column temperature of 40 ℃, and a flow rate of 1 mL/min.ResultsThe content of gastrodin and p-hydroxybenzyl alcohol inGastrodiaelatadecoction pieces was highest afterGastrodiaelatawas processed by water steaming for 30 min, followed by decoction in clear water for 15 min, decoction in 0.2% alum solution for 15 min, and slicing after decoction.ConclusionGastrodiaelatais optimally processed by water steaming for 30 min, and theGastrodiaelatadecoction pieces produced by this method have the highest content of gastrodin and p-hydroxybenzyl alcohol.
Gastrodiaelata; gastrodin; p-Hydroxybenzyl alcohol; process; high-performance liquid chromatography
国家科技部国际合作项目(2011DF31950)
沈肖晶(1990-),女,硕士研究生
金传山,jcs4@sohu.com
R284
A
10.3969/j.issn.2095-7246.2014.06.022
2014-09-02)
