HPLC法测定维吾尔药散寒药茶中桂皮醛的含量
2014-09-11···
· · ·
1.新疆喀什地区药品检验所,新疆 喀什 844000;2.新疆维吾尔自治区人民医院北院药剂科,新疆 乌鲁木齐 830000
HPLC法测定维吾尔药散寒药茶中桂皮醛的含量
司马义江·阿布都热西提1阿迪力江·热加甫2买买斯迪克·台外库力1
1.新疆喀什地区药品检验所,新疆 喀什 844000;2.新疆维吾尔自治区人民医院北院药剂科,新疆 乌鲁木齐 830000
目的建立散寒药茶中桂皮醛的含量测定方法。方法采用高效液相色谱法,流动相为甲醇-5%甲醇溶液(50∶50);流速1 mL·min-1;检测波长290 nm;柱温:25℃;进样量:10 μL;分析方法:外标法。结果桂皮醛在10.0~250.9 μg·mL-1范围内线性良好(r=0.999 5),精密度RSD为0.72%(n=5),平均回收率为97.34%,RSD为1.84%(n=8)。结论该方法简便、准确、测得结果稳定重现性好,可作为该制剂的质量控制方法。
散寒药茶;桂皮醛;HPLC;含量测定
散寒药茶是由新疆维吾尔族名药之一,具有调解寒性气质,养胃,助食,爽神等功效。用于湿寒所致的消化不良,关节骨痛,腰腿痛,头痛神疲。药茶由小豆蔻、缬草、茴芹果、肉桂、草果、肉桂子、高良姜、荜苃、小茴香、丁香、桅子、芹菜籽等十二味药材混合,粉碎,过筛,混匀制成。属部颁标准—维吾尔药分册收录品种[1]。这十二味药材中丁香具有温中降逆,补肾助养功能、用于脾胃虚寒,呃逆呕吐,食少吐泻,心腹冷痛,肾虚阳痿[2]。部颁标准仅采用定性鉴别试验来控制该制剂的质量,研究该药物的含量测定方法可以更好的反映和控制该制剂的内在质量。
1 仪器和试药
日本岛津公司LC 20AT高效液相色谱系统;岛津uv-2450紫外可见分光光度计; 德国赛多利斯BP211D型分析天平;上海必能超声波有限公司CQX25-12型超声波清洗器。桂皮醛对照品(批号:110710-201217,中国药品生物制品鉴定所);散寒药茶(批号:130728、130933、131245,新疆维吾尔药业有限责任公司);甲醇为色谱纯(美国TEDIA试剂公司);水为重蒸馏水;其它试剂均为分析纯。所有色谱用试剂均用0.45gm微孔滤膜过滤。
2 方法与结果
2.1 色谱条件 色谱柱Inertsil ODS-SP(250×4.6mm 5μm);流动相:甲醇-5%甲醇溶液(50∶50);流速1mL·min-1;检测波长:290 nm;柱温:25℃;进样量:l0μL;分析方法:外标法[2]。
2.2 溶液的制备 精密称取桂皮醛对照品0.100 39g,置100mL容量瓶中,加流动相解制成每1mL中含1.003 9mg的溶液,作为对照品储备液,精密量取对照品储备液10mL置100mL容量瓶中,加流动相稀释至刻度,摇匀,制成每1mL中含0.100 39mg的溶液作为对照品溶液。取样品1g,精密称定,置具塞锥形瓶中,精密加入流动相50 mL,密塞,称定重量,超声处理(功率250W,频率50kHz)30min,擦干,放冷,再称定重量,用流动相补足减失的重量,用微孔滤膜(0.45μm)滤过,取续滤液即得供试品溶液。按散寒药茶原标准的处方、工艺制备不含桂皮醛的阴性对照样品,按供试品溶液的制备方法制备阴性对照溶液。
2.3 方法学考察
2.3.1 专属性试验 分别取对照品溶液、供试品溶液及阴性对照溶液,在“2.1项”的色谱条件下测定。结果:供试品溶液相应色谱峰与对照品桂皮醛一致。桂皮醛对照品保留时间为11.9min,理论塔板数大于10 000。阴性对照溶液无相应的色谱峰出现。
2.3.2 线性关系考察 精密量取对照品储备液(1.003 9mg·mL-1)1.0、2.5、5.0、10.0、15.0、20.0、25.0mL,分别置100mL量瓶中,加流动相稀释至刻度,摇匀,分别取10μL,按“2.1项”色谱条件下操作,以7次测定的峰面积平均值。以峰面积A为纵坐标,桂皮醛对照品溶液浓度(μg·mL-1)为横坐标进行线性回归,得回归方程为:A=103 128C+152 182,r=0.999.5(n=7)。结果表明,桂皮醛进样量在10.0~250.9μg范围为与峰面积线性关系良好。
2.3.3 精密度实验 精密量取对照品溶液储备液(1.003 9mg·mL-1)10mL置100mL量瓶中加流动相稀释至刻度,摇匀,取10μl,重复进样5次,以峰面积计算RSD(n=5) 为0.72%。说明本法及仪器精密度良好。
2.3.4 稳定性实验 取同一批号本品(批号为131 245),按“2.2项”方法配制溶液,分别于0、1、2、4、6h进样,进样量为10μl,测定桂皮醛的峰面积,RSD为1.4%,表明峰面积基本无变化,说明供试品溶液在12h内稳定。
2.3.5 加样回收率 精密量取已知含量的样品(批号为131245,桂皮醛含量5.327mg·g-1)称取1g,精密称定,置50mL容量瓶中,精密加入桂皮醛对照品溶液储备液(浓度为1.003 9mg·mL-1)5mL,再加流动相适量密塞,超声处理(功率250W,频率50kHz)30min,放冷,加流动相至刻度,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,作为加样回收率样品。同法制备8份加样回收率样品。按照样品测定项下的方法测定含量,计算回收率,结果见表1。
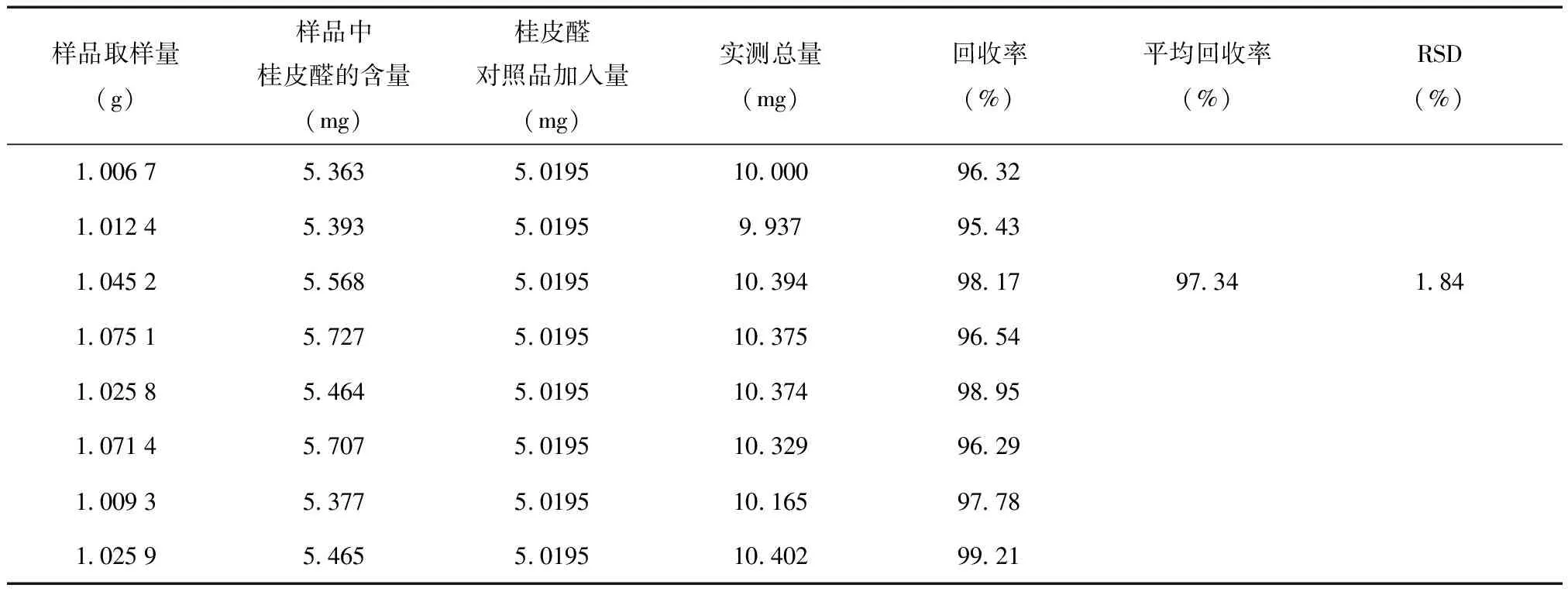
表1 加样回收率实验结果(n=8)
2.4 样品测定 取3批样品按“2.2项”方法制备供试品溶液,按“2.1项”色谱条件下测定,按外标法计算桂皮醛的含量。结果见表2。
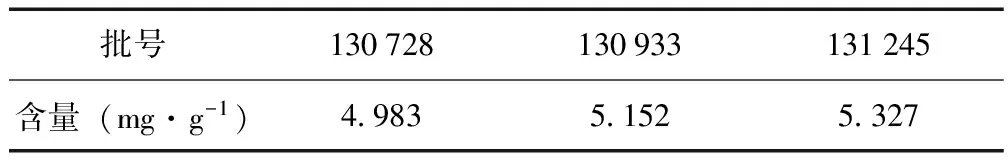
表2 散寒药茶中桂皮醛的含量测定结果(n=3)
3 讨论
3.1 检测波长的选择 取桂皮醛对照品适量,用流动相溶解并稀释成0.1mg·mL-1溶液,用紫外可见分光光度计于200~400nm处进行扫描,从其紫外图谱中可见其在225nm、288nm处有最大吸收,虽然在225nm处吸收比较强,但是干扰也比较大。故选择参考文献[2]中所规定的波长(290nm)为检测波长。
3.2 流动相的选择[3]参考文献报道的方法试验,流动相用甲醇-水(65:35)[3],甲醇-水(58:42)[4],由于散寒药茶处方中有十多味药材,杂峰较多,桂皮醛的分离效果不佳,通过不断改变甲醇与水的比例及流速,选定甲醇-5%甲醇溶液(50:50)及流速1mL·min-1比较合适,分离度及保留时间适宜,故选择甲醇-5%甲醇溶液(50:50)为流动相。
本实验对不同批号的散寒药茶,在不同的时间(30min,60min)进行超声处理进行测定,均能检出桂皮醛,其含量无明显差异,所以选择超声处理30min。通过实验研究,建立了散寒药茶桂皮醛含量的测定方法,方法简便,快速,重现性好,结果准确,可作为散寒药茶的质量控制方法。
[1]药典委员会.卫生部药品标准(维吾尔药分册)[S].1998:155.
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:4.
[3]余小平.高效液相色谱法测定丁香中丁香酚的含量[J].中国药物分析杂志,2008,28(6):975-976.
[4]吴军侠,赵红侠.高效液相色谱法测定蒙药暖宫七味散中丁香酚含量[J].中国药业,2010,19(5):31-32.
DeterminationofCinnamicaldehydeinUygurMedicinePreparationSanhanyaochabyHPLC
Simayijiang Abudurexiti1,Adilijiang Rejiapu2,maimaisidike taiwaikuli1
1.Kashi Institute for Drog Control,Kashi 844000,China;2.Department of pharmacy,North Hospital of Xinjiang Uygur Autonomous Region people′s Hospital,urmqi 830000,China
ObjectiveTo establish the determination method for Cinnamic aldehyde in sanhan yaocha .MethodsUsing HPLC with mobile phase of methanol,5% methanol solution (50∶50);the flow rate was lmL·min-1;the detection wavelength of 290 nm;column temperature: 25 ℃; sample size: l0 μ L; analysis method: the external standard method.ResultsCinnamic aldehyde. in 10.0~250.9μg· mL-1range of good linearity(r= 0.9995), method precision was RSD=0.72%(n=5), the average recovery was 97.34%, RSD was 1.84% (n=8).ConclusionsThe method is simple, accurate, stable and reproducible results, can be used as the quality control of the preparation method.
Sanhan yaocha;Cinnamic aldehyde;HPLC;content determination
司马义江·阿布都热西提 (1973-),男,大学本科,副主任药师,E-mail:simayi1102@126.com
R284.1
A
1007-8517(2014)11-0018-02
2014.04.16)
