可注射更昔洛韦温敏型原位凝胶剂的研究
2014-09-08王祺玥沈雁涂家生
王祺玥,沈雁,涂家生
(中国药科大学药学院药剂教研室,江苏 南京 210009 )
·药学研究· PHARMACEUTICAL RESEARCH
可注射更昔洛韦温敏型原位凝胶剂的研究
王祺玥,沈雁,涂家生*
(中国药科大学药学院药剂教研室,江苏 南京 210009 )

目的:构建温敏型三嵌段共聚物,研究其理化性质以及用其制备的可注射更昔洛韦温敏型原位凝胶剂的制剂特性。方法:以聚乙二醇(PEG)作为亲水嵌段,丙交酯(LA)和β-丁内酯(β-BL)的无规共聚物PBLA作为疏水嵌段,采用开环聚合法合成温敏型三嵌段共聚物PBLA-PEG-PBLA,并对其理化性质进行表征,考察其溶液的胶凝温度/临界凝胶浓度、流变学性质、通针性和溶蚀行为以及以更昔洛韦作为模型药物、用其制得的可注射载药温敏型原位凝胶剂的体外释放特性。结果:合成的PBLA-PEG-PBLA嵌段共聚物重均分子质量在6 000左右,多分散系数为1.5左右;其溶液临界凝胶浓度(g•mL-1)为5%~10%,质量浓度(g•mL-1)在10%~25%时胶凝温度为31~35 ℃,接近并略低于体温;其凝胶在低温下储能模量与黏度较小,当温度接近相转变温度后两者迅速增大;其载药凝胶剂累计释放量经拟合显示遵循一级动力学方程,并呈扩散释药机制。结论:较低质量浓度[10%~15%(g•mL-1)]的PBLA-PEG-PBLA更符合玻璃体注射要求,更适用于制备可注射载药温敏型原位凝胶剂。
温敏型三嵌段共聚物;PBLA-PEG-PBLA;更昔洛韦;可注射载药原位凝胶剂;相转变温度;储能模量;体外释放
原位凝胶作为一种新型递药系统,具有可于病变部位局部给药、延长释药周期、降低给药剂量、避免手术植入痛苦等特点。用作药物制剂的理想的注射型原位水凝胶至少应具备3种特性:1)可注射;2)可生物降解和组织相容性;3)适宜的胶凝速度与凝胶强度。当前,温敏型原位水凝胶的制备材料主要是具有生物相容性和可生物降解的聚酯聚醚类嵌段聚合物[1~6]。
更昔洛韦(ganciclovir,GCV)化学名为9-(1,3-二羟基-2-丙氧甲基)鸟嘌呤,是合成的核苷类抗病毒药,其作为第1个治疗人体巨细胞病毒(CMV)感染有效的药物,可阻断病毒DNA的合成及延伸[7]。目前国内上市的更昔洛韦制剂主要有注射剂、片剂和滴眼剂等,其中,滴眼剂用于眼部疾病治疗时,生物利用度低,作用时间短,最重要的是,其难以使药物通过角膜吸收而抵达眼后部,对视网膜、脉络膜和玻璃体疾患起不到作用;而全身使用常规剂量的更昔洛韦时,眼后组织中的药物浓度依旧很低,且易产生全身毒性[8]。但在治疗眼后部疾病时,通过玻璃体注射手段给药,往往能取得良好的效果[9]。
本文以聚乙二醇(PEG)作为亲水嵌段,丙交酯(LA)和β-丁内酯(β-BL)的无规共聚物PBLA作为疏水嵌段,通过开环聚合反应构建嵌段共聚物PBLA-PEGPBLA,合成一种适宜于玻璃体注射的新型温敏型凝胶材料,并以更昔洛韦作为模型药物,对用PBLA-PEGPBLA制备的载药温敏型原位凝胶剂的理化性质和制剂特性进行研究。
1 材料
1.1 仪器
AV-300型超导核磁共振波谱仪(瑞士Bruker 公司);Discovery HR-3混合型流变仪(美国TA仪器公司);STY-1渗透压测定仪(天大天发科技有限公司);SHZ-82A水浴恒温振荡器(常州国华电器有限公司);752N紫外可见分光光度计(上海精密科学仪器有限公司);凝胶渗透色谱仪,包括LC-20AT泵、RID-10A示差折光检测器、LC Solution工作站和Lab Solution GPC再解析软件(日本Shimadzu公司);TA.XTPlus质构仪(英国Stable Micro System公司)。
1.2 药品与试剂
D, L-LA(济南岱罡生物科技有限公司,批号:20130607);β-BL(Sigma-Aldrich化学公司,批号:MKBJ3709V);PEG 1500(Sigma-Aldrich化学公司,批号:BCBF0698V);异辛酸亚锡(Sigma-Aldrich化学公司,批号:SLBC8056V);GCV(湖北康宝泰精细化工有限公司,批号:20130511);聚苯乙烯(美国Varian公司,批号:20128-5)。乙腈和四氢呋喃均为色谱纯(美国Tedia公司),其他试剂均为国产分析纯;实验用水为实验室自制去离子水。
2 方法
2.1 PBLA-PEG-PBLA的合成
参照文献[10],称取PEG 1500和D, L-LA适量,置于干燥三颈烧瓶中,油浴加热至130 ℃,磁力搅拌下持续抽真空2 h,以除去PEG 1500和D, L-LA中的残留水分;随后,于氮气保护下,加入配比量的β-BL和占混合反应物总质量0.3%的异辛酸亚锡,反复抽真空,再在氮气保护下,升温至150 ℃,反应8 h;反应完成后,冷却至室温,加蒸馏水适量,在75 ℃水浴中反复洗涤3次,除去未反应的单体或低分子质量产物,冷冻干燥,即得目标产物(合成路线见图1),密封低温保存。

2.2 PBLA-PEG-PBLA核磁共振图谱的检测
采用AV-300核磁共振波谱仪,以氘代氯仿(CDCl3)为溶剂,四甲基硅烷(TMS)为内标,在室温(25 ℃)条件下,对合成的PBLA-PEG-PBLA样品进行核磁共振氢谱(1H NMR)检测。
2.3 PBLA-PEG-PBLA分子质量及其分布的测定
通过凝胶渗透色谱法(GPC)测定PBLA-PEG-PBLA样品的分子质量及其分布。在四氢呋喃(THF)为流动相、流速为1.0 mL·min-1、柱温为40 ℃、进样量为20 μL的色谱条件下,以聚苯乙烯为标准品,使用凝胶渗透色谱仪,对PBLA-PEG-PBLA样品进行检测,并记录色谱图,结果用LC Solution再解析软件处理。
2.4 PBLA-PEG-PBLA溶液相转变温度的测定
分别精密称取不同质量的PBLA-PEG-PBLA样品,加入去离子水,磁力搅拌溶解,制得质量浓度(g·mL-1)为5%、10%、15%、20%、25%、30%的样品溶液;分别量取2 mL不同质量浓度的样品溶液至西林瓶中,置于恒温水浴,升温范围为25~50 ℃,每升温0.5 ℃的平衡时间为2 min,观察西林瓶倾斜或倒置后样品溶液的流动性,若其在60 s内不流动即视为凝胶状态。
2.5 PBLA-PEG-PBLA溶液流变学性质考察
分别量取不同质量浓度的PBLA-PEG-PBLA样品溶液适量,加入混合型流变仪的测试盘上,使之完全充满两板间隙,37 ℃扫描线性范围,确定线型频率为1 Hz,应变幅度为0.1%,升温范围为25 ℃~40 ℃,升温速率为1 ℃·min-1,并以储能模量(G′)、黏性模量(G′′,即耗损模量)和复合黏度(η)为观察指标,将G′= G′′时的温度视为嵌段共聚物凝胶的相转变温度[11]。
2.6 PBLA-PEG-PBLA溶液通针性考察
保持环境温度为25 ℃,将质量浓度(g·mL-1)为20%的PBLA-PEG-PBLA样品溶液吸于1 mL注射器中,固定于质构仪平台,质构仪配备P/50R探头。设定程序,使用5 kg力量感应源,实验前速率为10 mm·s-1,实验速率和返回速率均为1 mm·s-1,测试距离为20 mm,感应力为0.2 g。记录探头感应力随探头移动距离的变化[12]。
2.7 PBLA-PEG-PBLA凝胶溶蚀行为考察
将不同质量浓度的PBLA-PEG-PBLA样品(批次:0702)溶液置于试管中,称重,于37 ℃恒温振荡,水浴静置10 min,待溶液完全转化为凝胶后,加入等温的磷酸盐缓冲液(PBS)4 mL作为溶蚀介质,同时开启摇床振荡,转速为100 r · min-1;分别于设定时间点(1、2、3、5、7、9、11、13、15和17 d),完全移出溶蚀液并挥干水分,称重后,补加等温的PBS继续溶蚀。通过计算得到溶蚀后剩余凝胶的质量,以未溶蚀凝胶百分比对时间作图,得到PBLA-PEG-PBLA凝胶的溶蚀曲线。
2.8 载药PBLA-PEG-PBLA溶液的制备
称取一定量PBLA-PEG-PBLA样品,加入pH为8.0、浓度为 0.05 mol·L-1的PBS,磁力搅拌溶解,加入处方量GCV,磁力搅拌至完全溶解,制得载药PBLA-PEGPBLA溶液。
2.9 载药PBLA-PEG-PBLA凝胶体外释放行为考察
称取GCV适量,配制质量浓度为100 mg·L-1的GVC储备液,分别精密吸取0.5、1、1.5、2、2.5和3 mL储备液至25 mL容量瓶中,去离子水定容,制得系列GCV标准溶液,采用紫外可见分光光度计,在252 nm处测定其吸光度。以GCV标准溶液的吸光度对相应质量浓度进行线性回归,得标准曲线:A=0.0427C+0.0156,r=0.9998。可见,GVC在2 ~12 mg·L-1的质量浓度范围内线性良好。
参照文献[13],采用无膜溶出模型,分别移取不同质量浓度的载药PBLA-PEG-PBLA溶液2 mL至试管中,于37 ℃恒温水浴中静置10 min,待溶液完全转化为凝胶后,加入4 mL PBS作为释放介质,启动摇床,设定转速为100 r·min-1;分别于1、2、3、4、8、12、24、36、48、60、72、84、96、120和144 h,停止震荡,移出所有溶出液,加入等量等温的PBS,继续释放实验;取出的溶出液经稀释,于波长252 nm处测定其吸光度,通过标准曲线方程计算绘制累计释放曲线。
3 结果
3.1 PBLA-PEG-PBLA的理化性质表征
3.1.1 化学结构与分子组成 依据所测1H NMR,确定合成的PBLA-PEG-PBLA的化学结构和分子组成。1H NMR(300 MHz,δ):1.29、1.59、2.59、3.64、3.93、4.28、5.16,各峰归属见图2。

图2 PBLA-PEG-PBLA的1H NMR谱图Figure 21H NMR spectrogram of PBLA-PEG-PBLA
3.1.2 分子质量及其分布 PBLA-PEG-PBLA的各原料单体进样后,LA的出峰时间在11 min左右,β-BL出峰也在10.5 min之后。而PBLA-PEG-PBLA进样后,出峰在8 min左右,且色谱图中未出现任何原料单体峰,表明此合成产物具有较高纯度。
通过GPC,以聚苯乙烯作为标准品,建立标准曲线方程:M = aX3+bX2+cX+d,r = 0.9999。其中,a = 7.111949e-3,b = -0.1791834, c = 1.037673,d = 3.414738。
由聚苯乙烯为标准品所测PBLA-PEG-PBLA的重均分子质量(Mw)、数均分子质量(Mn)及多分散指数(PDI,即Mw/Mn)如表1所示。

表1 PBLA-PEG-PBLA的分子质量及多分散系数Table 1 Molecular weight and PDI of PBLA-PEG-PBLA
由表1可见,通过GPC测定所得PBLA-PEGPBLA的Mn在4 000左右,Mw在6 000左右,PDI在1.5左右,分子质量分布较窄。
3.1.3 共聚物溶液相转变温度与临界凝胶浓度 共聚物的溶胶-凝胶相转变温度对于原位凝胶给药系统的成功设计至关重要。相转变温度过低,原位凝胶在常温下就有可能变为凝胶态,这对凝胶系统的给药带来很大的麻烦;而相转变温度过高,原位凝胶在注射入人体后仍可能保持溶胶态,便不能保证凝胶在给药部位的适宜滞留时间和缓释效果。
经检测,PBLA-PEG-PBLA在溶液中的质量浓度会对其溶胶-凝胶相转变温度产生明显影响,即随着溶液中共聚物质量浓度的增加,其相转变温度呈下降趋势:共聚物质量浓度(g·mL-1)在10%~25%之间时,其溶胶-凝胶相转变温度均在30~35 ℃之间,略低于体温,而质量浓度大于25%时,其溶液黏度明显增加,胶凝温度明显下降,致使其在常温下即成凝胶态,无法注射;共聚物质量浓度为5%时,在整个温度测量范围内均无法形成凝胶,随着温度的升高,其溶液产生白色沉淀,直接形成混悬液(见图3)。因此,PBLAPEG-PBLA溶液的临界凝胶浓度(g·mL-1)应在5%~10%之间。

图3 PBLA-PEG-PBLA溶液相图Figure 3 Phase diagram of PBLA-PEG-PBLA solution
3.1.4 共聚物溶液流变学性质 经检测,分别得到不同质量浓度的PBLA-PEG-PBLA溶液在相转变过程中其G′和G′′随着温度的变化曲线,其中质量浓度(g·mL-1)为15%时的变化曲线如图4所示。
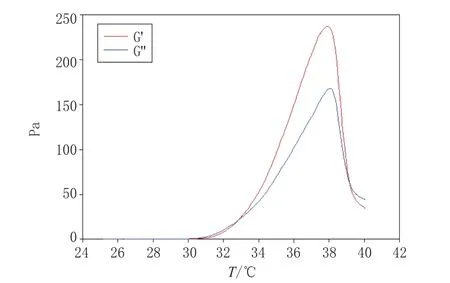
图4 15% PBLA-PEG-PBLA溶液在相转变过程中G′和G′′随着温度的变化曲线(线性频率为1Hz)Figure 4 Variance curve of G′ and G′′ of 15% PBLAPEG-PBLA solution with the temperature in phase transition process
由图4可见,在温度低于31 ℃时,PBLA-PEGPBLA溶液的G′和G′′均极小,表现为牛顿流体的性质;随着温度的升高,当温度处于31~35 ℃时,共聚物溶液的G′和G′′均迅速增加,表明凝胶的形成,且G′的增加更为迅速,超过了G′′,两条曲线相交于一点,此点对应的温度即为共聚物溶液的相转变温度;在温度超过38 ℃以后,共聚物溶液的G′和G′′均迅速下降,并再次相交,表明共聚物在温度继续升高后由凝胶态转化为沉淀,交点即为凝胶-沉淀相转变温度。
从图4中可明显看出PBLA-PEG-PBLA的溶胶-凝胶相转变温度即两条曲线的初始交点位于33 ℃附近。而且,随着共聚物溶液浓度的增加,其胶凝温度也略有下降,这同前述小瓶翻转法的测定结果在数值趋势上非常接近。表2对比了小瓶翻转法和流变学方法测定的PBLA-PEG-PBLA(批次:0702)胶凝温度值。

表2 小瓶翻转法与流变学方法所测不同质量浓度PBLAPEG-PBLA溶液的溶胶-凝胶相转变温度Table 2 Sol-gel temperatures of PBLA-PEG-PBLA solution of different concentrations determined by the Reversing method and Rheology method
图5则显示了PBLA-PEG-PBLA溶液在37 ℃时G′和G′′随着剪切频率的变化曲线。

图5 37 ℃时PBLA-PEG-PBLA溶液G′和G′′随着剪切频率的变化曲线Figure 5 Variance curve of G′ and G′′ of PBLA-PEGPBLA solution with the shear frequency at 37 ℃
由图5可见,在37℃时,PBLA-PEG-PBLA溶液的G′和G′′均随着剪切频率呈非线性增加的趋势,且最初G′均大于G′′,说明该温度条件下,此共聚物体系的弹性大于黏性,即共聚物溶液形成了凝胶;但当剪切频率上升到一定程度后,共聚物体系的G′′重新超过G′,即体系的黏性大于弹性,这可能是由于剪切频率过大后,破坏了凝胶的三维结构,体系黏度下降,凝胶重新具备流动性所致。
G′是描述凝胶固态性质的特征参数,广泛用于对凝胶强度的科学量度。图6便显示,随着溶液中PBLAPEG-PBLA质量浓度的增加,其G′呈现极明显的增加,即共聚物凝胶强度随着其质量浓度的增加而增加。

图6 不同质量浓度PBLA-PEG-PBLA溶液在相转变过程中G′随着温度的变化曲线(线性频率为1Hz)Figure 6 Variance curve of G′ of different concentrations of PBLA-PEG-PBLA solution with the temperature in phase transition process
黏度是温敏型原位凝胶重要的流变学特性。在室温条件下,PBLA-PEG-PBLA溶液的黏度略高于普通注射液,且不同质量浓度的共聚物溶液其黏度差距也不明显,即共聚物溶液与普通注射液的黏度并无明显差别;但随着温度的升高,共聚物溶液的黏度开始迅速增加,并呈浓度依赖性,即黏度随着其质量浓度的增加而增加(见图7)。

图7 不同质量浓度PBLA-PEG-PBLA溶液与普通注射液的黏度随着温度的变化曲线Figure 7 Variance curve of viscosities of different concentrations of PBLA-PEG-PBLA solution and ordinary injection with the temperature
3.2 PBLA-PEG-PBLA溶液通针性
通针性是决定可注射材料与制剂能否研制成功的关键性质,主要以注射时所需的压力和压强以及顺滑程度来衡量。通针性考察时所测参数主要包括注射活塞的初始滑动力(plunger-stopper breakloose force,PBF,即使注射活塞开始移动时所需的力)、最大滑动力(maximum force,,Fmax,即在整个注射过程中活塞所受到的最大阻力)和动态滑动力(dynamic glide force,DGF,即持续注射时活塞所受到的阻力)。
由于注射部位的特殊性,玻璃体注射用针头的型号有着明确的规定。美国眼科交流学会发布的玻璃体内注射指南中规定,玻璃体注射所用针头应为长度是1/2~5/8 in(1 in= 25.4 mm)的27号或更小的针头。使用比27号更粗的针头易引起患者的不适,而规定针头的长度则是为了减少注射时针头伤及视网膜或其他眼内结构的危险。
通针性实验显示,针头规格越细,PBLA-PEGPBLA溶液通过针头时所遇到的动态滑动阻力越大,其通过27 G×12.9 mm针头时所需DGF明显最大,而通过24 G×20 mm针头时所需DGF明显较小(见图8);共聚物溶液的整个注射过程中所需的Fmax与PBF相同,两者并没有随着针头规格的变化而产生明显的变化,说明注射过程中所遇到的起始阻力受针头型号的影响较小,故推测影响起始阻力的主要因素可能是注射器针筒的横截面积及吸取的液体体积。
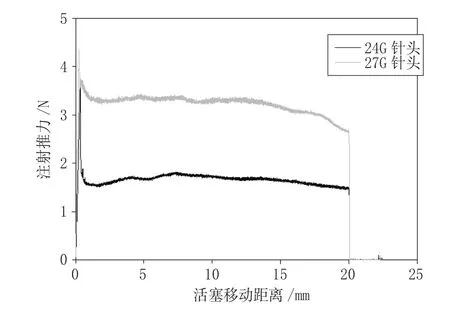
图8 以1mm·s-1速率推注PBLA-PEG-PBLA溶液(20%)通过配有不同规格针头的1 mL注射器时所需推力Figure 8 Required forces to inject PBLA-PEG-PBLA solution (20%) from 1 mL syringers equipped with different specifications of the needles into air at 1 mm·s-1
此外,PBLA-PEG-PBLA溶液中共聚物质量浓度对Fmax、PBF和DGF产生显著影响:推注质量浓度(g·mL-1)为25%的共聚物溶液时所需DGF约为4 N,而注射普通注射液时仅需1 N(见图9)。这说明,随着共聚物质量浓度的增加,注射共聚物溶液时所遇到的动态阻力也会增大,注射原位凝胶剂的难度将大于普通注射液,故在保证制剂载药量和释放特性等基本不变的前提下尽可能减少共聚物的使用量。

图9 以1mm·s-1速率推注不同质量浓度PBLA-PEGPBLA溶液与普通注射液通过配有27 G×12.9 mm针头的1 mL注射器时所需推力Figure 9 Required forces to inject PBLA-PEG-PBLA solutions with different concentration or ordinary injection from 1 mL syringer equipped with 27 G×12.9 mm needle into air at 1 mm·s-1
3.3 PBLA-PEG-PBLA凝胶溶蚀特性
从凝胶溶蚀曲线可见,不同质量浓度(g·mL-1)的PBLA-PEG-PBLA凝胶溶蚀行为均呈现先快后慢的趋势:1 d时,凝胶溶蚀非常迅速,其中10%共聚物凝胶溶蚀了约35%,15%共聚物凝胶则溶蚀了约15%;从2 d开始,凝胶的溶蚀速率呈递减之势,直至基本稳定,每两天的溶蚀量均占溶蚀总量的4%~5%,其中10%共聚物凝胶溶蚀速率略快于15%共聚物凝胶;3 d后,可明显观察到凝胶出现软化,10%共聚物凝胶尤为显著,凝胶的流动性明显增加,同时凝胶表面溶蚀产生的碎片明显增加(见图10)。

图10 不同质量浓度PBLA-PEG-PBLA凝胶溶蚀曲线Figure 10 Erosion curves of different concentrations of PBLA-PEG-PBLA gel
3.4 载药PBLA-PEG-PBLA凝胶体外释放特性
从载药凝胶累积释放曲线可见,GCV在不同质量浓度的PBLA-PEG-PBLA凝胶中释放均比较迅速,在质量浓度(g·mL-1)为15%的共聚物凝胶中其24 h释放量约为45%,96 h后基本释放完全,最终平台期释药超过85%(见图11)。将累计释药量进行拟合,发现药物释放符合一级动力学,呈扩散机制。该共聚物凝胶有明显的突释行为,但其中共聚物质量浓度越高,药物突释量便越少。

图11 载药PBLA-PEG-PBLA凝胶累积释放曲线
4 讨论
NMR及GPC检测结果表明,本文合成的PBLAPEG-PBLA分子质量与嵌段比较适宜。且对该共聚物性质的考察发现,其在10%~20%(g·mL-1)的质量浓度范围内具有良好的温敏性和可注射性,为其用于制备可注射原位凝胶制剂创造了初步条件。
以GVC为模型药物的PBLA-PEG-PBLA凝胶体外释放实验结果表明,该共聚物凝胶在24 h内释药量超过40%,累计释药量可超过85%,持续释药时间约为96 h,具有缓释效果,但也存在明显的突释现象。载药PBLA-PEG-PBLA凝胶发生突释的原因主要是GCV在水中的溶解度较好,其在pH为7的水中溶解度达 4.3 g· L-1,在载药凝胶的形成过程中,因GCV并没有完全进入由胶束内核聚集构成的疏水部分,部分存在于胶束与胶束之间的亲水部分,致使其通过扩散机制快速释放;其次,可能是由于凝胶中含有的少量低分子共聚物,其降解速度更快,且其疏水嵌段长度减小,致使凝胶强度下降,凝胶内部三维结构的空隙增大,导致药物释放迅速。
鉴于PBLA-PEG-PBLA凝胶具有突释效应,其更适宜负载高疏水性或大分子药物,而对亲水性药物较难包载。不过,对其疏水嵌段进行修饰改造,有可能改善其对亲水性药物的包载问题。
嵌段共聚物原位凝胶良好的理化性质及安全性使其成为极具发展前景的药物载体,而PBLA-PEG-PBLA作为具有优良性质的新型温敏型嵌段共聚物,为制备理想的可注射载药原位凝胶提供了新的可能,也将促进该类共聚物在药物制剂中的应用研究。
[1]Yu L, Ding J. Injectable hydrogels as unique biomedical materials[J]. Chem Soc Rev, 2008, 37(8): 1473-1481.
[2]Li Z, Guan J. Thermosensitive hydrogels for drug delivery[J]. Expert Opin Drug Deliv, 2011, 8(8): 991-1007.
[3]Yang H, Kao W. Thermoresponsive gelatin/monomethoxy poly (ethylene glycol)–poly (D, L-lactide) hydrogels: formulation, characterization, and antibacterial drug delivery[J]. Pharm Res, 2006, 23(1): 205-214.
[4]董吉, 蒋曙光, 平其能. 注射型原位凝胶植入剂的研究进展[J]. 药学进展, 2007, 31(3): 109-113.
[5]乔明曦. 注射用温敏型PLGA-PEG-PLGA嵌段共聚物合成及其应用研究[D]. 沈阳: 沈阳药科大学, 2005.
[6]Elstad N L, Fowers K D. OncoGel (ReGel/paclitaxel)—clinical applications for a novel paclitaxel delivery system[J]. Adv Drug Deliv Rev, 2009, 61(10): 785-794.
[7]耿海明. 更昔洛韦眼用凝胶剂的研究[D]. 沈阳: 沈阳药科大学, 2007.
[8]Janoria K G, Boddu S H, Wang Z, et al. Vitreal pharmacokinetics of biotinylated ganciclovir: role of sodium-dependent multivitamin transporter expressed on retina[J]. Ocul Pharmacol Ther, 2009, 25(1): 39-49.
[9]Smith T J, Pearson P A, Blandford D L, et al. Intravitreal sustainedrelease ganciclovir[J]. Arch Ophthalmol, 1992, 110(2): 255-258.
[10]Xu Y, Shen Y, Xiong Y, et al. Synthesis, characterization, biodegradability and biocompatibility of a temperature-sensitive PBLA-PEG-PBLA hydrogel as protein delivery system with low critical gelation concentration[J]. Drug Dev Ind Pharm, 2014, 40(9):1264-1275.
[11]刘静, 秦国伟, 蒲春生. 温敏凝胶流变性能动力学研究[J]. 功能材料, 2012, 43(4): 454-456.
[12]Cilurzo F, Selmin F, Minghetti P, et al. Injectability evaluation: an open issue[J]. AAPS PharmSciTech, 2011, 12(2): 604-609.
[13]杨辛欣, 李超英. 眼部给药系统体内外评价方法的研究进展[J]. 中国新药杂志, 2008, 17(13): 1101-1104.
Study on Injectable Thermosensitive In-situ Hydrogel as Ganciclovir Delivery System
WANG Qiyue, SHEN Yan, TU Jiasheng
( Department of Pharamaceutics, School of Pharmacy, China Pharmaceutical University, Nanjing 210009, China)
Objective: To construct thermosensitive triblock copolymer and to investigate its physicochemical properties and the characteristics of the injectable thermosensitive in-situ hydrogel as ganciclovir (GCV) delivery system prepared with the copolymer. Methods: A thermosensitive PBLA-PEG-PBLA triblock copolymer was synthesized with polyethylene glycol (PEG) as the hydrophilic block and PBLA random copolymer comprising lactide(LA) and β-butyrolacton(β-BL) as the hydrophobic block by ring-opening polymerization. Its physicochemical properties were characterized as well as the gelation temperature/critical gel concentration, rheological property, syringeability and dissolution behavior of its solution and in vitro release property of the drug-loaded injectable thermosensitive in-situ hydrogel prepared with GCV as a model drug and the copolymer were investigated. Results: The average molecular weight (Mw) of the synthesized PBLA-PEG-PBLA copolymer was about 6 000 with a narrow polydispersity (PDI) of approximate 1.5. The critical gel concentration (g • mL-1)of its solution was between 5% to 10% and gelation temperature of its solution was about 31-35 ℃ which was slightly lower than body temperature at the concentration(g • mL-1) range of 10%-25%. The storage modulus and viscosity of the hydrogel solution were low (below Ts-g) , but could increase rapidly when temperature reached Ts-g,. The cumulative release curve of the drug-loaded hydrogel followed the one-order kinetics with a diffusion-release mechanism. Conclusion: Low concentrations(10%-15% g • mL-1) of PBLA-PEG-PBLA copolymer conforms more completely to the requirements of intravitreous injection of copolymers and is applicable to the preparation of the drug-loaded injectable thermosensitive in-situ hydrogel.
thermosensitive triblock copolymer; PBLA-PEG-PBLA; ganciclovir; drug-loaded injectable in-situ hydrogel; sol-gel transition temperature; storage modulus; in vitro release
R318.08 ; R944.9
A
1001-5094(2014)10-0754-07
接受日期:2014-04-23
*通讯作者:涂家生,教授;
研究方向:药物新剂型与新技术;
Tel:025-83271305; E-mail:jiashengtu@aliyun.com
