exendin-4类似物EW的降糖活性的研究
2014-09-07唐玲陆怡吴晓琰
唐玲 陆怡 吴晓琰
(1.上海市北站医院内科,上海 200070;2.复旦大学附属华山医院老年科,上海 200040)
中华医学会糖尿病学会2007年6月—2008年5月的一项全国性横断面调查研究[1]发现,我国糖尿病患者达9200万,20岁以上人群中年龄标化的糖尿病患病率高达9.7%,其中2型糖尿病占90%以上。据英国前瞻性糖尿病研究(UK prospective diabetes study,UKPDS)、糖尿病心血管风险控制行动(action to control cardiovascular risk in diabetes,ACCORD)及糖尿病和心血管病行动(action in diabetes and vascular disease,ADVANCE)报道,常用的6大类治疗糖尿病的药物(双胍类、磺脲类、格列奈类、噻唑烷二酮类、α-糖苷酶抑制剂及胰岛素)均不能长期有效地降低血糖,也不能阻止2型糖尿病及其并发症的进展[2-3]。此外,这些降糖药物的安全性也尚待阐明。
胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)是由小肠黏膜分泌的多肽,多肽长30个氨基酸,餐后其在血清中的浓度迅速增高,半衰期1.5~2.1 min[4]。GLP-1对2型糖尿病患者有以下作用:血糖依赖性地刺激胰腺β细胞分泌胰岛素;增加胰腺β细胞体积;抑制胰腺α细胞分泌胰高血糖素及中枢性抑制食欲等。GLP-1由血浆中的二肽基肽酶4(dipeptidyl peptidase-4,DPP4)酶解,由肾脏及其他蛋白酶如人中性内肽酶24.11(neutral endopeptidase 24.11,NEP24.11)酶解清除,前者是主要途径[5]。GLP-1受体途径治疗是目前治疗糖尿病的新途径[5-9]。GLP-1受体途径药物包括GLP-1受体激动剂及DPP4酶抑制剂。
GLP-1受体激动剂exendin-4含39个氨基酸,与GLP-1受体结合并激活受体,模拟GLP-1的功能。其N端的序列是His、Gly,能够抵抗DPP4,半衰期3~5 h,是中效的抗糖尿病药物,具有良好的降糖作用,可单独应用或与其他口服抗糖尿病药物及胰岛素联用[10-15]。GLP-1还可使体质量持续减轻,并有助于改善多项心血管危险因素[16]。由于exendin-4较人源GLP-1的末端肽链延长了9个氨基酸,故有免疫源性,40%~50%患者注射后可在血浆中检测到不同滴度的抗体[17]。
Wu等[18-19]设计了一种新的exendin-4类似物EW(PCT/CN2009/001321), 飞行质谱(MALDI-MS)分析证明符合设计,并在小鼠体内初步证实了其降糖活性。本研究旨在进一步研究EW的降糖活性及安全性。
1 资料与方法
1.1 实验动物 C57BL/6小鼠(雄性,8周,体质量约20 g);db/db小鼠(雄性,8周,体质量约40 g)及昆明鼠(雄性,8周,体质量约30 g)均由中国科学院上海实验动物中心提供。饲养房间温度(22±2)℃,12 h照明/12 h黑暗循环,饮水,给予标准啮齿类动物饮食供应。动物实验遵循“北京医科大学动物照料及福利委员会”准则。
1.2 材料 分析纯葡萄糖(上海国药集团化学试剂公司),葡萄糖测定试剂盒(北京鼎国生物技术有限公司),人胰岛素及exendin-4(美国Lilly公司)。EW样品为本实验室通过大肠杆菌表达合成,见文献[18-19]。
1.3 方法
1.3.1 血浆葡萄糖测定方法 C57BL/6小鼠和db/db小鼠禁食18 h后,用毛细管取10 μL尾静脉血,转入肝素化微量离心管中,离心后将血浆保存于-20 ℃。采用葡萄糖氧化酶法测定血浆葡萄糖。
1.3.2 各药物在C57BL/6小鼠中的降糖作用 按照随机数字表,将C57BL/6小鼠随机分为3组(n=10),取空腹血后每组小鼠分别腹腔注射EW(2 μg EW,100 μL的0.9%氯化钠液)、exendin-4(2 μg exendin-4,100μL的0.9%氯化钠液)、100 μL的0.9%氯化钠液;3组均于即刻及每隔2 h腹腔注射20%葡萄糖300 μL(60 μg),共5次。每次腹腔注射葡萄糖后20 min取尾静脉血,测定血糖。
1.3.3 各药物在db/db小鼠中的降糖作用 按照随机数字表,将db/db小鼠随机分为3组(n=3),取空腹血后每组小鼠分别腹腔注射低浓度EW溶液(2 μg EW,100 μL的0.9%氯化钠液)、高浓度EW溶液(5 μg EW,100 μL的0.9%氯化钠液)、100 μL的0.9%氯化钠液;3组均于即刻及每隔4 h腹腔注射20%葡萄糖300 μL(60 μg),共3次。每次腹腔注射葡萄糖前及腹腔注射葡萄糖后30 min取尾静脉血,测定血糖。
1.3.4 C57BL/6小鼠中EW对胰岛素的增敏作用 C57BL/6小鼠禁食18 h后,按照随机数字表将其随机分成6组(n=3)。其中3组毛细管取10 μL尾静脉血,测得血糖为基础血糖(base),取血后每组小鼠分别腹腔注射胰岛素0.3、1.0、2.0 μg,随后即刻腹腔注射20%葡萄糖300 μL(60 μg),腹腔注射葡萄糖后20 min取10 μL尾静脉血,测定血糖;另外3组C57 BL/6小鼠取空腹血后每组小鼠(n=3)分别腹腔注射胰岛素0.3 μg、EW 0.2 μg、胰岛素0.3 μg+EW 0.2 μg后,即刻腹腔注射20%葡萄糖300 μL(60 μg),腹腔注射葡萄糖后20 min取10 μL尾静脉血,测定血糖。
1.3.5 EW的急性毒性实验 按照随机数字表将昆明鼠随机分为3组(n=10),每组分别一次腹腔注射EW 0.1 mg/100 μL的0.9%氯化钠液、EW 0.2 mg/100 μL的0.9%氯化钠液及100 μL的0.9%氯化钠液,观察小鼠1周内存活数量。
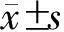
2 结 果
2.1 各药物在C57BL/6小鼠中的降糖作用 腹腔注射葡萄糖前EW组、exendin-4组及0.9%氯化钠液组平均血糖分别是(6.39±1.37)mmol/L、(5.87±1.16)mmol/L及(6.18±1.15)mmol/L (P>0.05)。4次葡萄糖注射后,0.9%氯化钠液组平均血糖逐渐上升至(25.04±2.10)mmol/L ,而EW组及exendin 4组平均血糖分别是(8.54±2.10)mmol/L 及(6.93±1.84)mmol/L,后2组间差异无统计学意义,但2组与0.9%氯化钠液组比较差异有统计学意义(P<0.01)。0、2、4、6 h腹腔注射葡萄糖后,EW组及exendin-4组血糖均维持在正常范围内,8 h腹腔注射葡萄糖后EW组及exendin-4组血糖明显上升,2组间差异无统计学意义,但与0.9%氯化钠液组差异仍有统计学意义(P<0.01)。见图1。
2.2 各药物在db/db小鼠中的降糖作用 腹腔注射葡萄糖前EW 2 μg组、EW 5 μg组及0.9%氯化钠液组平均血糖分别是(21.33±5.10)mmol/L、(20.46±3.15)mmol/L 和(19.37±2.92)mmol/L (P>0.05)。第1次腹腔注射葡萄糖30 min后,0.9%氯化钠液组血糖显著上升至(26.9±4.75)mmol/L,而EW 2 μg组及EW 5 μg组平均血糖分别为(18.16±1.90)mmol/L及(12.87±2.63)mmol/L,与0.9%氯化钠液组比较差异有统计学意义(P<0.01),且EW 2 μg组及EW 5 μg组间差异有统计学意义(P<0.01),EW治疗剂量增大,降糖效果明显。第1次腹腔注射葡萄糖1 h后,0.9%氯化钠液组平均血糖为(22.23±3.52)mmol/L,而EW 2 μg组及EW 5 μg组平均血糖分别为(15.00±2.72)mmol/L 及(10.87±1.59)mmol/L,与0.9%氯化钠液组比较差异有统计学意义(P<0.01),且EW 2 μg组及EW 5 μg组差异仍有统计学意义(P<0.01),EW 5 μg组降糖效果较好。第一次腹腔注射葡萄糖4 h后EW 2 μg组、EW 5 μg组与0.9%氯化钠液组平均血糖差异均有统计学意义(P<0.01),EW 2 μg组及EW 5 μg组间差异亦有统计学意义(P<0.01)。第2次腹腔注射葡萄糖30 min后测定平均血糖,EW组与0.9%氯化钠液组差异有统计学意义(P<0.01),且EW 2 μg组及EW 5 μg组间差异仍有统计学意义(P<0.01)。第5次腹腔注射葡萄糖8 h后EW 2 μg组、EW 5 μg组与0.9%氯化钠液组平均血糖差异无统计学意义(P>0.05)。第3次腹腔注射葡萄糖30 min后测定平均血糖,EW组与0.9%氯化钠液组差异有统计学意义(P<0.01),且EW 2 μg组及EW 5 组差异仍有统计学意义(P<0.01)。见图2。
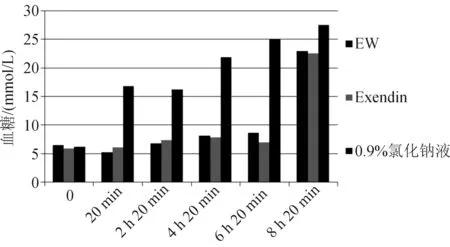
图1 腹腔注射5次60 μg葡萄糖后C57BL/6小鼠的血糖水平
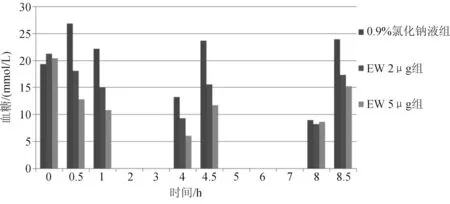
图2 腹腔注射3次60 μg葡萄糖后db/db小鼠的血糖水平
2.3 C57BL/6小鼠中EW对胰岛素的增敏作用 胰岛素的降低血糖作用呈剂量依赖性,当胰岛素剂量为0.3 μg时,无明显降糖效果,而当胰岛素剂量为2 μg时,降糖效果明显。见图3右图。当注射胰岛素0.3 μg及EW 0.2 μg时发现血糖无明显下降,而当注射胰岛素0.3 μg+EW 0.2 μg时血糖下降明显,说明EW对胰岛素有增敏作用。见图3左图。
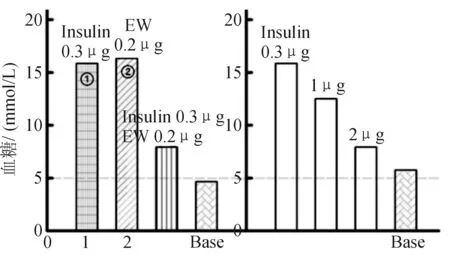
图3 EW对胰岛素的增敏作用
2.4 安全性 昆明鼠腹腔注射0.1 mg EW/100 μL的0.9%氯化钠液、0.2 mg EW/100 μL的0.9%氯化钠液及0.9%氯化钠液后观察1周,所有小鼠均存活,证明应用EW安全。
3 讨 论
exendin-4可与GLP-1受体结合而激活受体,它的N-端序列(His、Gly、Glu)不被DPP4所识别(DPP4通常迅速切断GLP-1的N-端的His、Ala、Glu序列),exendin-4在体内半衰期比GLP-1长。将exendin-4缩短至32个氨基酸,并更换一些氨基酸,设计得到exendin-4类似物EW,将EW串联后在E.coli中表达,通过胰蛋白酶定点切断获得重组EW,EW分子量为3581.5 Da。
C57BL/6小鼠是具有2型糖尿病倾向的小鼠模型,其基线血糖基本正常,给糖后其血糖水平明显高于正常鼠模型昆明鼠。本研究显示,EW在C57BL/6小鼠体内有良好的降糖活性,仅1次给予EW或exendin-4后,每隔2 h给予糖负荷,降糖作用可保持6 h以上,而且2 μg的EW与2 μg的exendin-4降糖效果无显著差异。这表明EW的降糖作用及有效作用时间与exendin-4相当,故exendin-4 C-端的7个氨基酸对于exendin-4在体内的生物活性并非必须。32个氨基酸的EW,从长度和结构而言,更接近人源的GLP-1;从理论上而言,可以减少过敏反应的产生,增加安全性。1次给予2 μg的EW,无明显低血糖反应,证明EW的降糖机制是血糖依赖的,故避免了低血糖,增加了安全性。1次给予2 μg的EW后,反复给予60 μg葡萄糖,血糖保持稳定8 h,说明EW是一个中效的抗糖尿病药物。
db/db小鼠是2型糖尿病鼠模型,空腹血糖即有增高,给糖后血糖进一步增高。本研究显示,EW在db/db小鼠中有血糖依赖的降糖作用,无明显低血糖反应,增加EW剂量可以使降糖效果更为显著。
本研究在C57BL/6小鼠中,进一步将小剂量的EW与小剂量的胰岛素合用,结果发现,EW对胰岛素有增敏作用。目前对exendin-4增加胰岛素敏感性的研究并不多,有待进一步研究。
昆明鼠是正常小鼠模型,本研究对昆明鼠腹腔注射超大剂量的EW,所有小鼠均存活,验证了EW的安全性。
综上所述,EW具有良好的生物体内降糖活性及安全性,是一种很有前景的抗糖尿病药物,它能通过基因工程大规模廉价的生产获得,值得进一步研究。
[1]Yang W,Lu J,Weng J,et al.Prevalence of diabetes among men and women in China [J].N Engl J Med,2010,362(12):1090-1101.
[2]Turner RC,Cull CA,Frighi V,et al.Glycemic control with diet,sulfonylurea,metformin,or insulin in patients with type 2 diabetes mellitus:progressive requirement for multiple therapies (UKPDS 49).UK Prospective Diabetes Study(UKPDS) Group[J].JAMA,1999,281(21): 2005-2012.
[3]Nathan DM.Finding new treatments for diabetes--how many,how fast...how good?[J].N Engl J Med,2007,356(5):437-440.
[5]Drucker DJ,Nauck MA.The incretin system:glucagon-like peptide-1 receptor agonists and dipeptidyl peptidase-4 inhibitors in type 2 diabetes[J].Lancet,2006,368(9548):1696-1705.
[6]Jellinger PS.Focus on incretin-based therapies:targeting the core defects of type 2 diabetes[J].Postgrad Med,2011,123(1):53-65.
[7]Gallwitz B.The evolving place of incretin-based therapies in type 2 diabete[J].Pediatr Nephrol, 2010,25(7):1207-1217.
[8]Gallwitz B.GLP-1 Agonists and dipeptidyl-peptidase IV Inhibitors[J].Handb Exp Pharmacol, 2011,(203):53-74.
[9]Davidson JA.Incorporating incretin-based therapies into clinical practice:differences between glucagon-like Peptide 1 receptor agonists and dipeptidyl peptidase 4 inhibitors[J].Mayo Clin Proc,2010,85(12 Suppl):S27-S37.
[10]Heine RJ,Van Gaal LF,Johns D,et al.Exenatide versus insulin glargine in patients with suboptimally controlled type 2 diabetes:a randomized trial[J].Ann Intern Med,2005,143(8): 559-569.
[11]DeFronzo RA,Ratner RE,Han J,et al.Effects of exenatide(exendin-4) on glycemic control and weight over 30 weeks in metformin-treated patients with type 2 diabete[J].Diabetes Care,2005, 28(5):1092-1100.
[12]Buse JB,Henry RR,Han J,et al.Effects of exenatide(exendin-4) on glycemic control over 30 weeks in sulfonylurea-treated patients with type 2 diabetes[J].Diabetes Care,2004,27(11): 2628-2635.
[13]Kendall DM,Riddle MC,Rosenstock J,et al.Effects of exenatide(exendin-4) on glycemic control over 30 weeks in patients with type 2 diabetes treated with metformin and a sulfonylurea[J].Diabetes Care,2005,28(5):1083-1091.
[14]Guerci B,Martin CS.Exenatide:its position in the treatment of type 2 diabetes[J].Ann Endocrinol(Paris),2008,69(3):201-209.
[15]Hansen KB,Knop FK,Holst JJ,et al.Treatment of type 2 diabetes with glucagon-like peptide-1 receptor agonists[J].Int J Clin Pract,2009,63(8):1154-1160.
[16]Klonoff DC,Buse JB,Nielsen LL,et al.Exenatide effects on diabetes,obesity,cardiovascular risk factors and hepatic biomarkers in patients with type 2 diabetes treated for at least 3 years[J].Curr Med Res Opin,2008,24(1):275-286.
[17]Gallwitz B.Benefit-risk assessment of exenatide in the therapy of type 2 diabetes mellitus[J].Drug Saf,2010,33(2):87-100.
[18]Wu XY,Lu Y,Zhao H,et al.EW,a novel recombinant analogue of exendin-4 expressed in Escherichia coli[J].SCI RES ESSAYS,2011,6(14):2941-2949.
[19]吴晓琰,施晓梅,陆怡.重组exendin-4类似物EW的制备及其体内降糖活性分析[J].中国临床医学,2013,20(3):263-266.
