新型1,1-双二茂铁基丁烷衍生物的合成*
2014-08-30李纯毅王晓莉邓起发
李纯毅,王晓莉,邓起发,付 渊
(1.内蒙古化工职业学院,内蒙古 呼和浩特 010010;2.鄂尔多斯市环境监测站,内蒙古 鄂尔多斯 017000)
·快递论文·
新型1,1-双二茂铁基丁烷衍生物的合成*
李纯毅1,王晓莉1,邓起发2,付 渊1
(1.内蒙古化工职业学院,内蒙古 呼和浩特 010010;2.鄂尔多斯市环境监测站,内蒙古 鄂尔多斯 017000)
1,1-双二茂铁基丁烷和乙酸酐经Friedel-Crafts酰基化反应得6-乙酰基-1,1-双二茂铁基丁烷(2);2经LiAlH4还原得6-α-羟乙基-1,1-双二茂铁基丁烷(3);3经消除反应合成了6-乙烯基-1,1-双二茂铁基丁烷(4)。2~4为新化合物,其结构经1H NMR,IR,MS和元素分析表征。
1,1-双二茂铁基丁烷;酰化反应;还原反应;消去反应;合成
具有芳香性过渡金属(Fe)π络合物的二茂铁及其衍生物,由于能在茂环上进行多种反应而制备具有不同结构和功能的化合物,因而具有重要价值和广泛的应用前景[1]。其中不少该类化合物可作为航天工业燃速催化剂,但是单核的二茂铁类化合物具有明显的迁移和挥发问题。而双核二茂铁类化合物可大大改善二茂铁及其衍生物作为燃速催化剂存在的挥发和迁移问题[2]。双核二茂铁基烷的酰化衍生物及相应的醇是合成其他双核二茂铁衍生物重要的中间体[3]。而双二茂铁基烷的α-羟烷基类衍生物的分子中由于茂环的增多以及高活性官能团的引入,增加了燃速催化剂的分子量和分子极性,从而降低了其挥发性和迁移性,而且该类化合物的含铁量高,双二茂铁基又是连在叔碳原子上,具有很高的抗氧化性[4]。
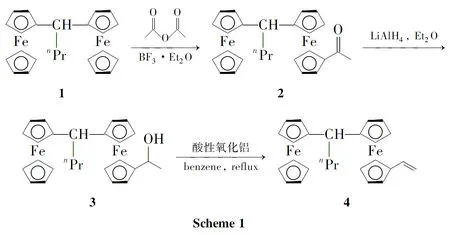
本文以1,1-双二茂铁基丁烷(1)和乙酸酐经Friedel-Crafts酰基化反应制得6-乙酰基-1,1-双二茂铁基丁烷(2);2经LiAlH4还原得6-α-羟乙基-1,1-双二茂铁基丁烷(3);3经消除反应合成了6-乙烯基-1,1-双二茂铁基丁烷(4,Scheme 1)。2~4为新化合物,其结构经1H NMR,IR,MS和元素分析表征。
1 实验部分
1.1 仪器与试剂
MERCURY-300型超导核磁共振仪(CDCl3为溶剂,TMS为内标);NEXUS-670型傅立叶红外光谱仪(KBr压片);ZAB-HS型双聚焦高分辨有机质谱仪(离子源温度:200℃,离子源能量:电子伏特,收集电流:220VA);Perkin Elmer 2400型元素分析仪。
1按文献[5]方法合成;柱层析用氧化铝,100目~200目;其余所用试剂均为分析纯。其中,二氯甲烷用无水CaCl2干燥一周,再经P2O5回流6h后蒸馏;苯和乙醚经无水CaCl2干燥一周后,在二苯甲酮存在下加入钠片回流至深蓝色后蒸馏;镁为新制镁屑。
1.2 合成
(1)2的合成
在三口瓶中加入乙酸酐1.53g(15mmol)与二氯甲烷30mL,搅拌下于室温滴加三氟化硼乙醚2.1mL(16.5mmol)的二氯甲烷(30mL)溶液。滴毕得络合物溶液A。
在三口瓶中加入12.9g(6.8mmol)和二氯甲烷30mL,搅拌使其溶解;通氮气,加热至回流,缓慢滴加溶液A(5h),滴毕,反应10min(由黄色逐渐变为紫红色)。冷却至室温,用15wt%乙酸钾水溶液水解,分液,水相用二氯甲烷(3×30mL)萃取,合并有机相和萃取液,依次用水、饱和碳酸钠溶液和水洗涤,无水碳酸钾干燥,蒸干溶剂得暗红色黏稠液体,用苯溶解后经中性氧化铝柱层析(洗脱剂:苯,收集第二带产物)纯化得橙色黏稠液体21.6g,产率60.7%;1H NMRδ: 4.07,4.36,4.69(m,17H),3.15(t,1H),2.36(s,3H),1.85(m,2H),1.37(m,2H),0.97(t,3H);IRν: 3092,2957,2927,2869,1669,1455,1376,821cm-1;Anal.calcd for C26H28OFe2: C 66.67,H 6.00,found C 66.93,H 6.45。
(2)3的合成
在三口瓶中加入LiAlH40.66g和绝对乙醚60mL,搅拌下缓慢滴加22.43g(5.19mmol)的绝对乙醚(60mL)溶液(5h),滴毕(由橙红色逐渐变为透明黄色),冰水浴冷却,滴加3mL水分解剩余LiAlH4(立刻有大量白色黏稠物生成,粘在瓶璧上)。过滤,水相用乙醚(3×30mL)萃取,合并有机相和萃取液,用水洗至中性,用无水MgSO4干燥,旋蒸脱溶,用苯溶解后经反复碱性氧化铝柱层析(洗脱剂:苯→乙醚,收集第二带产物)纯化得黄色黏稠液体32.00g,产率85.1%;1H NMRδ: 4.51(m,1H),4.07(m),3.19(t,1H),1.90(m,2H),1.41(m,3H),0.97(t,3H);IRν: 3552,3415,3091,2959,2929,2869,1458,1375,819cm-1;Anal.calcd for C26H30OFe2: C 66.38,H 6.38,found C 66.14,H 6.49。
(3)4的合成
在三口瓶中依次加入32.0g(4.29mmol),酸性氧化铝1.0g和苯12mL,搅拌下回流反应5h。冷却至室温,过滤,滤液旋蒸脱溶,用苯溶解后经碱性氧化铝柱层析(洗脱剂:石油醚→乙醚,收集第一带产物)纯化得黄色黏稠液体41.92g,产率97.5%;1H NMRδ: 4.06(m,17H),3.19(t,1H),1.91(m,2H),1.45(m,2H),1.00(t,3H),6.43(q,1H),5.34(q,1H),5.05(q,1H);IRν: 3089,2959,2869,1629,1460,1379,817cm-1;Anal.calcd for C26H28Fe2: C 69.03,H 6.19,found C 69.58,H 6.52。
2 结果与讨论
2.1 表征
(1)1H NMR
1H NMR分析表明,2的δ2.4处吸收峰归属乙酰基中甲基氢质子;茂环质子的吸收峰为化学位移相近的多重峰,与文献[6]报道类似。
3的δ4.5处吸收峰归属α-碳原子上的氢质子,由于相邻甲基质子和醇羟基质子的偶合作用,被裂分成多重峰;δ1.8处的吸收峰归属羟基氢;与羟基相连碳上甲基质子的化学位移移向高场,出现在δ1.4处,这是由于尽管在2和3中均有氧的吸电子效应,但羰基中双键的各向异性效应对周围的烷基质子产生去屏蔽作用,在羰基被还原后,这种效应消失,故烷基质子的化学位移移向高场[7]。
4结构中的CH2=两个质子的化学环境不同:一个与双二茂铁基处于顺式,一个为反式,所以吸收峰位置有所不同,分别在δ5.0和δ5.3,相应的耦合常数分别为23.0Hz和14.0Hz;CH=氢质子的吸收峰裂分为四重峰(6.47,6.43,6.41和6.37),偶合常数分别为23.0Hz和14.0Hz,说明δ5.0和δ5.3处的氢质子与δ6.4处的氢质子具有邻碳偶合关系,而δ5.0与δ5.3处的氢是同碳偶合关系。
(2)MS
MS分析表明,4的基峰为m/z506,而不是m/z452的分子离子峰,这可能是因为二茂铁中的铁原子有空的3d轨道,和碎片1,3-丁二烯容易形成配合物[8]。该配合物离子具有很高丰度。同样,和乙烯基相连的二茂铁也能够和一个1,3-丁二烯分子形成配合物,具有m/z560离子峰,但由于铁原子的位阻大,配合物的形成有一定困难,所以该峰的丰度较低(8%)。与4相比,2的基峰为分子离子峰,而不是配合物的离子峰;同时没有2和两个1,3-丁二烯分子形成的配合物的离子峰。这说明乙酰基的存在阻碍了1,3-丁二烯分子和铁的配合:一方面,与乙酰基相连的二茂铁中的铁不能和1,3-丁二烯配合;另一方面,不与乙酰基相连的二茂铁中的铁和1,3-丁二烯的配合能力也大大降低。
2.2 合成
在2的合成中,我们选择在温和的反应条件下进行。实验采用了三氟化硼-酸酐体系进行酰化反应,并且确定了较好原料配比条件,即n(1)∶n(酸酐)∶n(三氟化硼)=1∶2∶2[2]。1有两个二茂铁基,当一个二茂铁发生取代反应后,对另一个二茂铁的茂环钝化作用较小,位阻也较小,在同样的条件下既可发生一元取代反应,也可发生二元取代反应。1的酰化反应位置在6-位[6],这是由于位阻体现在与桥碳相连的两个茂环之间,由于烷基的存在,使得这两个茂环的空间位阻增强,在2-位和3-位上取代的可能性很小。2,2-双二茂铁基丙烷在进行单酰化反应时,主要发生在6-位,当进一步酰化时,由于位阻效应和电子效应的共同作用,酰化反应只能发生在异核6′-位[6],通过合适的反应物比例可提高一元酰化产物的产率。
[1] 钱延龙,陈新滋.金属有机化学与催化[M].北京:化学化工出版社,1997.
[2] 王晓莉,温国华,温国永,等.(2,2-双二茂铁基烷)-6,6′-二酰基取代衍生物的合成与表征[J].化学试剂,2006,8:481-482。
[3] 边占喜,王健春,李逢泽.多二茂铁基二氮杂已烷及其过渡金属配合物的合成[J].应用化学,1995,12(2):37-41.
[4] 董彬.烯基取代2,2-双二茂铁基丙烷及其均聚物的合成与表征[J].功能材料,2012,Ⅱ(43):197-201.
[5] 旭昀.一些双二茂铁基烷的合成与表征[D].呼和浩特:内蒙古大学,2000.
[6] 王晓莉.6-丙酰基-6′-丁酰基(2,2-双二茂铁基丙烷)及其还原产物的合成与表征[J].内蒙古师范大学学报自然科学版,2009,38(3):296-298.
[7] 宁永成.有机化合物结构鉴定与有机波谱学[M].北京:科学出版社,2000.
[8] 荣国斌译.波谱数据表-有机化合物的结构解析[M].上海:华东理工大学出版社,2002.
[9] 于世林,李寅蔚.波谱分析法[M].重庆:重庆大学出版社,2002.
SynthesisofNovel1,1-BisferrocenylbutaneDerivatives
LI Chun-yi1,WANG Xiao-li1,DENG Qi-fa2,FU Yuan1
(1.Inner Mongolia Chemical Engineering Professional College,Huhhot 010010,China;2.Erdous Municipal Environmental Monitoring Station,Erdous 017000,China)
6-Acetyl-hydroxyethyl-1,1-bisferrocenylbutane(2)was prepared by the Friedel-Crafts reaction of 1,1-bisferrocenylbutane with acetic anhydride.2was reduced with LiAlH4to 6-α-hydroxyethyl-1,1-bisferrocenylbutane(3).6-Vinyl-1,1-bisferrocenylbutane(4)was synthesized by elimination reaction of3.2~4were new compounds and the structures were characterized by1H NMR,IR,MS and elemental analysis.
1,1-bisferrocenylbutane;Friedel-Crafts reaction;reduction;elimination reaction;synthesis
2014-02-27
内蒙古自然科学基金资助项目(200711020204)
李纯毅(1959-),男,汉族,天津人,副教授,主要从事基础化学的教学和科研工作。
王晓莉,硕士研究生,实验师,E-mail: 404782509@qq.com
O627.8
A
1005-1511(2014)05-0657-03
