吉西他滨与紫杉醇单药治疗老年晚期非小细胞肺癌的疗效及生活质量对比研究
2014-08-29郭彩虹卢桂龙郭宏伟李文文李莉郝玮韩磊
郭彩虹 卢桂龙 郭宏伟 李文文 李莉 郝玮 韩磊
·论著·
吉西他滨与紫杉醇单药治疗老年晚期非小细胞肺癌的疗效及生活质量对比研究
郭彩虹 卢桂龙 郭宏伟 李文文 李莉 郝玮 韩磊
目的探讨吉西他滨(Gemcitabine)和紫杉醇(Paclitaxel)单药治疗老年人晚期非小细胞肺癌的疗效及生活质量对比。方法收集2009年1月至2013年1月接受治疗的老年晚期非小细胞肺癌62例,患者随机分为G组和P组,每组31例。G组采用吉西他滨单药化疗;P组采用紫杉醇单药化疗,所有患者进行随访,收集生存情况。2组疗效进行判定和QLQ-30生活质量对比研究。结果G组、P组总有效率分别为29.0%、29.0%。G组中位生存期为11个月,3年生存率为6.5%,P组中位生存期为11个月,3年生存率为3.2%。G组患者毒副反应发生率与P组相似,但骨髓抑制发生率G组高于P组(P<0.05)。2组生活质量差异无统计学意义(P<0.05)。结论2组方案在治疗老年晚期非小细胞肺癌的近期和远期疗效相当,但毒副作用有轻微差异,2组患者生活质量无差异。
老年人,癌,非小细胞肺;肿瘤分期;疗效;生活质量
肺癌作为当今对人类健康危害最大的恶性肿瘤之一,其发病率在逐年上升的趋势,肺癌的治疗预后差,我国患者五年生存率仅为10%[1]。肺癌分为小细胞肺癌(small-cell-lung carcinoma,SCLC)和非小细胞肺癌(non-small-cell carcinoma,NSCLC)。非小细胞肺癌是肺癌的主要类型,占75%~80%[2]。大多数患者在被确诊时,已是ⅢB~Ⅳ期,中位生存期仅在8~10个月,已失去进行手术的机会。全身化疗成为患者的首选治疗方案,近些年来随着吉西他滨、多西紫杉醇的新药出现,晚期NSCLC患者的疗效有所改善[3]。本次通过我院接受治疗的老年晚期NSCLC分为吉西他滨单药组和紫杉醇单药组,分析两种药物单独作用患者治疗情况,并进行随访,探讨吉西他滨或紫杉醇单药治疗老年晚期非小细胞肺癌的疗效及生活质量,报道如下。
1 资料与方法
1.1 一般资料 收集2009年1月至2013年1月在我院接受治疗的年龄≥70岁老人年晚期NSCLC患者62例,男45例,女17例;年龄70~85岁,平均年龄(71±3)岁。依据国际抗癌联盟(UICC)第7版TNM分期标准,ⅢB期34例,Ⅳ期28例。鳞癌患者35例,腺癌患者27例。90%患者并发高血压、脑梗死、糖尿病、冠心病、胃炎、慢性气管炎。ECOG评分1~2分。将患者随机分为,吉西他滨单药化疗(G组),紫杉醇单药化疗组(P组)。2组一般资料有均衡性。
1.2 纳入与排除标准 (1)纳入标准:①首先通过病理组织学诊断,属于ⅢB~Ⅳ期的晚期非小细胞肺癌的患者,年龄≥70岁;②单药化疗前,1个月内未接受化疗、3个月内未接受放疗;③ECOG评分在0~2分;④化疗前,患者无肝肾功能障碍、无心电图异常、无颅内转移、脑转移(经放疗控制,不依赖激素的脑转移患者应该允许入组);外周血白细胞>4.0×109/L,血红蛋白>80 g/L,血小板>100×109/L;⑤ 纵隔内存在至少1个>1 cm的可测量的病灶。(2)排除标准:患者生存期≤3个月。
1.3 用药方法 (1)G组患者:吉西他滨(江苏豪森药业股份有限公司)1 000 mg/m2第1、8天静脉滴注;(2)P组患者:紫杉醇(北京协和药厂)60~90 mg/m2,d1,d8静脉输入,在静脉滴注紫杉醇之前12 h、6 h给予地塞米松10~20 mg口服,前30~60 min给予苯海拉明50 mg肌内注射,静脉注射法莫替丁20 mg,输液期间行心电监护,密切监测血压、脉搏、心率、呼吸等生命体征。化疗期间常规止吐、保胃。21 d为1周期,治疗期间每周检查血常规1次、肝肾功能1次,在进行2周期治疗后行CT及其他相关检查,入选病例均完成2周以上的化疗治疗。
1.4 观察指标 (1)疗效评价:依据世界卫生组织(WHO)实体瘤疗效评定标准,疗效分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。总有效率(RR)=(CR+PR)/总例数×100%。(2)毒副反应为急性和亚急性毒副反应的评价标准,主要统计3、4级的毒副反应情况。(3)生活质量评估使用癌症患者生命质量测定表(QLQ-C30),其中包括5个内容(身体功能、角色功能、情感功能、认知功能、社会功能)。分数越高,表明具有越高的生活质量。分两个时间基线,分别是:入院时,治疗3个月后。
2 结果
2.1 2组疗效比较 G组有效率为29.0%(9/31);P组有效率为29.0%(9/31)。在对2组患者中不同病理类型和不同临床分期类型的分层分析发现,在G组中,鳞癌、腺癌、ⅢB期、Ⅳ期的总有效率分别为29.4%、33.3 %、28.6%和23.1%;而P组患者中,鳞癌、腺癌、ⅢB期、Ⅳ期的总有效率分别为37.5%、38.9%、20.0%和15.4%,2组不同病理类型和临床分期间差异无统计学意义(P>0.05)。见表1、2。
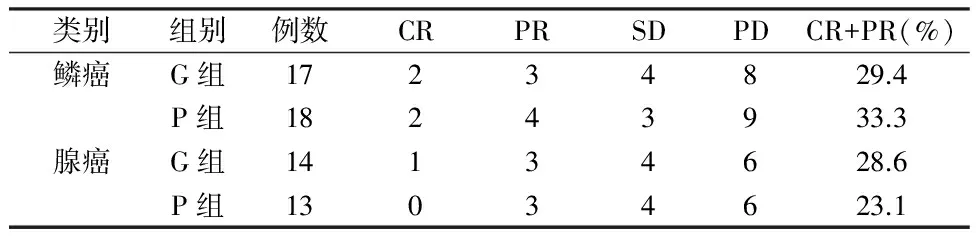
表1 2种化疗方案在不同病理类型疗效比较 n=31,例
2.2 2组不良反应比较 (1)血液系统毒性:P组出现白细胞减少22例(71.0%),贫血17例(54.9%),血小板减少18例(58.1%)。其中Ⅲ~Ⅳ度骨髓抑制13例(41.9%)。G组出现白细胞减少25例(80.6%),贫血18例(58.1%)。血小板减少10例(32.3%)。(2)其他系统毒性:2组其他系统毒性主要表现为恶心、呕吐、脱发、腹泻。G组出现恶心、呕吐19例,脱发6例,腹泻6例;P组出现恶心、呕吐12例、脱发9例,腹泻4例。Ⅲ~Ⅳ度反应主要为腹泻,其中G组1例。P组1例,2组比较差异无统计学意义(P>0.05)。2组肝肾功能损伤、便秘及变态反应发生率较低,程度较轻,未影响治疗。未出现化疗相关性死亡。G组患者的3、4级白细胞减少、血小板减少、贫血和骨髓抑制的发生率与P组比较,差异有统计学意义(P<0.05)。见表3。
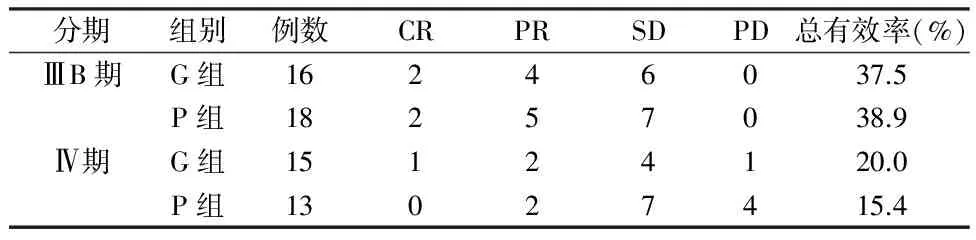
表2 2种化疗方案在不同临床分期疗效比较 n=31,例

表3 2种化疗方案患者的主要毒副反应比较 n=31,例(%)
注:与G组比较,*P<0.05
2.3 2组生活质量比较 入院时,2组患者在各维度的生活质量评分2组间差异无统计学意义(P>0.05)。治疗后3个月,2组患者在各维度的生活质量评分2组间差异无统计学意义(P>0.05),2组患者各维度生活质量在治疗3个月后和入院时比较,差异无统计学意义(P>0.05),患者在进行化疗后生活质量有上升趋势,但与入院时比较差异无统计学意义(P>0.05)。见表4。

表4 2组入院及治疗后3个月生活质量比较 ±s
2.4 2组患者生存率分析 随访至2013年6月30日,G组患者中位生存期为11个月,3年生存率为6.5%,P组患者G组患者中位生存期为11个月,3年生存率为3.2%,经Log-rank分析显示,2组患者生存率差异无统计学意义(P>0.05)。见图1。

图1 2组患者3年生存曲线
3 讨论
肺癌是世界范围内最常见的癌症之一,发病率居高不下,近年来呈现出不断升高的趋势。临床I级患者5年生存率在50%~70%,临床ⅢA级患者生存率在10%~30%[4,5]。而ⅢB~Ⅳ期,中位生存期仅在8~10个月,姑息性化疗成为晚期NSCLC患者治疗的重要手段之一。
国外多中心研究,对707例≥70岁的老年患者人组,随机接受长春瑞滨单药化疗、吉西他滨单药化疗或长春瑞滨+吉西他滨联合化疗,结果显示两药联合组与单药组相比,在缓解率、疾病进展期、生存率或生活质量等方面无明显优势,提示两药联合组的毒性反应高于单药组[6]。吉西他滨在Ⅱ期或Ⅲ期单药治疗具有良好的缓解率,有效率为21.7%~38.5%,可提高患者的生活质量[7]。紫杉醇是近年研究较多的新型抗微管剂,其联合顺铂方案已成为晚期NSCLC的一线治疗方案之一,有效率22%~47%[6]。
在本次以吉西他滨为单药治疗和以紫杉醇为单药治疗的2组中疗效相当,差异无统计学意义(P>0.05)。在对两组患者临床分期、病理类型分层研究发现,采用吉西他滨或紫杉醇时在鳞癌、腺癌、ⅢB期、Ⅳ期的患者疗效差异无统计学意义(P>0.05)。在对患者的3年生存状态进行随访发现,采用吉西他滨组患者中位生存期为11个月,3年生存率为6.5%;采用紫杉醇组患者中位生存期为11个月,3年生存率为3.2%。2组经Log rank分析未发现在生存状态中的差异。提示在单独采用吉西他滨或紫杉醇在治疗患者的治疗效果和生存状态相似。
国外文献报道,在对452例Ⅲ期NSCLC患者分别采用顺铂+紫杉醇和顺铂+吉西他滨方案治疗,患者的中位生存期分别为9.97个月和10.49个月,并且1年生存率比较发现,差异无统计学意义(P>0.05)[7]。本次研究中两组中位生存期均为11个月,均大于国内外情况,可能为病例相对较少所致。Rajeswaran等[8]在对以顺铂或卡铂为基础的化疗方案与不含铂类的化疗方案进行对比,结果发现铂类药物能略提高患者1年生存率,但差异无统计学意义(P>0.05)。本次研究生存期同以往报道[9]添加铂类化疗药物患者生存期相似。因此,研究结果提示,铂类可能并非治疗非小细胞肺癌的必须基础要。
本次在对药物毒副反应分析发现,在采用紫杉醇单独用药化疗时的毒副反应与采用吉西他滨单独用药化疗方案相似,G组患者骨髓抑制发生率为39%,明显高于P组的13%,吉西他滨组骨髓抑制显著,G组血小板减少轻微高于P组,但差异无统计学意义(P>0.05),2组主要毒副反应是骨髓抑制。吉西他滨作为抗代谢药物,导致DNA合成和修复过程中所需的脱氧核苷酸减少,主要毒副作用是骨髓抑制[10]。而紫杉醇主要通过促进微管蛋白聚合抑制解聚、抑制细胞有丝分裂,骨髓抑制主要与剂量相关。随后对2组患者进行生活质量的回馈调查,生活质量2组相似。
综上所述,单独采用吉西他滨或紫杉醇用药在老年患者近期、远期疗效相当,在生活质量方面相似。在毒副反应中,吉西他滨骨髓抑制发生率明显高于紫杉醇。但本次研究总样本量较少,尚需大样本多中心临床研究进一步证实。
1 张伟,宋立永,王飞.周围型小肺癌的CT诊断与鉴别诊断.河北医药,2012,34:2940-2941.
2 王辰生,李红方,梁冰锋,等.肺小细胞癌和鳞状细胞癌中VEGF表达与预后相关性分析.河北医药,2013,35:1029.
3 娄广媛,李铁,古翠萍,等.吉西他滨单药及联合卡铂治疗初治的老年晚期非小细胞肺癌疗效观察.中华医学杂志,2010,90:100-102.
4 姚继方,张泽峰,齐战,等.经支气管壁针吸活检对肺癌诊断的临床意义.河北医药,2010,32:1750-1751.
5 张黎,姜姗,干银娣,等.血清肿瘤标记物联合检测在肺癌诊断中的应用价值.河北医药,2013,35:2442-2443.
6 Gridelli C1,Perrone F,Gallo C,et al.Chemotherapy for elderly patients with advanced non-small-cell lung cancer: the Multicenter Italian Lung Cancer in the Elderly Study (MILES) phase III randomized trial.J Natl Cancer Inst,2003,95:362-372.
7 Kosmidis PA,Kalofonos HP,Christodoulou C,et al.Paclitaxel and gemcitabine versus carboplatin and gemcitabine in patients with advanced non-small-cell lung cancer.A phase III study of the Hellenic Cooperative Oncology Group.Ann Oncol,2008,19:115-122.
8 Rajeswaran A,Trojan A,Burnand B,et al.Efficacy and side effects of cisplatin- and carboplatin-based doublet chemotherapeutic regimens versus non-platinum-based doublet chemotherapeutic regimens as first line treatment of metastatic non-small cell lung carcinoma: a systematic review of randomized controlled trials.Lung Cancer,2008,59:1-11.
9 郑爱青,郑培,于金明,等.吉西他滨单药或联合卡铂治疗老年晚期非小细胞肺癌疗效观察.武警医学,2011,22:501-504.
10 张青,刘孟琦,高丽环,等.紫杉醇与吉西他滨在中晚期非小细胞肺癌放射治疗中增敏疗效比较.河北医药,2012,34:1630-1631.
10.3969/j.issn.1002-7386.2014.22.019
102600 北京市,首都医科大学大兴医院内六科
韩磊,102600 北京市,首都医科大学大兴医院内六科;
E-mail:zulia0606@163.com
R 734.2
A
1002-7386(2014)22-3413-03
2014-05-13)
