复眠颗粒制剂工艺研究
2014-08-09关晓清杨玉霞侯志宏于秀华
关晓清,杨玉霞,侯志宏,于秀华,3
(1.中国人民解放军第208医院,长春 130062;2.吉林大学药学院,长春 130021;3.长春中医药大学,长春 130117)
复眠颗粒的处方是由醋青皮、酸枣仁等数味中药组成,具有滋阴养血、养心安神、疏肝理气等作用。青皮中主要有效成分为黄酮类,如橙皮苷等[1-3],故以橙皮苷的含量为考察指标,笔者对复眠颗粒的生产工艺中提取次数、提取时间和加水量进行了工艺优选研究。
1 仪器与材料
1.1 仪器 LC-2010A型高效液相色谱仪(日本岛津),C18柱(4 mm×25 cm,5 μm),SPD-10AVP检测器,Labmda-25型紫外可见分光光度计(美国PE分析仪器厂),恒温水浴锅(江苏省医疗器械厂),CP225D型双量程电子分析天平(德国Sartoris),AMW220D型电子分析天平(日本岛津),JH2102电子天平(上海精密科学仪器有限公司),101-1A型数显式电热恒温干燥箱(上海阳光实验仪器有限公司)。
1.2 药品 橙皮苷对照品购于中国药品生物检定所,批号为110721-201014,供含量测定用,所用试剂均为色谱纯、分析纯。
2 方法与结果
2.1 吸水率的测定 称取1/10处方量的各药材,放入带盖容器中,加入总药材量10倍量的水,每隔30 min测量吸水量,直到吸水量不再增加为止,计算吸水率。通过测量和计算,吸水率为187%,即首次煎煮时要多加2倍量的溶剂。
2.2 正交试验因素与水平 水煮过程中可能的影响因素有提取次数、提取时间、加水量,以所得出膏率和青皮中橙皮苷含量为考核指标,按4因素3水平进行正交试验。因素与水平列表见表1。

表1 水煎L9(34)正交试验因素水平表
2.3 供试样品的制备 取原处方量1/5的各药材,精密称定,置于容器中,按表1进行试验。煎煮后放置30 min,滤过,滤液适当浓缩至100 mL容量瓶中,加蒸馏水定容至刻度,摇匀,即得母液,备用。
2.4 出膏率的测定 精密吸取母液20 mL,于已编号的干燥恒重的蒸发皿中,水浴蒸干,105 ℃干燥3 h,迅速取出,放入干燥器中,冷却30 min,迅速精密称定,计算浸膏率。结果见表2~3。
2.5 橙皮苷含量测定[4-7]
2.5.1 色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填料,甲醇-水(31:69)为流动相,检测波长284 nm。流速为1.0 mL/min,理论塔板数按橙皮苷计算应不低于3 000。
2.5.2 对照品溶液的制备 取橙皮苷对照品适量,加甲醇制成每1 mL含橙皮苷0.1 mg的溶液(实际称样量10.71 mg,用甲醇溶解并定容至100 mL量瓶中,摇匀。每1 mL含橙皮苷0.107 1 mg)。
2.5.3 标准曲线的绘制 分别精密吸取对照品溶液2,5,10,15,20,25 μL,注入液相色谱仪,按正文方法测定,结果回归方程为Y=1 532 797.74X+62.15,r=0.999 9。线性范围0.214 2~2.677 5 μg。见图1。
2.5.4 供试品溶液的制备 分别精密量取供试品溶液的1~9号提取液1 mL或2 mL,分别定容于250 mL量瓶中,并稀释至刻度,摇匀,即得。
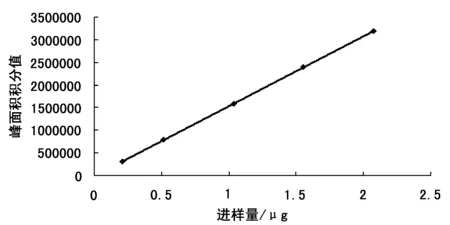
图1 橙皮苷标准曲线图
2.5.5 样品测定 分别精密吸取1号供试品溶液5 μL,2,3,4,5,6,7,8,9号均进样2 μL,对照品溶液10 μL,分别注入高效液相色谱仪,测定样品中橙皮苷含量。测定结果见表2、表4。
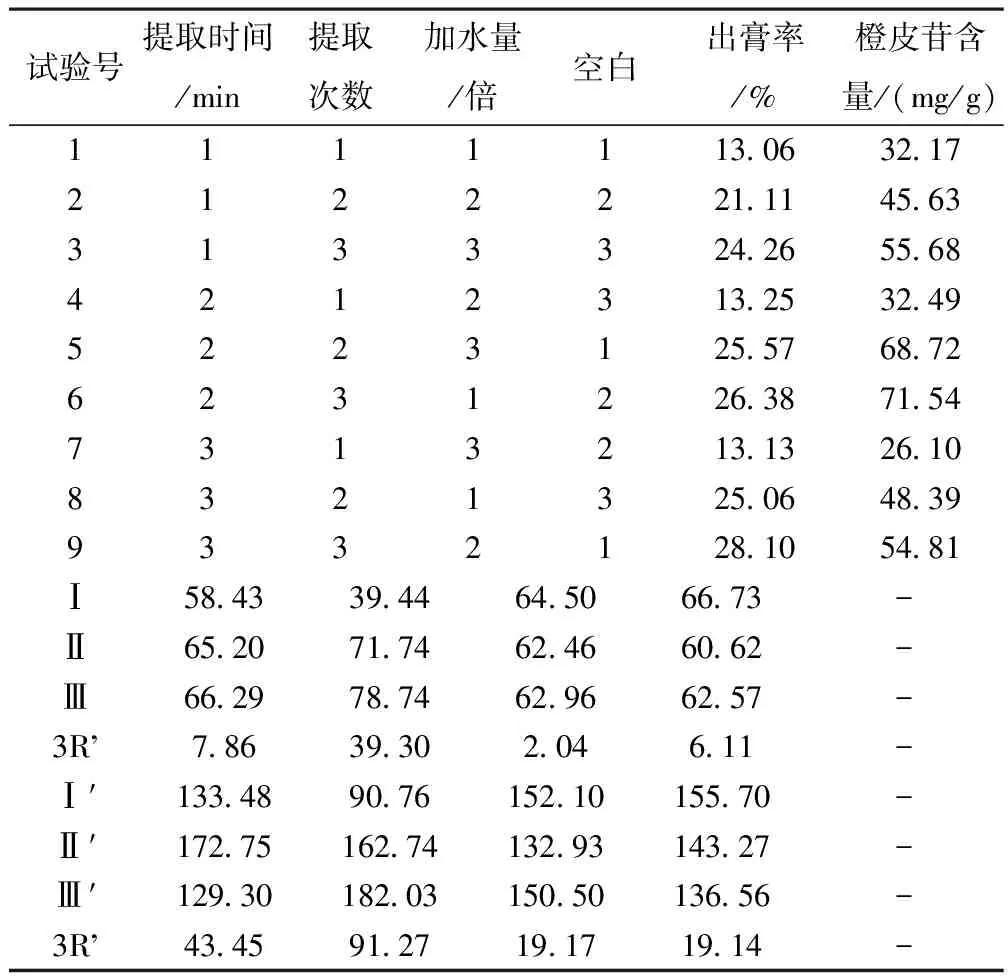
表2 正交试验数据
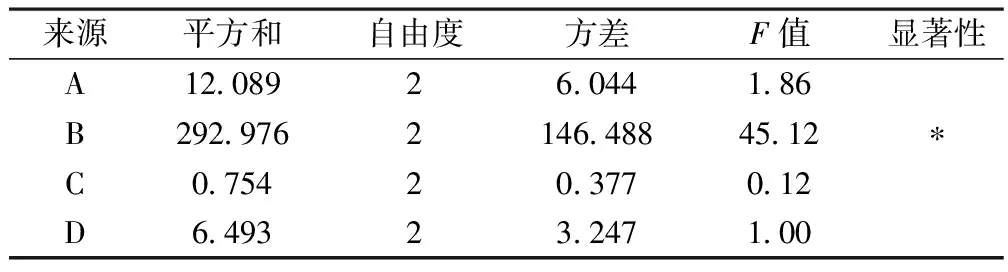
表3 出膏率方差分析

表4 橙皮苷含量方差分析
根据出膏率和橙皮苷含量方差分析结果:B>A>C,B(提取次数),有统计学意义,且B3>B2>B1,A(提取时间)和C(加水量),无统计学意义。最佳工艺为A2B3C1,即加10倍量的水,提取3次,每次90 min。
2.6 制剂成型性研究
2.6.1 辅料种类及用量[8]中药颗粒制剂成型辅料的筛选,应以辅料用量少、水溶性大、成型性好为原则。经过多次试验摸索,考察了糊精、淀粉、蔗糖等多种辅料对制剂成型性的影响。蔗糖黏合力强,在干燥、常温下十分稳定,与大多数药物不起作用,价格低,可改善药物的不良口味。但由于蔗糖为白色结晶,因此在制粒前粉碎并过80~100目筛,使成品颗粒均匀,避免混合后产生小白点。糊精是颗粒剂常用的稀释剂[9]。不同浓度的乙醇是制粒的首选润湿剂。
取干浸膏粉50 g,加入适量的不同辅料,不同浓度乙醇制粒,干燥,观察颗粒的情况。结果见表5。

表5 辅料选择试验表
根据实验结果,选择蔗糖和糊精为制粒的辅料。药粉与辅料总量比为1:1,其中辅料用量为蔗糖与糊精比为1:1,75%乙醇为润湿剂制粒。验证试验:按上述条件制湿颗粒,效果良好,符合工艺要求。
2.6.2 湿颗粒干燥温度的选择[10-11]对湿颗粒的干燥,选用了不同温度,干燥8 h,观察颗粒的干燥情况,并测定水分。结果见表6。

表6 湿颗粒干燥温度试验表
根据实验结果,选择80 ℃为湿颗粒干燥温度。
2.6.3 颗粒的流动性考察 取颗粒成品测定休止角,考察颗粒的流动性。方法:固定漏斗法。结果见表7。
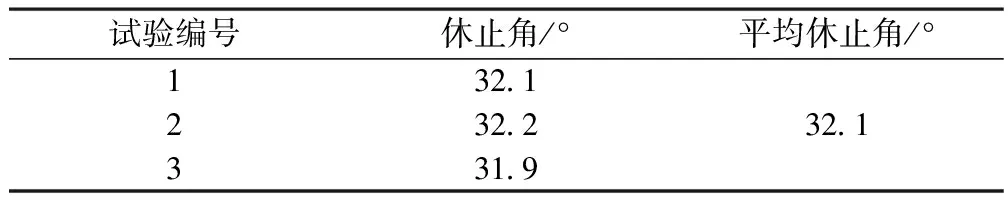
表7 颗粒休止角的测定
由上表可见,颗粒休止角为32.1°,表明颗粒流动性良好。
3 小结
3.1 制剂提取方法的依据 本处方是在临床汤剂的基础上研制开发,即各药味均采用水煎处理。为了更好地结合临床经验,采用水煎提取方法。
3.2 青皮的主要化学成分为黄酮类 《中国药典》2010年版一部中以橙皮苷为对照进行鉴定。提取方法有水提[12]、醇提[13],测定方法常用高效液相色谱法[14]。本制剂参照《中国药典》的方法进行了测定,方法简便,准确。
[1]Taylor,Daniel J,Mallory,Laurel J,Lichstein,Kenneth L.,et al.Comorbidity of chronic insomnia with medical problems[J].Sleep,2007,30:213-218.
[2]张丽萍,夏猛.失眠症的治疗现状分析及思考[J].环球中医药,2011,4(1):66-69.
[3]高顺平,邬国栋,刘全礼.青皮的研究进展[J].包头医学院学报,2014,30(1):139-140.
[4]林发荣.煎煮过程中饮片吸水量的探讨[J].黑龙江中医药,2003,30(3):50.
[5]国家药典委员会.中华人民共和国药典[M].北京:化学工业出版社,2010:76.
[6]韩剑,张昭良,田仁明.用正交试验探讨青皮提取工艺对橙皮苷的影响[J].中国中医药科技,2012,19(6):515-516.
[7]卢静华,孙洪章.均匀设计优化青皮中橙皮苷的提取工艺[J].辽宁医学院学报,2012,33(6):534-535.
[8]江丽芸.中药辅料的研究[J].中国实用医药,2012,7(36):248-250.
[9]廖才智.β-环糊精的应用研究进展[J].化工科技,2010,18(5):69-72.
[10]王美玲.中药颗粒剂质量标准的研究[J].黑龙江科学,2014,5(3):98.
[11]孙远功,鲁来政,胡燕.维生素C泡腾片颗粒干燥工艺研究[J].中国药师,2000,3(4):203.
[12]李凤林,李青旺,冯彩宁,等.天然黄酮类化合物提取方法研究进展[J].中国食品添加剂,2008(5):60-64.
[13]赵国建,王向东,王焕.提取方法对核桃青皮多酚提取效果的影响[J].农业工程学报,2012,28(1):351-354.
[14]刘冬晓,郑国华,张远远.高效液相色谱法测定青皮中橙皮苷的含量[J].湖北中医杂志,2011,33(9):74-75.
