硝酸钙与硝酸钠二元相变蓄热材料的制备与性能
2014-08-08纪育楠赵长颖徐治国
纪育楠,赵长颖,徐治国
(上海交通大学动力机械与工程教育部重点实验室,上海200240)
蓄热技术是解决能源供需矛盾,从而提高能源利用率的有效手段。目前显热蓄热技术已经较为成熟,但有蓄热密度较低、放热过程温度变化较大等缺点;相比之下,相变蓄热技术蓄热密度大,放热过程温度变化小,应用前景广泛[1-2]。在众多相变材料中,盐类以其较低的黏度和蒸汽压、较广的温度应用范围和较低的成本,成为中高温相变蓄热的首选材料[3-5]。
根据卡诺定理,更高的热源温度可以带来更高的能量转换效率,然而实际情况中,更高的温度会导致高额投入成本以及严重的腐蚀问题,因此中低温的太阳能热发电技术更有经济优势[6]。通过查阅大量相变材料的综述文章[1-5],可以发现相变点在300℃以下的混合盐大致可以分为三类,其中一种是以锂盐为主的,但由于目前锂盐高昂的价格,无法应用于蓄热材料;另一种是以碱为主,但由于碱的化学活性较高,容易吸收酸性物质(如二氧化碳,硫化物等)而变质,对于密闭性有较高的要求;最后一种是包含有毒(如亚硝酸盐)或者腐蚀性较强(如氯化盐)的成分。实际上可供选择的相变蓄热材料十分有限。
硝酸盐在中高温下稳定性较好,且具有低黏度,低腐蚀性和高蓄热密度等优点[7],被众多研究人员采用作为相变蓄热材料。吴志根等[8]采用NaNO3作为相变蓄热材料来研究多孔介质在高温相变蓄热中的强化换热特性;Iverson等[9]测试了solar salt(60%NaNO3-40%KNO3,质 量 分 数,下同),Hitec salt(53%KNO3,40%NaNO2and 7%NaNO3)和一种低熔点四元混合盐[2.3%KNO3,39.4%Ca(NO3)2,12.1%NaNO3,6.1%LiNO3]的热物性并评估其作为相变蓄热材料的性能;Roget等[10]研究了KNO3-LiNO3二元混合盐和KNO3-NaNO3-LiNO3三元混合盐的相变蓄热特性。然而,他们所采用的这些混合硝酸盐最初是以传热流体为目的开发出来的,核心要求是尽量低的熔点和尽量高的使用温度[11-13]。而作为相变蓄热材料,需要的是与热源相匹配的相变温度,较高的相变焓,以及在相变温度范围内具有良好的稳定性。另一方面,作为蓄热介质的用量要比传热流体大得多,因此成本也成为一个重要的考虑因素。在各种硝酸盐中,硝酸钙与硝酸钠价格低廉,Protsenko[14]得到了这两者二元混合的相图。由于其作为传热流体的性能并不突出,没有进一步对其的研究。本文从相变蓄热材料的角度出发,通过混合硝酸钙与硝酸钠这两种廉价的硝酸盐,制得一种中温相变蓄热材料,并测试了其循环稳定性、比热容与腐蚀性,结果表明其在相变蓄热领域有应用前景。
1 实验样品制备
首选,用分析天平按不同摩尔比(从1∶9到9∶1)量取不同质量的硝酸钠和四水硝酸钙(分析纯,国药集团化学试剂有限公司生产,质量分数大于99%),放在坩埚中置于电炉加热。四水硝酸钙首先熔化并将硝酸钠也一并溶解形成透明液体。将此透明液体搅拌使之混合均匀,然后放回电炉中继续加热到300℃并保持5h,再冷却至室温,得到混合盐样品。
将不同配比硝酸钙和硝酸钠混合样品通过同步热分析仪(PerkinElmer,STA 8000)进行测试,在20mL/min的N2吹扫下,以10℃/min的升温速率,从120℃加热到350℃。由于样品容易吸潮,且可能在制备过程中晶格形成不完善,第一次加热得到的曲线波动较为杂乱。从第二次加热开始,曲线得到很好的重现,因此认为第一个熔化凝固循环除去了水分且消除了热力学势,可以将第二次循环得到的参数作为其物性参数。其升温STA曲线如图1所示。由图1中可以发现虽然混合物的配比不同,但都在220℃时开始出现一个吸热峰,该吸热峰为其最低共熔点。不同配比的STA曲线对应的相变焓与相变点如表1所示,可以发现随着硝酸钙含量的增加,其相变焓逐渐减小,其中硝酸钙与硝酸钠摩尔比为9∶1的混合样品相变焓甚至只有10.4kJ/kg,比硝酸钙和硝酸钠单独熔化时的相变焓低得多,因此很可能这些样品只是少部分熔化。将硝酸钙含量高的样品在STA的加热腔中加热到300℃,揭开腔盖,发现样品仍然呈块状,明显没有熔化。实验结果表明,硝酸钙与硝酸钠两者不能以任意比例互熔;当硝酸钙的含量高时,硝酸钠只是与其中一部分形成共晶熔融盐。硝酸钠的含量越少时,形成的共晶熔融盐就越少,因此才会测到单位质量的相变焓越少,而相应的熔点变化不大。
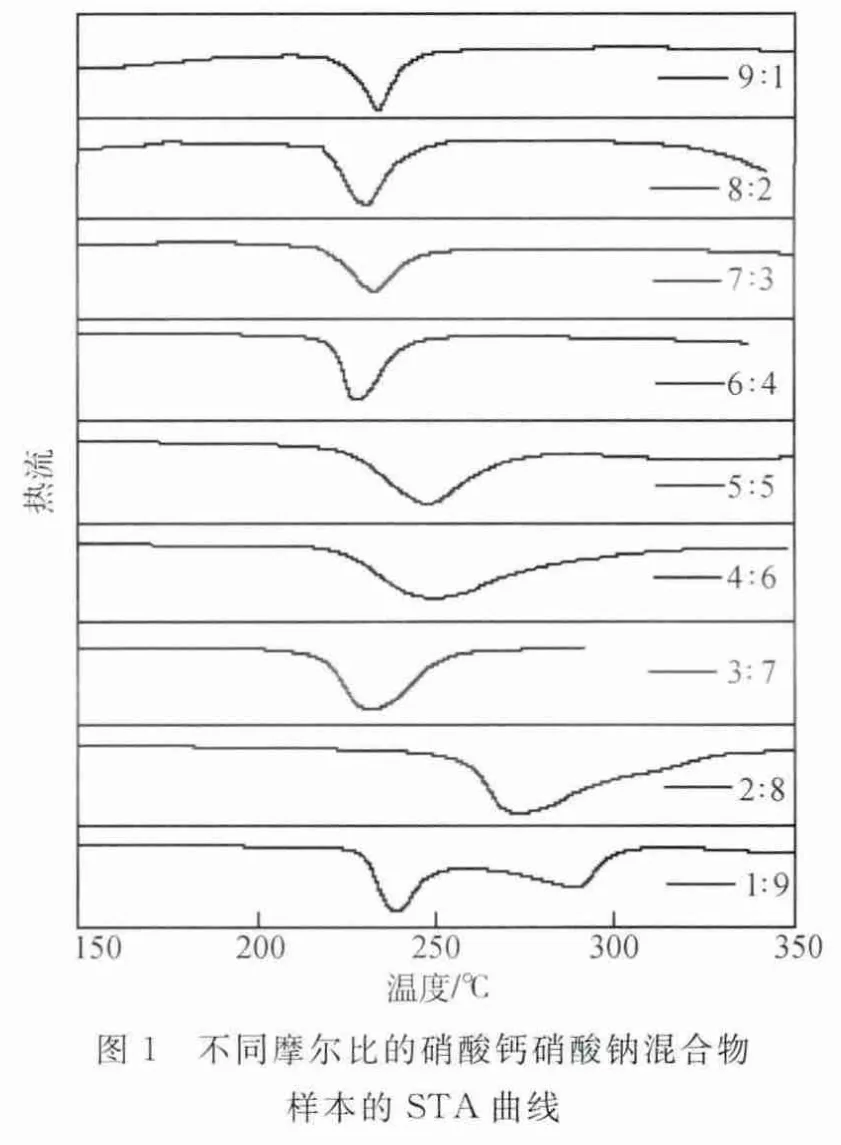
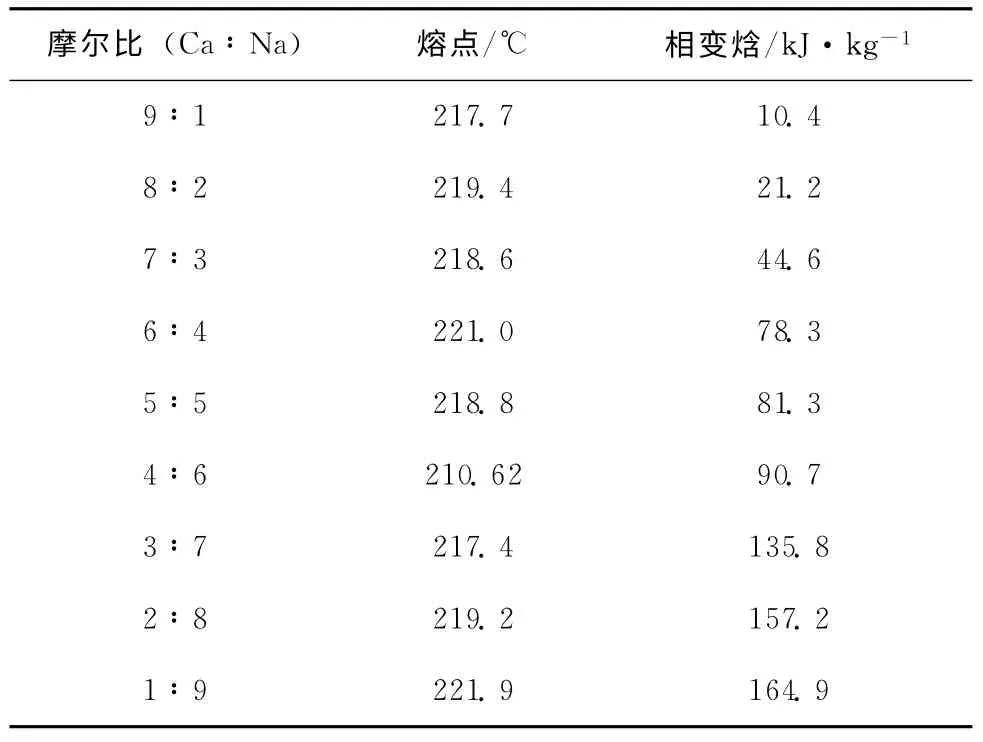
表1 不同硝酸钙和硝酸钠混合盐的熔点和对应的相变焓
在不同配比中,硝酸钙与硝酸钠摩尔比为3∶7和2∶8样品相变焓较高,分别是135.8kJ/kg和157.2kJ/kg。硝酸钙与硝酸钠摩尔比1∶9的样品焓值相比2∶8的样品只有微弱提高,而价格低廉的硝酸钙含量高可以有效降低成本,因此认为3∶7和2∶8的样品为较佳的比例,将对其进行进一步的测试。
2 循环稳定性测试
选择3∶7与2∶8的样品进行循环稳定性测试,将样品以10℃/min的升温速率从80℃加热至350℃,保温1min后再以同样的速率降温至80℃,以此循环,其吸热与放热曲线如图2所示。由图2中可以发现,两者的吸热峰重现性很好,表明其凝固放热性能稳定。放热峰均有2个,且随循环次数的增多,较低温度的放热峰逐渐向较高温度的放热峰靠拢,其靠拢速度逐渐减慢并趋于稳定。这说明其放热过程随着循环次数的增多,逐渐由亚稳定相达到相平衡。循环期间,样品的质量保持稳定,说明在350℃以下稳定性良好。对比两个配比的放热性能,可以发现硝酸钙与硝酸钠摩尔比为3∶7的样品经过多次放热后两个放热峰最终基本合成一个窄峰,说明其放热区间比较集中,即凝固放热过程温度变化较小;而2∶8的样品其两个吸热峰的距离仍较大,放热区间较大,即凝固放热过程中温度变化较大。相比之下,3∶7的样品相变放热的性能更好,因此认为它是更好的配比。
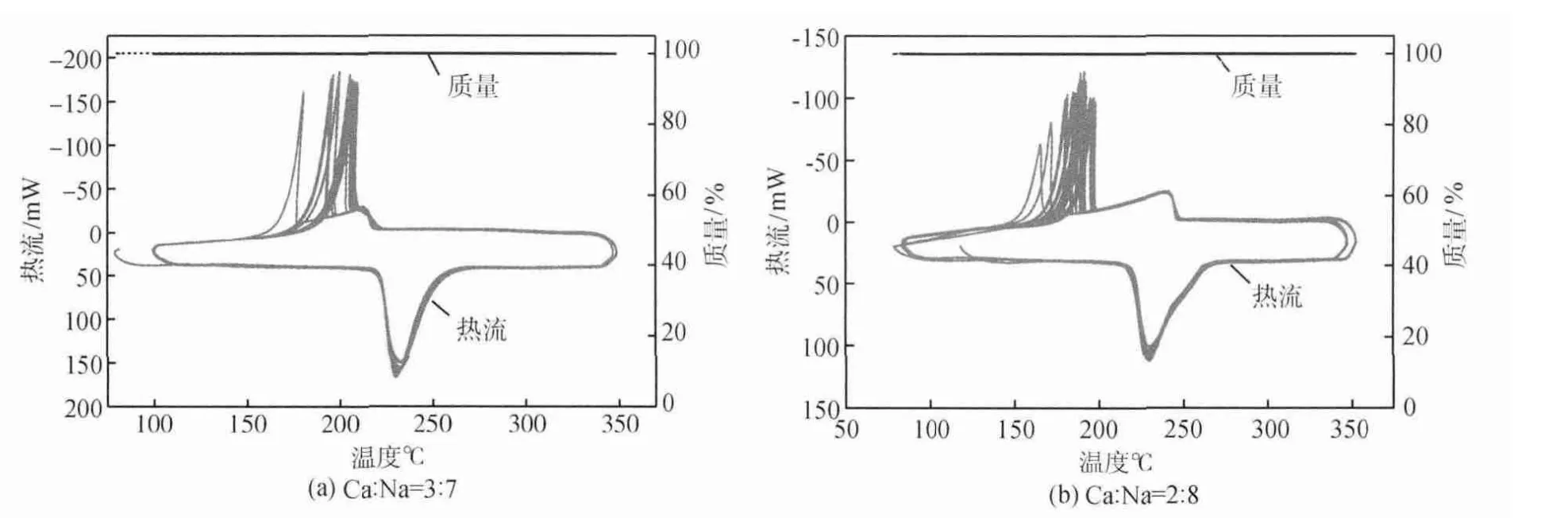
图2 硝酸钙与硝酸钠摩尔比为3∶7与2∶8的样品循环曲线
3 比热容测试
尽管相变蓄热利用相变焓来储存热量,但实际过程中,相变蓄热与显热蓄热是分不开的。一方面,相变材料在温度达到相变点之前必然会有一段显热蓄热的阶段,另一方面,由于相变材料本身的导热率低,其内部各部分之间的温差较大,一些部分开始相变的同时,也有一些部分仍未相变。实际应用中,相变蓄热材料的蓄热量包括熔化之前的显热部分,相变潜热部分以及熔化之后的显热部分,因此比热容也是一个重要参数。本实验将3∶7的样品用DSC(PerkinElmer,DSC 8000)测试,通过三线法,即测定空白曲线,作为标样的蓝宝石升温曲线和试样的升温曲线来得到试样的比热容曲线。为了防止相变过程影响比热容的测量,实验避开了相变温度的区间,分别测量了固态时100~200℃和液态时250~350℃的比热容,如图3所示。
4 腐蚀性测试
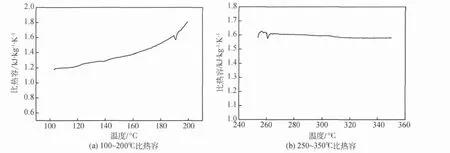
图3 硝酸钙与硝酸钠摩尔比为3∶7样品的比热容
相变材料在应用中离不开与金属材料的直接接触。相比其他熔融盐,硝酸盐的低腐蚀性是其一个突出的优点。Goods等[15]对混合硝酸钾和硝酸钠的腐蚀性进行了研究,304不锈钢经过三种不同配比硝酸钾和硝酸钠混合盐7000h的浸泡后,损失质量均小于10mg/cm2,说明其腐蚀性微弱。本文选择了常见的三种不锈钢201、304、316L和铝合金1060,制成20mm×20mm×1.5mm的片状试样,用SiC砂纸打磨,再经丙酮清洗并干燥称重。将金属片试样浸没在盛硝酸钙与硝酸钠为3∶7熔融盐的陶瓷坩埚中,放入电炉中,温度设定为350℃,每20h取出一次,用丙酮清洗,干燥,再称重。不同种类金属片的质量随时间变化如图4所示,可以发现,这四种金属片的质量变化非常小,可以认为硝酸钙与硝酸钠为3∶7的熔盐对这四种金属的腐蚀性很微弱,可以应用于实际工程中。
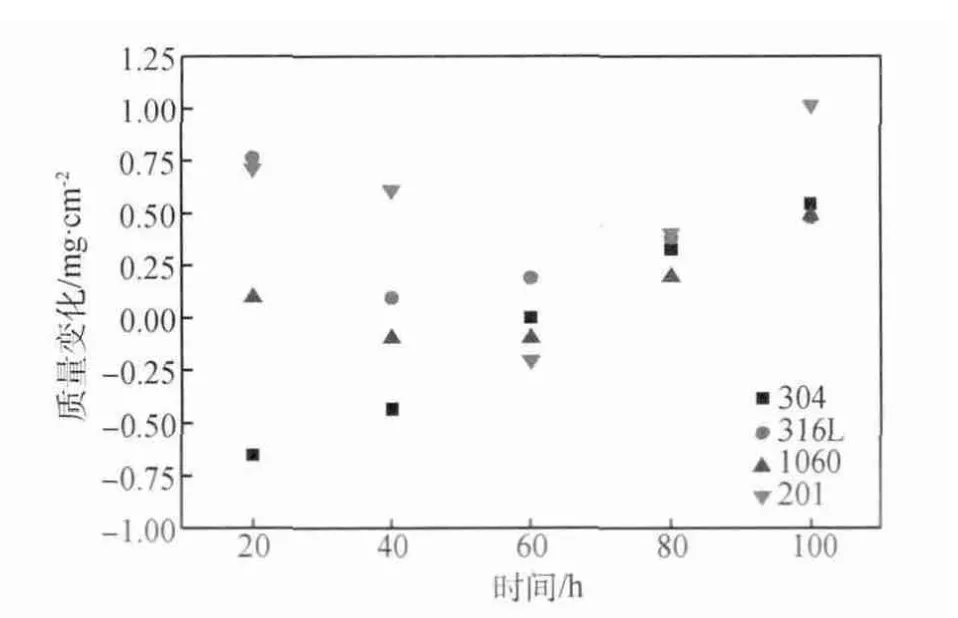
图4 不同金属的质量变化
5 经济性分析
如前文所述,由于相变蓄热材料的用量庞大,因此成本是其规模化应用的一个重要影响因素。尽管不同种类硝酸盐的价格不断变化,但由高到底的顺序排列基本固定如下:硝酸锂>硝酸钾>硝酸钠>硝酸钙。调查近期不同种类硝酸盐的价格,四水硝酸钙为1300元/吨(由于硝酸钙在常温下极易吸湿,并没有无水硝酸钙出售,市面上买到的都是常温下性质稳定的四水硝酸钙),硝酸钠为3200元/吨,硝酸钾为7800元/吨。以此折算,硝酸钙与硝酸钠摩尔比为3∶7的混合盐价格约为2800元/吨。作为对照,应用广泛的solar salt具有相近的熔点(220℃)和相变焓(161kJ/kg),其价格折合为5040元/吨。3∶7的混合盐相比solar salt的价格降低约45%,大大降低了应用成本,具有很好的经济性。
6 结 论
本文从蓄热材料的角度出发,本文将硝酸钙与硝酸钠按不同摩尔比进行混合以得到一种高性价比的中温相变材料。经过实验测试,硝酸钙与硝酸钠摩尔比为3∶7的共晶熔融盐性能最佳,其熔点为217.4℃,相变焓为135.8kJ/kg。在多次吸热放热循环中,循环稳定性良好,质量保持稳定。实验同时测定了该配比混合盐的比热容与腐蚀性,该混合盐与常见的不锈钢201、304、316L和铝合金1060具有良好的相容性。相比与之相变蓄热能力相当的solar salt,其成本大幅减少,具有良好的规模化应用前景。
[1] Zabla B,Marin J M,Cabeza L F,et al.Review on thermal energy storage with phase change:Materials,heat transfer analysis and applications[J].AppliedThermal Engineering,2003,23:251-283.
[2] Sharma A,Tyagi V V,Chen C R,et al.Review on thermal energy storage with phase change and applications[J].RenewableandSustainableEnergyReviews,2009,13:318-345.
[3] 左远志,丁静,杨晓西.中温相变蓄热材料研究进展[J].现代化工,2005,25(12):15-19.
[4] Kenisarin M M.High-temperature phase change material for thermal energy storage[J].RenewableandSustainable EnergyReviews,2010,14:955-970.
[5] 葛志伟,叶锋,Lasfargues M,等.中高温储热材料的研究现状与展望[J].储能科学与技术,2012,1(2):89-102.
[6] Jriri T,Rogez J,Bergman C,et al.Thermodynamic study of the condensed phases of NaNO3,KNO3and CsNO3and their transitions[J].ThermochimicaActa,1995,266:147-161.
[7] 彭强,丁静,魏小兰,等.硝酸熔盐体系在能源利用中的研究进展[J].现代工业,2009,29(6):17-22.
[8] 吴志根,赵长颖,顾清之.多孔介质在高温相变蓄热中的强化换热[J].化工学报,2012,63(s1):119-122.
[9] Iverson B D,Broome S T,Kruizenga A M,et al.Thermal and mechanical properties of nitrate thermal storage salts in the solid-phase[J].SolarEnergy,2012,86:2897-2911.
[10] Roget F,Favotto C,Rogez J.Study of the KNO3-LiNO3and KNO3-NaNO3-LiNO3eutectics as phase change materials for thermal storage in a low temperature solar power plant[J].SolarEnergy,2013,95:155-169.
[11] Zhao C Y,Wu Z G.Thermal property characterization of a low melting-temperature ternary nitrate salt mixture for thermal energy storage systems[J].SolarEnergy Materials&SolarCells,2011,95:3341-3346.
[12] Peng Q,Ding Jing,Wei Xiaolan,et al.The preparation and properties of multi-component molten salts[J].AppliedEnergy,2010,87:2812-2817.
[13] Bauer T,Pfleger N,Laing D,et al.High-temperature molten salts for solar power application[J].MoltenSalts Chemistry,2013:415-438.
[14] Protsenko P I,Bergman A G.Binary system Ca(NO3)2-NaNO3[J].Russ.J.Gen.Chem.,1950,20:1421-1431.
[15] Goods,S.H.,Bradshaw,R.W.Corrosion of stainless steels and carbon steel by molten mixture of commercial nitrate salts[J].JournalofMaterialsEngineeringand Performance,2004,13(1),78-87.
