口捷爽复方泡腾片稳定性考察
2014-07-18王晓瑜王英楠
王晓瑜,张 磊,陈 辉,王英楠
·药学研究·
口捷爽复方泡腾片稳定性考察
王晓瑜1a,2,张 磊1a*,陈 辉1a,王英楠1b
目的 考察口捷爽复方泡腾片的稳定性,并初步确定其有效期。方法 观察并测定复方泡腾片在强光、高温及高湿度等环境下的性状、崩解时限、重量差异、发泡量、酸度、含量等指标的变化。结果 加速试验与长期试验中各项考察指标均无明显变化,符合药品质量标准的相关规定。结论 口捷爽复方泡腾片在加速试验和长期试验条件下稳定,可初步预测该制剂的有效期1年。
替硝唑;盐酸左氧氟沙星;泡腾片;稳定性
0 引言
口捷爽复方泡腾片为天津后勤学院附属医院研制的一种用来抑制牙菌斑形成的新型片剂,其可抑制变形链球菌的生长和菌斑的形成,进而预防龋病[1]。泡腾片是一种遇水可放出大量二氧化碳气体而达到快速崩解作用的新型片剂。该剂型具有迅速溶解,吸收快、生物利用度高等优点[2],且携带、使用方便,水中分布均匀,兼具了固体制剂和液体制剂的特点。口捷爽复方泡腾片将盐酸左氧氟沙星和替硝唑这两种不同类型的抗菌药制备成片,提高了药物的崩解和溶出速度,方便使用,有着较好的临床应用前景。本文对口捷爽复方泡腾片的稳定性进行考察,确定制备和储存条件。
1 仪器与材料
高效液相色谱仪CTO-10AS VP(日本岛津公司);UV-754紫外分光光度仪(上海第三分析仪器厂);RCZ-8A智能药物溶出仪(天津大学精密仪器厂)。 材料:盐酸左氧氟沙星(中国药品生物制品检定所,批号20091204);替硝唑(中国药品生物制品检定所,批号20100314);口捷爽复方泡腾片(自制,批号:120312,120314,120317)。
2 方法
参考《中国药典》2010年版二部附录ⅠA片剂部分与查阅文献[3],确定考察项目为性状、鉴别、崩解时限、重量差异、含量、发泡量、酸度等7项。
2.1 性状 肉眼观察其色泽,光洁度。本品淡黄色,表面光洁,片子完整。
2.2 鉴别
2.2.1 对照品溶液配制 分别取盐酸左氧氟沙星和替硝唑对照品适量,精密称定,用流动相(0.05 mol/L的磷酸二氢钾水溶液-甲醇-乙腈60∶15∶25)溶解制成每1 mL中含有盐酸左氧氟沙星和替硝唑为0.01 mg的溶液。
2.2.2 供试品溶液配制 取泡腾片细粉适量(约相当于盐酸左氧氟沙星5 mg、替硝唑5 mg),精密称定,加流动相溶解制成1 mL中含有盐酸左氧氟沙星和替硝唑为0.01 mg的溶液,滤过备用。
2.2.3 高效液相色谱法鉴别 精密量取对照品溶液、供试品溶液各20 μL进样,并记录色谱图,结果供试品色谱在与对照品色谱相应的位置上,显示有相同的峰,如图1~图3。
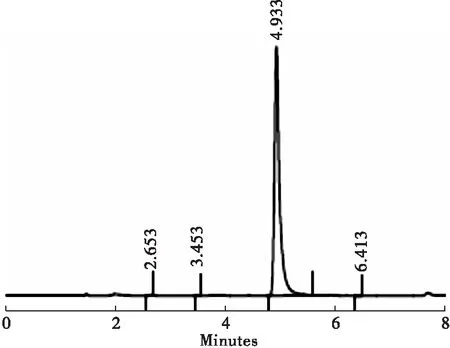
图1 盐酸左氧氟沙星的高效液相色谱

图2 替硝唑的高效液相色谱
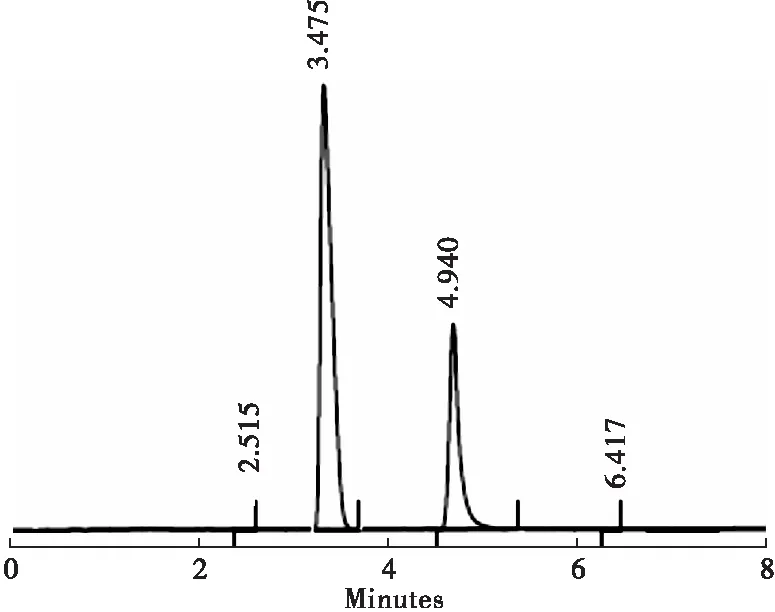
图3 复方泡腾片的高效液相色谱
2.3 崩解时限 取本品6片,分别置于250 mL烧杯,烧杯内盛有200 mL水中,水温为常温,待片剂或碎片周围的气体停止逸出时,片剂应溶解或分散在水中,无聚集的颗粒停留,各片均在5 min内崩解。
2.4 重量差异 取药片20片,精密称定总质量,求得平均片重后,再分别精密称定各片的质量,称定的药片质量与平均片重(500 mg)相比较,不超出重量差异限度(475~525 mg)。
2.5 含量测定 取本品10片,精密称定,研细,精密称取适量(拟相当于盐酸左氧氟沙星和替硝唑20 mg)置100 mL量瓶中,加流动相溶解至刻度,摇匀,滤过。精密量取续滤液1 mL,置10 mL量瓶中,加流动相稀释至刻度,摇匀。精密量取20 μL注入液相色谱仪,记录色谱图,按标准曲线法计算含量即得。每片含量为100 μg左右[4]。
2.6 发泡量 取25 mL带塞试管10支,每只试管分别加入精密称取的纯化水2 mL,置于37 ℃水浴中5 min后,各管中分别投人本品1片,密塞20 min,观察最大发泡量的体积,平均大于6 mL。
2.7 酸度 取本品20片,分别加15 ℃纯化水100 mL使其完全溶解,使用酸度计测定其pH值,pH值为4.5 ±0.2。
3 稳定性试验
3.1 影响因素试验 取本品3批样品去除包装,分别于高温(60 ℃)、高湿(25 ℃),相对湿度(90±5)%、光照 (4500±500)Lx条件下放置10 d,考察各指标,并与0 d数据比较。结果见表1。
由表1可见,在强光照射下,样品随时间延长,颜色有所加深并且含量逐渐下降,说明本品对光敏感,宜避光保存。高温(60 ℃)条件下,样品含量下降明显,在40 ℃条件下同法进行试验,含量无明显变化。说明本品不耐高温,适宜室温保存。高湿度试验中样品增重40%以上,并且发泡量降低,说明本品不耐湿,宜封闭保存,且包装内应放干燥剂。
3.2 加速试验 取双层铝塑复合膜包装的样品3批。于(40±2)℃、相对湿度(75±5)%条件下,放置6个月,分别于1,2,3,6个月末取样测定,测定结果与0个月比较。结果见表2。
3.3 长期试验 取双层铝塑复合膜包装的样品3批,于(25±2)℃,相对湿度(60±10)%的条件下放置12个月,于3,6,9,12个月取样测定,结果与0个月比较。结果见表3。
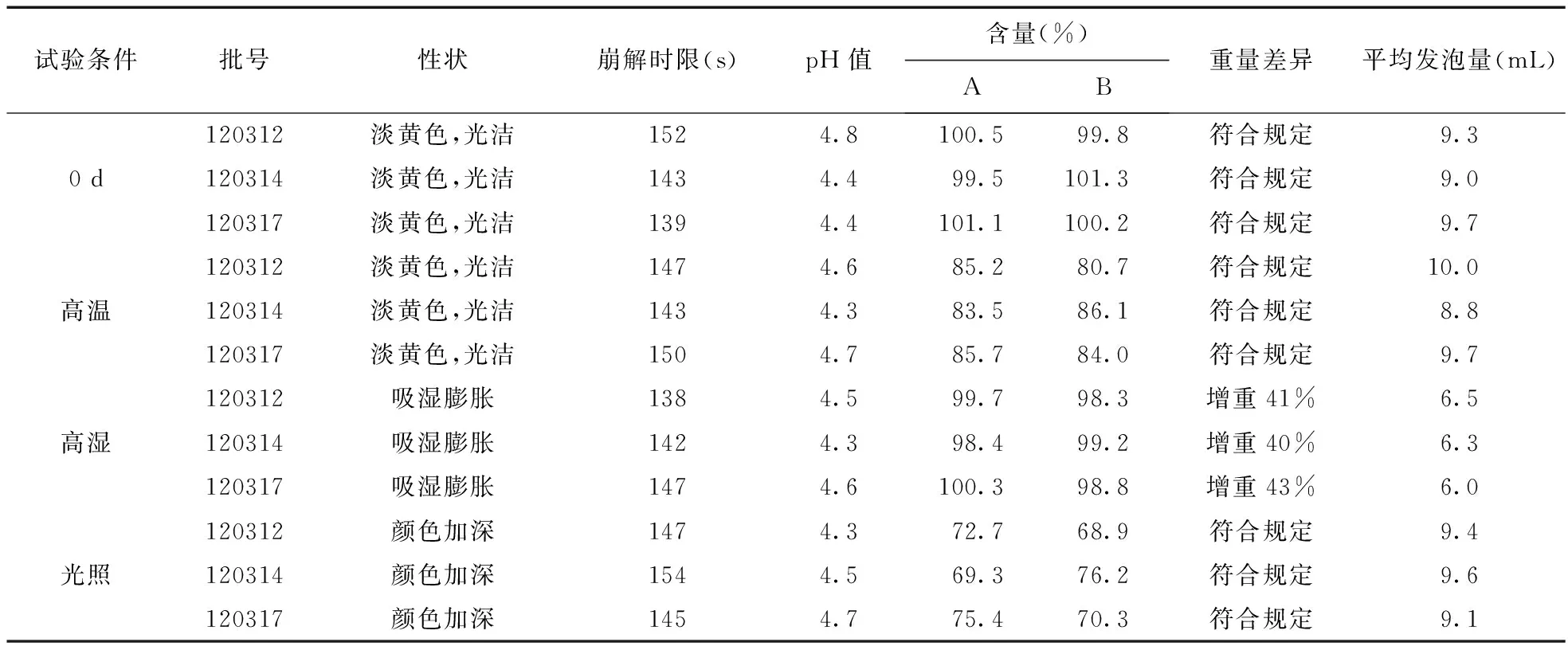
表1 影响因素试验结果
注:A为盐酸左氧氟沙星,B为替硝唑,下同
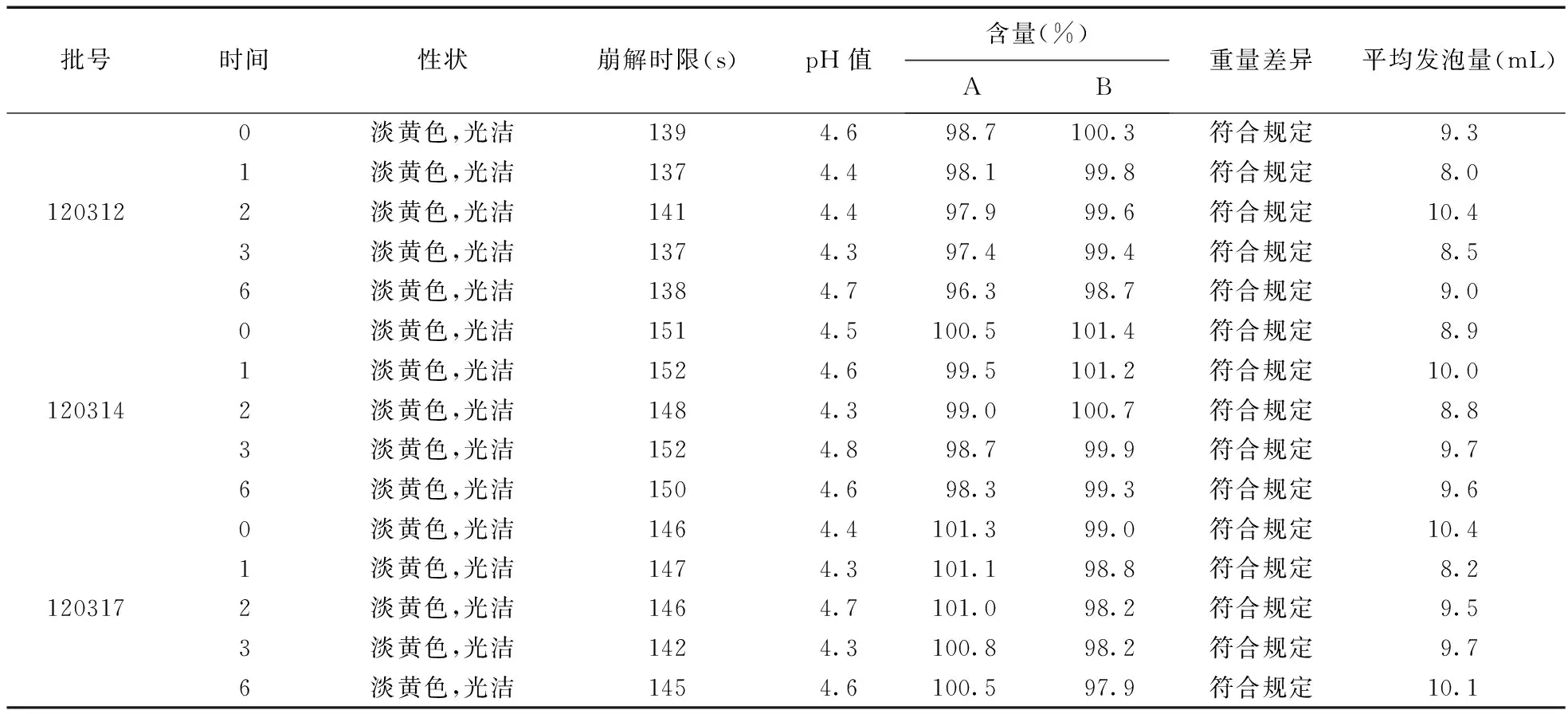
表2 加速试验结果
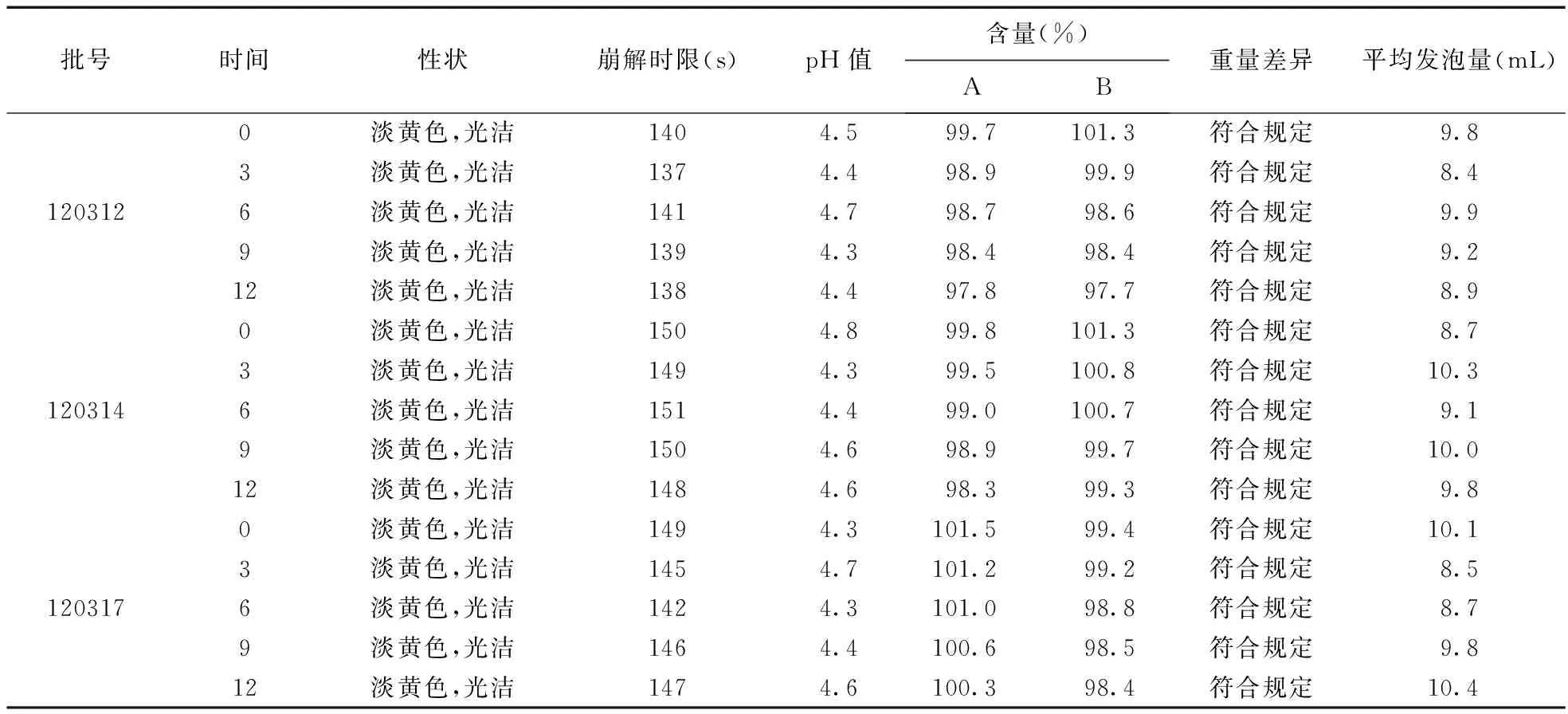
表3 长期试验结果
由表2和表3可见,样品在加速试验和长期试验中,性状、崩解时限、pH值、含量、重量差异和平均发泡量等指标均符合质量要求。
4 讨论
泡腾片中含有的酸源和碱源,较容易吸湿,而本品选用的酸源枸椽酸,引湿性较强[5]。因此,在高湿度试验中本品吸湿膨胀,在高湿环境下泡腾片迅速吸收空气中的水分,使得片剂中的辅料枸椽酸和碳酸氢钠遇水产生泡腾作用,故发泡量降低。本品中所含的主药替硝唑和盐酸左氧氟沙星分别为硝基咪唑类抗菌药和喹诺酮类抗菌药,两者均为遇光不稳定药品,需避光保存,因此,在强光条件下主药含量降低。
药品稳定性研究的目的是通过对药品在不同条件下主要质量指标随时间变化的规律进行的研究,为药品的包装形式、保存条件的确定和有效期的建立提供依据。本品的加速试验和长期试验的结果显示,口捷爽复方泡腾片6个月和12个月的各项指标均无明显变化。初步预测其有效期为一年。稳定性结果表明,本品在室温避光干燥的条件下稳定性良好,在暂定有效期的一年内可保证该制剂的安全和有效性。
[1] 刘继铁,张磊,朱铁梁,等.口捷爽漱口液对牙菌斑清除效果的临床试验研究[J].武警医学院学报,2008,17(12):1068-1070.
[2] 杨丽君,李健和.黎血塞通泡腾片的制备及质量控制[J].中南药学,2009,7(8):570-574.
[3] 刘倩,郑国华,程璐,等.咽舒饮泡腾片稳定性考察[J].中国药师,2011,14(9):1361-1362.
[4] 张磊,朱铁梁,张莉,等.替硝唑与盐酸左氧氟沙星复方泡腾片的制备与质量控制[J].中国医院药学杂志,2009,29(2):110-113.
[5] 张瑞斌,王春艳.替硝唑阴道泡腾片生产工艺研究[J].黑龙江医药,2008,21(1):43-45.
Inspection of the stability of Koujiesuang compositate effervescent tablets
WANG Xiao-yu1a,2,ZHANG Lei1a*,CHEN Hui1a,WANG Ying-nan1b
(a.Department of Pharmacy,b.Department of Oncological Surgery,Tianjin 300162,China;2.Xinjiang Provincial Corps Hospital,Chinese People′s Armed Police Forces,Urumqi 830002,China.)
Objective To investigate the stability and its validity of Koujiesuang compound effervescent tablets.Methods Several indexes such as characteristics,disintegration time,weight variation,foam volume,acidity and content were observed and measured.Results The index of the tablets including accelerated test and long-term test inspection had no significant changes,and reached the standard of quality of the tablets according to regulations.Conclusion Koujiesuang compound effervescent tablets have satisfactory stability in the accelerated test and long-term test.The effective date of expiration of the tablets is expected for a year.
Tinidazole;Levofloxacin hydrochloride;Effervescent tablets;Stability
2013-00-00
1.武警后勤学院附属医院a.药剂科,b.肿瘤外科 天津 300162;2.武警新疆总队医院,乌鲁木齐 830002
武警医学院青年基金资助项目(WYQ2006-13)
*通信作者
