拜新同联合拉贝洛尔治疗早期妊娠合并高血压的疗效及安全性
2014-07-02王湘江张敏肖纯
王湘江,张敏,肖纯
(惠州市第三人民医院ICU1、心血管内科2、心血管医学中心3、,广东惠州 516002)
·论著·
拜新同联合拉贝洛尔治疗早期妊娠合并高血压的疗效及安全性
王湘江1,张敏2,肖纯3
(惠州市第三人民医院ICU1、心血管内科2、心血管医学中心3、,广东惠州 516002)
目的比较拜新同联合拉贝洛尔和拜新同联合氢氯噻嗪治疗妊娠合并慢性高血压的疗效及安全性。方法在门诊收集早期妊娠(1个月)合并高血压2级患者100例,随机分为拜新同/拉贝洛尔组(观察组)和拜新同/氢氯噻嗪组(对照组),每组50例,分别观察两组降压效果和头晕、低血压、电解质紊乱等不良反应的发生情况,共观察6个月。结果6个月后两组收缩压和舒张压均显著下降[观察组收缩压由入组时的(165±18)mmHg下降至(130±10)mmHg,舒张压从(100±12)mmHg下降至(75±16)mmHg;对照组收缩压由入组时的(160±16)mmHg下降至(134±13)mmHg,而舒张压由(106±12)mmHg下降至(80±13)mmHg)],且组间差异无统计学意义(P>0.05);两组治疗前后肝、肾功能无明显变化,但对照组患者的血钾显著降低,尿酸、血糖明显升高[入组时血钾浓度为(4.0±0.3)mmol/L,6个月后血钾浓度为(3.4±0.3)mmol/L;尿酸则由(337±69)mmol/L升高至(410±100)mmol/L;血糖入组时(5.0±0.3)mmol/L,治疗6个月后血糖浓度为(6.0±0.6)mmol/L](P<0.05),且头晕、电解质紊乱等不良反应的发生率显著高于观察组(对照组不良反应发生率为26%,观察组不良反应发生率为4%)(P<0.01)。结论拜新同联合拉贝洛尔与拜新同联合氢氯噻嗪治疗早期妊娠合并高血压2级患者具有同等降压效果,但拜新同联合拉贝洛尔方案在安全性方面优于拜新同联合氢氯噻嗪方案。
拜新同;拉贝洛尔;氢氯噻嗪;妊娠合并慢性高血压;联合治疗
大量临床资料表明,超过70%的高血压患者需要两种及以上抗高血压药物方可使血压达标,而妊娠期高血压疾病,特别是妊娠合并慢性高血压患者既要适度控制血压,预防或延缓由血压升高所致的靶器官损害的发生,同时还要兼顾孕、产妇及胎儿的安全问题,这无疑增加了临床对此类人血压控制的难度[1]。因此,在临床工作中,我们除了要保证降压疗效的同时,尽可能减轻药物不良反应,联合用药不仅可以使血压尽快达标,而且可以减轻大剂量单药带来的不良反应。本研究采用了2012年妊娠期高血压疾病血压管理中国专家共识中推荐的联合降压方案[2],即采用前瞻性随机对照的方法评价拜新同联合拉贝洛尔或氢氯噻嗪治疗妊娠合并慢性高血压的疗效及安全性。
1 资料与方法
1.1 一般资料选取2011年1月至2013年4月期间在惠州市第三人民医院心血管内科及妇产科门诊就诊的早期妊娠合并高血压病2级的孕妇共100例。
1.1.1 入选标准(1)孕前即已确诊为原发性高血压;(2)近期妊娠(一个月内),且血压为160~180/ 100~110 mmHg(1 mmHg=0.133 kPa);(3)年龄≥18岁;(4)血尿酸、电解质、血糖、血脂、肝肾功能、血常规均正常者。
1.1.2 排除标准(1)合并心肌病、风心病、先心病等各种心脏疾病者;(2)各种疾病所致继发性高血压者;(3)近期内有感染者;(4)肝肾疾病及恶性肿瘤;(5)一个月内做过大手术或有过大的创伤,严重贫血。
1.1.3 分组入选的100例孕妇按照随机及平行对照原则,分为拜新同/拉贝洛尔(观察组)50例和拜新同/氢氯噻嗪(对照组)50例。观察组平均(28±4.21)岁,对照组平均(27±3.32)岁。两组用药前一般情况,如体重、血压、心率、肝肾功能、血脂、血钾及血糖比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法观察组最初给予拜新同(30 mg/片,20101201)30 mg/d和盐酸拉贝洛尔(200 mg/片,20101023)0.2 g/d;对照组予以拜新同30 mg/d,以及氢氯噻嗪(25 mg/片,20101124)25 mg/d。以上药物由山东黄海制药公司提供。2周后血压未达标者拉贝洛尔(观察组)或氢氯噻嗪(对照组)剂量加倍,1个月仍未达标者,将拜新同加至60 mg。在整个观察研究过程中若出现明显不良反应,如头痛、头晕、乏力、低血压、血管神经性水肿、严重电解质紊乱、血糖及血尿酸代谢异常等,可根据孕妇情况将相应药物减量,若减量后无明显改善者,应果断终止研究并根据病情换用合适药物继续治疗。总观察期为6个月。
1.3 监测指标治疗后2周及6个月内每个月进行随访,随访时间定为上午9点前。监测指标包括:血压(BP)、心率(HR)、实验室检查(血常规、尿常规、肝肾功能、血脂、血糖、血电解质、血尿酸),询问并记录不良反应,如头痛、头晕、乏力、血管神经性水肿、低血压等,同时记录下每次实验室检查异常指标。
1.3.1 BP监测每次随访在同一时间及地点,由同一医生使用欧洲高血压指南推荐的电子血压计测坐位血压,测量前安静休息至少10 min,袖带置于左手臂肘上3 cm,血压计与心脏在同一水平面上,连续测血压三次,每次间隔2 min,取三次平均值。
1.3.2 HR监测由上述同一医生听诊后记录心率,连续听三次,每次间隔2 min,取三次平均值。
1.3.3 实验室及自觉症状入选时、治疗后3个月及6个月进行血常规、尿常规、肝肾功能、血脂、血电解质、血糖、血尿酸检测,并记录下异常指标,同时询问并记录患者自觉症状,如头痛、头晕、乏力、血管神经性水肿、低血压等。
1.3.4 降压效果评价按照1997年4月全国心血管会议修订标准评定。显效:舒张压<90 mmHg (1 mmHg=0.133 kPa)且较基线值降低≥10 mmHg,或与基线值相比降低≥20 mmHg;有效:舒张压<90 mmHg但较基线值降低<10 mmHg,或与基线值相比降低10~19 mmHg;无效:未达到上述标准者。以显效和有效合并计算总有效率。
1.3.5 药物不良反应研究期间详细观察有无药物不良反应(ADR)发生,并记录下患者自觉症状、发生时间、处理方式及转归情况。ADR评定标准:(1)肯定与药物有关;(2)很可能与药物有关;(3)可能与药物有关;(4)可能与药物无关;(5)肯定与药物无关。上述五种评定标准中,前三者为ADR,统计为ADR发生率。若因药物不良反应而无法完成本次研究者,不进行疗效统计,但列入ADR统计中
1.4 统计学方法本实验采用SPSS17.0进行数据分析,计量资料用均数±标准差(±s)表示,各组治疗前后监测指标采用配对t检验,两组间比较也采用t检验,计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗的随访率比较前4个月两组的随访率为100%,随访至第5个月,对照组有两名孕妇因血糖升高而退出研究,随访率为96%,观察组一孕妇因不慎流产而终止研究,随访率为98%。随访至第6个月,对照组一孕妇因搬家而失访,观察组无人失访,对照组中最终完成研究47例,观察组49例,随访率分别为94%和98%。
2.2 两组患者的降压效果比较两组孕妇在入组时平均收缩压(SBP)和舒张压(DBP)差异无统计学意义(P>0.05)。6个月时,与入组时比较,两组SBP与DBP均明显降低,差异有统计学意义(P<0.01),两组间比较差异无统计学意义(P>0.05),见表1。两组间降压幅度差异也无统计学意义(P>0.05),见表2。观察组患者在治疗3个月及6个月后血压达标率较对照组略高,但差异无统计学意义(P>0.05),见表3。
表1 两组治疗前后血压比较(±s)
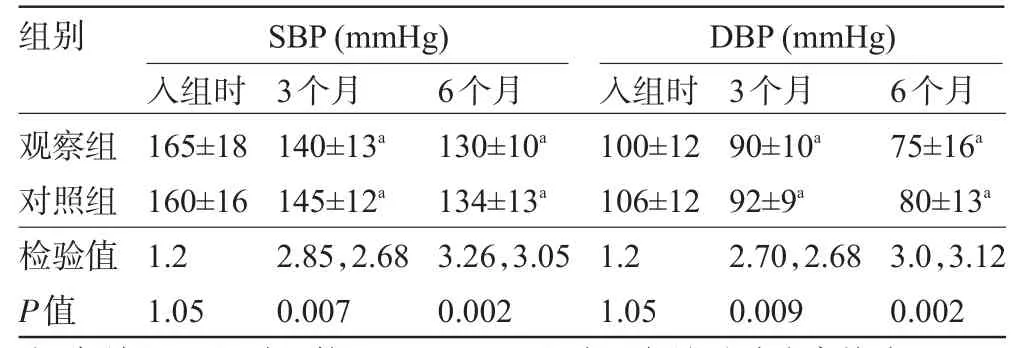
表1 两组治疗前后血压比较(±s)
注:与该组入组时比较,aP<0.01。两组在3个月后随访率均为100%,而6个月后,观察组有49例继续参与随访,对照组则只有47例。
组别SBP(mmHg)DBP(mmHg)观察组对照组检验值P值入组时165±18 160±16 1.2 1.05 3个月140±13a145±12a2.85,2.68 0.007 6个月130±10a134±13a3.26,3.05 0.002入组时100±12 106±12 1.2 1.05 3个月90±10a92±9a2.70,2.68 0.009 6个月75±16a80±13a3.0,3.12 0.002
表2 两组治疗后降压幅度比较(±s)

表2 两组治疗后降压幅度比较(±s)
组别SBP(mmHg)DBP(mmHg)观察组对照组检验值P值3个月25±13 16±8 2.85,2.68 0.007 6个月30±11 26±12 3.26,3.05 0.002 3个月10±8 14±9 2.70,2.68 0.009 6个月25±9 26±10 3.0,3.12 0.002

表3 两组治疗后达标率比较(%)
2.3 两组生化指标比较两组孕妇治疗前后血常规、尿常规、肝功能、肾功能、血脂无明显变化。治疗3个月后,对照组血糖较入组时升高,差异具有统计学意义(P<0.05),尿酸则较入组时明显升高(P<0.01);治疗6个月后,对照组血钾降低、尿酸及血糖较入组时明显升高,差异有统计学意义(P<0.01),而观察组治疗6个月后,血钾、尿酸、血糖较入组时差异无统计学意义(P>0.05),见表4。
表4 两组治疗前后生化指标比较(±s)

表4 两组治疗前后生化指标比较(±s)
注:与同组入组时比较,bP<0.05,aP<0.01。
组别观察组对照组时间入组时3个月6个月入组时3个月6个月血钾(mmol/L) 4.1±0.3 4.1±0.4 4.2±0.3 4.0±0.3 3.9±0.4 3.4±0.3a空腹血糖(mmol/L) 5.3±0.4 5.4±0.4 5.2±0.3 5.0±0.3 5.4±0.4b6.0±0.6a血尿酸(μmol/L) 340±69 343±61 350±75 337±69 395±87a410±100a
2.4 不良反应比较治疗6个月后,观察组出现轻度面部潮红、头痛各1例,ADR发生率为4%;对照组出现低钾4例、高尿酸3例、高血糖4例、头晕2例,ADR发生率为26%。观察组ADR发生率明显低于对照组,差异具有显著统计学意义(P<0.01)。
3 讨论
高血压是心脑血管疾病的独立危险因素,严重威胁着人们的健康。全世界的防治工作已深入开展,对其研究也日益广泛,而像妊娠合并慢性高血压这样的特殊人群,其健康关系到孕妇及胎儿的健康,因此对其防治极为重要。
拜新同(硝苯地平控释片)是钙通道阻滞剂家族中的一员,主要作用于细胞膜L-型钙通道,抑制钙内流而使细胞内钙离子浓度降低,导致小动脉的扩张,总外周阻力下降而发挥降压作用。对各种高血压均有良好的降压效果,大量临床试验证实[3-4],拜新同不仅具有降压作用强、速度快等优点,而且其对血脂、血糖、电解质无影响。拉贝洛尔属于肾上腺受体阻断药,它对α、β受体的阻断作用选择性不强,临床主要用于中、重高血压的治疗。两者合用,后者能消除拜新同因扩血管作用所产生的反射性心动过速,从而减少ADR。噻嗪类利尿剂是临床广泛应用的一类口服利尿剂和降压药,氢氯噻嗪是该来药物的原型药物,脂溶性较高,口服吸收迅速而完全,它通过增强氯化钠和水的排出,产生温和持久的利尿及降压作用。与硝苯地平合用,能减少利尿剂的剂量,减少副作用,减轻ADR。同时,氢氯噻嗪能消除硝苯地平扩血管可能引起的水钠潴留,并增强期降压效果,因此,硝苯地平和氢氯噻嗪合用在降低血压和减轻不良反应方面具有协同作用。
本研究证实了拜新同联合拉贝洛尔或氢氯噻嗪治疗妊娠合并慢性中度高血压有显著的效果,两种联合降压方式的降压幅度比较差异无统计学意义(P>0.05),且两组有效率和达标率相当,说明两种联合方式的降压疗效差异无统计学意义,这与对原发性高血压患者降压的研究相似[5-6]。同时,本研究还发现,两种治疗方案在整个研究过程中对肝功能、肾功能、血脂影响较小,对照组血糖升高、低钾、高尿酸发生率明显高于观察组,表明拜新同联合氢氯噻嗪降压时,应注意监测血糖、电解质、血尿酸。之前的报道较多的是噻嗪类利尿剂对电解质、尿酸影响较大[7-8],其升高血糖的报道较少,这可能与妊娠期机体代谢功能紊乱有关,噻嗪类利尿药对妊娠期高血压患者是否安全可靠,尚需大规模的临床研究证实。
总之,拜新同联合拉贝洛尔或氢氯噻嗪均有显著的降压效果,拜新同联合拉贝洛尔这种治疗方案对妊娠期高血压患者肝肾功能、电解质、血脂、血糖等的影响甚小,而且在妊娠早期对胎儿影响甚小(数据未给出);而拜新同联合氢氯噻嗪治疗方案对妊娠期高血压患者血钾、血糖和血尿酸均有一定的影响,在治疗过程中注意定期复查血钾、血糖和血尿酸,故联合治疗时,不推荐首选利尿剂,对妊娠前已经在使用氢氯噻嗪的患者,且妊娠中合并水肿而必须继续使用利尿剂者,一定要严密监测上述指标。因此,拜新同联合拉贝洛尔是妊娠合并慢性高血压患者更为理想的降压治疗方案。
[1]Cushman WC,Ford CE,Cutler JA,et al.Success and predictors of blood pressure control in diverse North American settings:the antihypertensive and lipid-lowering treatment to prevent heart attack trial (ALLHAT)[J].J Clin Hypertens(Greenwich),2002,4(6):393-404.
[2]中国医师协会高血压专业委员会.妊娠期高血压疾病血压管理中国专家共识[J].中华高血压杂志,2012,20(11):1023-1027.
[3]Rezaei Z,Sharbaf FR,Pourmojieb M,et al.Comparison of the efficacy of nifedipine and hydralazine in hypertensive crisis in pregnancy[J].Acta Med Iran,2011,49(11):701-706.
[4]Giannubilo SR,Bezzeccheri V,Cecchi S,et al.Nifedipine versus labetalol in the treatment of hypertensive disorders of pregnancy[J]. Arch Gynecol Obstet,2012.286(3):637-642.
[5]Schoenberger JA,Glasser SP,Ram CV,et al.Comparison of nitrendipine combined with low-dose hydrochlorothiazide to hydrochlorothiazide alone in mild to moderate essential hypertension[J].J Cardiovasc Pharmacol,1984,6(Suppl 7):1105-1108.
[6]Ohman KP,Weiner L,von Schenck H,et al.Antihypertensive and metabolic effects of nifedipine and labetalol alone and in combination in primary hypertension[J].Eur J Clin Pharmacol,1985.29(2):149-154.
[7]Lapuerta P,Franklin S.The risks and benefits of initial irbesartan/ hydrochlorothiazide combination therapy in patients with severe hypertension[J].J Clin Hypertens(Greenwich),2009,11(5):277-283.
[8]Dorsch MP,Gillespie BW,Erickson SR,et al.Chlorthalidone reduces cardiovascular events compared with hydrochlorothiazide:a retrospective cohort analysis[J].Hypertension,2011,57(4):689-694.
Clinical efficacy and safety of Nifedipine Controlled-release Tablets combined with Labetalol in patients with early gestational hypertension.
WANG Xiang-jiang1,ZHANG Min2,XIAO Chun3.Intensive Care Unit1,Department of Cardiology2,Cardiovascular Medical Center3,the Third People's Hospital of Huizhou,Huizhou 516002,Guangdong, CHINA
ObjectiveTo compare the effect and safety of Nifedipine Controlled-release Tablets combined with labetalol and Nifedipine Controlled-release Tablets combined with hydrochlorothiazide in patients with early gestational hypertension.MethodsWe collected 100 patients with early gestational hypertension from the Outpatient Department.The patients were randomly divided into two groups and treated by Nifedipine Controlled-release Tablets combined with labetalol(the observation group)and Nifedipine Controlled-release Tablets combined with hydrochlorothiazide(the control group),with 50 patients in each group.The patients were followed up for 6 months.The clinical effect and adverse reactions(dizziness,hypotension,electrolyte disturbances)were observed.ResultsSix months later,the systolic and diastolic blood pressures were significantly reduced in the two groups.The systolic pressure decreased from (165±18)mmHg to(130±10)mmHg and the diastolic pressure decreased from(100±12)mmHg to(75±16)mmHg in the observation group;meanwhile,the systolic pressure decreased from(160±16)mmHg to(134±13)mmHg and the diastolic pressure decreased from(106±12)mmHg to(80±13)mmHg in the control group,with no statistically significant difference between the two groups(P>0.05).The serum potassium decreased from(4.0±0.3)mmol/L to(3.4±0.3)mmol/L;the uric acid increased from(337±69)mmol/L to(410±100)mmol/L;the glucose increased from(5.0±0.3)mmol/L to (6.0±0.6)mmol/L,P<0.05.The incidence of adverse reactions in the observation group was significantly less than that in control group:with 26%in the control group and 4%in the observation group.ConclusionBoth Nifedipine Controlled-release Tablets combined with labetalol and Nifedipine Controlled-release Tablets combined with hydrochlorothiazide could obviously reduce the blood pressure in patients with gestational hypertension,but Nifedipine Controlled-release Tablets combined with labetalol is safer.
Nifedipine Controlled-release Tablets;Labetalol;Hydrochlorothiazide;Gestational hypertension; Combined treatment
R714.24+6
A
1003—6350(2014)03—0329—04
2013-06-24)
10.3969/j.issn.1003-6350.2014.03.0128
肖纯。E-mail:hyxiaoc@medmail.com
