发光纳米材料和量子点化学传感及其机理
2014-06-26晋卫军
晋卫军
(北京师范大学化学学院,北京100875)
0 引言
发光量子点在无机阳离子或阴离子、以及有机分子和生物分子识别方面正在发挥着重要作用。文献已经报道了许多灵敏的和选择性的体系,甚至在某些特殊方面的应用是专属性的。但在传感机理方面存在不少问题,有的得到了充分证明,而大多数是合理推测出来的。而对传感机理的认识,是设计新颖、灵敏的传感器的关键环节。所以,该评述首先介绍了量子点化学传感的光物理的及化学过程,指出其中可能的问题和解决的策略,以期抛砖引玉,使读者在设计具有灵敏和选择性的量子点传感器方面有所收益。然而,需要说明的是,现在的相关文献浩瀚如海,该文尽量选择一些有代表性的予以介绍,挂一漏万在所难免,希请谅解。
1 纳米材料或量子点荧光/磷光的起源
1.1 无机半导体量子点
如图1所示,在半导体材料中,当一个电子从价带被激发到导带后,导带中的电子与价带中留下的带正电的空穴,通过库仑作用形成一个类氢原子的束缚态,被称为激子(exciton)。激子半径1~10 nm,键合能~10 meV,如ZnS半导体激子半径大约2.3 nm。在此情况下,导带和价带之间的能隙(Energy or band gap,Eg)较小,相应的能量位于红外区,发光效率很低,不具有分析化学的应用价值。
然而,当半导体材料的三维尺寸落在纳米级别时,也就是说,当半导体材料颗粒的尺寸与其激子半径在同一数量级或更小时,激子的运动就变得受限于纳米粒子内。量子限制效应(quantumconfinement effect)就表现出来了。即微结构材料三维尺度中至少有一个维度与电子德布罗意(deBroglie)波长相当时,导带和价带间隙随半导体纳米粒子尺寸的减小而增加,并且能带由连续态变成分立 (discreted)的状态。所以,量子点(Quantum Dot)就是把激子束缚在三维空间的半导体纳米结构材料。
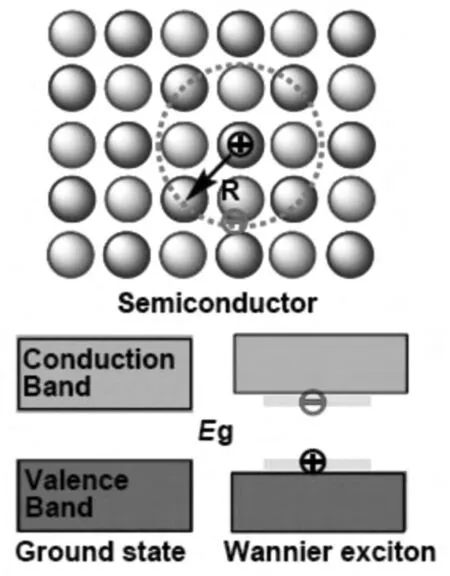
图1 典型无机半导体Wannier激子示意图Fig.1 Wannier exciton in typical inorganic semiconductors(Radius~ 100 Å,Bonding enengry~ 10 meV)
一些半导体纳米粒子,如CdS,CdSe,ZnO及Cd3As2等,所呈现的量子尺寸效应可由Brus提出的尺寸效应公式表达[1~3]:质中,由于界面效应引起体系介电增强的现象);第四项:有效里德堡能。由上式可以看出:随着粒子半径的减少,其吸收光谱发生蓝移。
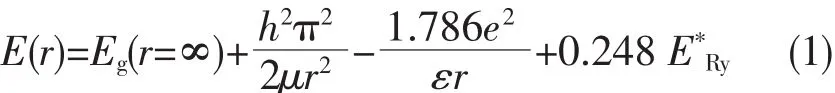
物理学上,把纳米粒子看作一个陷阱或势阱(potential well),在此势阱中激子的能级水平可以用一个简化的模型来表示,即方程式(2):

式中,a为粒子的半径;meff为激子的有效质量。电子态呈量子化分布,且能级随势阱尺寸的减小而增大。激子复合发光的波长范围由红外区蓝移到可见和紫外区,发光量子产率也逐步显著增加。为了生物标记,人们经常希望合成发光波长位于红区(如大于650 nm)的量子点,但付出的代价是,此时量子点的量子产率会显著降低。
表面结构影响量子点的性质。由于表面的原子排布不规则,因配位不饱和产生的悬空键,导致高的活性和表面缺陷。所以表面结构对其性质产生的显著影响。表面缺陷会俘获电子或空穴,引起量子产率下降及光稳定性变差。稍后将会提到,核壳结构的量子点可以提高其化学和光稳定性[4]。形态对量子点的光学性能也有影响,如球形量子点,其光发射性质是非偏振的,或者是圆偏振的,而梭形/棒形的量子点则会发射沿长轴的完全线偏振光[5]。因此,改变量子点的晶体组成、粒径、形态以及表面配体,对进一步拓宽量子点的应用具有重要的意义。
1.2 金属离子掺杂的无机半导体量子点
在晶体的价带和导带之间,由于晶格畸变或掺杂会产生一些独立的局部能级。所以,如图2
式中r为粒子半径,μ为激子折合质量,h为普朗克常数。第二项:量子限域能(蓝移);第三项:介电限域能(红移)(介电限域:纳米粒子分散在介所示,金属离子掺杂的纳米晶体的发光可能源于几种状态。一是激子从导带或较浅俘获态a的直接复合,产生量子尺寸效应的荧光发射,波长较短。如ZnS纳米粒子位于420 nm或450 nm左右的蓝色荧光。第二,起源于较深的俘获态b的发光,寿命可能较长,通常称之为磷光。另外一种途径,如图2中所示,电子从导带或较浅的能级布居到掺杂金属离子的激发态能级,由此回到基态或较低能级的光辐射,也叫做磷光。 以Mn2+为例(右),在ZnS本体相中Mn2+离子的橙光发射(~590 nm)源于其自旋禁阻的(spin-forbidden)4T1态到6A1基态的发射,寿命长达ms级或更长,即余辉较长。因为Mn的d电子被外层的s电子所屏蔽(电子组态[Ar]3d54s2),所以 Mn2+的 d电子波函数是定域的,受量子限域效应的影响较小,即纳米ZnS中Mn2+的能级不会因为纳米粒子尺寸的变化而显著移动。当然,基质晶体场对Mn2+的发光量子产率和发光波长有一定影响,但不存在量子限域效应。再者,本来Mn2+的4T1-6A1辐射跃迁是自旋禁阻的,可是在ZnS基质的四面体晶体场中由于弱的自旋-轨道耦合作用 (spin-orbital coupling),使得这一自旋禁阻的跃迁变得部分允许。另一方面,金属离子本身的吸光系数很小,而纳米晶体的吸收系数较高,可以通过如图2所示的途径将能量传递到4T1态。所以,可把纳米晶体看作掺杂离子的天线分子,类似于稀土配合物中稀土离子发光的光物理途径。Cu2+的掺杂有时候可能是以Cu+形式存在的,这种情况下共激活剂Cl-或 Al3+是必要的[6~7],以起到电荷补偿作用,使得激活剂(即发光中心)Cu+更容易进入晶格。许多情况下杂质Fe、Co、Ni等可能充当猝灭剂的作用,要小心去除。
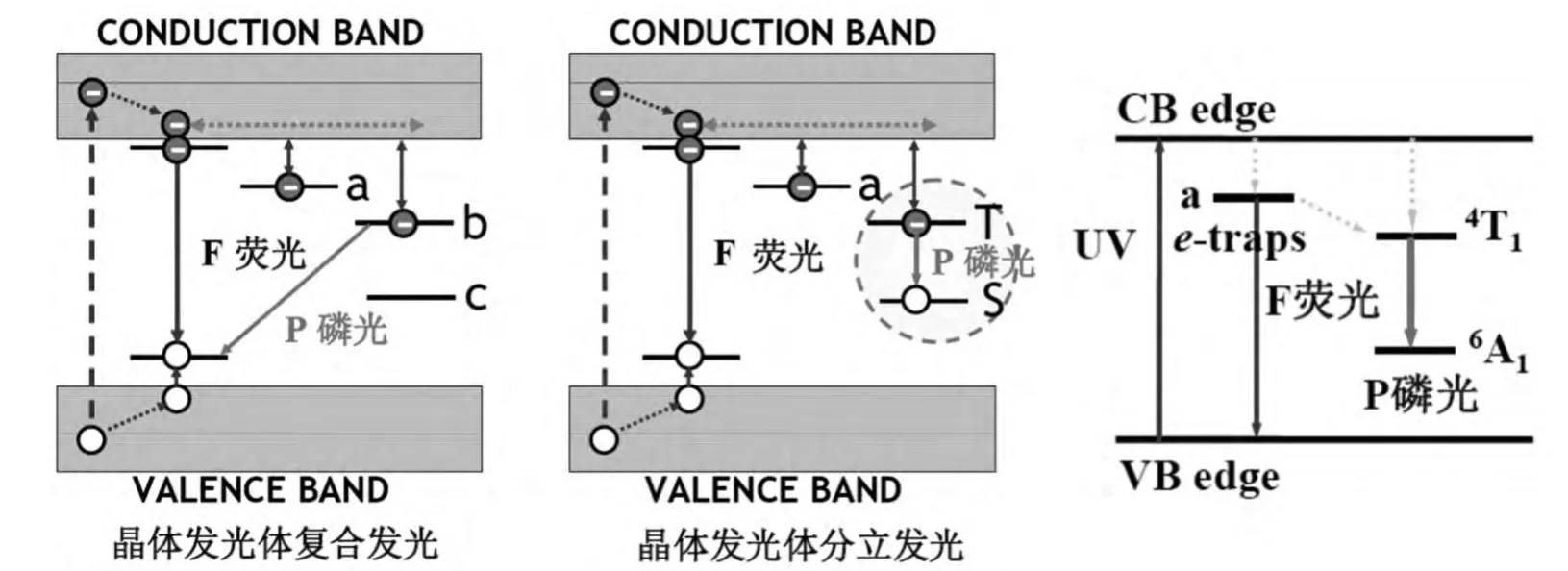
图2 晶体纳米粒子光致发光示意图。a表示较浅的俘获态能级(trap),b表示较深的俘获态能级,c表示较深俘获态的空穴。左:非掺杂状态的发光示意图;中:掺杂状态的发光示意图;右:Mn2+离子的磷光辐射跃迁Fig.2 Photoluminescence of crystal semiconductor nanoparticles
已有综述文章介绍金属离子掺杂量子点荧光探针或示踪剂的应用情况[8]。常见的掺杂金属离子(除稀土离子外)包括:Co2+[9~13],发光源于4T1-4A2跃迁。激子复合发光大约330 nm,缺陷发射大约 530 nm,而 Co2+发光大约 680 nm (从localized Co2+d-levels,4T1(P),2T1(G),2E(G)态到4A2(F)态的跃迁)[10],或 570 nm[13],或者 3.2 μm(4T2(F)到4A2(F))[11]。Ni2+发光源于3T2-3A2跃迁,发光从498 nm 到 520 nm 都有报道[9,14~16]。Mn2+发光源于4T1-6A1跃迁,大约590 nm,是研究最多的一种掺杂金属离子[17~24]。Pb2+发光源于3P0-1S0跃迁,大约725 nm[25]。 Cu2+或 Cu+发光[6~7,26~27]具有较宽的波长范围,如500 nm到大约750 nm等都有报道。ZnS纳米粒子激子发光大约470 nm,而其中掺杂的Cu2+发光在500 nm,绿光。掺杂Ag+发光位于蓝区[28],报道较少。
掺杂金属离子的发光多源于三线态或其他多重态,与其自旋多重性不同的基态能级之间的跃迁是自旋禁阻的,属于磷光,寿命长达毫秒级以上,因此可以方便地利用一般的荧光分光光度计完成荧光和磷光的同时测量。通过发光衰减特征的测量可以区分磷光源于较深的俘获态,还是掺杂离子态(Cu2+/Cu+)[25];表面键合和晶格键合的Mn2+也具有不同的衰减特征[29]。
1.3 金属纳米粒子和金属团簇
大尺寸的金属纳米粒子本身并不具发光特性,尽管它们具有通过表面等离子体波(Plasma)增强有机染料或其它纳米粒子发光的性质[30~33],尤其具有增强Raman信号的优良特性[34~35]。
金属纳米粒子可以看作由带正电的核和带负电荷的自由电子组成。当电磁辐射波作用于粒径远小于其辐射波长的球形金属纳米粒子时,核和电子云的反向移动,使得电子密度在局部区域分布不均匀,出现偶极。当电子云远离核时,由电子和核之间的库仑引力产生的恢复力使得电子向相反方向移动,形成了电子在电磁波的操纵下的纵向振荡。如果,电磁辐射频率与自由电子的集体振荡频率相当时则产生共振。这种情况仅发生在金属纳米粒子表面的局部区域,此即局域表面等离子体共振[30]。如图3所示,这种次级的电磁辐射,对吸附于粒子表面一定范围(~3 nm或更远)的分子产生激励作用,从而增强分子荧光或Raman散射[31],或局域表面等离子体共振散射[32]。
但是,在团簇水平,许多金属离子可以在可见区发光,而且具有高的量子产率。其实,早在20世纪60年代,久保(Kubo)采用一种电子模型求得金属纳米晶粒的能级间距δ为:

式中:Ef为费米势能,N为粒子中的总电子数。该式指出,能级的平均间隔随着粒子的直径减小而增大,电子的移动变得更加困难,能隙变宽。
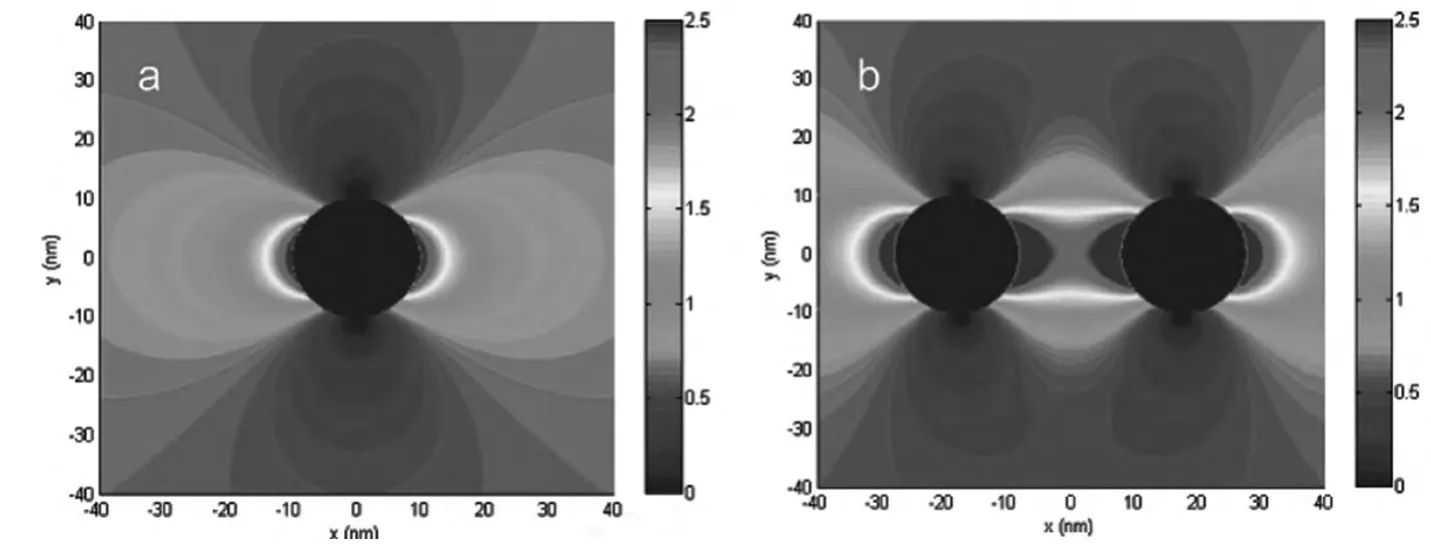
图3 在X-轴方向引起场振荡的金属银纳米粒子局域表面等离子体发射示意图[33]Fig.3 Electric fields near silver nanoparticle monomer(a)and dimer(b)were calculated by FDTD model under an incident light of 635 nm.Note the incident light is propagating along the y-axis and is polarized along the x-axis[33]
金簇(Au Clusters)在1 nm左右具有离散的电子态,没有等离子体波特性。在此粒径尺度,金簇的发光源于Au 5d10→6sp的带间跃迁或配体-金属电荷转移跃迁[36]。金簇的发光与粒径也有关系,如,Au7421 nm,Au8455 nm,Au9470 nm[36],Au25640 nm[37]等。据报道,金纳米粒子(nano-Au particles)发光的短寿命组分可能起源于纳米金的核[38],而长寿命组分可能起源于表面局域态,即配体-金属电荷转移跃迁[39~40]。
纳米金粒子的荧光可用于生物成像[41],并且利用纳米金粒子的吸光特征随单分散和聚集状态的变化,在可视比色分析中已显示巨大应用价值。
银团簇也是非常重要的一类发光的金属团簇,广泛应用于生物示踪探针或化学生物传感[42~48]。
1.4 硅点、碳点和石墨烯点
发光的多孔硅直接由单晶硅腐蚀而得,基体由纯硅原子组成,表面分布Si-O或Si-H键。而硅点通常采用硅氧烷或其他含硅化合物还原合成,化学反应速度快,恐难形成如单晶硅那样的晶体结构,缺陷较多[49~52]。据报道,电化学方法制备的硅点可以达到单晶硅级的结构水平[53~54]。激光光解也被认为是一种合成高质量硅点的方法[55~56]。
碳点和石墨烯点也同样存在类似问题。合成碳点的原料五花八门,经微波降消解或水热合成,如甘油 glycerol[57],蜡烛烟苔[58],草莓[59],葡萄[60],绿草[61],茧丝[62],豆奶[63],橘皮[64],菱皮[65]或柚子皮[66],豆腐渣等等。在这种情况下,原料中固有的一些生物发光的物质,或共轭化合物残存在烧焦的“碳糊”中,极有可能形成分子发光中心。许多碳点中的C含量仅为50%左右,氧和氮元素含量高,也许可以佐证这种猜想。图4表示以草莓为原料制备的碳点并用于Hg2+离子测定。
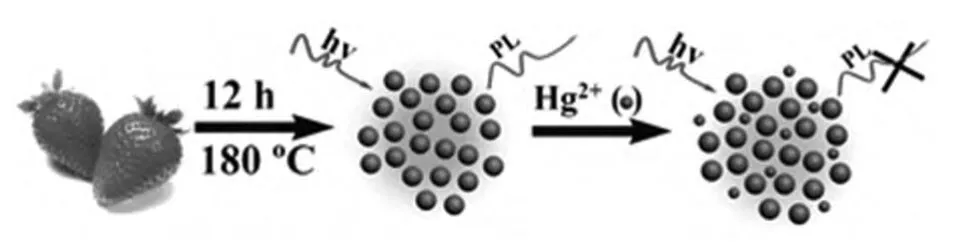
图4 碳点制备过程以及对Hg2+的响应示意图(碳点的荧光发射波长随激发波长变化而变,并且强度从短波长到长波长依次减弱。检测Hg2+时采用激发344 nm,发射 427 nm)[59]Fig.4 Schematic illustration of the preparation process for the C-dots and their application for Hg2+detection
然而,石墨烯点[67],就像多孔硅的纳米颗粒一样,基体组成是确定的,主要为石墨碳。小颗粒/单片层的石墨烯边缘或面内的碳被部分氧化,存在C=O、C-O或C-N等键合基团(hydroxyl,epoxy,carbonyl and carboxylic acid groups)。发光也主要来源于整体的或局域的π共轭体系,或n-π共轭体系,或n-π非共轭基团的发光,是否具有一定的量子限域效应值得进一步研究。
关于碳点的发光机理,图5为Sun等[57]提出的表面钝化的碳点发光机理示意图,图6为Fan等[68]提出的石墨烯点酰肼发光基团发光机理示意图。黑色材料是光的陷阱,但在纳米尺寸碳材料的确具有一些奇特的光学性质。其实,可以看出,关于所谓的碳点/石墨烯点的发光机制,确切的机理仍然是不清楚的,依据研究者使用的具体材料和具体反应体系,各圆其说,缺乏整体的和一般的解释。如图7(left)所示,水热法制备的碳点具有规整的结构,结构参数确认具有石墨结构[59]。如图7(right)所示,而利用石墨电极作为原料,电化学法制备的碳点具有石墨结构[69],类似于石墨烯点或碳纳米管点。无论石墨烯点或其他碳点,由于C元素的电子结构所决定,不大可能形成像半导体(ZnS、CdSe、Si等)量子点那样的激子结构。如前所述,石墨烯点表面或石墨烯片层边缘的化学基团是引起发光的决定性因素。因此,可以把石墨烯点或碳点的发光看作Frenkel激子的辐射复合。而这种激子定域于材料局部的化学基团,如芳香基,C=O 基,C=O(NH2-NH2-),或它们的组合等。
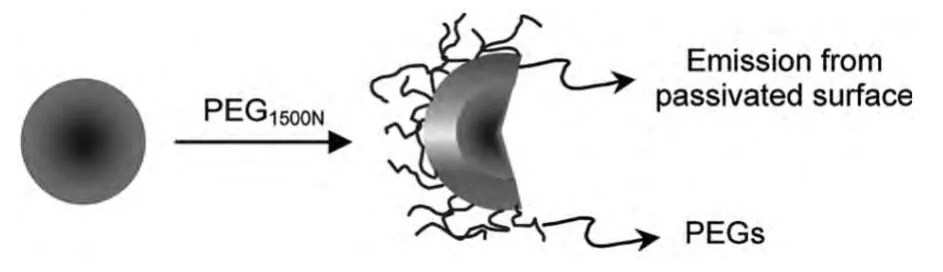
图5 表面钝化发光机制示意图[57]Fig.5 Emission from the passivated surface
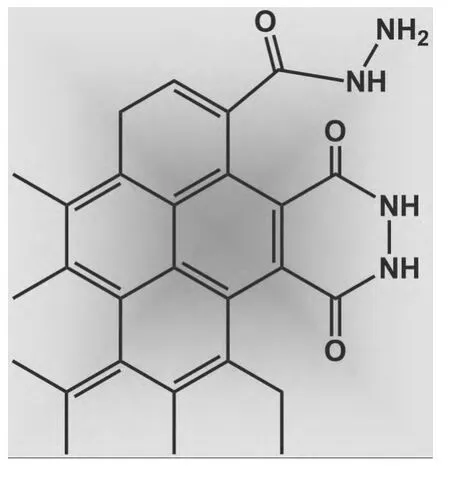
图6 在石墨烯边缘修饰的酰肼发光基团(hydrazide groups)的局部结构[68]Fig.6 Schematic illustration of the edge modified GQD structure determined by theoretical calculation

图7 碳点的TEM照片(左[59],中[60]和右[69])Fig.7 The TEM image of the CPs(left[59],middle[60]and right[69])(the lattice plane with an interfringe distance of 0.254 nm,0.203 nm,0.32 nm corresponding to the(100),(102),(002)planes of sp2 graphitic carbon)
除了上述提及的各种纳米材料或量子点,异质结(heterojunction),如 Au-Ag,Ag-Fe异质结等纳米材料或量子点/棒/线也是有用的传感材料[70]。
2 量子点或其它纳米材料荧光/磷光猝灭及增强的一般途径
2.1 电子或空穴的俘获
图8显示了量子点光致发光猝灭的一般途径。A表示电子溢出到量子点表面陷阱被捕获,正常的e--h+复合受阻,发光猝灭,如吸附在表面的吸电子猝灭剂O2或Cu2+等;B表示量子点外表面富电子组分,如胺和NO自由基等,将电子注入到空穴,相当于被表面陷阱捕获,正常的e--h+复合受阻,发光猝灭[71]。
2.2 量子点表面组成的变化对其发光的猝灭或增强
改变量子点表面的电荷和组成,就有可能改变核e--h+的复合重组。因此,基于不同的目的,可以合成比核材料具更宽禁带或更窄禁带的核-壳型量子点,如图9所示。前者Type I有效减少了表面俘获,显著改善了量子点发光量子产率[72~73],而后者更适用于基于电子转移的光化学或太阳能转化器件研究。从化学传感机理的角度,往往通过表面状态的变化,减少电子或空穴的捕获态,增强发光。这相当于在原量子点表面生成带隙更宽的壳层;或者,在原量子点表面生成带隙更窄的壳层,电子更容易泄露,或空穴更容易捕获,产生猝灭现象。在猝灭剂与量子点的反应过程中,生成的壳层材料,有时也会充当新的发光中心[74]。
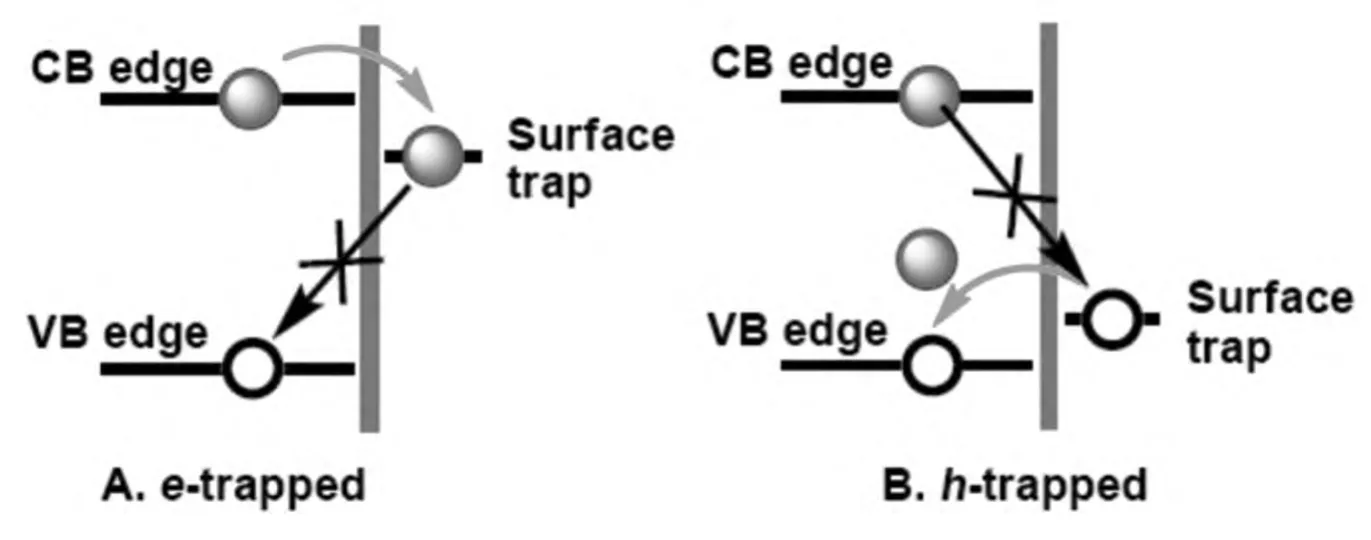
图8 量子点发光猝灭的一般途径Fig.8 General quenching mechanism of QD photoluminescence
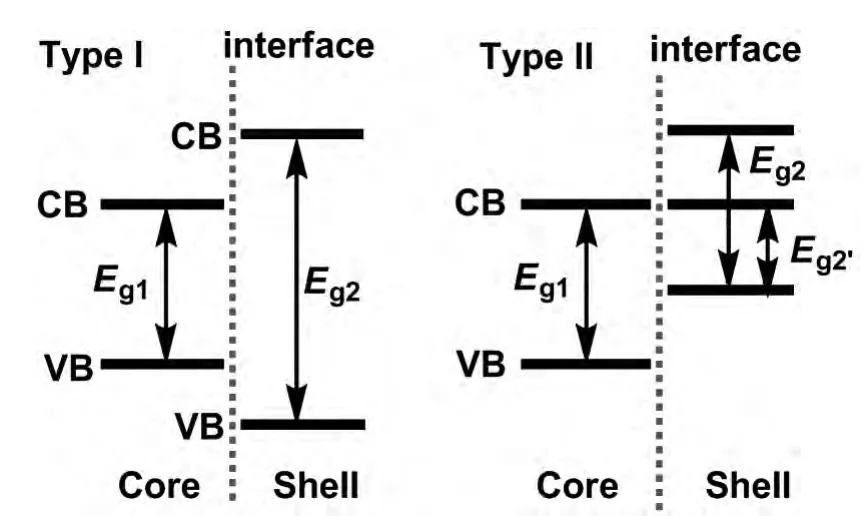
图9 两种典型的核壳型量子点能带示意图:带隙更宽的壳层(TypeⅠ)v.s.带隙更窄的壳层(TypeⅡ)Fig.9 Two types of core/shell QDS:shell with wider band gaps in TypeⅠ;shell with narrower band gaps in TypeⅡ
2.3 顺磁效应或电子自旋交换猝灭
一氧化氮和氧分子,包括有机的稳定自由基都是顺磁性物种,也是适度的电子受体,与有机分子能形成碰撞络合物,或许借助介于类似内、外重原子效应的过程,增加非辐射的S1→T1系间窜越速率kISC或辐射与非辐射的T1→S0跃迁速率,从而引起荧光或磷光的增强或猝灭[75]。顺磁性组分引起荧光猝灭的自旋交换机制可以表示如下[76]:
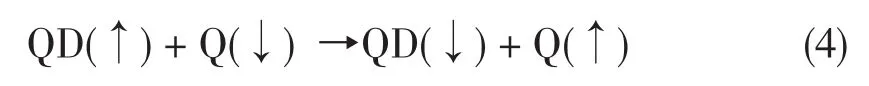
式中QD表示量子点,Q表示自由基猝灭剂,箭头表示自旋电子及其状态。然而,在许多情况下,自由基与量子点间电子转移也应该是一种重要途径[77~78]。实际上,就是电子自旋交换转移。
顺磁性金属离子如Fe2+(d6)、Co2+(d7)和Cu2+(d9)等,对荧光的猝灭机理,可能也是通过增加kISC(S1-T1)而实现的[79~81]。 同样可以通过增加非辐射的kISC(T1-S0)而实现磷光猝灭。当然,顺磁性金属离子对荧光猝灭作用的选择性还可能与荧光受体基团具体的螯合过程有关。
针对量子点发光猝灭或增强的以上三个方面,在此剖析一些具体例子。由于纳米粒子具有较多的表面缺陷,如在其外表面包覆带隙比其本身带隙大的材料,将能有效地消除表面缺陷,使荧光增强;反之,则使荧光猝灭。如汪乐余等[82]报道,在 pH=11.5的 CdS纳米溶胶中,加入 Cd2+可在CdS纳米粒子的表面形成一层Cd(OH)2,因Cd(OH)2的带隙较CdS大,因而荧光增强。而加入Cu2+,则在CdS纳米粒子的外表面包覆了一层Cu(OH)2,因Cu(OH)2的带隙较CdS小,因而荧光猝灭。当然,这些猜测仍然需要更多的实验证据去确认。
多聚磷酸、L-半胱氨酸(L-cysteine)和巯基甘油修饰的 QDs的粒径分别是 5、3和 3.5 nm[83]。对应的荧光峰值是650、460和560 nm。多聚磷酸(Polyphosphate)稳定的CdS量子点,对所有 M+和M2+敏感,没有选择性;L-半胱氨酸修饰的CdS量子点仅对Zn2+有响应,增强发光;所谓的表面态的钝化(activation of surface states)应该是前面提到的宽禁带作用。而Cu2+和Fe3+引起α-硫代甘油(Thioglycerol)修饰的CdS量子点发光猝灭。推测Cu2+被还原为Cu+。CdS量子点表面CdS+-Cu+组分,其能级低于CdS本身的能级,为窄带隙材料,导致CdS量子点的荧光猝灭且发光红移。Fe3+猝灭归于内滤效应,可借助形成FeF63-而掩蔽。
Aiexv等[84]推测,当Cu2+离子接近CdS量子点表面时,会被迅速地还原为一价Cu+离子,阻断激子复合。同时,吸附或键合在量子点表面的Cu+离子形成CuxS(x=1,2)层,引起表面电荷密度的变化,影响激子能级,从而在荧光猝灭的同时,还会使得量子点的发射峰发生红移。
Li等[85]观察到,Zn2+增强半胱胺酸包裹的CdTe 量子点和量子棒(Q-Rods)发光,而 Mg2+、Mn2+、Ni2+、Co2+等猝灭其发光。Zn2+离子与 CdTe 量子点之间的作用附合Langmuir吸附模式,Co2+离子对CdTe量子点荧光的猝灭作用符合Stern-Volmer方程模式。虽然该文没有讨论机理,但仍然可以推测,Zn2+的作用导致形成宽禁带的保护或钝化层。其他离子则属于顺磁性的猝灭。Cd2+增强左旋肉碱(L-carnitine)修饰的CdSe/ZnS核壳量子点位于550 nm的发光。量子点的左旋肉碱层是 铵 基 ,带 正 电 荷[86]。 “S–-Ag+”吸附在 L-cysteine-CdS表面,形成CdS/AgS类壳层结构,可以认为是宽带隙层,使原发光中心更有效,增强发光,并形成新的发光中心[87]。
在柠檬酸(citric acid)缓冲液中,Ag+引起巯基乙酸修饰的CdSe量子点荧光猝灭[74]。同时,在更长的波长范围产生新的宽带发光谱。由于更强的亲合作用,Ag+部分取代量子点表面的Cd2+,在CdSe量子点表面形成超细的Ag2Se颗粒。一方面,表面状态的变化,加速非辐射的e--h+重组,引起543 nm处发光猝灭;而另一方面,Ag2Se颗粒作为新的发光中心,由于尺寸分布较宽,发光带也较宽,处于625~650 nm。反应原理为:
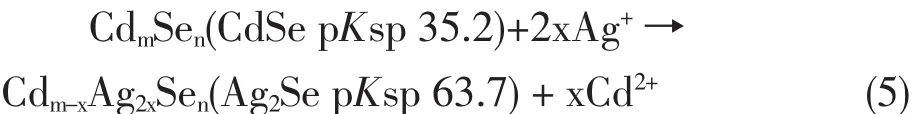
Fe3+和Cu2+应属于同一类型猝灭机理,而Ag+和Hg2+等离子可能为另一类型猝灭机理。Maria Teresa等[88]采用以2-巯基乙酸进行表面处理过的CdSe量子点测定Cu2+,结果显示共存离子Na+、K+、Ca2+、Mg2+、Zn2+、Mn2+和 Co2+对测定不产生干扰;Fe3+离子的干扰可加入NaF使其形成FeF63-去除;而Ag+和Hg2+离子将会影响测定结果。但是由Ag+和Hg2+离子产生的荧光猝灭信号远小于Cu2+离子,只要Ag+和Hg2+离子的浓度不高于1 mg/mL,Ag+和Hg2+离子的干扰可以忽略,就能实现高灵敏度、高选择性测量溶液中的Cu2+。
Li等[89]观察到,Hg2+选择性猝灭以硫化杯芳烃包裹的CdSe/ZnS量子点荧光,检出限达15 nmol/L。猝灭中,荧光峰红移,长波长处荧光曲线飘高。 而 Mg2+、Ca2+、Cu2+、Zn2+、Mn2+、Co2+、Ni2+等离子影响非常弱。作者按照软硬酸碱理论解释猝灭机理,即软酸Hg2+离子和软碱硫的结合力最大。如图10所示,实际上就是硫配体向Hg2+转移电荷,导致S:→Zn2+的配位解离,量子点表面电荷密度变化,引起荧光猝灭,且红移。
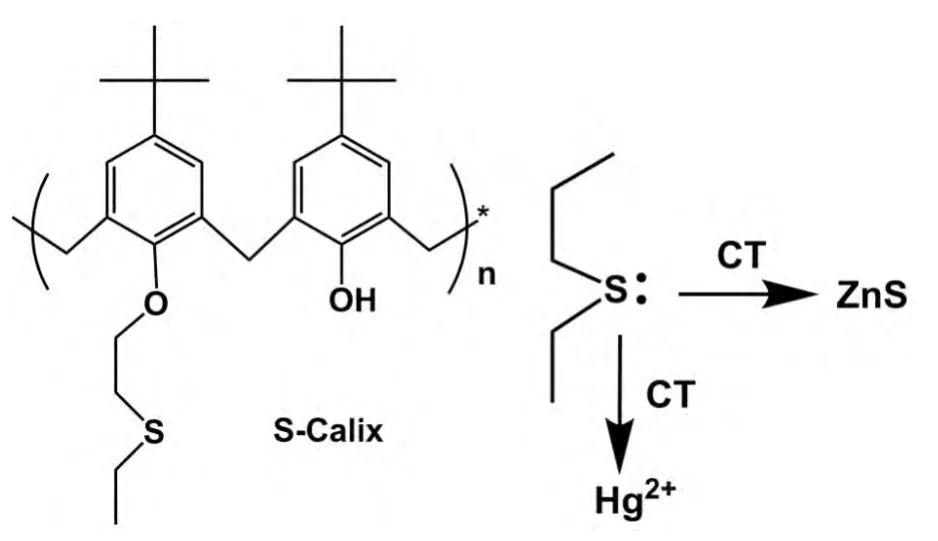
图10 硫配体电荷转向Hg2+,导致S:→Zn2+的配位解离Fig.10 Dissociation of S:→Zn2+coordination due to stronger S:→Hg2+charge transfer
金属Pb2+离子引起的荧光猝灭与硫的相对键合强度相关[90],Pb-S 的 Ksp值是3×10-7,低于Zn-S(2×10-4)和 Cd-S(8×10-7),因此 Pb2+离子的加入,导致QDs的外层配体被取代脱落,如图11所示,QDs聚沉,荧光猝灭,检出限:20 nmol/L。

图11 Pb2+和Cd2+配体交换示意图Fig.11 Coordination exchange between Pb2+and Cd2+
Ag+增强L-半胱氨酸修饰的CdS量子点荧光,而 Cu(Ⅱ),Hg(Ⅱ),Co(Ⅱ),Ni(Ⅱ)猝灭其发光,Hg2+的猝灭最显著。作者提出了如下的表面取代作用(化学式似乎不平衡,原文如此)[91]。
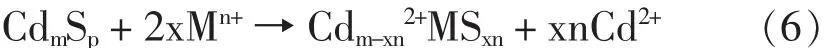
由硫化物的Ksp可见,上述取代是可能的。
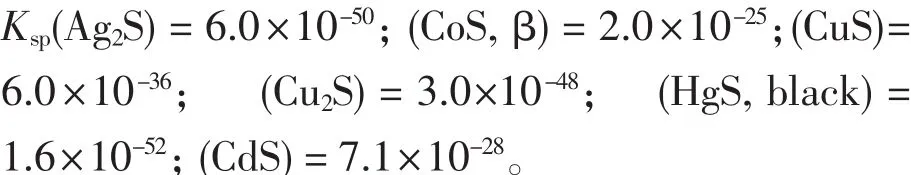
图12表明,只有当Hg2+离子和I-离子共存时才能猝灭三乙醇胺修饰的CdSe量子点荧光[92]。这种独特的猝灭行为可用于选择性和灵敏的测定Hg2+离子和I-离子,这是第一例利用量子点互易地识别阴、阳离子的报道。实验表明,I-离子是Hg2+离子与QDs之间电荷转移的桥梁,Hg2+与I-离子形成稳定的络合物并通过静电作用结合在量子点表面,进而从量子点到汞离子发生有效的电子转移,导致量子点的荧光猝灭。如此高选择性的原因是,Hg2+离子和I-离子具有最大的累计稳定常数,阴离子辅助转移Hg2+离子。如图13所示,随着汞离子的加入,QDs的荧光寿命显著下降,这证明猝灭至少部分是动态的,电荷转移过程是存在的。
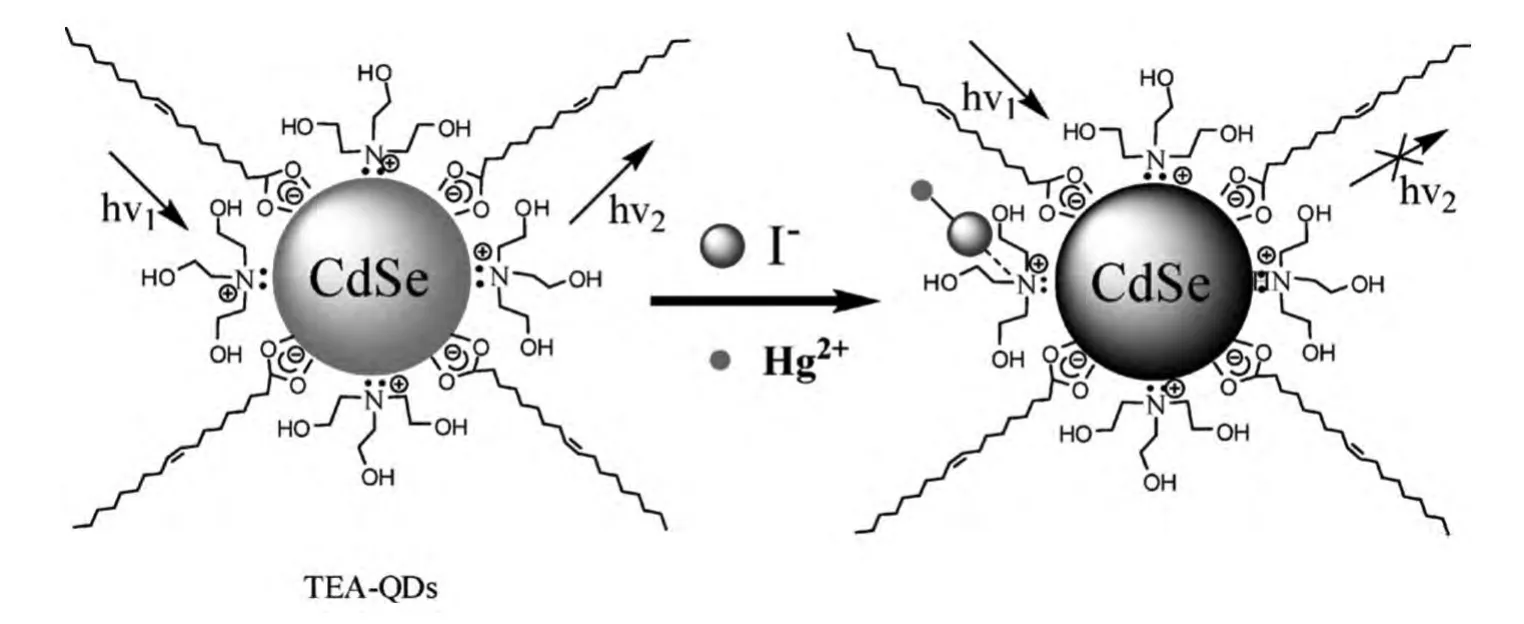
图12 Hg2+和I-离子与QDs相互作用的示意图Fig.12 Schematic illustration of the interactions between TEA-CdSe QDs and Hg2+·I-
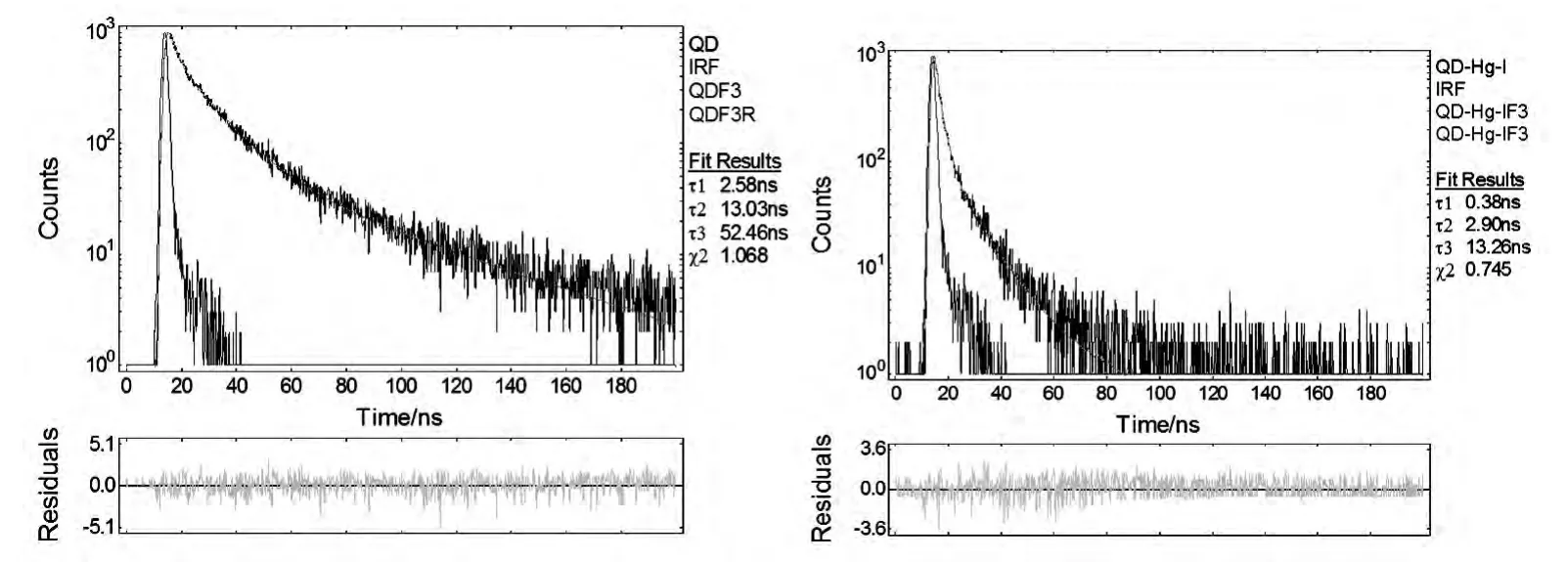
图13 Hg2+和I-离子引起QDs荧光衰减曲线变化(左:QDs;右:同时加入Hg2+和I-离子后)Fig.13 Decay curves of QDs fluorescence by pairing Hg2+and I-ions
3-巯基丙酸(3-MPA)修饰的ZnS掺Mn量子点对金属离子的响应特性:Cd2+增强磷光,而其它试验过的金属离子均猝灭磷光,猝灭的速率常数 (kq L·mol-1·s-1) 如下,Cd2+,-0.097×106;Co2+,6.12×106;Pb2+,2.76×106;Cu2+,0.1×106。钴离子和铅离子表现最显著的猝灭作用,而Cu2+离子猝灭作用稍弱,其他金属离子的猝灭作用更弱。然而,所有试验过金属离子对L-Cystein修饰的ZnS掺Mn量子点均表现为猝灭作用,几种猝灭速率常数较大的金属离子为, Hg2+, 39.4×106;Co2+,15.5×106;Cu2+,11.0×106;Pb2+,6.5×106[18]。
谢剑炜等[19]观察到,铅离子猝灭L-Cystein修饰的Mn掺杂ZnS量子点磷光。推测,LCysteine羧基先与表面发强磷光的Mn2+静电结合,而加入的Pb2+与羧基键合作用强于Mn2+,而将表面结合的Mn2+替换下来,重新占据一定的电子或空穴,使磷光猝灭。
Hg2+离子可以选择性的猝灭由柚子皮作为碳源制备的碳点的荧光[66]。并且当更强的Hg2+螯合剂-半胱氨酸加入时,Hg2+会脱离碳纳米粒子表面使其荧光恢复。作者推测,Hg2+可通过电子或能量转移使碳纳米粒子发生荧光猝灭。实际上,如果通过电子转移猝灭荧光,那么Hg2+被还原为低价,这时加入半胱氨酸也恐难恢复发光。所以,笔者推测,极大的可能性是重原子效应引起的猝灭。即,Hg2+仅络合在碳点表面,并无价态变化。所以,当加入更强的配位剂时,Hg2+可以通过竞争性配位而远离碳点表面,脱离有效的重原子效应范围。
Liu等[93]利用碳点-罗丹明B硅胶球建立比率型传感器,Cu2+选择性地猝灭硅胶球外面碳点的荧光,而内部罗丹明B的荧光不受其影响。
除了金属阳离子,利用发光量子点或其他纳米材料建立阴离子传感体系也是非常有意义的,氰根(cyanide)检测可以作为典型。如图14所示,Jin等[94]首次考察了利用CdSe量子点荧光猝灭灵敏检测阴离子氰根的可行性,氰根通过捕获空穴而阻止激子复合,量子点的荧光寿命随氰根浓度的增加而缩短,具有单指数衰减特征。
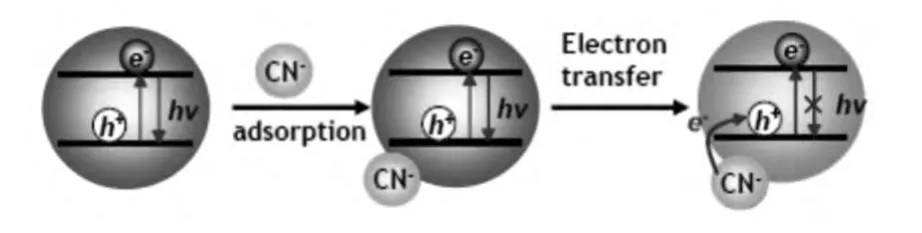
图14 CdSe量子点检测CN-机制示意图Fig.14 The response mechanism of CN-quenching fluorescence of CdSe QDts
2008年,Hall等[95]采用 CdSe/ZnS量子点实现氯离子传感。量子点外层配体为3-巯基丙酸和光泽精(lucigenin),荧光峰位置是500,540和620 nm。随着氯离子浓度的增加,位于540 nm的发光减弱,而位于620 nm的发光减弱增强,对氯离子的检出限为0.29 mmol/L。
Yan等[96]通过图15证明,NO通过如下两步猝灭三乙醇胺(TEA)修饰的CdSe量子点发光。第一,消耗量子点表面吸附的氧分子,改变了量子点表面状态,俘获激子引起发光高效猝灭;进一步自身吸附于量子点表面,通过电子自旋交换转移猝灭发光。
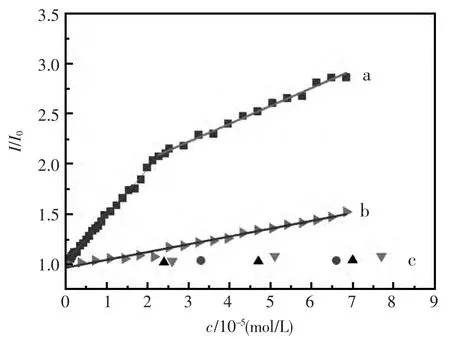
图15 一氧化氮猝灭三乙醇胺修饰的CdSe量子点荧光的Stern–Volmer曲线Fig.15 Stern–Volmer quenching plot of TEA-CdSe-QDs with increasing concentration of NO(a).non-deoxygenated solution;(b).deoxygenated solution purged with N2;(c).Effect of increasing concentrations of NO3-,NO2-and 4-hydrogen-TEMPO on the luminescence of TEA-CdSe-QDs
Shi等[97]率先实现了利用CdSe量子点识别硝基甲苯类爆炸物。如图16所示,推测目标物穿过量子点表面的十八烯酸(oleic acid)层,通过捕获电子引起发光猝灭,检出限TNT:3.12×10-9mol/L (0.71 ng/mL); DNT: 5.10×10-9mol/L(0.93 ng/mL)。
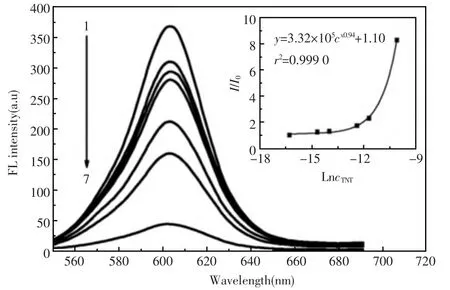
图16 TNT对CdSe量子点荧光的猝灭光谱Fig.16 Fluorescence quenching spectra of CdSe QDs with increasing concentration of TNT(The concentration,c,of quenchers represents,respectively,from no.1 to 7:0.0,8.0×10-8,4.0×10-7,8.0×10-7,4.0×10-6,8.0×10-6,4.0×10-5 mol/L;Y and x represent I0/I and lnc,respectively,in insets and I and I0are the fluorescence intensity of QDs in the presence and in the absence of quencher,respectively.)
Yan 等[30]观察到,抗坏血酸(ascorbic acid)能够萃取Mn掺杂ZnS量子点表面的Mn2+和Zn2+,产生更多的空穴并被Mn2+俘获,进而产生Mn3+。而抗坏血酸又能还原Mn3+到Mn2+,并产生激发态Mn2+,因此增强了Mn2+离子磷光。基于此建立了抗坏血酸的分析方法。
如图17所示,三聚氰胺(melamine)吸附于DNA包覆的银纳米簇(DNA-Ag NCs)表面,使得簇表面状态更加完整,发光增强,从而建立了痕量三聚氰胺的检测方法[98]。
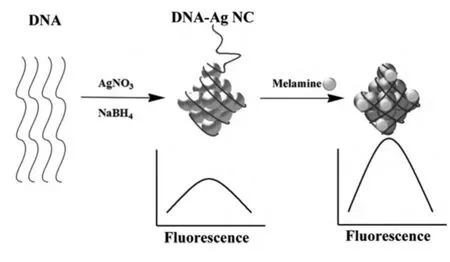
图17 利用银纳米簇发光增强检测三聚氰胺示意图Fig.17 Determining principle of melamine by enhancing Ag-cluster fluorescence
利用发光的金纳米簇 (AuNCs@GSH)检测ATP非常简便。Fe3+首先选择性的猝灭金纳米簇的荧光。而Fe3+与磷酸基的高亲合络合作用也是选择性的,在磷酸盐或ATP的存在下,发光得以恢复,检测原理如图18所示[99]。
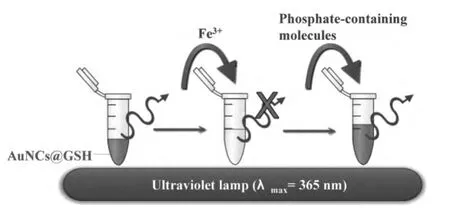
图18 利用发光的金纳米簇(AuNsC@GSH)检测ATP原理示意图Fig.18 Determining principle of ATP by enhancing AuNsC@GSH fluorescence
2.4 偶极-偶极相互作用或其它途径引起的荧光猝灭
Förster共振能量转移(FRET)是引起供体荧光猝灭的一种重要途径,通常发生在10到100 Å的距离范围,因此又叫做长程能量转移(long range ET)。Förster共振能量转移荧光猝灭现象被广泛地应用于化学或生物传感设计中。有机的荧光染料分子间,或其与生物大分子间的这种能量转移可以通过偶极-偶极作用机制得到非常好的理解[100~101]。然而,纳米粒子之间,或纳米粒子与有机的荧光染料或生物大分子间的荧光猝灭现象是否适合偶极-偶极作用机制一直是一个争议的课题。一般来讲,纳米粒子也可以看作一个偶极振荡子,因此偶极-偶极作用机制也是适用的[102~104]。但是,虽然同属于偶极-偶极作用,有机染料分子作为能量供体与金纳米粒子的FRET,与有机染料分子间的FRET有所不同。金纳米粒子作为能量受体,在其表面属于各向同性的偶极向量分布,从而可以接受来自于给体的能量。FRET转移效率高,而且转移效率与距离的关系从正比于1/R6到正比于1/R4都有可能[105~107]。
目前,经常令人生疑的是,基于量子点或纳米材料体系的能量转移的距离可能远大于偶极-偶极作用机制的极限距离,比如在70~100 nm(700-1000 Å)的程度上发生[105]。 其实,纳米材料,尤其金属量子点/簇也许会通过新的途径,比如等离子体基元/波(plasma)-偶极作用,从而在更远的距离上发生无辐射的能量转移,值得探索。还有,如果供受体间发生比偶极-偶极相互作用更强的激子耦合时,电子转移速率也会从1/R6依赖性变化到1/R3依赖性。
借助Förster能量转移途径设计离子化学传感的一种体系如图19所示,利用15-Crown-5衍生物分别修饰绿色的和红色的量子点,在K+离子存在下形成 “绿色量子点-15-crown-5/K+/15-crown-5-红色量子点”三明治型络合物,两个量子点的空间距离大约~26 Å,处于Förster能量转移范围之内,在430 nm激发光下,发生由绿色荧光体向红色荧光体的能量转移,此消彼涨[108]。
2.5 亲金(Aurophilicity)/亲金属(metallophilicity)作用
闭壳层的金属离子之间具有强的专属性的色散相互作用,形成所谓的亲金键,或亲金属键,键合能大约7~12 kcal/mol[109]。尤其重金属离子之间更倾向于这种作用[110~112],Au+(4f145d10)和 Au+之间的作用是最强的[109,113],其他如Hg2+(4f145d10)和 Au+,Hg(Ⅱ)和 Pt(Ⅱ),Hg(Ⅱ)和 Pd(Ⅱ),Ag+(3d10)和 Au+,Cu+(3d10)和 Ag+等[111]。
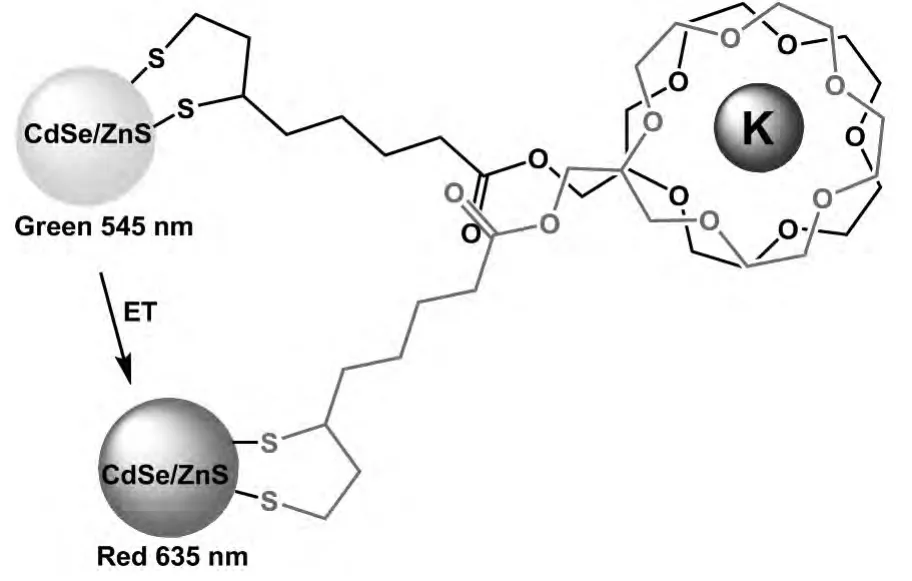
图19 绿色和红色量子点间Förster能量转移示意图Fig.19 Förster RET between green and red QDs
如图20所示,由25个金原子组成的金纳米晶体/簇,发射最大位于640 nm的红色荧光。表面少量的Au+(~17%)增强了该簇的稳定性,而正是这些少量的Au+离子与Hg2+强的专属性的相互作用,使得金簇的荧光猝灭,从而建立Hg2+的荧光传感器[37]。
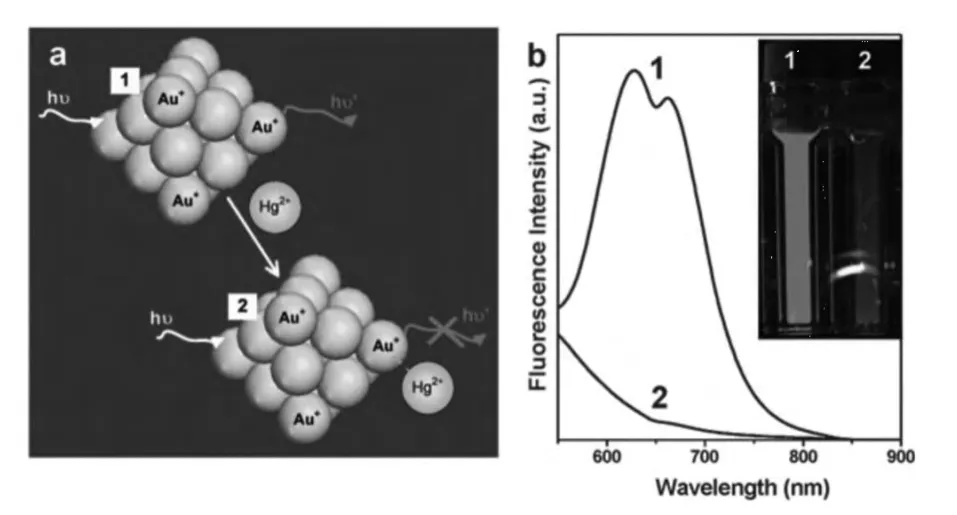
图20 (a)高亲和性的Hg2+–Au+亲金属键(b)发射光谱(插图 为金纳米簇悬浮液加入汞离子前后发光变化的照片)Fig.20 (a)high-affinity metallophilic Hg2+–Au+bonds(b)emission spectra(λex=470 nm)and(inset)photographs under UV light(354 nm)of Au NCs(20 mmol/L)in the(1)absence and(2)presence of Hg2+ions(50 mmol/L).
3 结论
发光量子点在化学传感方面的确具有许多独到之处。量子点的类型、表面状态和配体的特点决定了选择性。当涉及相同配位原子时,有的对Hg2+有选择性,而有的对Pb2+或其它离子有选择性。所以,量子点表面的配体在决定对金属离子或其它待测组分的选择性方面发挥着重要的作用。在响应机理方面,除了与有机荧光染料有许多相似之处外,纳米材料也有其自身的特点。然而,当触及响应机理时,大多以推测为主,证据欠充分。今后,应该在机理的求证方面给予更多思考。另外,新型发光量子点的开发也是化学传感值得研究的领域。
[1]Brus L E.Electron-electron and electron-hole interactions in small semi-conductor crystallites:The size dependence of the lowest excited electronic state[J].J.Chem.Phys.,1984,80:4 403~4 409.
[2]KayanumaY.Quantum-size effects of interacting electrons and holes in semiconductor microcrystals with spherical shape[J].Phys.Rev.B.,1988,38:9 797~9 805.
[3]Wang Y,Herron N.Nanometer-sized semiconductor clusters:materials synthesis,quantum size effects and photophysical properties[J].J.Phys.Chem.,1991,95:525~532.
[4]Hines M A,Guyot-Sionnest P.Synthesis and Characterization of Strongly Luminescing ZnS-Capped CdSe Nanocrystals[J].J.Phys.Chem.,1996,100:468~471.
[5]Yang W D,Manna L,Wang L W,et al.Linearly Polarized Emission from Colloidal Semiconductor Quantum Rods[J].Science,2001,292(5524):2 060~2 063.
[6]Zhang X,Li L,Dong X,et al.Luminescence properties of Cu and Cu,Al doped ZnS quantum dots[C].Proc.SPIE 6782,Optoelectronic Materials and DevicesⅡ,67822Ⅰ(Nov.19,2007).
[7]Corrado C,Hawker M,Livingston G,et al.Enhanced Cu emission in ZnS:Cu,Cl/ZnS core-shell nanocrystals[J].Nanoscale,2010,2:1 213~1 221.
[8]Liu S Y,Su X G.The synthesis and application of doped semiconductor Nanocrystals[J].Anal.Methods,2013,5:4 541~4 548.
[9]Schwartz D A,Norberg N S,Nguyen Q P,et al.Magnetic Quantum Dots:Synthesis,Spectroscopy,and Magnetismof Co2+-and Ni2+-Doped ZnO Nanocrystals[J].J.Am.Chem.Soc.,2003,125:13 205~13 218.
[10]Lommens P,Loncke F,Smet P F,et al.Dopant Incorporation in Colloidal Quantum Dots:A Case Study on Co2+Doped ZnO[J].Chem.Mater.,2007,19:5 576~5 583.
[11]Zhang J J,Yu P,Chen S Y,et al.Doping-induced emission of infrared light from Co2+-doped ZnSe quantum dots[J].Res.Chem.Intermed.,2011,37:383~388.
[12]Tsai T Y,Birnbaum M.Characteristics of Co2+:ZnS saturable absorber Q-switched neodymium lasers at 1.3 μm[J].J.Appl.Phys.,2001,89:2 006~2 012.
[13]Zou W S,Qiao J Q,Hu X,et al.Synthesis in aqueous solution and characterisation of a new cobalt-doped ZnS quantum dot as a hybrid ratiometric chemosensor[J].Anal.Chim.Acta.,2011,708,134~140.
[14]Murugadoss G,Kumar M R.Synthesis and optical properties of monodispersed Ni2+-doped ZnS nanoparticles[J].Appl.Nanosci.,2014,4:67~75.
[15]Pang P,Lu M,Xu D,et al.Luminescence characteristics of ZnS nanoparticles co-doped with Ni2+and Mn2+[J].Opt.Mater.,2003,24:497~502.
[16]Yang P,Lu M K,Xu D,et al.Strong Green Luminescence of Ni2+-Doped ZnS Nanocrystals[J].Appl.Phys.A,2002,74:257~259.
[17]He Y,Wang H F,Yan X P.Exploring Mn-Doped ZnS Quantum Dots for the Room-Temperature Phosphorescence Detection of Enoxacinin Biological Fluids[J].Anal.Chem.,2008,80:3 832~3 837.
[18]段玉娇,李文婷,申前进,等.ZnS掺Mn磷光量子点对金属离子传感机理的探讨 [J].化学传感器,2011,31(2):26~32.
[19]陈娟,孙洁芳,郭磊,等.锰掺杂硫化锌量子点室温磷光检测铅离子[J].分析化学,2012,40(11):1 680~1 685.
[20]Zou W S,Dong S,Ge X,et al.Room-Temperature Phosphorescence Chemosensorand Rayleigh Scattering Chemodosimeter Dual-Recognition Probe for 2,4,6-Trinitrotoluene Based on Manganese-Doped ZnS Quantum Dots[J].Anal.Chem.,2011,83:30~37.
[21]Wang H F,Li Y,Wu Y Y,et al.Ascorbic Acid Induced Enhancement of Room Temperature Phosphorescence of Sodium Tripolyphosphate-Capped Mn-Doped ZnS Quantum Dots:Mechanism and Bioprobe Applications[J].Chem.Eur.J.,2010,16:12 988~12 994.
[22]He Y,Wang H F,Yan X P.Self-Assembly of Mn-Doped ZnS Quantum Dots/Octa (3-aminopropyl)octasilsequioxane Octahydrochloride Nanohybrids for Optosensing DNA[J].Chem.Eur.J.,2009,15(22):5 436~5 440.
[23]Irvine S E,Staudt T,Rittweger E,et al.Direct lightdriven modulation of luminescence from Mn-doped ZnSe quantum dots[J].Angew Chem.Int Ed.,2008,47:1~5.
[24]Pradhan N,Battaglia D M,Liu Y,et al.Efficient,stable,small,and water-soluble doped ZnSe nanocrystal emitters as non-cadmium biomedical labels[J].Nano Lett.,2007,7:312~317.
[25]Ehlert O,Osvet A,Batentschuk M,et al.Synthesis and spectroscopic investigations of Cu-and Pb-doped colloidal ZnS nanocrystals[J].J.Phys.Chem.B,2006,110:23 175~23 178.
[26]Srivastava B B,Jana S,Pradhan N.Doping Cu in semiconductor nanocrystals:some old and some new physical insights[J].J.Am.Chem.Soc.,2011,133,1 007~1 015.
[27]Xie R,Peng X.Synthesis of Cu-doped InP nanocrystals(d-dots)with ZnSe diffusion barrier as efficient and color-tunable NIR emitters[J].J.Am.Chem.Soc.,2009,131(30):10 645~10 651.
[28]Shen Q,Liu Y,Xu J,et al.Microwave induced centerdoping of silver ions in aqueous CdS nanocrystals with tunable,impurity and visible emission[J].Chem.Commun.,2010,46:5 701~5 703.
[29]Chung J H,Ah C S,Jang D J.Formation and distinctive decay times of surface-and lattice-bound Mn2+impurity luminescence in ZnS Nanoparticles[J].J.Phys.Chem.B,2001,105:4 128~4 132.
[30]Willets K A,Yan Duyne R P.Localized surface plasmon resonance spectroscopy and sensing[J].Annu.Rev.Phys.Chem.,2007,58:267~297.
[31]Pan S,Rothberg L J.Enhancement of platinum octaethyl porphyrin phosphorescence near nanotextured silver surfaces[J].J.Am.Chem.Soc.,2005,127:6 087~6 094.
[32]Zhang J,Fu Y,Liang D,et al.Single-cell fluorescence imaging using metal plasmon-coupled probe 2:singlemolecule counting on lifetime image[J].Nano letters,2008,8:1 179~1 186.
[33]Zhang J,Fu Y,Chowdhury M H,et al.Metal-enhanced single-molecule fluorescence on silver particle monomer and dimer:coupling effect between metal particles[J].Nano Lett.,2007,7:2 101~2 107.
[34]Graham D,Goodacre R.Chemical and bioanalytical applications of surface enhanced Raman scattering spectroscopy[J].Chem.Soc.Rev.,2008,37:883~883.
[35]La S,Grady N K,Kundu J,et al.Tailoring plasmonic substrates for surface enhanced spectroscopies[J].Chem.Soc.Rev.,2008,37:898~911.
[36]Huang C C,Yang Z,Lee K H,et al.Synthesis of highly fluorescent gold nanoparticles for sensing mercury(Ⅱ)[J].Angew Chem.Int.Ed.,2007,46:6 824~6 828.
[37]Xie J P,Zheng Y,Ying J Y.Highly selective and ultrasensitive detection of Hg2+based on fluorescence quenching of Au nanoclusters by Hg2+–Au+interactions[J].Chem.Commun.,2010,46:961~963.
[38]Zheng J,Nicovich P R,Dickson R M.Highly fluorescent noble-metal quantum dots[J].Annu.Rev.Phys.Chem.,2007,58:409~431.
[39]Miller S A,Womick J M,Parker J F,et al.Femtosecond relaxation dynamics of Au25L18-monolayer-protected clusters[J].J.Phys.Chem.C.,2009,113:9 440~9 444.
[40]Wang G,Huang T,Murray R W,et al.Near-IR luminescence of monolayer-protected metal clusters[J].J.Am.Soc.Chem.,2005,127:812~813.
[41]Shang L,Azadfar N,Stockmar F,et al.One-pot synthesis of near-infrared fluorescent gold clusters for cellular fluorescence lifetime imaging[J].Small.,2011,7:2 614 ~2 620.
[42]Yuan X,Setyawati M I,Tan S A,et al.Highly luminescent silver nanoclusters with tunable emissions:cyclic reduction–decomposition synthesis and antimicrobial properties[J].NPG Asia Materials,2013,5:e39.
[43]Shang L,Dong S,Nienhaus G U.Ultra-small fluorescent metal nanoclusters:synthesis and biological applications[J].Nano Today.,2011,6:401~418.
[44]Yeh H C,Sharma J,Han J J,et al.A DNA-silver nanocluster probe that fluoresces upon hybridization[J].Nano Lett.,2010,10:3 106~3 110.
[45]Guo W,Yuan J,Dong Q,et al.Highly sequence-dependent formation of fluorescent silver nanoclusters in hybridized DNA duplexes for single nucleotide mutation identification[J].J.Am.Chem.Soc.,2009,132:932 ~934.
[46]Yang S W,Vosch T.Rapid detection of microrna by a silver nanocluster DNA probe[J].Anal.Chem.,2011,83:6 935~6 939.
[47]Yu J,Choi S,Dickson R M.Shuttle-based fluorogenic silver-cluster biolabels[J].Angew.Chem.Int.Ed.,2009,48:318~320.
[48]Fu Y,Lakowicz J r.Enhanced fluorescence of Cy5-labeled oligonucleotides near silver island films:a distance effect study using single molecule spectroscopy[J].J.Phys.Chem.B,2006,110(45):22 557~22 562.
[49]Liu P P,Na N,Huang L Y,et al.The Application of amine-terminated silicon quantum dots on the imaging of human serum proteins after PAGE[J].Chem.Eur.J.,2012,18:1 438~1 443.
[50]Sudeep P K,Emrick T.Functional Si and CdSe quantum dots:synthesis,conjugate formation,and photoluminescence quenching by surface interactions[J].ACS Nano,2009,3:4 105~4 109.
[51]Rosso-Vasic M,Spruijt E,Lagen B van,et al.Alkylfunctionalized oxide-free silicon nanoparticles:synthesis and optical properties[J].Small.,2008,4:1 835~1 841.
[52]Warner J H,Hoshino A,Yamamoto K,et al.Water-soluble photoluminescent silicon quantum dots[J].Angew.Chem.,2005,117:4 626 ~4 630.or Angew.Chem.Int.Ed.,2005,44:4 550~4 554.
[53]Zhang Y,Han X,Zhang J,et al.Photoluminescence of silicon quantum dots in nanospheres[J].Nanoscale,2012,4:7 760~7 765.
[54]Kang Z H,sang C H A T,Zhang Z D,et al.A polyoxometalate-assisted electrochemical method for silicon nanostructures preparation:from quantum dots to nanowires[J].J.Am.Chem.Soc.,2007,129:5 326~5 327.
[55]Erogbogbo F,Yong K T,Roy I,et al.Biocompatible luminescent silicon quantum dots for imaging of cancer cells[J].ACS Nano.,2008.2(5):873~878.
[56]Li X,He Y,Talukdar S S,et al.Process for preparing macroscopic quantities of brightly photoluminescent silicon nanoparticles with emission spanning the visible spectrum[J].Langmuir.,2003,19:8 490~8 496.
[57]Sun Y P,Zhou B,Lin Y,et al.Quantum-sized carbon dots for bright and colorful photoluminescence[J].J.Am.Chem.Soc.,2006,128:7 756~7 757.
[58]Liu H,Ye T,Mao C.Fluorescent carbon nanoparticles derived from candle soot[J].Angew.Chem.,Int.Ed.,2007,46:6 473~6 475.
[59]Huang H,Lv J J,Zhou D L,et al.One-pot green synthesis of nitrogen-doped carbon nanoparticles as fluorescent probes for mercury ions[J].RSC Adv.,2013,3:21 691~21 696.
[60]Huang H,Xu Y,Tang C J,et al.Facile and green synthesis of photoluminescent carbon nanoparticles for cellular imaging[J].New J.Chem.,2014,38:784~789.
[61]Liu S,Tian J,Wang L,et al.Hydrothermal treatment of grass:a low-cost,green route to nitrogen-doped,carbonrich,photoluminescent polymer nanodots as an effective fluorescent sensing platform for label-free detection of Cu(Ⅱ)ions[J].Adv.Mater.,2012,24:2 037~2 041.
[62]Zhu C,Zhai J,Dong S.Bifunctional fluorescent carbonnanodots:green synthesis via soy milk and application as metal-free electrocatalysts for oxygen reduction[J].Chem.Commun.,2012,48:9 367~9 369.
[63]Li W,Zhang Z,Kong B,et al.Simple and green synthesis ofnitrogen-doped photoluminescentcarbonaceous nanospheres for bioimaging[J].Angew.Chem.,Int.Ed.,2013,52:1~6.
[64]Prasannan A,Imae T.One-pot synthesis of fluorescent carbon dots from orange waste peels[J].Ind.Eng.Chem.Res.,2013,52:15 673~15 678.
[65]Mewada A,Pandey S,Shinde S,et al.Green synthesis of biocompatible carbon dots using aqueous extract of T.bispinosa peel[J].Mater Sci.Eng C.,2013,33(5):2 914~2 917.
[66]Lu W,Qin X,Liu S,et al.Economical,green synthesis of fluorescent carbon nanoparticles and their use as probes for sensitive and selective detection of mercury(Ⅱ)ions[J].Anal.Chem.,2012,84(12):5 351~5 357.
[67]Shen J,Zhu Y,Yang X,et al.Graphene quantum dots:emergentnanolightsfor bioimaging,sensors,catalysis and photovoltaic devices[J].Chem.Commun.,2012,48:3 686~3 699.
[68]Zhang M,Bai L,Shang W,et al.Facile synthesis of water-soluble,highly fluorescent graphene quantum dots as a robust biological label for stem cells[J].J.Mater.Chem.,2012,22:7 461~7 467.
[69]Li H T,He X D,Kang Z H,et al.Water-soluble fluorescent carbon quantum dots and photocatalyst design[J].Angew.Chem.,Int.Ed.,2010,49:4 430~4 434.
[70]Nicewarner-Peña S R,Freeman R G,Reiss B D,et al.Submicrometer metallic barcodes[J].Science,2001,294:137~141.
[71]Gooding A K,Gómez D E,Mulvaney P.The effects of electron and hole injection on the photoluminescence of CdSe/CdS/ZnS nanocrystal monolayers[J].ACS Nano,2008,2:669~676.
[72]Bao H,Gong Y,Li Z,et al.Enhancement effect of illumination on the photoluminescence of water-soluble CdTe nanocrystals:toward highly fluorescent CdTe/CdS coreshell structure[J].Chem.Mater.,2004,16:3 853~3 859.
[73]Kim S,Fisher B,Eisler H J,et al.Type-II quantum dots:CdTe/CdSe(core/shell)and CdSe/ZnTe(Core/Shell)heterostructures[J].J.Am.Chem.Soc.,2003,125:11 466~11 467.
[74]Liang J G,Ai X P,He Z K,et al.Functionalized CdSe quantum dots as selective silver ion chemodosimeter[J].Analyst,2004,129:619~622.
[75]Vo-Dinh T.Room Temperature Phosphorimetry for Chemical Analysis[M].John Wiley&Sons,New York,1984.page 32.
[76]Hof M,Hutterer R,Fidler V.Fluorescence spectroscopy in biology.advanced methods and their applications to membranes,proteins,DNA,and cells [M].(2004),‘SpringerSerieson Fluorescence,3’,Heidelberg:Springer,290,ISBN 3-540-22338-X.
[77]Scaiano J C,Laferrière M,Galian R E,et al.Non-linear effects in the quenching of fluorescent semiconductor nanoparticles by paramagnetic species[J].Stat.Sol.A,2006,203:1 337~1 343.
[78]Lin F,Pei D,He W,et al.Electron transfer quenching by nitroxide radicals of the fluorescence of carbon dots[J].J.Mater.Chem.,2012,22:11 801~11 807.
[79]Kemlo J A,Shepard T M.Quenching of excited singlet states by metal ions[J].Chem.Phys.Lett.,1977,47:158~162.
[80]Varnes A W,Dodson R B,Wehry E L.Fluorescence quenching studies[J].J.Am.Chem.Soc.,1972,94:946~950.
[81]Volchkov V V,Ivanov V L,Uzhinov B M.Induced intersystem crossing at the fluorescence quenching of laser dye 7-amino-1,3-naphthalenedisulfonic acid by paramagnetic metal ions[J].J.Fluoresc.,2010,20(1):299 ~303.
[82]汪乐余,朱英贵,朱昌青,等.硫化镉纳米荧光探针荧光猝灭法测定痕量铜[J].分析化学,2002,30(11):1 352~1 354.
[83]Chen Y F,Rosenzweig Z.Luminescent CdS quantum dots as selective ion probes[J].Anal.Chem.,2002,74:5 132~5 138.
[84]Aiexv,Isarox John,Ch Rysochoos.Surface patterns induced by Cu2+ions on BPEI/PAA layer-by-layer assembly[J].Langmuir,1997,13(12):3 142~3 146.
[85]Li J,Bao D S,Hong X,et al.Luminescent CdTe quantum dots and nanorods as metal ion probes[J].Colloids and Surfaces A:Physicochem.Eng.Aspects,2005,257-258:267~271.
[86]Li H B,Zhang Y,Wang X Q.L-Carnitine capped quantum dots as luminescent probes for cadmium ions[J].Sensors and Actuators B,2007,127:593~597.
[87]Chen J L,Zhu C Q.Functionalized cadmium sulfide quantum dots as fluorescence probe for silver ion determination[J].Anal.Chim.Acta,2005,546:147~153.
[88]Fernández-Argüelles M T,Jin W J,Costa-Fernández J M,et al.Surface-modified CdSe quantum dots for thesensitive and selective determination of Cu(Ⅱ)in aqueous solutions by luminescent measurements[J].Anal.Chim.Acta,2005,549:20~25.
[89]Li H,Zhang Y,Wang X,et al.Calixarene capped quantum dots as luminescent probes for Hg2+ions[J].Mater.Lett.,2007,61:1 474~1 477.
[90]Ali E M,Zheng Y G,Yu H H,et al.Ultrasensitive Pb2+detection by glutathione-capped quantum dots[J].Anal Chem,2007,79:9 452~9 458.
[91]Chen J L,Zheng A F,Gao Y C,et al.Functionalized CdS quantum dots-based luminescence probe for detection of heavy and transition metal ions in aqueous solution[J].Spectrochim.Acta.A.,2008,69:1 044~1 052.
[92]Shang Z B,Wang Y,Jin W J.Triethanolamine-capped CdSe quantum dots as fluorescent sensors for reciprocal recognition of mercury(Ⅱ)and iodide in aqueous solution[J].Talanta,2009,78:364~369.
[93]Liu X,Zhang N,Bing T,et al.Carbon dots based dual-emission silica Nanoparticles as a ratiometric nanosensor for Cu2+[J].Anal.Chem.,2014,86:2 289~2 296.
[94]Jin W J,Fernández-Argüelles M T,Costa-Fernández J M,et al.Photoactivated luminescent CdSe quantum dots as sensitive cyanide probes in aqueous solutions[J].Chem.Comm.,2005:883~885.
[95]Ruedas-Rama M J,Hall E A H.A quantum dot-lucigenin probe for Cl-[J].Analyst,2008,133:1 556~1 566.
[96]Yan X Q,Shang Z B,Zhang Z,et al.Fluorescence sensing of nitric oxide in aqueous solution by triethanolamine modified CdSe quantum dots[J].Luminescence,2009,24:255~259.
[97]Shi G H,Shang Z B,Wang Y,et al.Fluorescence quenching of CdSe quantum dots by nitroaromatic explosives and their relative compounds [J].Spectrochim.Acta Part A,2008,70:247~252.
[98]Han S,Zhu S,Liu Z,et al.Oligonucleotide-stabilized fluorescent silver nanoclusters for turn-on detection of melamine[J].Biosensors and Bioelectronics,2012,36:267~270.
[99]Li P H,Lin J Y,Chen C T,et al.Using gold nanoclusters as selective luminescent probes for phosphate-containing metabolites[J].Anal.Chem.,2012,84:5 484~5 488.
[100]Förster T.Intramolecular energy migration and fluorescence[J].Ann.Phys.,1948,2:55~75.
[101]Stryer L,Haugland R P.Energy transfer-a spectroscopic ruler[J].Proc.Natl.Acad.Sci.USA,1967,58:719 ~726.
[102]Medintz I L,Mattoussi H.Quantum dot-based resonance energy transfer and its growing application in biology[J].Phys.Chem.Chem.Phys.,2009,11:17~45.
[103]Medintz I L,Goldman E R,Lassman M E,et al.A fluorescence resonance energy transfer sensor based on maltose binding protein[J].Bioconjugate Chem,2003,14:909~918.
[104]Braslavsky S E,Fron E,Rodríguez H B,et al.Pitfalls and limitations in the practical use of Förster’s theory of resonance energy transfer[J].Photochem.Photobiol.Sci.,2008,7:1 444~1 448.
[105]Ray P C,Fortner A,Darbha G K.Gold nanoparticle based FRET assay for the detection of DNA cleavage[J].J.Phys.Chem.B,2006,110:20 745~20 748.
[106]Griffin J,Singh A K,Senapati D,et al.Size-and distance-dependent nanoparticle surface-energy transfer(NSET)method for selective sensing of hepatitis C virus RNA[J].Chem.Eur.J.,2009,15:342~351.
[107]Darbha G K,Ray A,Ray P C.Gold nanoparticle-based miniaturized nanomaterial surface energy transfer probe for rapid and ultrasensitive detection of mercury in soil,water,and fish[J].ACS Nano,2007,1:208~214.
[108]Chen C Y,Cheng C T,Lai C W,et al.Potassium ion recognition by 15-crown-5 functionalized CdSe/ZnS quantum dots in H2O[J].Chem.Commun.,2006,3:263~265.
[109]Schmidbaur H.The aurophilicity phenomenon:a decade of experimental findings,theoretical concepts and emerging application[J].Gold Bulletin.,2000,33(1):3~10.
[110]Pyykkö P.Theoretical chemstry of gold[J].Angew.Chem.,Int.Ed.,2004,43:4 412~4 456.
[111]Kim M,Taylor T J,Gabbai F P.Hg(Ⅱ)Pd(Ⅱ)metallophilic interactions[J].J.Am.Chem.Soc.,2008,130:6 332~6 333.
[112]Burini A,Fackler J P,Jr Galassi R,et al.Supramolecular chain assemblies formed by interaction of a molecular acid complex of mercury with-base trinuclear gold complexes[J].J.Am.Chem.Soc.,2000,122:11 264~11 265.
[113]Assadollahzadeh B,Schwerdtfege P.A comparison of metallophilic interactions in group 11 [X–M–PH3]n(n=2-3)complex halides(M=Cu,Ag,Au;X=Cl,Br,I)from density functional theory[J].Chem.Phy.Lett.,2008,462:222~228.
