琥珀酸美托洛尔的合成分析
2014-06-07彭坤王京凯李晗
彭坤 王京凯 李晗
琥珀酸美托洛尔(Metoprolol Succinate,1),化学名为(±)-1-异丙氨基-3-[4-(2-甲氧乙基)苯氧基]-2-丙醇琥珀酸盐,是英国阿斯利康公司研制的β1受体阻滞剂,新型琥珀酸美托洛尔缓释片于1986年在欧美上市,商品名为倍他乐克。琥珀酸美托洛尔的选择性是剂量依赖的,缓释片血药浓度的峰值明显低于同剂量的普通平片,使得该剂型有相对更高的β1受体选择性。美托洛尔无β受体激动作用,几乎无膜激活作用。在治疗剂量上,美托洛尔对支气管平滑肌的收缩作用弱于非选择性的β受体阻滞剂,该特性使之能与β2受体激动剂合用,治疗有支气管哮喘或其他明显的阻塞性肺病的患者。美托洛尔对胰岛素释放及糖代谢的影响小于非选择性β受体阻滞剂,因而也可用于糖尿病患者。正是由于这么多的优势,美托洛尔已迅速被广大临床医生接受,成为全球目前使用最为广泛的β受体阻滞剂,是治疗高血压、冠心病、慢性心力衰竭和心律失常的常用药物之一[1-10]。
1 材料与方法
1.1 一般资料 琥珀酸美托洛尔(1)的合成方法报道较多[11-16],综合来看主要分以下两种:一是以乙酰化的3-[4-(2-甲氧基乙基苯氧基)]-1,2-环氧丙烷为起始物料反应,最后经过催化氢化得到美托洛尔碱,再与琥珀酸反应可以得到产品[17]。本方法中的制备工艺虽然较简单,只需一步反应即可得到美托洛尔碱,但起始物料1,2-环氧-3-[4-(1-乙酰基-2-甲氧基乙基苯氧基)]-丙烷无法直接购得,需要自制。二是以对甲氧基乙基苯酚为起始物料,通过与环氧氯丙烷、异丙胺、琥珀酸反应生成琥珀酸美托洛尔[17-19]。方法中描述的制备工艺在较多文献中采用,但工艺中使用四丁基溴化铵、聚乙二醇等相转移催化剂,实验操作繁琐;且工艺中使用二氯甲烷等溶剂,产生大量废液,不易回收,污染环境,增加生产成本。
本研究参照上述方法,对现有的琥珀酸美托洛尔制备工艺进行改进,其合成路线见图1,以对甲氧基乙基苯酚(2)为原料,在氢氧化钠作用下与环氧氯丙烷取代生成3-[4-(2-甲氧乙基-苯氧基]-1,2-环氧丙烷(3),再在异丙醇中与异丙胺开环加成得到1-异丙氨基-3-[4-(2-甲氧乙基)-苯氧基]-2-丙醇(4),即美托洛尔,最后与琥珀酸反应生成琥珀酸美托洛尔(1),总收率约55%。
1.2 仪器与试剂 DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限公司);YP2102电子天平(上海光正医疗仪器有限公司);EYELA N-1100型旋转蒸发仪(日本东京理化);Agilent 1260型高效液相色谱仪(美国安捷伦)。对甲氧基乙基苯酚(浙江普洛医药可以有限公司,工业级);氢氧化钠(天津市广成化学试剂有限公司,分析纯);环氧氯丙烷(国药集团试剂有限公司,分析纯);异丙醇(常州市先正化工有限公司,分析纯);异丙胺(天津市科密欧化学试剂有限公司,分析纯);乙酸乙酯(天津市广成化学试剂有限公司,分析纯);无水乙醇(天津市博迪化工股份有限公司,分析纯);琥珀酸(天津大茂化学试剂厂,分析纯)。
1.3 琥珀酸美托洛尔的合成路线图 见图1。
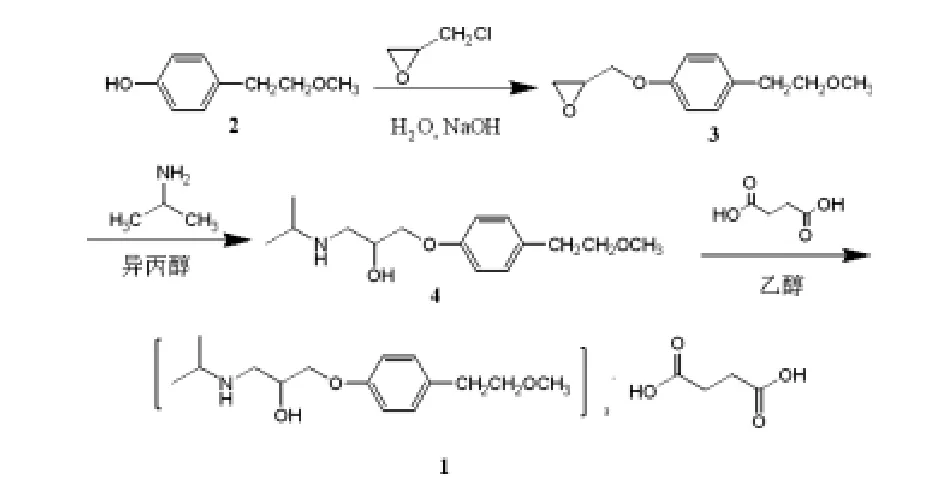
图1 琥珀酸美托洛尔的合成路线
1.4 实验过程
1.4.1 3-[4-(2-甲氧乙基)-苯氧基]-1,2-环氧丙烷的制备 向反应瓶中加入氢氧化钠(8.8 g,0.22 mol)和纯化水(100 mL),固体溶解后加入(2)(30.4 g,0.2 mol),充分溶解后,滴加环氧氯丙烷(24.05 g,0.26 mol),滴加完毕加热至80 ℃,反应半小时。反应完毕后停止加热冷却至室温。加入乙酸乙酯(100 mL×2)萃取,合并有机层,纯化水(200 mL×2)洗涤有机层,分液,有机相用无水硫酸钠干燥。过滤,滤液减压浓缩得到油状物(3)(38.7 g,收率92.9%),直接用于下步反应。
1.4.2 1-异丙氨基-3-[4-(2-甲氧乙基)-苯氧基]-2-丙醇的制备 将(3)(38.7 g,0.18 mol)和异丙醇(100 mL)加入反应瓶中,充分搅拌溶解,滴加异丙胺(53.7 g,0.91 mol),滴毕升温回流搅拌2 h。反应完毕后停止加热,冷却至室温。减压蒸馏得到浓缩液,后加入乙酸乙酯(200 mL)搅拌至完全溶解,加入18%盐酸调至弱酸性,加纯化水萃取,保留水相。在搅拌条件下向水相中加入饱和氢氧化钠溶液,调至溶液呈弱碱性。经乙酸乙酯(100 mL×2)萃取,合并有机层,纯化水(200 mL×2)洗涤有机层,分液,有机相用无水硫酸钠干燥,后经减压蒸馏得到油状物(4)(38.7 g,收率77.9%),直接用于下步反应。
1.4.3 琥珀酸美托洛尔的制备 称取琥珀酸(9.8 g,0.083 mol)加至乙醇(100 mL)中,60 ℃下搅拌溶解,将(4)(38.7 g,0.14 mol)和乙醇(100 mL)加入反应瓶中并搅拌溶解,加热至40 ℃,滴加琥珀酸的乙醇溶液到反应液中,滴毕,升温至回流继续反应2 h。反应完后,降至室温搅拌析晶。析晶完毕后,用布氏漏斗抽滤,得到白色晶体,80 ℃烘干,最终得到(1)(36.0 g,收率 76.1%),mp135~138 ℃(文献 [11]:136~138 ℃)。纯度≥99%,色谱条件:用十八烷基硅烷键合硅胶为填充剂的C18柱250 mm×4.6 mm,ф5 μm;流动相:称取乙酸铵1.9 g溶解于810 mL纯化水中,加磷酸13 mL,冰醋酸10 mL搅拌均匀,再加入三乙胺1.2 mL,搅拌均匀,用0.45 μm滤膜过滤后,与乙腈19 0mL混合均匀,脱气备用;流速为1.2 mL/min;检测波长265 nm;柱温 30 ℃;进样量 20 μL。MS-ESI(m/z):268[M+H]+;1H NMR(DMSO-d6)δ: 7.13(d, 2H), 6.85(d, 2H), 3.97(m, 1H), 3.89(m, 2H), 3.47(t, 2H),3.23(s, 3H), 2.98(m, 1H), 2.87(dd, 1H), 2.73(t,2H), 2.71(m, 1H), 2.26(s, 4H), 1.09(d, 6H)。
2 结果
依照上述方法,投入起始物料(2)30.4 g试验,制得中间体(3)38.7 g,收率92.9%;进而制得中间体(4)38.7 g,收率77.9%;最后与琥珀酸反应生成(1)(琥珀酸美托洛尔)36.0 g,收率76.1%,总收率55.1%(以起始物料0.2 mol计算),纯度≥99%(以面积归一化法计算纯度)。
3 讨论
目前,琥珀酸美托洛尔的合成方法大都存在产物纯度低,收率低,操作步骤繁琐,所用试剂毒性较大产生大量废液等问题。参考文献[12]中所述方法采用乙酰化的3-[4-(2-甲氧基乙基苯氧基)]-1,2-环氧丙烷为起始物料,一步反应制得美托洛尔,虽然较为简便,但此原料无法直接购得,需要自制,成本相对较高。参考文献[6]中使用氢化钠、甲醇钠、苯、氯仿等高毒性试剂,存在安全隐患。在重复参考文献[10]中所述方法时,得到产物无法达到文献中的收率和纯度。
本研究在上述现有方法的基础上,通过大量试验,克服各方法中的缺点,摸索出一种琥珀酸美托洛尔新的合成方法。本方法操作简便,条件温和,各步中间体为油状物,无需固化烘干可直接用于下步投料,且尽量采用水、乙酸乙酯等低毒性试剂作为反应溶剂,同时又提高了收率,得到高纯度的产品,所得琥珀酸美托洛尔纯度在99%以上,总收率约55%,适合工业化绿色生产。
[1]周娜,光雪峰.琥珀酸美托洛尔片在高血压病治疗中的优势[J].药物临床研究与应用,2008,1(6):868-869.
[2]包恩义,谭冰,王志国.老年快速房颤患者在应用美托洛尔片控制心室率的基础上加用稳心颗粒疗效观察[J].中国医学创新,2013,10(7):24-25.
[3]管高峰,李正武.琥珀酸美托洛尔片的降压效果评价[J].检验医学与临床,2009,12(6):1989-1990.
[4]王迎军.探讨美托洛尔治疗充血性心力衰竭的临床疗效[J].中国医学创新,2012,9(24):106-107.
[5]仇丽琴.美托洛尔分别联合氨氯地平和依那普利治疗高血压成本效果分析[J].中国医学创新,2011,8(26):167-168.
[6]梁艳红,张丹参.美托洛尔在心血管疾病中的应用进展[J].张家口医学院学报,2012,15(2):39.
[7]晏明海,王光权.美托洛尔对不同机制心律失常的疗效观察[J].中国医学创新,2010,7(25):92-93.
[8]Dimpfel H, Wilfried L, Prof D.Metoprolol for the treatment of schizophrenia related diseases:EP,1378235[P].2004-01-07.
[9]史景卫.美托洛尔在慢性充血性心力衰竭治疗中的临床观察[J].中国医学创新,2011,8(27):49-50.
[10]吕绍昆.美托洛尔、西地兰治疗快速性心率失常的疗效观察[J].中国医学创新,2011,8(30):126-127.
[11]杨俊,吴峰,张静,等.一种规模化制备琥珀酸美托洛尔的方法:CN,102432476 A[P].2012-05-02.
[12]Josep M,Ribalta B, de Esplugues L,et al.Industrial process for obtaining an aryloxypropanolamine:US,5082929[P].1992-01-21.
[13]Gyllenhaalo,Vessman J.Potential of packed column supercritical fluid chromatography for the separation of Metoprolol from closely related compounds[J].Journal of Chromatography A,1999,839(25):141-148.
[14]田建文,张小林.美托洛尔合成研究的最新进展[J].江西化工,2003,3(1):4-5.
[15]李 雪 梅.一 种 美 托 洛 尔 的 制 备 方 法:CN,200810115092.2[P].2008-06-16.
[16]张培龙,薛为哲,林卓,等.美托洛尔的制备方法:CN,201010267321.X[P].2010-08-31.
[17]Koskenniska L A,Arto J K,Reijo J T.Process for the preparation of 1-isopropylamino-3-(4-(2-methoxy-ethyl)-phenoxy)-2-propanol:EP,0041760A1[P].1981-12-09.
[18]S·帕尔默,M·斯登奎斯特.制造美多洛尔的新方法:CN,1237958A[P].1999-12-08.
[19]宋光伟,姚国新,陈刚,等.美托洛尔的合成新工艺研究[J].中国药物化学杂志,2010,2(93):44-46.
