UV法测定清洁验证中残留物依帕司他的含量
2014-06-01杨玉琴季洪英洪丽萍黄加秀李竞梅包卫国
杨玉琴 季洪英 洪丽萍 黄加秀 李竞梅 包卫国
依帕司他为醛糖还原酶抑制药, 以可逆地抑制与糖尿病性并发症的发病机制相关的多元醇代谢中葡萄糖转化为山梨醇的醛糖还原酶而发挥作用, 其制剂唐林(依帕司他片)是本公司生产的主打畅销品种, 由于其对糖尿病神经性病变的治疗中的显著疗效而受到广大患者的一致好评。本文主要围绕依帕司他清洁验证中的残留物开展研究, 本文参考药典方法[1]对主活性成分依帕司他的定量分析进行了研究和验证,结果表明UV法简便, 准确, 可以用于依帕司他的定量分析。
根据擦拭取样的残留量、设备中的总残留限度、设备总内表面积计算得出依帕司他的残留量LD值为5.3 μg/cm2,试验中模拟设备材质的平板面积为100 cm2, 取样回收率为100%, 换算为理论取样量为530 μg, 于50 ml量瓶中以无水乙醇溶解并稀释至刻度, 得到浓度约为10.6 μg/ml的溶液, 作者以此浓度开展相关研究和验证。
1 仪器与试药
瑞士Mettler Toledo XP205 电子分析天平, 美国Agilent8453紫外分光光度计等。
依帕司他对照品(批号为:100618-200401)购于中国药品生物制品检定所, 试剂均为分析纯, 水为超纯水。
2 方法与结果
2.1 紫外条件与方法 石英比色池规格:1 cm;检测波长:292 nm;溶剂:无水甲醇;狭缝宽度:1.0 nm。
2.2 对照品溶液的配制 精密称取依帕司他对照品适量,加流动相溶解制成每1 ml含265 μg的对照品贮备液。
2.3 线性关系试验 分别精密吸取上述对照品贮备液适量,用无水乙醇稀释制成浓度分别为:2.6 μg/ml、5.3 μg/ml、10.6 μg/ml、21.2 μg/ml、26.5 μg/ml、53 μg/ml的溶液 , 分别在 292 nm的波长处测定吸光度, 平行试验两份, 建立标准曲线, 以依帕司他浓度为横坐标(X), 其吸光度值为纵坐标(Y), 得回归方程为: Y=0.0358X-0.0061 相关系数r=1.0000.
结果表明依帕司他在 2.67 μg/ml~53.74 μg/ml范围内 , 依帕司他对照品溶液浓度和其吸光度值具有良好的线性关系。2.4 检测限(LOD)和定量限(LOQ) 以无水乙醇的空白溶液校零后, 测定空白的吸光度值11次, 对11次的结果求标准偏差值, 作为背景噪音。检测限对应的信噪比为3:1, 定量限对应的信噪比为10:1, 将所得结果与线性关系试验中所得标准曲线的斜率相除即得检测限和定量限, UV法测定依帕司他的检测限 (LOD)为 :0.013 μg/ml, 定量限 (LOQ)为 0.044 μg/ml。
2.5 精密度试验 取浓度为10.608 μg/ml的依帕司他对照品溶液, 按样品测定项下方法操作, 重复测定6次, 结果依帕司他的吸光度的均值为0.37653, RSD值为0.1%, 表明该方法精密度良好。
2.6 稳定性试验 取浓度为10.808 μg /ml的供试品溶液,按样品测定项下方法在25℃下放置考察, 在放置0、2、4、6、8 h后分别测定一次, 共测定5次, 5次吸光度值的RSD值为1.0%, 表明供试品溶液在8h内稳定。
2.7 重复性试验 取批号为13070111的样品, 按照“2.9”项下方法制备6份供试液, 结果依帕司他含量均值为100.40%,RSD为0.3%。
2.8 加样回收率试验 采用加样回收法。计算得平均回收率为99.60%, RSD为0.2%, 结果见表1。
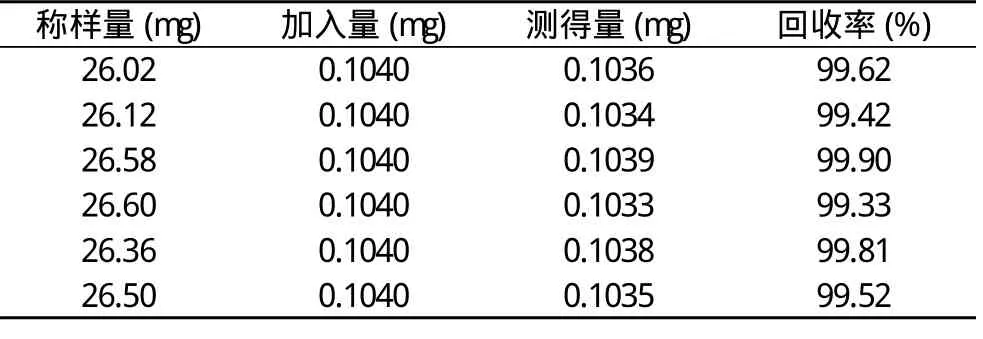
表1 加样回收率试验结果(n=6)
2.9 样品含量测定 取本品, 精密称定适量, 置100 ml量瓶中, 加无水乙醇振摇使依帕司他溶解并稀释至刻度, 摇匀,再精密量取2 ml, 置50 ml量瓶中, 加无水乙醇稀释制成每1ml溶液中约含10.6 μg的溶液, 作为供试品溶液。
3 小结
上述试验的验证结果表明UV法测定依帕司他清洁验证中的残留物依帕司他的含量可行, 该方法可用于依帕司他的定量分析。分别选取不同厂家和不同种类的溶剂作为擦拭溶剂, 结果选择无水乙醇为擦拭溶剂较适宜, 因为依帕司他在无水乙醇中溶解完全, 且无水乙醇为挥发性溶剂, 可以在将残留物依帕司他擦拭完全的同时有效减少溶剂残留。
[1] 国家药典委员会、中国药典(二部) .北京:化学工业出版社,2010.
