三维电极处理氨氮废水的电化学反应特性
2014-05-11周德鸿陈卫国罗范忠强
姜 辉,周德鸿,陈卫国罗 斌,范忠强
(中山大学化学与化学工程学院,广东 广州 510275)
三维电极处理氨氮废水的电化学反应特性
姜 辉,周德鸿,陈卫国*,罗 斌,范忠强
(中山大学化学与化学工程学院,广东 广州 510275)
采用无短路电流的电极粒子串作为三维电极的填充材料,以更好地揭示其电化学反应特性.研究证实在电化学反应过程中涉及到两个阶段,80min前氨氮的去除机理主要是与在粒子电极阴极端产生的羟基自由基发生电氧化反应,80min后少量的中归反应起到协同作用,从而达到更佳的去除效果.实验结果还说明随着槽电压的增大,氨氮去除率不断增大;当电压为25V,pH值为10的情况下得到较大的去除率.
三维电极;氨氮废水;电极粒子串
传统的氨氮处理方法包括:吹脱法、化学沉淀法、折点氯化法等[1].因工序复杂而且可能会造成第二次污染.近年来,利用复极性三维电极反应器处理低浓度氨氮废水成为一种相对有效且绿色环保的废水处理方法.常规的三维电极体系,是在传统由两块主极板组成的电解槽中加入导电粒子衍化而成[2].复极性三维电极[3]是指在两馈电极板间填充粒子,粒子与馈电极不接触,并在电场作用下复极化成为第三极.反应器中电化学反应存在着电极粒子上用于电氧化反应的电流以及无效的短路电流.因此,若要深入了解三维电极体系的电化学反应特性,最有效的方法是消除短路电流[4].
本实验利用以活性炭为基体,附载铁、铜、锰、锌、锆、铈的氧化物为活性组分的电极粒子,采用规整电极粒子串的填充方式,作为三维电极使得各电极粒子之间不互相接触,从而有效地消除短路电流的影响[5].研究复极性三维电极反应器的电化学反应特性以及对低浓度氨氮废水的处理的最佳实验条件.
1 实验部分
1.1 实验原理
电化学方法是目前使氨氮转换成N2的一种较为优良的脱氮方法,氨氮的去除主要有阳极的直接电氧化作用和阴极的间接氧化作用.
通常认为氨氮的阳极直接电氧化过程中在阳极上失去3个电子后被氧化成氮气和水[6].
在电极粒子阴极端,负氧离子的还原产生了H2O2,进而生成了·OH[7],氨氮在·OH的作用下氧化成氮气和水[8].
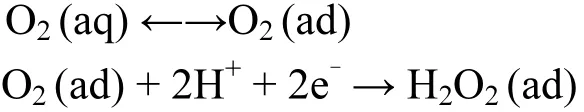

NOχ+ NH3+H+→ N2+ H2O (或溶液中发生氨氮的中归反应)
1.2 实验仪器

图1 自制复极性三维电极电解槽Fig.1 Home-made cell of bipolar three-dimensional-electrode
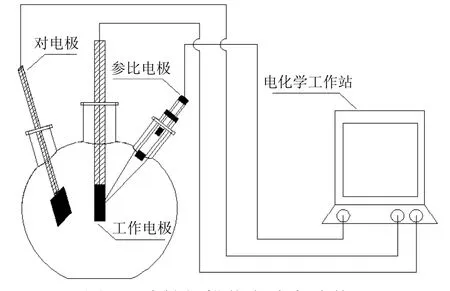
图2 线性扫描伏安法实验装置Fig.2 Reactor of linear sweep voltammetry
1.3 实验方法
采用外标法来确定溶液体系中氨氮浓度以及总氮浓度,根据国标法HJ535-2009[9],低浓度废水可用纳氏比色法进行氨氮的测量.
取C0=50mg/L硫酸铵母液100mL,放入电极粒子串,按照吸附实验操作使电极粒子串在实验前预先达到吸附平衡.分别探索电极粒子、槽电压、初始pH值、外加盐对硫酸铵电解的影响,三维电极和馈电极两类电极对氨氮废水的去除效果的比较,以及对氨氮去除机理进行初步的探索.
线性扫描伏安法:配制 0.0036mol/L硫酸钠溶液100mL,注入图2所示实验装置中.利用电化学工作站分别进行0~1.6V和-1.6~0V的线性扫描伏安实验,得到对应的电流-电位曲线.装置主要由一个100mL三口烧瓶、参比电极和对电极组成,对电极使用铂片,鲁金毛细管尖端与工作电极间距为1mm.工作电极的粒径为φ4×10mm,负载了活性组分的活性炭粒子组成的三维电极粒子,一端用银丝连接,并用环氧树脂胶封、固定.为防止银丝与反应液接触氧化,银丝一端套于玻璃管内,并在玻璃管内填充的环氧树脂.
恒电位法:配制 C0=50mg/L,pH=2.5的硫酸铵溶液150mL.分别取25mL注入图3所示实验装置中,利用电化学工作站,调节工作电极电位为-1.2, -0.8,-0.4,0.4,0.8,1.2下电解15min,取样1mL,利用纳氏比色法测量其氨氮浓度,并计算氨氮去除率.
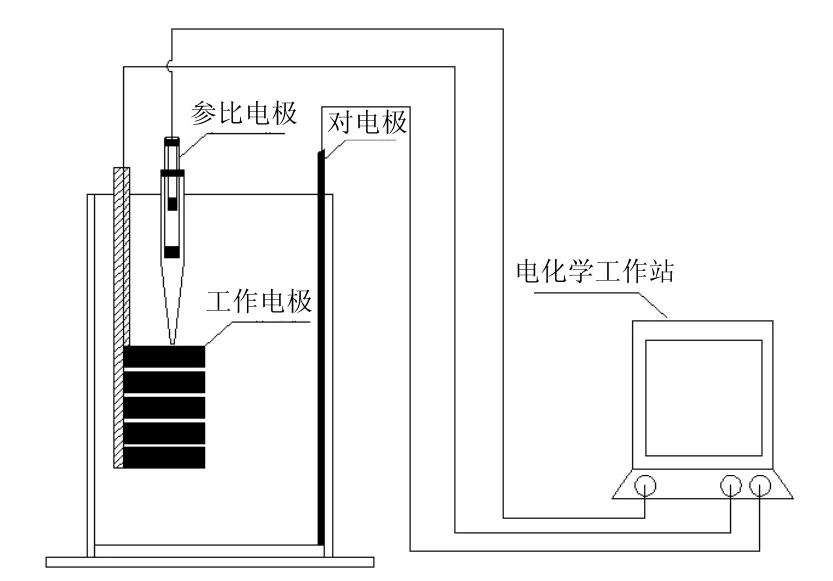
图3 自制单极性三维电极电解槽Fig.3 Home-made cell of single-polar three-dimensional-electrode
单极性三维电极电解槽如图3所示.由有机玻璃制成,长×宽×高为45mm×11mm×63mm,用304不锈钢板做对电极.用鲁金毛细管作为参比电极,测量工作电极与溶液的液接电位,鲁金毛细管尖端与工作电极间距1mm.工作电极由5粒φ4×14mm,附载了活性组分的活性炭粒子组成的三维电极粒子排,将电极粒子并联且用环氧树脂胶封、固定.以银丝作为电极引出线,为防止银丝与反应液接触氧化,银丝一端套于玻璃管内,并在玻璃管内填充环氧树脂.制作时,应尽量使各粒子保持平行且在同一方向.工作时,电极粒子一端应与对电极平行.
2 结果与讨论
2.1 氨氮去除机理探讨
2.1.1 线性扫描伏安法探索电极粒子上发生的反应 利用线性扫描伏安法,可以从电流-电压曲线得出电极粒子上所发生的电化学反应.根据不同的 pH值,氨氮可存在两种形态——NH4+和NH3·H2O为主.如图4对电极粒子进行从0~1.4V的线性扫描,在析氧突变电位前,没有出现明显的氧化还原特征峰,说明电极上没有氨氮的直接电化学反应发生;在对电极粒子进行从-1.4~0V的线性扫描中(图 5),其中分别在 pH值为 2.5、10和等量硫酸钠的条件下三组电流-电压曲线分别在-0.3、-1、-0.8出现较为明显的析氧峰,由此可推测电极粒子吸附溶解氧先生成负离子氧,然后再转化成初生态H2O2,继而生成的·OH再进行脱氮电化学反应,将氨氮氧化成N2和水.

图4 各pH值下线性扫描伏安法(0~1.4V)Fig.4 LSV from 0~1.4V at different pH
2.1.2 恒电位法探索电极粒子阴极端和阳极端对氨氮消除所起作用 在三维电极体系中,电极粒子在复极性环境下同时存在阴极端和阳极端且各处电位不同,为了进一步检验伏安法的结论,利用图3反应装置进行针对性的研究.由图6可看出,同一 pH值下,电极粒子作为阴极时氨氮去除率均比作为阳极时高,且作为阴极时氨氮去除率随电位升高而迅速减小.这说明三维电极反应以阴极端反应为主.电极粒子作为阳极,pH值为2.5时,0.4、0.8、1.2下氨氮去除率很低,说明阳极端直接氧化的贡献率不大.另外,电极粒子作为阴极时,在溶液体系为 pH值较大的环境下,氨氮以NH3·H2O存在,虽其从溶液主体到粒子表面传质主要靠浓度扩散,速率远不及 NH4+,但是碱性有利于·OH的形成,所以总的去除率是上升的;溶液体系在 pH值较低的环境下,阴极析氢反应变得容易,与生成·OH的反应发生竞争,使·OH产量下降,但是氨氮去除的总趋势是不变的.
2.1.3 总氮与氨氮去除的相关性 利用图 1装置研究了在pH=10,E=25V的反应条件下总氮浓度的变化.从图7可知,随着电解时间的推移,总氮浓度和氨氮浓度均有减少.因此在120min反应时间内,从总氨氮量降低说明模拟氨氮废水是以N2的形式去除的.

图5 各pH值下线性扫描伏安法(-1.4~0V)Fig.5 LSV from -1.4~0V of different pH

图6 电极粒子在不同pH值、单极性环境下反应15min氨氮去除率Fig.6 Removal rate of ammonia with single-polar particle electrodes at different initial pH

尽管总氮与氨氮浓度都在降低,但在电解开始和结束时,总氮浓度均高于氨氮浓度,说明模拟废液中有少量硝酸根等其他氮的氧化物生成.
这种现象还可以从图7中过氧化氢累积曲线看出,在反应的120min内,生成H2O2的量逐步上升但是总量比较少,反应结束时,最大生成量也只有5.7mg/L.因此可以认为,在前 80min氨氮的去除主要是在粒子电极阴极端产生的羟基自由基的电氧化作用.80min后随着 H2O2的产生量增加,除了有粒子电极电氧化作用,同时由于存在氮的氧化物中间体的生成使得在溶液中产生中归反应.从氧化还原反应原理上讲,对于多价态的氮氧化物中间体存在,可以发生一系列电化学反应释放出 N2,这种过程会随着 H2O2量的增加而逐渐增强,而关于溶液中归反应的贡献率问题将另文加以研究.

图7 氨氮、总氮及过氧化氢浓度随时间的变化Fig.7 Concentrations changes of ammonia, total azote and H2O2wieh reaction time
2.1.4 三维电极与馈电极对氨氮去除率的比较(E=25V,pH=10,C0=50mg/L)如图8所示,在整个氨氮废水体系中馈电极(图8中的馈电极是以不锈钢材料做的电极板)在反应过程中对氨氮的去除贡献很低.这是因为在三维电极体系中,氨氮废水的降解主要发生在粒子电极上,这是因为粒子电极的复极化,有效增加了反应器的面体比,强化了物质传质效果,使得降解过程中的瞬时电流效率远高于馈电极,相当于平板电极反应器,故处理效果明显提高.
2.2 三维电极粒子反应器对氨氮去除的影响因素
2.2.1 槽电压对氨氮去除率的影响(pH=7.5, C0=50mg/L) 由于实验的电极粒子经过饱和处理,故而电极粒子本身的吸附效果可以忽略不计.在三维电极降解废水的过程中,槽电压的增加,电化学氧化反应的推动力增强;加大了阳极表面有机物的氧化速度;然而,槽电压升高,也会导致析氧等副反应的发生.利用图1反应器进行实验研究探索,由图9可知,在槽电压为5~25V的区间下,氨氮在反应120min后去除率随槽电压的增大而增大.在25V时取得最大值为72.3%.当槽电压大于25V以后,去除率增大幅度逐渐减少.可以认为,在处理中存在着一个最佳的槽电压.
2.2.2 初始 pH值对氨氮去除率的影响(E=25V, C0=50mg/L) 三维电极处理氨氮废水利用的是·OH的高氧化能力,然而不同的pH值对·OH的产生有着很重要的影响.从图10可以得出,当初始pH值为2.5时,氨氮去除率很小;当初始pH值大于2.5时,氨氮去除率显著上升;即初始 pH值越大,越有利于氨氮的去除.结果显示在初始pH=10反应时铵离子去除率达到 79.1%,且副反应和馈电极腐蚀反应不严重,但pH>10以后会加剧电极腐蚀.所以决定槽电压为25V,初始pH=10为本实验环境下最佳反应条件.

图9 不同槽电压下氨氮浓度随电解时间变化Fig.9 Concentrations changes of ammonia as time at different cell voltages

图10 不同初始pH下氨氮浓度随电解时间变化Fig.10 Concentrations changes of ammonia as time at different initial pH
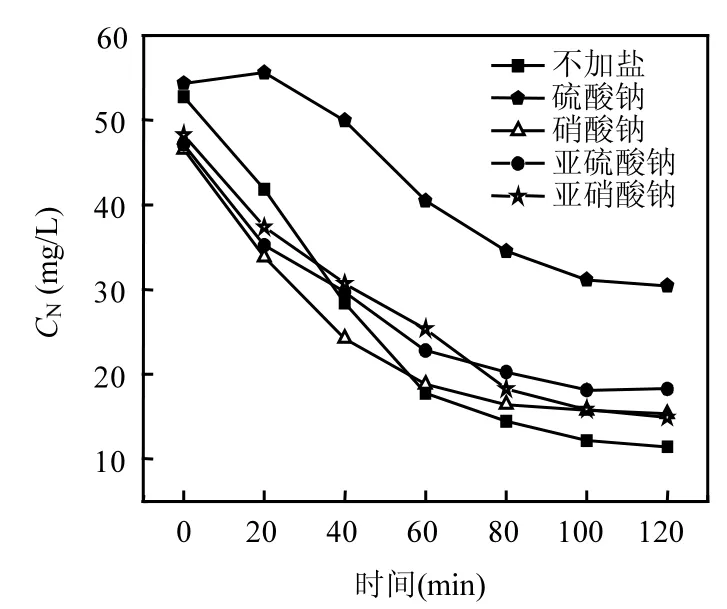
图11 外加不同的盐氨氮浓度随电解时间变化Fig.11 Concentrations changes of ammonia as time at different salts added
2.2.3 外加盐对氨氮去除率的影响(E=25V, pH=10, C0=50mg/L) 在三维电极体系中,电导率的大小对氨氮废水的降解有着重要的影响,这是因为电导率的大小影响着槽电压的分配,使得馈电极上和粒子电极上的电压发生改变,进而影响电极粒子上反应推动力的大小.溶液电导率增大使槽电压主要消耗在两馈电极的液接电势上,电极粒子上反应推动力减少.如图11,外加盐时氨氮的浓度在120min的最终去除率均不及不加盐的一组多.因此,在三维电极降解氨氮废水时应该减少或者避免加入电解质盐分.然而在外加盐中,氨氮去除率最大的是外加亚硝酸钠一组,氨氮去除率达到 69.2%.这是因为亚硝酸钠与氨氮发生归中反应转化为N2的结果.
3 结论
3.1 在电化学反应过程中,证实80min前氨氮的去除机制主要是在粒子电极的阴极端产生的羟基自由基发生电氧化反应所致,80min后其他中归反应起到协同作用,从而达到更佳的去除效果.
3.2 槽电压在0~5V时,氨氮的去除率基本为零;随着槽电压的增大,氨氮去除率不断增大;当电压超过25V时,副反应急剧增强,超过25V的那部分电压主要参与副反应,对主反应基本没有贡献,因此基于本实验认定在槽电压为25V时,去除率最大.
3.3 在槽电压一定下,初始pH值越大,氨氮去除率越高,但pH值超过10后对设备的腐蚀程度加大从而会进一步影响整个系统的去除效果,所以确定pH=10,E=25V为本研究的最理想工作参数.
3.4 外加盐不利于氨氮的去除;且氨氮的去除率随添加盐的浓度升高而降低.
[1] 白雁冰.折点加氯法脱氨氮后余氯的脱除 [J]. 环境科学与管理, 2008,33(11):102-108.
[2] Zhou Ding, Cai Weimin,Wang Qunhui. A study on the use of bipolar-particles-electrodes in decolorization of dyeing effluents and its principle [J]. Water Sci. Tech., 1986,19(34):391-400.
[3] 王 丽,周德瑞,张秋华,等.复合型三维电极固定床电化学反应器电势分布 [J]. 哈尔滨理工大学学报, 2003,8(5):24-26.
[4] 纪庆升.非均电场对三维电极体系性能的影响 [D]. 广州:中山大学, 2007:65.
[5] 钟锐超,周德鸿,陈卫国,等.2011.粒子电极堆放方式对三维电极体系性能的影响 [J]. 环境科学学报, 31(10):2174-2178.
[6] 陈金銮.氨氮的电化学氧化技术及其应用研究 [D]. 北京.清华大学, 2008:209.
[7] 陈卫国,朱锡海.电催化产生 H2O2和·OH及去除废水中有机污染物的应用 [J]. 中国环境科学, 1998,18(2):148-150.
[8] Zhou Minghua, Fu Wenjing, Gu Heyan, et al. Nitrate removal from groundwater by a novel three-dimensional electrode biofilm reactor [J]. Electrochimica Acta, 2007,52:6052-6059.
[9] HJ 535-2009 水质氨氮的测定-纳氏试剂分光光度法 [S].
Preliminary exploration of electrochemical reaction characteristics in three-dimensional electrode treatment ammonia wastewater.
JIANG Hui, ZHOU De-hong, CHEN Wei-guo*, LUO Bin, FAN Zhong-qiang
(Chemistry and Chemical Engineering, Sun Yet-sen University, Guangzhou 510275, China). China Environmental Science, 2014,34(10):2551~2555
Electrode particle string, which has no short-circuited current, was used as the filling material of three-dimensional electrode to better reveal the characteristics of electrochemical reaction. The results revealed that the removal of ammonia during electrochemical reaction involved two steps: before 80min, it was mainly caused by the electrochemical oxidation reaction between ammonia and hydroxyl radicals generated at the cathode particle electrode; after 80min, small amount of normalized reactions provided synergy effect to achieve better removal rate. Experimental results also showed an improvement of ammonia removal rate with the increase in cell voltage. The highest removal rate was achieved under pH 10 with the voltage of 25V.
t:three-dimensional-electrode;ammonia containing waster;electrode particles string (home-made regular electrode particle)
X703
:A
:1000-6923(2014)10-2551-05
姜 辉(1988-),男,湖南娄底人,中山大学硕士研究生,主要从事高浓度含盐有机废水的研究.
2013-12-31
* 责任作者, 副教授, chenwg@mail.sysu.edu.cn
