聚阴离子型锂离子电池正极材料Li3V2(PO4)3的研究进展
2014-05-10邓玲陈善华吴骏邱娟
邓玲,陈善华,吴骏,邱娟
(成都理工大学材料与化学化工学院,四川成都 610059)
在二次电池之中,锂离子电池具有高电压(3.6 V)、小的体积(比Ni-H 电池小30%)、轻的质量(比氢-镍电池轻 50%)以及高的比能量(140 Wh/kg)等优点[1-3],已经成为二次电池的发展重点。
聚阴离子型锂离子电池正极材料是含有四面体或八面体的阴离子结构单元(XOm)n-(X=P、S等)的一系列化合物的总称[4]。这些结构单元主要是通过共价键连成三维的网络结构,形成一些由其他金属离子(Mn+)占据的、更高配位的间隙,使得聚阴离子型的锂离子电池正极材料具有和其他锂离子电池正极材料不一样的晶体结构,而这种结构决定正极材料突出的电化学性能。现在研究较多的是有橄榄石[5-6]和 NASICON[7]这两种结构类型的聚阴离子型化合物的锂离子电池正极材料。
在过渡金属元素中,V的化学性质非常活泼,是非常典型的多价过渡金属元素。研究发现,较之LiFePO4,单斜结构的Li3V2(PO4)3化合物拥有更高的放电电压(3.6,4.1,4.6 V)、更高的锂离子扩散系数和能量密度 (碳包覆后达到2 330 mWh/cm3)[8],是现在有发展潜力的大容量、高功率的锂离子电池正极材料之一[9]。
1 Li3V2(PO4)3的晶体结构
Li3V2(PO4)3的结构属于NASICON结构,具有单斜晶系和斜方晶系两种晶型[10-11]。由于单斜结构的Li3V2(PO4)3电化学性能优于斜方结构的Li3V2(PO4)3,已经成为研究重点。其为 P21/n,晶胞参数[12]为:a=0.866 2 nm,b=0.816 24 nm,c=1.210 4 nm,β =90.452°。Li3V2(PO4)3的晶体结构(图1)中,四面体(PO4)和八面体(VO6)通过共用一个氧原子而形成一个三维骨架结构,每个八面体(VO6)周围有6个四面体(PO4),而每个四面体(PO4)周围有4个八面体(VO6)[13]。这样每个单晶都由4个A2B3(B=PO4,A=VO6)单元构成了一个通道较大的三维网状的结构,允许Li+快速嵌脱而结构稳定,即使3个Li+完全脱嵌,框架仍然稳定存在。

图1 Li3V2(PO4)3的晶体结构Fig.1 The crystal structure of Li3V2(PO4)3
2 Li3V2(PO4)3的充放电性能
Li3V2(PO4)3中 V的价态是 +3,其3个 Li+完全脱嵌,形成了V2(PO4)3,这个时候 V就以V+4/V+5的混合价态而存在,有利于电子传输。Li3V2(PO4)3的充放电反应可以表示为[10]:
充电反应

放电反应

Li+随着充电的进行而脱出,它的晶体结构不会发生改变,仍然具有单斜结构,但随着Li+的逐渐脱出,Li3V2(PO4)3的晶胞参数则逐渐减小(表1),从而导致脱出2个Li+后晶胞体积减小约8%[7],但是使用化学氧化的方法脱出3个Li+后,晶胞体积反而增大。由此可知,Li3V2(PO4)3的结构非常稳定,所以其电化学性能较好[14]。
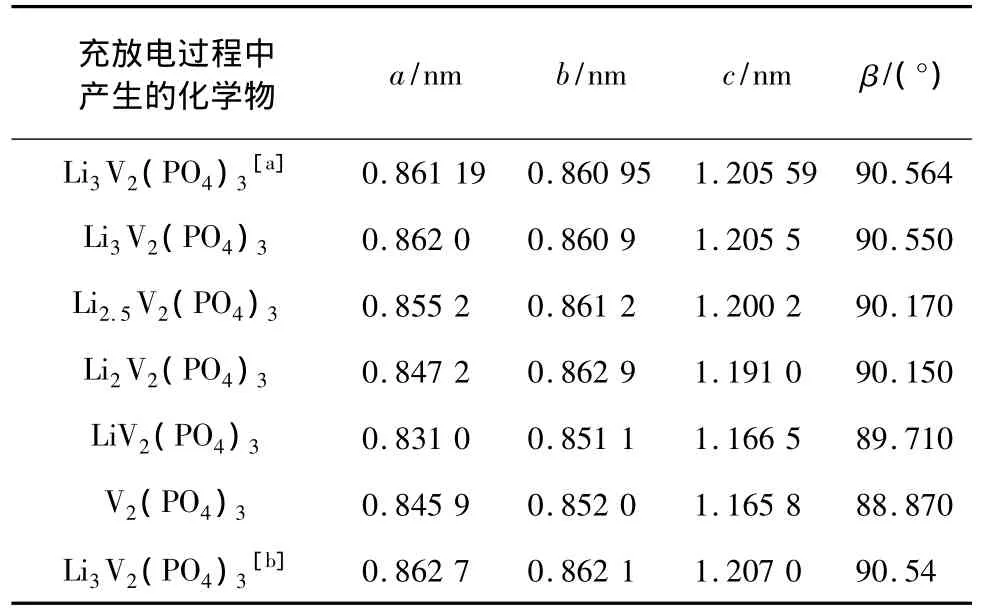
表1 Li3V2(PO4)3在充放电过程中晶胞参数变化[7]Table 1 The cell parameters change of Li3V2(PO4)3 during charging and discharging
图2为Li3V2(PO4)3的充放电曲线(3.0 ~4.8 V电压区间)[15]。
由图2可知,其充放电特性与其他正极材料有明显的区别,主要表现在:Li3V2(PO4)3的充放电曲线出现4个电压平台。电压在3.0 ~4.3 V的范围内时,Li3V2(PO4)3可以可逆的脱嵌2个Li+,这时它的理论容量是132 mAh/g,而电压在3.0~4.8 V范围内时,其充放电曲线存在4个电压平台,每一个Li3V2(PO4)3可以可逆脱嵌3个 Li+,理论容量197 mAh/g[13],前 2 个平台对应第 1 个 Li+的脱嵌与嵌入,当中第1个平台对应于:Li3V2(PO4)3→Li2.5V2(PO4)3;第 2个 平 台 对 应 于 转 变Li2.5V2(PO4)3→ Li2V2(PO4)3。第 3 个平台对应于第2个Li+的脱嵌与嵌入,相应于Li2V2(PO4)3→Li1V2(PO4)3的转变。前3个平台都对应于V3+/V4+电对的氧化还原反应。第4个平台对应于第3个Li+的脱嵌与嵌入,对应于 Li1V2(PO4)3→V2(PO4)3的转变,同时1个V4+被氧化为V5+。

图2 在3.0~4.8 V电压范围内Li3V2(PO4)3的电化学电位谱Fig.2 The electrochemical potential spectrum of Li3V2(PO4)3in the voltage of 3.0 ~4.8 V
3 Li3V2(PO4)3的合成方法
Li3V2(PO4)3的合成方法主要有:高温固相法、溶胶-凝胶法、水热法、微波控温固相合成法等。
3.1 高温固相法
高温固相法[16-17]是合成 Li3V2(PO4)3的最简单、最有效的方法,根据还原剂的不同,可以分为碳热还原法[18-19]和氢气还原法[20]。Barker等[21]采用碳热还原的方法合成Li3V2(PO4)3/C复合材料,在3.0 ~4.3 V 范围内,0.5C,1C 倍率下的放电电容量分别是 130,118 mAh/g,3C倍率下的电容量为108 mAh/g,循环 500次后比容量保持率达到77.4%。Fu等[22]采用氢气还原的方法,利用 LiF 为Li源合成Li3V2(PO4)3,具有优良的电化学性能,在3.0~4.3 V电压之内,1C放电倍率下的首次的放电电容量是158 mAh/g,循环50次后比容量保持率达到94%。
3.2 微波控温固相合成法
微波控温固相合成法的合成时间比传统的方法短,晶粒生长快,原子结构特别是Li位和晶胞参数都会出现一定的偏差,其制得的Li3V2(PO4)3的容量损失较严重。Yang等[23]采用微波控温固相合成的方法合成 Li3V2(PO4)3,在3.0~4.3 V 的电压内最大的放电电容量是132 mAh/g,在3.0~4.8 V 电压内首次的放电电容量是183.4 mAh/g,循环50周后的放电电容量是123.7 mAh/g,电容量保持率很高。
3.3 溶胶-凝胶法
溶胶-凝胶法[24-25]是将原料溶解在水中而形成均匀溶液,之后再加入有机的络合剂来将金属离子固定,最后调节pH值来使其形成凝胶,再通过干燥、研磨、热处理等过程制得所需要的材料。Huang等[26]采用溶胶-凝胶法制备Li3V2(PO4)3/C复合材料,在3.0~4.3 V 的电压内,0.2C 倍率下的电容量是132 mAh/g,5C倍率下的放电电容量可以达到理论值的95%,并且具有很好的循环性能,循环200次后的电容量基本没变。Yan等[27]采用溶胶-凝胶法合成 Li3V2(PO4)3,在 3.0 ~4.3 V 电压内,0.5C倍率下的首次放电电容量是123.79 mAh/g。
3.4 水热法
水热法也属于液相化学法,在密封的容器中用水作为溶剂在高温高压下进行液相化学反应。Sun等[28]以 CH3COOLi·2H2O、NH4H2PO4、NH4VO3以及EG为原料,用水热的方法合成直径为60 nm左右、长为几百nm~1 μm的Li3V2(PO4)3纳米带,其具有良好的电化学性能,在0.1C倍率下的首次的放电电容量是178 mAh/g,在0.5C倍率下的首次的放电电容量是172 mAh/g,在1.0C倍率下的首次的放电电容量是170 mAh/g,在2.0C倍率下的首次的放电电容量是167 mAh/g,在5.0C倍率下的首次的放电电容量是164 mAh/g。
3.5 喷雾沉积法
将各原料溶解在一定量的去离子水中,加入丙二醇和乙醇进行稀释,得到绿色前驱体,然后将其移到金属的注射器中,再以石墨片作为底层,并且使针与底层间的距离保持为3 cm,并施以12.5 kV直流电压,最后将沉积的样品在Ar气氛下700℃热处理8 h。Wang 等[29]以 H3PO4、NH4VO3、LiNO3·H2O、葡萄糖为原料,通过喷雾沉积的方法合成Li3V2(PO4)3,具有好的电化学性能,在 3.0 ~4.3 V范围内,1C倍率下的放电电容量是118 mAh/g,24C倍率下的放电电容量是80 mAh/g。
3.6 流变相反应法
在较低的温度下,使得固体反应物处于流变的状态,从而增强固体粒子之间的有效接触。其具有煅烧时间较短、合成温度较低、颗粒较细并且分布均匀 等 特 点。 Chang 等[30]以 V2O5、Li2CO3、NH4H2PO4、PEG为原料,采用流变相反应方法制备Li3V2(PO4)3/C复合材料,具有较好的倍率性能和循环稳定性。在3.0~4.8 V电压范围内,0.1C倍率下首次放电电容量是189 mAh/g,在0.2C倍率下首次放电电容量是177 mAh/g,在1C倍率下首次放电电容量是170 mAh/g,在2C倍率下首次放电电容量是169 mAh/g,在5C倍率下首次放电电容量是159 mAh/g。
3.7 液相球化法
使用丁苯橡胶分散剂作为粘结剂,许多亚微米级的颗粒被粘在一起而形成团聚的颗粒,提高Li+在材料中的扩散系数。侯春平等[31]以LiOH·H2O、NH4H2PO4、V2O5和碳粉作为原料,通过液相球化的方法合成Li3V2(PO4)3/C,有很好的电化学性能:在3.0~4.3 V范围内的最大放电电容量是126.67 mAh/g,首次的充放电效率是 95.6%,循环40周后其电容量保持率是98.2%。在3.0~4.8 V范围内的最大放电电容量是170.47 mAh/g,首次的充放电效率是97.5%,循环40周后其电容量保持率是83.9%。
4 Li3V2(PO4)3的改性研究
Li3V2(PO4)3虽然具有高比容量、高电位和良好的循环性能等优点,但是晶体结构中的金属离子相隔较远,影响电子迁移率,导致其电导率低、高倍率的充放电性能差。所以要提高Li3V2(PO4)3的电性能就必须对其改性。
4.1 离子掺杂
掺杂金属离子[32]可以提高晶格内部的电子电导率和Li+的扩散系数,来提高电导率。因为这些金属离子的半径都小于 Li+和V3+。Chen等[33]采用溶胶-凝胶的方法制备掺杂Cr的Li3V2(PO4)3,属于单斜结构,充放电电容量和循环性能都得到提高,当掺杂量x=0.1时,在0.2C倍率下首次放电的电容量是171.4 mAh/g,然后循环100周后电容量保持率是78.6%;而在4C倍率下首次放电的电容量是130.2 mAh/g,循环100周后电容量损失10.8%。Huang等[34]用溶胶-凝胶法合成掺杂Mg元素的Li3V2(PO4)3,它具有优良的电化学性能,当掺杂量x=0.3时,在 0.2C倍率下的首次放电容量是130 mAh/g,循环100周后容量保持为118 mAh/g;在1C倍率下的首次放电电容量是128 mAh/g,循环100周后容量仍保持为118 mAh/g。Xia等[35]采用溶胶-凝胶法合成掺杂Nb的Li3V2-xNbx(PO4)3/C,研究表明,掺杂一定量的 Nb并不会破坏 Li3V2-(PO4)3的晶体结构,而会增大Li3V2(PO4)3晶胞的体积,有利于 Li+嵌脱。当掺杂量 x=0.15时,在0.5C倍率下首次放电的电容量是162.4 mAh/g,然后循环50次后容量保持率是86.6%。Liu等[36]采用微波固相法制备出Li3V2-xSnx(PO4)3/C,发现Sn没有破坏Li3V2(PO4)3晶体结构,当 x=0.05时,Li3V2(PO4)3的倍率性能和电化学稳定性都表现为最优,在2.5 ~4.5 V 电压之内,在0.5C 倍率下的首次放电的电容量是136 mAh/g。
4.2 表面碳包覆
表面碳包覆不仅可以改善Li3V2(PO4)3的导电性,也可以提高Li3V2(PO4)3的放电电位平台和电容量,主要原因:一是在高温惰性条件下,有机物可分解成C,分布在材料的表面,增加了材料的导电性;二是产生的C可以达到纳米数量级,并且可以细化产物的粒径以及扩大导电面积,这样有利于Li+的扩散;三是C还是还原剂,可以避免了V3+被氧化。Ren等[37]以葡萄糖为 C源,制备厚度约为10 nm的Li3V2(PO4)3/C。这种复合材料有很好的电化学性能,在0.2C和1C的倍率下的首次放电电容量是 127.8,120 mAh/g,循环 50 次后电容量为125.9,118 mAh/g。Wang 等[38]采用固相反应,以聚乙二醇为C 源,合成Li3V2(PO4)3/C,在3.0 ~4.3 V范围内,在5C倍率下的首次放电容量是106 mAh/g,循环700次后容量保持率是93%。
5 结束语
Li3V2(PO4)3正极材料具有高的比容量、高的工作电压、好的循环性能及好的安全性能等特点,有望代替 LiCoO2和 LiMn2O4、LiFePO4,成为下一代的新型动力电池正极材料。如果Li3V2(PO4)3在高电压充放电范围内循环性能、倍率性能和高低温性能等几个问题能够解决,Li3V2(PO4)3的电化学性能将会得到大大的提升。此外,也可采用第一性原理计算方法,通过对Li3V2(PO4)3体相和表面的考察,探究其电子结构,通过能带结构、态密度、部分态密度和布局分布,阐明材料自身结构对材料电化学性能的影响,通过与实验数据对比分析,探索电化学性能与材料微观结构的关系,为Li3V2(PO4)3的进一步改性研究提供理论依据。
[1]郭炳焜,徐徽,王先友,等.锂离子电池[M].长沙:中南大学出版社,2002:1-140.
[2]施志聪,杨勇.聚阴离子型锂离子电池正极材料研究进展[J].化学进展,2005,17(4):604-613.
[3]戴曦,唐红辉,杨平,等.LiFePO4正极材料的研究进展[J].材料导报,2005,19(8):69-71.
[4]杨改,应皆荣,姜长印,等.磷酸钒锂材料及全钒锂离子电池性能研究[J].华南师范大学学报:自然科学版,2009(A2):8-9.
[5]李丽,李国华,王石泉,等.磷酸钒锂正极材料的合成与性能研究[J].无机化学学报,2010,26(1):1-5.
[6]武俊萍.锂离子电池正极材料Li3V2(PO4)3的合成及性能研究[D].哈尔滨:哈尔滨工业大学,2007:4-15.
[7]唐联兴.磷酸钒锂的合成及电化学性能比较[D].长沙:中南大学,2009:8-11.
[8]Mi C H,Zhang X G,Zhao X B,et al.Effect of sintering time on the physical and electrochemical properties of LiFePO4/C composite cathodes[J].Journal of Alloys and Compounds,2006,424:327-333.
[9]Fang H S,Li L P,Li G S.Hydrothermal synthesis of electrochemically active LiMnPO4[J].Chemistry Letters,2007,36:436-437.
[10]陈权启.磷酸钒锂和磷酸铁锂离子电池正极材料研究[D].杭州:浙江大学,2009:11-22.
[11]赵鹏,王跃峰,李东林,等.锂离子电池正极材料磷酸钒锂的研究进展[J].应用化学,2009,38(10):1-4.
[12]郭孝东,刘恒,吴德桥,等.磷酸盐系锂离子电池正极材料的研究进展[J].材料导报,2010,23(4):1-3.
[13]Jang Y,Huang B,Chiang Y M,et al.Stabilization of LiMnO2in the α-NaFeO2structure type by LiAlO2addition[J].Electrochemical and Solid-State Letters,1998,1(1):13-16.
[14]王丹丹.Li3V2(PO4)3的制备及其改性研究[D].秦皇岛:燕山大学,2010:10-20.
[15]Saidi M Y,Barker J,Huang H,et al.Performance characteristics of lithium vanadium phosphate as a cathode material for lithium-ion batteries[J].JournalofPower Sources,2003(119/120/121):266-272.
[16]刘素琴,唐联兴,黄可龙,等.新型锂离子电池正极材料Li3V2(PO4)3的合成及其性能[J].中国有色金属学报,2005,15(8):1294-1299.
[17]Li Y Z,Liu X,Yan J,et al.Study on synthesis routes and their influences on chemical and electrochemical performances of Li3V2(PO4)3/carbon[J].Electrochimica Acta,2007,53:474-479.
[18]姜霖琳,田彦文,刘丽英.碳热还原法制备锂离子电池正极材料Li3V2(PO4)3的研究[J].材料与冶金学报,2006,5(2):115-118.
[19]刘素琴,唐联兴,黄可龙,等.碳热还原法合成正极材料 Li3V2(PO4)3及其性能[J].电源技术,2006,30(6):473-476.
[20]Yin S C,Grondey H,Strobel P.Electrochemical property:Structure relationships in monoclinic Li3-yV2(PO4)3[J].American Chemical Society, 2003, 125(34):10402-10411.
[21]Barker J,Saidi M Y,Sworer J L.Lithium ion phosphor-oli-vines prepared by a novel carbothermal reduction method[J].Electrochemical and Solid-State Letters,2003,6(3):A53-A55.
[22]Fu P,Zhao Y M,Dong Y Z,et al.Low temperature solidstate synthesis routine and mechanism for Li3V2(PO4)3using LiF as lithium precursor[J].Electrochimica Acta,2006,52(3):1003-1008.
[23]Yang G,Liu H D,Ji H M,et al.Temperature-controlled microwave solid-sate synthesis of Li3V2(PO4)3as cathode materials for lithium batteries[J].Journal of Power Sources,2010,195:5374-5378.
[24]Doeff,Marca M,Hu Y Q,et al.Effect surface carbon structure on the electrochemical performance of LiFePO4[J].Electrochemical and Solid-State Letters,2003,6:A207-A209.
[25]Moshurchak L M,Buhrmester C,Dahn J R.Spectro-electrochemical studies of redox shuttle overcharge additive for LiFePO4-based Li-ion batteries[J].Journal of the Electrochemical Society,2005,152:A1279-A1282.
[26]Huang H,Yin S C,Kerr T.Nanostructured composites:A high capacity,fast rate Li3V2(PO4)3/carbon cathode for rechargeable lithium batteries[J].Advanced Materials,2002,14(21):1525-1528.
[27]Yan J,Yuan W,Tang Z Y.Synthesis and electrochemical performance of Li3V2(PO4)3-xClx/C cathode materials for lithium-ion batteries[J].Journal of Power Sources,2012,209:251-256.
[28]Sun C W,Shreyas R,Dong Y Z,et al.Hydrothermal synthesis and electrochemical performance of Li3V2(PO4)3/C-based composites for lithium-ion batteries[J].ACS Applied Materials & Interfaces,2011,3(9):3772-3776.
[29]Wang L,Zhang L C.A Li3V2(PO4)3/C thin film with high rate capability as cathode material for lithium-ion batteries[J].Electrochemistry Communications,2010,12:52-55.
[30]Chang C X,Xiang J F,Shi X X.Rheological phase reaction synthesis and electrochemical performance of Li3V2(PO4)3/carbon cathode for lithium batteries[J].Electrochimica Acta,2008,53:2232-2237.
[31]候春平,岳敏.液相球化法合成新型正极材料磷酸钒锂[J].物理化学学报,2007,23(12):1954-1957.
[32]Chang S Y,Blicking J T,Chiang Y M.Electronically conductive phosphor olivines as lithium storage electrodes[J].Nature Mater,2002,2(1):123-128.
[33]Chen Y H,Zhao Y M,An X N.Preparation and electrochemical performance studies on Cr-doped Li3V2(PO4)3as cathode materials for lithium-ion batteries[J].Eletrochimica Acta,2009,54:5844-5850.
[34]Huang J S,Yang L.Synthesis and characterization of Li3V(2-2x/3)Mgx(PO4)3/C cathode material for lithium-ion batteries[J].Journal of Power Sources,2010,195:5013-5018.
[35]Xia Y,Zhang W H,Huang H,et al.Synthesis and electrochemical properties of Nb-doped Li3V2(PO4)3/C cathode materials for lithium-ion batteries[J].Materials Science and Engineering B,2011,176:633-639.
[36]Liu H P,Bi S F,Wen G X.Synthesis and electrochemical performance of Sn-doped Li3V2(PO4)3/C cathode material for lithium ion battery by microwave solid-state technique[J].Journal of Alloys and Compounds,2012,543:99-104.
[37]Ren M M,Zhou Z,Gao X P.Core-shell Li3V2(PO4)3/C composites as cathode materials for lithium-ion batteries[J].The Journal Physical of Chemistry C,2008,112:5689-5693.
[38]Wang J W,Liu J,Yang G L,et al.Electrochemical performance of Li3V2(PO4)3/C cathode material using a novel carbon source[J].Eletrochimica Acta,2009,54(28):6451-6454.
