液相纯碱法生产氧化铁黄技术研究
2014-05-04姚佐胜孙晓庆杜松松
姚佐胜,孙晓庆,杜松松
(铜陵瑞莱科技有限公司,安徽 铜陵 244000)
液相纯碱法生产氧化铁黄技术研究
姚佐胜,孙晓庆,杜松松
(铜陵瑞莱科技有限公司,安徽 铜陵 244000)
研究了以钛白副产硫酸亚铁和工业纯碱为主要原料,采用液相法生产氧化铁黄的生产技术。在晶种存在下用空气氧化硫酸亚铁,反应过程中连续滴加硫酸亚铁和纯碱,保持一定的亚铁浓度和pH,通过对颜料色光进展的控制可以得到从浅色黄到深色黄一系列色相的氧化铁黄产品。该工艺的成功研发,具有较好的社会、经济和环境效益。
钛白副产硫酸亚铁;液相法;氧化铁黄;纯碱
氧化铁黄又称羟基铁,简称铁黄,化学式为Fe2O3·H2O或FeOOH,呈黄色粉末状,并有从柠檬色到橙色一系列色光。铁黄的着色力几乎与铅铬黄相近,遮盖力不大于15 g/m2,耐光性达6~7级。氧化铁黄由于有良好的耐候性、遮盖力而广泛应用于建筑、油墨、橡胶及造纸等行业的着色[1]。目前国内外制备氧化铁黄的主要方法有空气氧化法[2]、氯酸钠氧化法[3]、胶体化学法[4]、羰基铁氧化法[5]等几种方法。氧化铁黄空气氧化法的传统生产工艺依旧是使用铁皮、硫酸亚铁和空气的固液气三相反应,其中作为原料的铁皮成本占到氧化铁黄生产成本的将近一半,且近年铁皮价格波动较大,极大压缩了企业利润空间,不利于企业稳定健康发展。当前利用钛白副产硫酸亚铁(以下简称“废副亚铁”)生产铁系颜料,往往局限于利用液相法生产氧化铁黑,对于液相法生产氧化铁黄的研究,其氧化过程中和酸所用的碱通常是氨水,中和后产生的硫酸铵回收成本高,处理难度大,处理不好容易造成严重的环境问题。笔者研究设计了以废副亚铁和工业纯碱为主要原料,采用全液相法生产氧化铁黄的工艺流程,该法在取得经济效益与环境效益的同时,易于实现全自动化控制。
1 液相法制备氧化铁黄工艺
1.1 主要原料
硫酸亚铁为铜陵本地钛白粉生产企业废副硫酸亚铁,纯碱和液碱系工业级原料。具体指标如下,硫酸亚铁:w(FeSO4·H2O)=85.20%;w(MgSO4·H2O)= 3.52%;w(MnSO4·H2O)=0.96%;w(TiO2)=0.58%;w(H2O)=6.30%;w(水不溶物)=2.54%。工业纯碱:w(Na2CO3)=98.50%;w(NaCl)=0.45%;w[硫酸盐(以SO42-计)]=0.02%;w(水不溶物)=0.02%;w(铁)= 0.003%;堆密度=0.88 g/cm3。工业液碱:w(NaOH)= 29.95%;w(NaCl)=5.02%;w(Na2CO3)=0.4%;w(Fe2O3)=
0.003%;密度=1.35 g/cm3。
1.2 废副亚铁净化
1.2.1 反应原理
TiOSO4+3H2O→Ti(OH)4↓+H2SO4
Fe+H2SO4→FeSO4+H2↑
Fe+Fe2(SO4)3→3FeSO4
1.2.2 工艺流程
在亚铁水解池中先加入过量铁粉,之后加水,用蒸汽加热升温,加入废副亚铁,在亚铁水解池溢流口处加絮凝剂,经自然沉降后,泵送至隔膜压滤机,滤液直接泵送至硫酸亚铁储罐备用,滤渣主要为钛渣,送至钛白生产企业加以重复利用。
1.3 铁黄晶种制备
1.3.1 反应原理
FeSO4+2NaOH→Fe(OH)2↓+Na2SO4
4Fe(OH)2+O2→4FeOOH↓+2H2O
1.3.2 工艺流程
将储罐中的硫酸亚铁泵送至晶种桶,加入30%(质量分数)的工业氢氧化钠,补水适量,pH调至4左右,通入少量并分布均匀的空气氧化,反应液先后经过墨绿色、灰绿色,直至料浆变成青黄色,晶种制备完成。
1.4 铁黄生成
1.4.1 反应原理
4FeSO4+O2+6H2O→4FeOOH↓+4H2SO4
H2SO4+Na2CO3→Na2SO4+H2O+CO2↑
1.4.2 工艺流程
液相法生产氧化铁黄,是在氧化桶中加入晶种,补水适量,通蒸汽升温至82℃左右,直接通空气氧化,并不断向氧化桶中补充硫酸亚铁溶液,使体系亚铁质量浓度为60~70 g/L,同时用5%(质量分数)的工业纯碱溶液(由工业纯碱固体粉末配制而成)中和氧化过程中生成的硫酸,以维持反应体系的pH为3~4,如此反应继续到反应终点。在整个氧化过程中,要严格控制反应温度、空气流量、亚铁浓度、工业纯碱浓度等工艺参数。完整工艺流程图见图1。
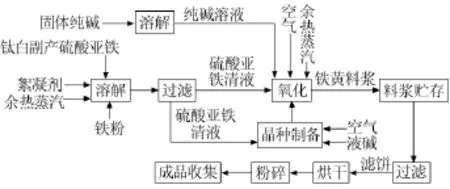
图1 液相纯碱法氧化铁黄工艺流程图
1.5 实验产品表征分析
1.5.1 产品技术指标
产品色光以铜陵瑞莱科技有限公司生产的铁黄920产品为标样,a、b值要求范围±0.5,详细数据见表1,产品技术指标见表2。
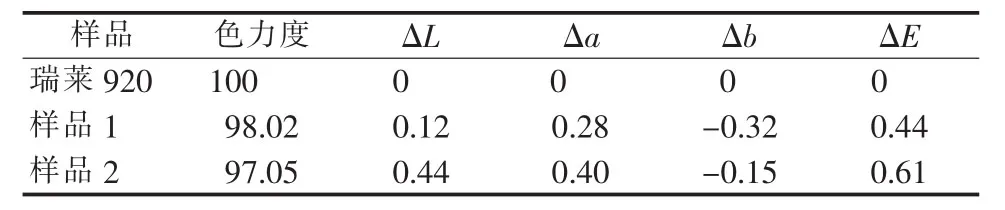
表1 产品色光数据

表2 产品技术指标
1.5.2 扫描电镜检测实验产品形貌
图2为传统方法生产的氧化铁黄产品的扫描电镜图,图3是在最佳条件下生产的氧化铁黄产品放大3万倍的扫描电镜图。通过比较图2和图3可看出,实验产品的晶体颗粒均匀分布在一起,呈针状结构,大大增强了颜料的着色力。

图2 氧化铁黄的扫描电镜图

图3 实验产品氧化铁黄的扫描电镜图
2 影响氧化因素的分析
保证晶种质量的前提下,氧化过程中影响产品质量的因素有温度、pH、空气量、纯碱浓度及氧化桶内的亚铁浓度。
2.1 氧化过程中温度的影响
固定pH、空气量、纯碱浓度及氧化桶内亚铁浓度进行单一变量实验,结果见表3。
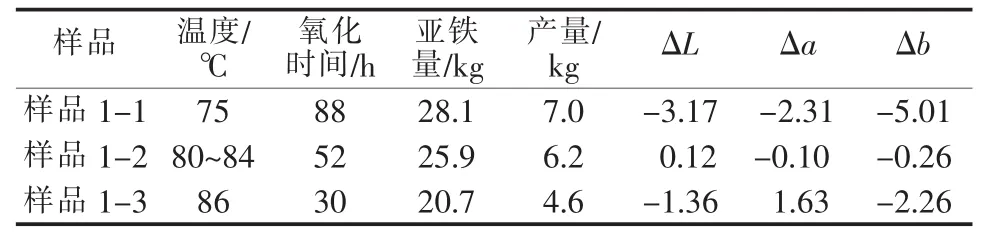
表3 温度对产品色光的影响
由上述实验对比数据可得出:温度控制在80~84℃范围内,形成的氧化铁黄色光最接近标样。如温度过高,Fe2+扩散速度加快,使向结晶中心扩散的Fe2+还未被氧化就进入晶格,产生黑色Fe3O4,同时会造成氧化时间缩短,单位产量降低,Δa值偏大,即产品偏红相。维持较低温度,则产生γ-FeOOH,且反应时间大大延长,产品色相萎暗。反应温度与产品色光关系图见图4。
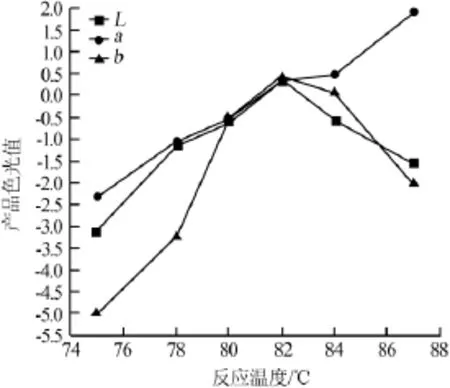
图4 反应温度与产品色光关系图
2.2 pH对产品色光的影响
控制单一变量pH,其他条件均不变,结果见表4和图5。
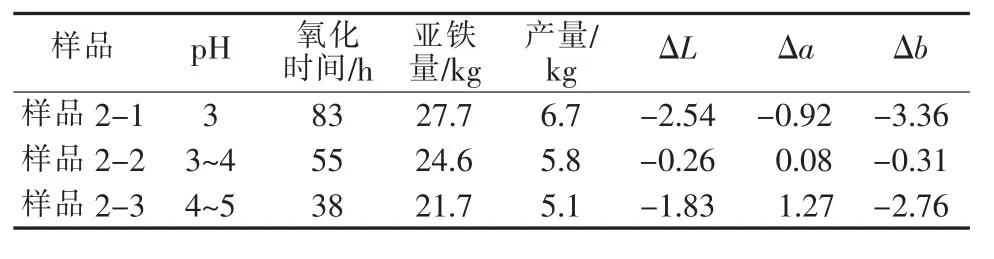
表4 pH对产品色光的影响

图5 pH与产品色光关系图
由表4及图5可得出,pH太低,氧化反应进程太慢,进而延长反应时间,色光较暗,且pH过低会导致铁黄分解,而降低产率(pH与氧化铁黄产率关系见图6)。若pH较高,氧化反应速度过快,不易控制反应终点,而且产品颜色发暗,因此氧化过程中pH一般控制在3~4较为合适。
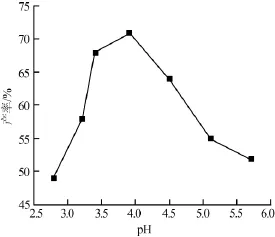
图6 pH与氧化铁黄产率关系
2.3 纯碱浓度对氧化的影响
纯碱质量分数选择为2%、5%、10%,其他均为最优条件,结果见表5。

表5 纯碱浓度对氧化的影响
图7为纯碱浓度与产品色光关系。由表5和图7可得:纯碱浓度较高,在氧化中和时,滴落点pH偏高,产生黑色Fe3O4,最终反应结束时物料色相偏暗,影响产品质量。使用低浓度纯碱,对产品色相虽无较大影响,但会将大量的水带入氧化体系中,增大动力消耗及降低单位产量。因此,纯碱最佳质量分数为5%左右。

图7 纯碱浓度与产品色光关系
2.4 氧化体系中硫酸亚铁含量对氧化的影响
除氧化体系中亚铁浓度外,其他均为最佳条件,结果见表6。
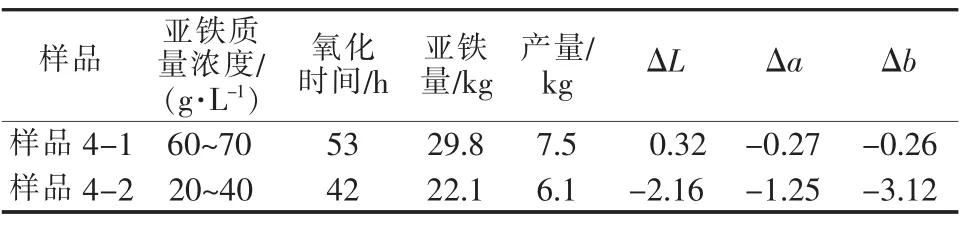
表6 硫酸亚铁含量对氧化的影响
图8为亚铁浓度与产品色光关系。从表6和图8可知:亚铁浓度较低时,产品色相暗淡,黄相较差。如果亚铁浓度较高,则后期滤液处理难度会加大。因此氧化体系中最佳亚铁质量浓度控制在60~70 g/L。
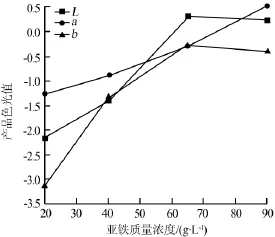
图8 亚铁浓度与产品色光关系
2.5 空气量的控制
氧化过程中,相比于传统工艺气、液、固三相之间的反应,本工艺具有先进性。传统生产方法使用铁皮,空气阻力大,分布不均;此方法使用碳酸钠作为中和剂,反应介质为液相,空气分布均匀,利于反应进行。具体空气量影响因素见表7。

表7 空气量的影响
图9为空气量与产品色光关系。结果表明:空气量过大时,会使得晶体生长过快,形成疏松而不规则的晶体,影响产品的着色力,且Δa偏大即色相偏红。空气量较小时,色光较暗,反应时间长。因此空气量控制在130 L/h较好。

图9 空气量与产品色光关系
3 结论
按照本工艺确定的条件,可生产出质量优良的氧化铁黄产品。与铁皮法相比,本工艺氧化阶段是气-液间的反应,易于实现自动化,且生产成本降低30%左右,拓宽了企业盈利空间。与传统氨水液相法相比,本工艺不存在含氮废水的问题,降低了污水处理成本,更经济环保,符合现代所倡导的绿色化工理念。综上所述,本工艺有成本低、无污染的特点,具有较好的经济、社会和环境效益。
[1]朱骥良,吴申年.颜料工艺学[M].2版.北京:化学工业出版社,2002:225-228.
[2]胡兵,龙化云,黄光斗.均匀沉淀法制备超微细透明氧化铁黄颜料[J].湖北工学院学报,2003,18(1):53-55.
[3]黄坚,龚竹青,冯刚.氯酸钠氧化法制备超细氧化铁黄的研究[J].广州化学,2007,32(2):17-21.
[4]胡鸿飞,李大成,吉红兵.纳米氧化铁的制备方法及进展[J].四川有色金属,2001(1):15-20.
[5]陈玉杰,魏琦峰.透明氧化铁黄制备工艺现状[J].上海涂料,2009,49(7):16-19.
联系方式:sunxiaoqing7648@sina.com
Study on iron oxide yellow prepared by liquid phase soda ash process
Yao Zuosheng,Sun Xiaoqing,Du Songsong
(Tongling RuilaiTechnology Co.,Ltd.,Tongling 244000,China)
Iron oxide yellow was produced by liquid phasemethod with the by-product ferrous sulfate of titanium white production and industrial soda ash asmain rawmaterials.In the presence of the crystal seed,ferrous sulfatewas oxidized by the air,and ferrous sulfate and soda ash were continuously added dropwisely in the reaction process.Series of iron oxide yellow products could be obtained from lightyellow to dark yellow bymaintaining ferrous concentration and pH and through controlling the colored lightprogress.The successof this technology research and developmenthad good social,economic,and environmentalbenefits.
by-product ferroussulfate of titanium white;liquid phasemethod;iron oxide yellow;soda ash
TQ138.11
A
1006-4990(2014)10-0046-04
2014-04-25
姚佐胜(1961—),男,本科,高级工程师,从事技术管理、规划发展、科研开发等工作,已发表论文10篇。
