pH敏感性葡萄糖印迹水凝胶的制备
2014-05-03吴淑梅何艳芬张卫英徐寅超林美露
吴淑梅,何艳芬,张卫英,徐寅超,林美露,李 晓
(福州大学 化学化工学院,福建 福州 350108)
水凝胶吸水溶胀但不溶解,兼有液体和固体的性质[1-3]。同时,水凝胶结构中存在大量的功能性基团,可作为吸附分离材料广泛应用于农林、园艺、医药、石油化工、建材、日用品和化妆品等领域[4-8]。目前,世界上至少有3.66亿人患有糖尿病,控制血糖浓度进而改善糖尿病患者的生活质量受到人们的高度关注[9-11]。口服葡萄糖吸附剂是控制血糖浓度的一种有效途径。葡萄糖吸附剂经胃进入小肠后,在肠内吸收糖分再排出体外,从而减少人体对糖的吸收[12]。纤维素、甲壳胺等天然高分子凝胶已用于葡萄糖吸附[13-14],但缺乏对胃肠pH差异的响应性,合成pH敏感性葡萄糖吸附凝胶的研究鲜见报道。
分子印迹是一种制备对目标分子具有识别性的功能高分子材料的新技术[15-16]。本工作采用简单、无毒的单体,同时引入pH敏感基团,并结合分子印迹技术,制备对环境pH具有敏感性、对葡萄糖具有较强吸附作用的葡萄糖印迹水凝胶,为进一步研究餐后血糖控制及智能给药体系提供一种新的材料。
1 实验部分
1.1 主要试剂及仪器
α-甲基丙烯酸(MAA):化学纯,国药(集团)上海化学试剂公司;甲基丙烯酸羟乙酯(HEMA):化学纯,三菱化工有限公司:丙烯酰胺(AM):分析纯,天津市大茂化学试剂厂;乙二醇二甲基丙烯酸酯(EGDMA):化学纯,Fluka公司;过硫酸铵(APS):分析纯,广东省化学试剂工程技术研究开发中心;二甲基亚砜(DMSO):分析纯,天津市福晨化学试剂厂;柠檬酸:优级纯,广东省化学试剂工程技术研究开发中心;十二水合磷酸氢二钠:分析纯,西陇化工股份有限公司;邻甲基苯胺:优级纯,上海晶纯试剂有限公司;葡萄糖:分析纯,国药集团化学试剂有限公司。
CL-200型集热式恒温加热磁力搅拌器:巩义市英峪予华仪器制造厂;Cary50型紫外-可见分光光度计:Varian公司;SHA-B型医用恒温振荡器:国华电器有限公司;510型pH计,EUTECH公司。
1.2 pH敏感性水凝胶的制备
称取一定质量的功能单体HEMA,MAA,AM于烧杯中,加入一定体积的水,室温下搅拌5 min;再加入一定量的交联剂EGDMA和引发剂APS,室温下继续搅拌10 min。将上述溶液转移到试管中,通氮10 min,密封,60 ℃下反应16 h,生成水凝胶。取出水凝胶切成小块,放于蒸馏水中浸泡,每隔一段时间换一次蒸馏水,然后置于50 ℃下真空干燥至恒重,即得pH敏感性水凝胶(即非印迹水凝胶,简称NIP)。
1.3 葡萄糖印迹水凝胶的制备
称取一定质量的葡萄糖与功能单体HEMA,MAA,AM于烧杯中,加入溶剂DMSO和水共10 mL,室温下搅拌5 min;再加入一定量的交联剂EGDMA和引发剂APS,室温下继续搅拌10 min。将上述溶液转移到试管中,通氮10 min,密封,60 ℃下反应16 h,生成水凝胶。取出水凝胶切成小块,放于甲醇-乙酸(体积比4∶1)洗脱液中洗脱葡萄糖,每隔2 h换一次洗脱液,然后用甲醇洗至中性,于50 ℃下真空干燥至恒重,即得葡萄糖印迹水凝胶(简称MIP)。
1.4 水凝胶溶胀度的测量
准确称取若干份一定质量(m0)的干凝胶,分别加入不同pH的磷酸氢二钠-柠檬酸缓冲溶液中,溶胀24 h后取出,用滤纸擦干表面溶液,称量溶胀后的水凝胶质量(m1),按式(1)计算水凝胶的溶胀度(SR):

1.5 水凝胶吸附量的测量
将NIP或MIP置于50 mL葡萄糖水溶液(质量浓度2 g/L)中,室温下振荡吸附24 h,采用邻甲基苯胺分光光度法测量剩余吸附液中葡萄糖的质量浓度[17],根据吸附前后葡萄糖质量浓度的变化计算水凝胶对葡萄糖的平衡吸附量Q(mg/g),并按式(2)计算印迹因子(α)。α体现了MIP与NIP在分子识别上的差异,α越大表明印迹效果越好。

式中,QI,QN分别为MIP和NIP对葡萄糖的平衡吸附量,mg/g。
2 结果与讨论
2.1 功能单体及交联剂用量对NIP溶胀度的影响
2.1.1 功能单体AM用量的影响
考察了不同AM用量时NIP溶胀的pH响应性,实验结果见图1。

图1 AM用量对NIP溶胀度的影响Fig.1 Effects of acrylamide(AM) dosage on the swelling ratio(SR) of pH-sensitive hydrogels(non-imprinted hydrogels,NIP).
由图1可见,NIP的溶胀度随缓冲溶液pH的增加先减小后增大;当pH达到7左右时,溶胀度变化不明显。这是由于在酸性介质中,随溶液酸性的增强,水凝胶分子链上酰胺基的质子化程度加大,水化作用增强,更多的水分子渗透到水凝胶内部,使得水凝胶的溶胀度变大。当pH>5时,虽然酰胺基的质子化能力减弱,但酰胺基逐渐水解生成羧基,羧基离解使水凝胶的亲水性更强,随pH的增加酰胺基的水解程度提高,故溶胀度显著增大。当pH=6~7时,羧基的离解度接近最大值,故溶胀度的变化趋于平缓。从图1还可看出,AM用量对NIP溶胀度有一定的影响,当pH较低时,NIP溶胀度随AM用量的增加呈先增后减的趋势,当AM用量为总单体质量的2%时,NIP的溶胀度最大。
2.1.2 功能单体MAA用量的影响
考察了不同MAA用量时NIP溶胀的pH响应性,实验结果见图2。由图2可见,NIP的溶胀度随缓冲溶液pH的增加基本呈先增后减的趋势,pH=6~7时溶胀度接近最大值。这是由于MAA含有可离子化的羧基基团,当pH逐渐增大时,水凝胶分子链上羧基基团的离子化程度增强,水凝胶的分子内氢键作用减弱,使得水凝胶的溶胀度变大;当pH增大到一定值后,可离子化羧基基团的离解度达到最高值,水凝胶的溶胀度达到最大值;继续增大pH,由于溶液中的离子浓度大于水凝胶内部的离子浓度,导致水凝胶失水收缩,溶胀度减小。由图2还可看出,NIP的溶胀度与MAA用量有关,当pH=6~7时,MAA用量越多,溶胀度越大。这是因为MAA用量越多,羧基基团的离子化效应越显著。

图2 MAA用量对NIP溶胀度的影响Fig.2 Effects of MAA dosage on the swelling ratio of NIP.
2.1.3 交联剂EGDMA用量的影响
交联剂是制备水凝胶的重要成分,交联剂用量会影响水凝胶的刚性和溶胀性。考察了不同交联剂用量时NIP溶胀的pH响应性,实验结果见图3。
由图3可见,NIP的溶胀度随交联剂EGDMA用量的增加呈减小的趋势。这是因为:当交联剂用量较少时,水凝胶的空间网络疏松,容易接纳更多的水;当交联剂用量少时,有更多的化学点与水分子作用。但交联剂用量过少时,水凝胶的空间网络难以形成,导致水凝胶的刚性不足。当交联剂用量增加时,水凝胶中的交联点增多,交联点间距变小,水凝胶的网络空间变小,溶胀度减小,但水凝胶的刚性较强。

图3 EGDMA用量对NIP溶胀度的影响Fig.3 Effects of EGDMA dosage on the swelling ratio of NIP.
2.2 NIP的pH响应可逆性
水凝胶的pH响应可逆性是指水凝胶能根据环境pH的变化而发生可逆的收缩和溶胀。选取3个不同交联度的NIP,考察其pH响应可逆性。先将NIP置于pH=7.0的缓冲溶液中溶胀24 h,然后移入pH=2.0的缓冲溶液中溶胀24 h,最后再置于pH=7.0的缓冲溶液中溶胀24 h,分别测其溶胀度,测量结果见表 1。

表1 NIP在缓冲溶液中的pH响应可逆性Table 1 Reversibility of the response to pH of NIP in buffer solution
由表1可见,NIP在缓冲溶液中具有明显的pH响应可逆性。当缓冲溶液pH=7.0时,由于羧基基团离解,NIP的亲水性增强,溶胀度变大;将NIP置于酸性溶液中之后,羧基基团的离解度下降,NIP的水化作用减弱,导致其收缩;而后又置于pH=7.0的缓冲溶液中,羧基基团又发生离解,NIP的亲水性增强,溶胀度变大。由此可见,NIP的收缩和溶胀与缓冲溶液的pH有关。
2.3 功能单体对MIP吸附性的影响
分别采用MAA和AM以及两者的混合物为功能单体制备了MIP与相应的NIP,考察两者对葡萄糖的吸附性,实验结果见表2。

表2 功能单体对MIP吸附效果的影响Table 2 Effects of the functional monomers on the adsorption of imprinted hydrogel(MIP)
从表2可看出,以MAA为功能单体制备的MIP对葡萄糖具有较好的识别性,其印迹因子达到1.73;以MAA和AM混合物为功能单体制备的MIP,其印迹因子降至1.15,明显小于以MAA为功能单体制备的MIP;而以AM为功能单体制备的MIP,其印迹效果最差,印迹因子仅为0.28。这是由于MAA分子上—COOH与葡萄糖分子上—OH的作用比AM分子上—NH2与葡萄糖分子上—OH的作用更强,因此以MAA为功能单体制备的MIP对葡萄糖的吸附量较高;而以MAA和AM混合物为功能单体制备的MIP,由于—COOH与—NH2之间消耗了部分氢键,导致它们与葡萄糖分子上—OH的结合数量减少,进而使吸附量降低。因此,采用MAA为功能单体制备的MIP印迹效果最好。
2.4 MIP的pH响应性
MIP内部存在具有特异识别性的孔穴,可能会导致MIP的空间网络结构不同于NIP,进而引起MIP与NIP在pH响应性方面存在差异。
图4(a)和(b)分别是以MAA以及MAA和AM混合物为功能单体制备的MIP和NIP在不同pH下的溶胀度。
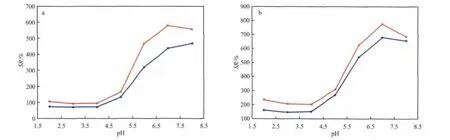
图4 MIP和NIP在不同pH下的溶胀度Fig.4 Swelling ratios of MIP and NIP at different pH.Reaction conditions referred to Table 2.
从图4可看出,随缓冲溶液pH的增大,MIP和NIP的溶胀度变化趋势一致,说明MIP与NIP具有相似的pH响应性;但在相同pH下,MIP的溶胀度小于NIP的溶胀度。这是因为MIP洗脱葡萄糖后,在其内部留下了识别葡萄糖的孔穴,该孔穴的存在限制了MIP的溶胀,导致MIP的溶胀度小于相应的NIP。
3 结论
1)以HEMA,MAA,AM为功能单体,EGDMA为交联剂,采用溶液聚合法合成了NIP。功能单体和交联剂的用量对合成的NIP的pH响应性均有不同程度的影响,且所合成的NIP在缓冲溶液中具有明显的pH响应可逆性。
2)在NIP的基础上制备了MIP,以MAA为功能单体制备的MIP具有较好的印迹效果,印迹因子可达1.73,且MIP的pH响应性与NIP一致,但其溶胀度小于NIP。
[1]Hoffman A S.Hydrogels for Biomedical Applications[J].Adv Drug Deliv Rev,2002,54(1):3-12.
[2]秦绪平,赵芳,冯圣玉.高力学强度水凝胶的研究进展[J].高分子材料科学与工程,2012,28(3):174-178.
[3]Lehto J,Vaaramaa K,Vesteinen E,et al.Uptake of Zine,Nickel,and Chromium by N-Isopropylacrylamide Polymer Gels[J].J Appl Polym Sci,1998,68(3):355-362.
[4]杨振,杨连利.水凝胶的研究进展及发展新动向[J].化工中间体,2007(1):5-10.
[5]孙波,米镇涛,邵仕香,等.微波法合成聚天冬氨酸水凝胶及其对Pb2+的吸附性能[J].石油化工,2004,33(12):1168-1172.
[6]Peppas N A,Hilt J Z,Khademhosseini A,et al.Hydrogels in Biology and Medicine:From Molecular Principles to Bionanotechnology[J].Adv Mater,2006,18(11):1345-1360.
[7]王锦堂,仲慧.温敏性水凝胶对蛋白质和酶浓缩分离性能[J].南京化工大学学报,1998,20(2):75-77.
[8]查刘生,王秀琴,邹先波,等.智能纳米水凝胶的制备及其刺激响应性能和应用研究进展[J].石油化工,2012,41(2):131-142.
[9]McCowen K C,Malhotra A,Bistrian B R.Stress-Induced Hyperglycemia[J].Crit Care Clin,2001,17(1):107-124.
[10]Matz K,Keresztes K,Tatschl C,et al.Disorders of Glucose Metabolism in Acute Stroke Patients[J].Diabetes Care,2006,29(4):792-797.
[11]张拥军.葡萄糖敏感高分子水凝胶材料[J].中国医疗器械信息,2009,15(5):18-20.
[12]Tennison S R.Phenolic-Resin Derived Activated Carbons[J].Appl Catal,A,1998,173(2):289-311.
[13]许素新,刘廷岳.离子交换纤维对桑叶多糖静态吸附和解吸的研究[J].时珍国医国药,2011,22(8):1943-1945.
[14]李沁华,刘宇涛,邹翰,等.以聚乙二醇为致孔剂的甲壳糖吸附、缓释葡萄糖的研究[J].暨南大学学报:自然科学与医学版,1995,16(3):81-84.
[15]Katz A,Davis M E.Investigations into the Mechanisms of Molecular Recognition with Imprinted Polymers[J].Macromolecules,1999,32(12):4113-4121.
[16]Nadia Adrus,Mathias Ulbricht.Molecularly Imprinted Stimuli-Responsive Hydrogels for Protein Recognition[J].Polymer,2012,53(20):4359-4366.
[17]曹培义,刘健,王继业.邻甲苯胺分光光度法测定甜饮料中的葡萄糖[J].职业与健康,2001,17(8):45-46.
