动态浊度法测定阿奇霉素中细菌内毒素含量
2014-05-02祝清芬范治云史国生
张 娟,祝清芬,范治云,魏 霞,史国生
(山东省食品药品检验研究院,山东 济南 250101)
阿奇霉素为大环内酯类抗生素,与红霉素的化学结构和作用机制有共同点,属抑菌性抗生素,对酸稳定,半衰期长[1],有较高的生物利用度。它可通过与细菌核糖核蛋白体的50 s亚单位结合妨碍肽链的延长,影响细菌蛋白合成而达到抑菌作用。其应用方便、疗程短、疗效肯定,具备理想抗生素的条件,对青霉素过敏及儿科患者更有实际意义[2]。其临床用于治疗各种敏感性细菌引起的上呼吸道感染、泌尿道感染和皮肤软组织感染[3-5]。细菌内毒素检查法是控制药物注射剂重要的安全性指标[6]。阿奇霉素的质量标准(内部标准)中规定了细菌内毒素检查项,限值规定应小于0.2 EU/mg。在实际工作中发现,某些样品由于pH等原因,对凝胶法细菌内毒素检查有明显的干扰作用。本试验中参照2010年版《中国药典(二部)》[7]细菌内毒素检查方法中的动态浊度法,对阿奇霉素中的细菌内毒素定量检测进行了研究,以寻求一种快速、准确的定量检测方法。
1 仪器与试药
BET-48G型细菌内毒素测定仪(天大天发科技有限公司);ZH-2型自动漩涡混合器(天津药典标准仪器厂);试验用试管、刻度吸管等玻璃器材按规定清洗,250℃干烤1 h除去外源性内毒素。阿奇霉素原料(烟台只楚药业有限公司,批号分别为1205004,1205005,1205006);细菌内毒素工作标准品(中国食品药品检定研究院,批号为150601-201174,规格为每支160 EU);细菌内毒素检查用水(BET用水,湛江安度斯生物有限公司,批号为1209030,规格为每支5 mL);动态浊度法鲎试剂(湛江安度斯生物有限公司,批号为1301212,可测内毒素范围0.01~10EU/mL,规格为 1.25 mL,有效期至2015年12月)。
2 方法与结果[7-9]
2.1 细菌内毒素标准曲线的建立和可靠性分析
设定标准曲线各点浓度为 2.0,0.5,0.125,0.03125 EU/mL。用BET用水稀释细菌内毒素标准品,使其最终浓度分别为2.0,0.5,0.125,0.03125 EU/mL,各取 0.1 mL,分别加至预先加有0.1 mL鲎试剂的反应管内,混合均匀,插入BET-48G型细菌内毒素检测仪进行检测,每个浓度重复3管,同时做阴性对照(NC)。以平均反应时间的对数(lg T)为纵坐标、内毒素浓度的对数(lg C)为横坐标绘制标准曲线,得回归方程lg T=-0.2369 lg C+2.8123,r=-0.9989(绝对值应大于 0.980),平行管之间的 RSD 均小于10%,阴性对照的反应时间大于标准曲线最低浓度的反应时间,细菌内毒素标准曲线成立。结果见表1。
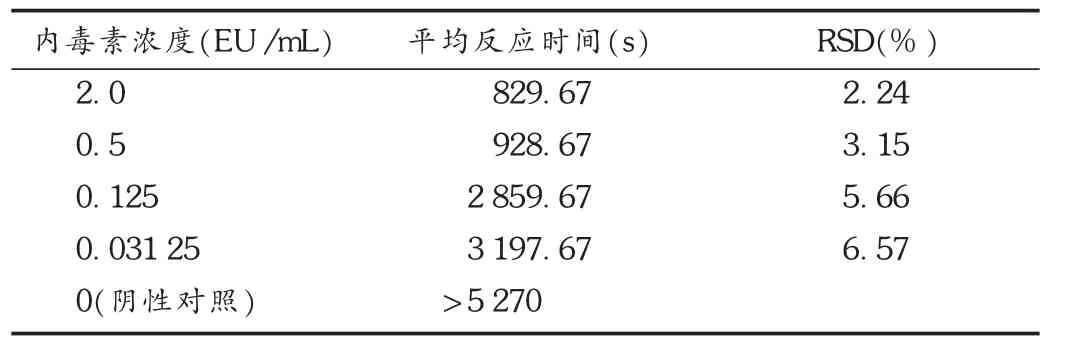
表1 细菌内毒素标准曲线及可靠性分析结果(n=3)
2.2 供试品制备及最小有效稀释质量浓度的确定
阿奇霉素在水中几乎不溶,在甲醇、丙酮、三氯甲烷、无水乙醇或稀盐酸中易溶。先采用0.05 mol/L稀盐酸溶解供试品,制得25 g/L的供试品溶液,用1 mol/L氢氧化钠溶液调节 PH至中性。本品细菌内毒素限值(L)为 0.2 EU/mg,标准曲线最低浓度(λ1)为 0.03125 EU/mL,供试品的 MVD = CL/λ1=160 倍,及最小有效稀释质量浓度为0.15625 g/L。
2.3 干扰试验
根据标准曲线内毒素浓度的设置,选择0.25EU/mL作为 λm。选择批号为1205004的阿奇霉素,用0.05 mol/L稀盐酸溶解供试品,制得25 g/L的供试品溶液,用1 mol/L氢氧化钠溶液调节pH至中性。用BET用水进行稀释,使其终质量浓度分别为2.5,1.25,0.625,0.3125,0.15625 g/L,作为供试品溶液(A 液),同时制备含上述供试品质量浓度并含内毒素浓度为 λm(0.25EU/mL)的溶液(B液)。分别取上述各液0.1 mL,加至预先加有 0.1 mL鲎试剂的反应管内,混合均匀,插入仪器内测定,每个浓度重复2管。测定结束后,按标准曲线回归方程分别计算出供试品溶液和含标准内毒素 λm的供试品溶液的内毒素含量,并计算该试验条件下的回收率(R)。结果见表 2。

表2 供试品干扰试验及供试品细菌内毒素测定结果(n=2)
由表 2可见,2.5 g/L及以下质量浓度时,回收率均在50%~200%,符合要求,因此建议采用2.5 g/L及以下质量浓度进行试验。另取批号为1205005和1205006的两批样品,分别制备2.5 g/L供试品稀释液(A液)和浓度相同的供试品且含内毒素浓度 λm(0.25 EU/mL)的溶液(B 液),依法检查。结果见表 2,B液回收率均在50%~200%,符合要求。
3 讨论
在2010年版《中国药典(二部)》中,阿奇霉素口服制剂有明确的标准规定,而对注射剂目前还没有相应标准。化学药品注射剂安全性检查法应用指导原则中规定,静脉用注射剂均应设细菌内毒素(或热原)检查项。为此,本研究中运用动态浊度法对阿奇霉素进行干扰试验和细菌内毒素含量的测定。阿奇霉素在水中几乎不溶解,根据其对酸稳定的性质,本研究中采用0.05mol/L稀盐酸将其溶解,并将pH调至中性后,进行干扰试验和细菌内毒素检查,解决了其溶解性的问题。
由阿奇霉素的干扰试验结果显示,阿奇霉素可用细菌内毒素动态浊度法进行检测,样品质量浓度为2.5 g/L时,细菌内毒素回收率在50%~200%内,即对试验无干扰,且3批样品的内毒素含量均在规定限值0.2 EU/mg以下。
动态浊度法能直观地反映样品中细菌内毒素含量,检测过程及结果处理完全通过仪器执行,具有快速、大范围定量的特性,使干扰试验在1~2次试验后完成,节约成本,克服了凝胶法检验结果只能判断产品的内毒素含量是否超标,而无法给出准确的含量的不足,避免了热原法由于家兔差异及人为主观判断所出现的假阳性或假阴性结果[10-11]。运用动态浊度法测定阿奇霉素中细菌内毒素较以往用凝胶法具有更低的检测下限,可较准确地反应样品中内毒素的含量,值得推广。
参考文献:
[1]Amsden GW.Advanced-generation macrolides:tissue-directed antibiotics[J].Int JAntimicrob Agents,2001,18(Suppl 1):S11-S15.
[2]吕昭云,岳天辉,李淑斌,等.国产阿奇霉素的临床疗效及安全性[J].中国医院药学杂志,2004,24(5):305-307.
[3]Amsden GW,Gray CL.Serum and WBC pharmacokinetics of 1500 mg of azithromycin when given either as a single dose or over a 3 day period in healthy volunteers[J].JAntimicrob Chemother,2001,47 (1):61.
[4]陈亦芳,李 寨,郝凤兰,等.Azithromycin的体外抗菌作用[J].中国抗生素杂志,1995,20 (3):178.
[5]Blondeau JM.Theevolution and roleofmacrolides in infectiousdiseases[J].ExpertOpin Pharmacother,2002, 3(8):1131.
[6]蔡 彤,张国来,李 波,等.84种注射用药品细菌内毒素检查法的方法学研究[J].中国药学杂志,2010,45(2):150-155.
[7]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录 99,附录 212.
[8]中国药品生物制品检定所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2010:310-321.
[9]祝清芬,魏 霞.动态浊度法定量测定多西他赛注射液中细菌内毒素的含量[J].中国药房,2011,22(1):54-55.
[10]范能全.动态浊度法检测刺五加注射液的细菌内毒素[J].中国药师,2011,14(1):59-60.
[11]王莉蓓,陈华龙,姜丽君.动态浊度法定量检测血栓通注射液中细菌内毒素[J].齐鲁药事,2011,30(1):27-28.
