小核酸制药产业发展模式探索
2014-05-02寿晶晶刘姝晶孙全亮
寿晶晶,刘姝晶,陈 燕,孙全亮
(国家知识产权局知识产权发展研究中心,北京 100088)
小核酸通过RNA干扰(RNAi)阻碍特定基因的翻译或转录,抑制致病蛋白质的合成,可以从基因水平根治疾病[1-2]。基于小核酸的RNA干扰技术被认为是目前最具潜力的基因治疗方法,因此成为各国的新药创制热点[3]。作为一个新兴的制药领域,国内外企业在发展小核酸制药产业上具有不同的特点。笔者以小核酸制药技术的专利数据为切入点,结合产业信息,探讨国内小核酸产业的发展模式。
1 产业背景
1998年,华盛顿卡耐基研究院的科学家Fire和麻省大学医学院的Mello首次利用特别设计的RNA分子阻断了特定蛋白质的合成,此后RNA干扰(RNAi)迅速成为最常用的基础研究工具[4]。2006年,Fire和Mello因发现这一现象被授予了诺贝尔医学奖。随后,诺华、辉瑞、罗氏、葛兰素史克(GSK)、赛诺菲安万特、阿斯利康、武田和协和等国际医药巨头公司强力介入,争相在小核酸领域进行布局。截至2010年,国际医药巨头通过收购、投资合作、自行研发等方式投入近百亿美元用于小核酸药物研究,但由于技术研发上的问题,大型制药公司逐渐对RNAi技术失去了信心。
小核酸制药产业分为上游、中游、下游3个环节,上游环节指研发阶段,包括基础研究和药物发现;中游环节是药物开发阶段,包括临床前试验和临床研究等内容;下游环节指药物的生产和销售阶段(见图1)。从技术研发方向来看,整个小核酸药物的技术链由靶点筛选、小核酸设计、合成、递送和分析评价5个方面,其中药物生产阶段的技术主要指制剂的生产,包括合成和递送。

图1 小核酸产业链和技术链
RNA分子容易在体内发生降解,稳定性较差。RNA分子只有到达机体正确部位才能发挥作用,相应的运输技术也尚未解决。因此,针对提高RNA分子稳定性的设计技术和RNA分子体内运输的递送技术成为小核酸制药产业的发展瓶颈[5-6]。由于设计和递送的问题无法解决,默克、诺华和辉瑞等大型制药企业终止或延缓了小核酸药物研究项目。
近期RNA干扰药物在临床试验和药物输送技术上的进展使医药企业重拾信心,再度进行行业布局。2012年,赛诺菲宣布扩大与Alnylam公司(阿尔尼拉姆公司)在RNA干扰研究领域的合作,将投入约7亿美元收购后者约12%的股份。同期,罗氏公司与Santaris公司进行战略合作,首先投入1000万美元支持此项研究计划,并设立总额高达1.3亿美元的里程碑基金。Santaris公司宣布,和葛兰素史克公司及施贵宝公司建立了研发合作关系。2013年,Dicerna医药公司再次募资6000万美元用于RNA干扰抗癌技术的研发。同年,美国Arcturus公司投入了500万美元支持其从Marina生物技术公司获得的RNA干扰技术和自主研发的纳米载药系统。国际制药企业近期的动作表明,小核酸制药再度成为制药行业的热点,未来将加速发展。
从小核酸产业发展阶段来看,包括中国在内的全球小核酸制药产业正处于产业孕育期。全球小核酸制药产业的发展集中在药物开发阶段。国外小核酸制药公司目前已有二十几种小核酸药物处于临床Ⅰ期或Ⅱ期研究中,涉及癌症、糖尿病、呼吸系统、眼部疾病和神经系统疾病等领域的治疗药物。其他有170多项药物处于临床前研究中,目前尚无药物进入Ⅲ期临床试验。国内小核酸产业发展也已进行到临床研究阶段,相关药物近期将进入临床试验。从我国药物研发的成果来看,小核酸产业发展虽然稍落后于国外企业,但就发展现状来看仍处在同一阶段。见表1。

表1 全球小核酸药物研发进展
2 国外小核酸制药企业的发展模式
全球小核酸企业众多,但经过近几年的发展,基本形成了两类具有代表性的企业,一类是默克、辉瑞和诺华等跨国医药巨头,另一类是规模较小的小核酸制药技术研发企业,如阿尔尼拉姆公司和夸克公司等。两类企业的发展模式截然不同,但在技术布局上又存在着共同点。
1)阿尔尼拉姆公司
阿尔尼拉姆公司是美国一家小型的小核酸生物制药公司,也是小核酸技术研发的引领者,在小核酸药物开发领域具有较强的技术实力。目前,阿尔尼拉姆公司在小核酸技术方面的全球专利申请达146件[7],进入临床Ⅰ期、Ⅱ期和前临床阶段的小核酸药物品种近30个。阿尔尼拉姆公司的技术发展脉络见图2。
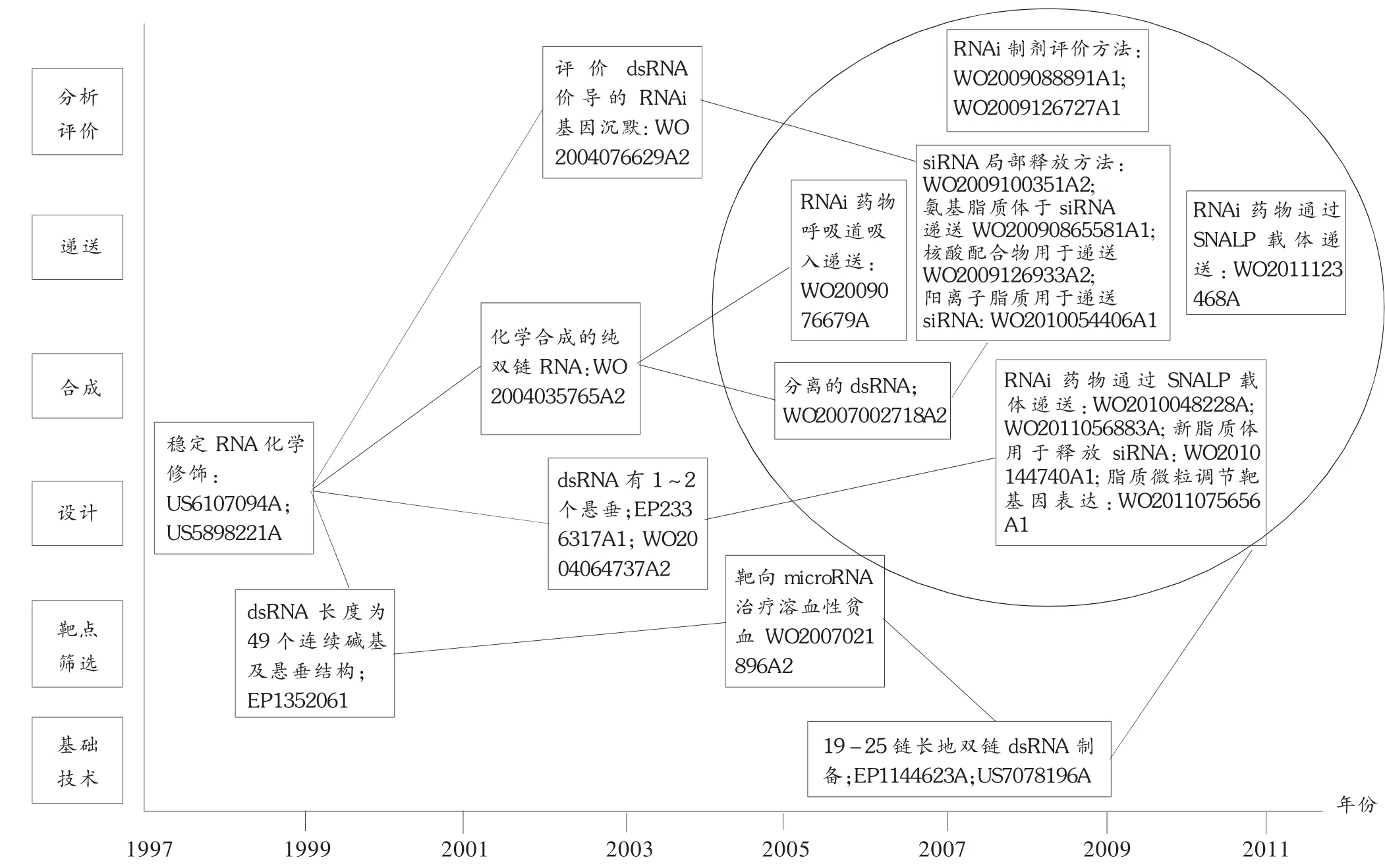
图2 阿尔尼拉姆公司技术脉络图
阿尔尼拉姆公司的专利技术主要通过自身研发获取。1997年,该公司首先掌握了设计领域的稳定RNA化学修饰技术;随后,研究领域向靶点筛选和小核酸合成技术领域扩展。2002年前,其技术研发主要集中在小核酸制药技术链的前端。
2003年开始,阿尔尼拉姆公司的研究领域除了靶点筛选、设计和合成,逐渐向递送技术和分析评价技术领域拓展,并于2003年获得了dsRNA介导的RNA干扰评价专利技术。2006年,获得RNA干扰药物呼吸道吸入的递送技术。在这段时期内,阿尔尼拉姆公司设计和合成领域的技术研发也逐渐向dsRNA方面扩展。2006年,由于图舍尔基础专利的保护范围较宽,出于回避风险和增强技术实力的目的,阿尔尼拉姆公司购买了图舍尔专利的全球独家许可权。可见,2003年至2007年是阿尔尼拉姆公司小核酸技术的扩张期,技术研究范围不断扩大,从技术链的前端延伸至后端,形成了完整技术链。
2007年后,阿尔尼拉姆公司的主要精力投入到了技术链后端的递送技术和分析评价技术领域,尤其是递送技术的研发。2008年取得了一系列突破,包括siRNA的局部释放技术,给药载体脂质体、核酸配合物、阳离子脂质和SNALP载体的制备。可见,2007年后的阿尔尼拉姆公司从大范围技术研发,集中到了关键技术的突破上,并在递送技术领域建立了较高的优势。
由于阿尔尼拉姆公司的规模较小,技术研发的集资投入主要来源于向其他企业授权许可其创始人所拥有的专利及初期研究成果而获得的转让费、特许权使用费或相关的预付费用等。通过与诺华、武田和GSK等众多医药大企业进行技术研发合作和专利许可协议等方式,累积吸引了十几亿美元的投资,支撑了企业后续发展。
因此,阿尔尼拉姆公司的发展采用纵向一体化发展模式[8],首先掌握前端环节的技术,随后技术不断向后端延伸,形成完整的技术链,再着力突破关键技术。
2)默克公司
默克公司是全球著名的医药跨国企业,从2000年开始进行小核酸药物开发技术的研发。截至2006年,默克公司在设计领域拥有申请专利5件,合成技术领域专利申请6件,递送技术方面专利申请4件,分析评价技术领域申请专利3件。从2006年各个技术环节的专利量上来看,默克公司在小核酸药物开发方面的技术实力并不强。
siRNA公司是较早从事小核酸药物开发技术研究的小型公司,但其技术实力较强。截至2006年,siRNA公司在设计领域拥有申请专利143件,合成技术领域专利申请10件,递送技术方面专利申请14件,分析评价技术领域申请专利4件。见表2。
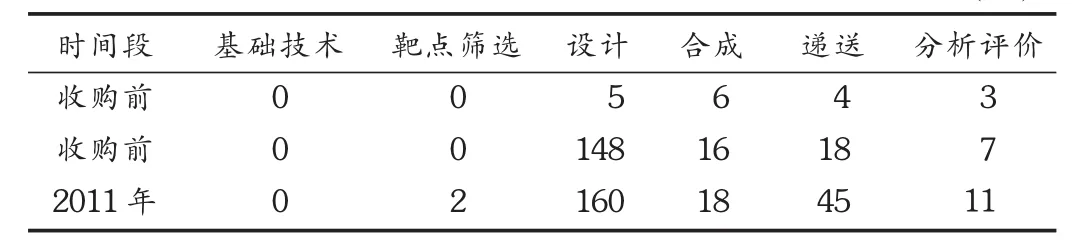
表2 2006年默克公司并购siRNA公司前后的专利申请量对比(件)
2006年,小核酸基因沉默技术发现者被授予诺贝尔奖,各大医药公司开始在小核酸制药领域频繁布局。出于公司战略布局考虑,默克公司2006年以11亿美元收购了siRNA公司。收购siRNA公司之后的默克公司拥有了小核酸药物开发技术完整的技术链,技术水平和研发实力显著增强。
因此,默克公司主要是凭借自身雄厚的资金实力,通过兼并小核酸技术研发企业迅速建立自身小核酸药物开发技术链,提高技术研发实力。实际上,类似于默克收购siRNA公司布局小核酸产业案例众多。这种横向兼并发展模式已成为全球医药巨头介入小核酸制药产业的主要途径。
3 国内小核酸制药企业现状
国内小核酸制药企业规模较小,如瑞博、百奥迈科等企业都属于小微型企业。受企业规模的限制,国内小核酸企业在技术研发模式上主要依靠自身技术创新,围绕某个技术环节进行突破,尚无企业具有完整的药物开发技术链。国内小核酸技术研发者的技术分布见表3。可见,专利技术分布在某一个或几个不同的技术环节上,如瑞博公司专利申请集中在靶点筛选、小核酸涉及和合成技术领域有专利申请,圣诺公司在递送技术方面相对有一定优势,但尚无技术能贯穿小核酸药物开发技术链。与国外制药企业在各技术环节广泛布局,同时又在递送技术环节进行技术储备的策略相比,国内技术研发者存在欠缺。

表3 国内主要申请人专利技术分布
4 国内小核酸制药产业发展模式分析
目前,我国小核酸制药产业在发展阶段上与国外相同,同处于产业孕育期。小核酸药物递送技术是制约国内外产业发展的主要瓶颈。国外发展重心在递送技术的突破上,国内重点在靶点筛选、合成和递送技术的研发。国内外小核酸产业发展现状比较见表4。
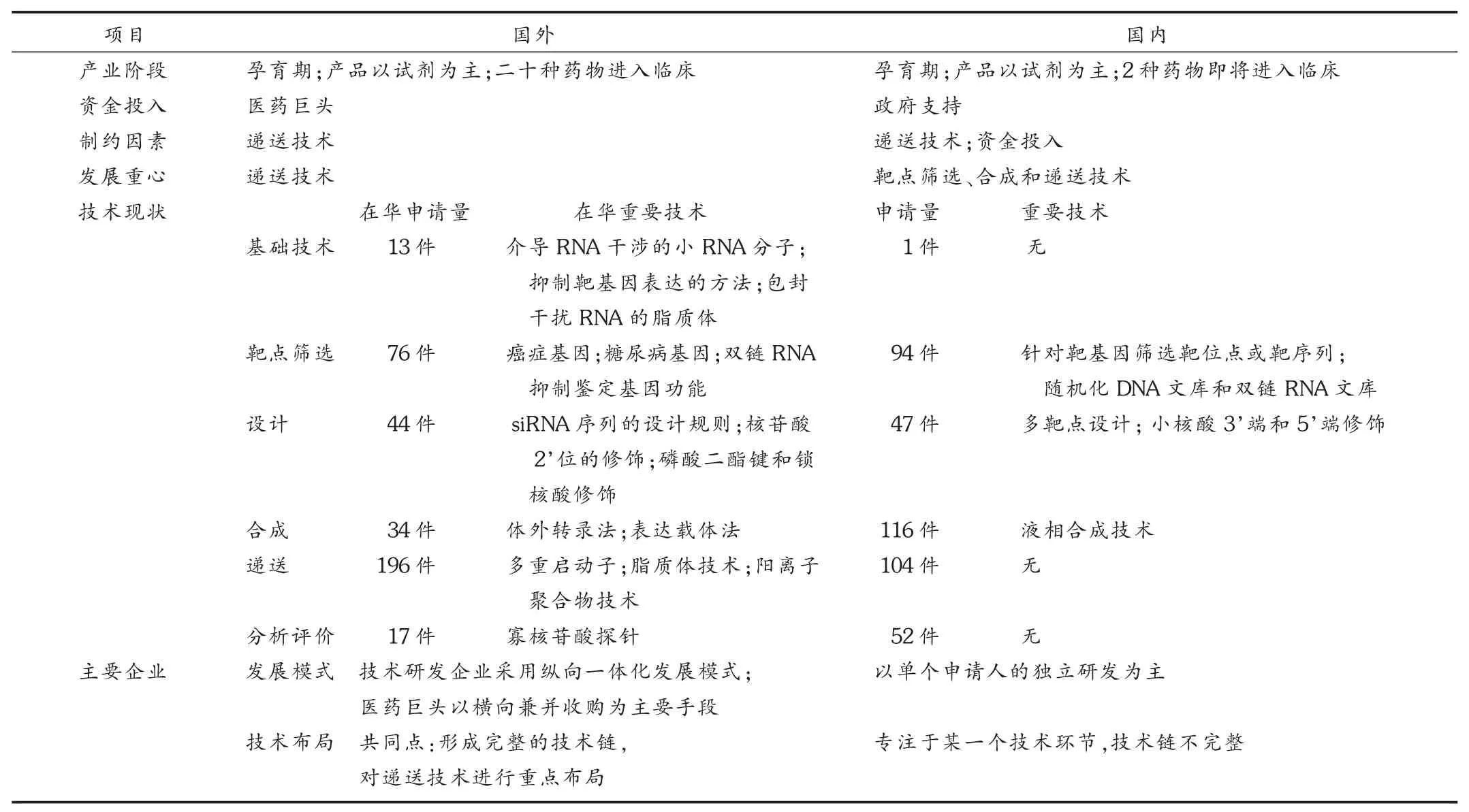
表4 国内外小核酸产业发展现状比较
与国外产业发展情况相比,我国小核酸产业发展具有两方面的优势,即靶点筛选、设计和合成领域的一些技术处于国际领先水平;国内技术研发者在各自专注的技术环节上具有技术特色。存在的问题有新药研发成本巨大,国内产业发展主要依靠政府支持,研发投入不足;单个企业技术链不完整,限制了药物的产品化;药物递送技术尚未取得突破;国外来华专利布局造成产业发展风险。这些问题制约着国内小核酸药物的产品化进程。
为实现追赶国外小核酸产业的发展步伐,谋求产业快速、良性发展的目标,急需解决目前产业发展中存在的问题和不足。从目前的发展现状来看,国内小核酸产业的主要需求是:掌握可行的小核酸药物开发技术,构建国内小核酸企业的完整药物开发技术链;保证技术的无风险实施,规避产业发展中潜在的专利风险。见图 3。
从构建国内小核酸企业药物开发技术链的角度来看,如阿尔尼拉姆公司的单一企业纵向一体化模式并不太适合我国小核酸产业的发展情况。首先,我国的生物医药产业发展相对于欧美及日本来说起步稍晚,虽然小核酸技术研究的某些方面已达到国际水平,但在技术的产业化方面,与国外先进水平相比还存在巨大差距。其次,目前我国小核酸企业规模小,尚未形成规模经济,而风险投资机制尚不完善,国内小核酸企业支撑着药物研发的巨额资金投入。
与纵向一体化模式相比,类似于默克公司的横向兼并模式相对具有可操作性。我国小核酸企业存在集中度低、企业规模小的特点,在发展过程中各自为阵的现象较为明显。横向兼并是小核酸企业做大做强的一种快速、直接、有效的途径,是企业整合国内现有技术资源的重要手段。规模相对较大的生物制药企业对一些具有发展潜力的小核酸企业进行兼并重组,不仅能为制药企业带来更多的优质资源,也能使企业具备更强大的实力,适当提高集中度及企业的影响力。横向兼并模式的主体是大型医药企业,但国内成熟医药企业对小核酸产业的关注程度不高,参与小核酸产业发展药企较少,因此通过引入国内大型医药企业对小核酸企业进行兼并重组,目前阻碍较大。
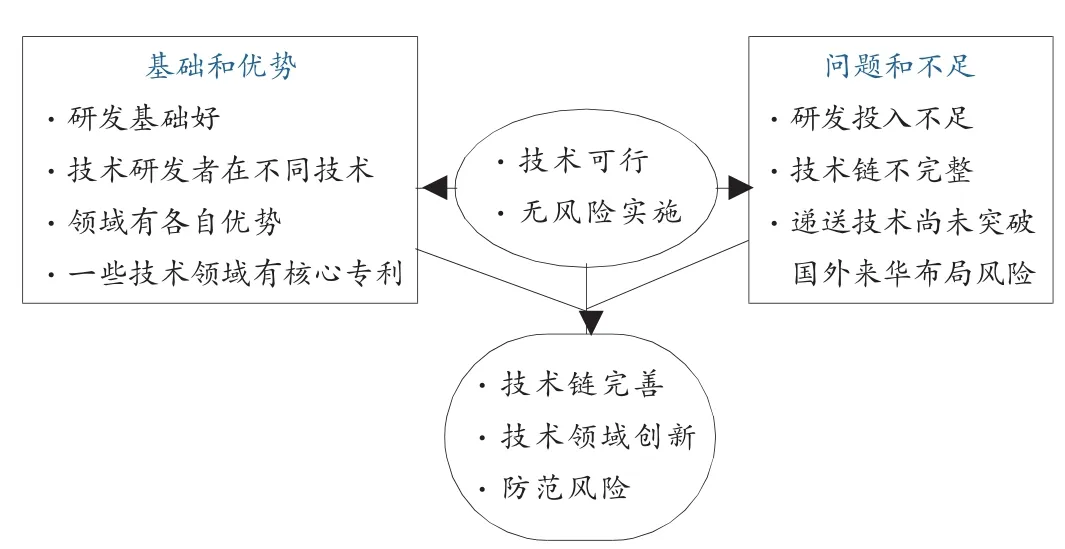
图3 国内产业发展需求
与以上两种模式相比,多主体共同参与的链式发展模式是一个较优的选择,见表5。这种模式的优势在于不同主体之间通过一定关系建立联系,共享资源和信息,共享收益。由于小核酸制药产业具有高技术、高投入和高风险的特征,就目前情况很难进行全技术链的研发。但国内企业在不同技术环节上具有技术优势,这样的发展模式有利于将小核酸企业紧密联合起来,以技术链各环节为基础,分工协作,各取所需,形成优势互补、共同发展的良好局面(见图4)。综上所述,多主体共同参与的链式发展模式是国内小核酸产业发展的较优选择。
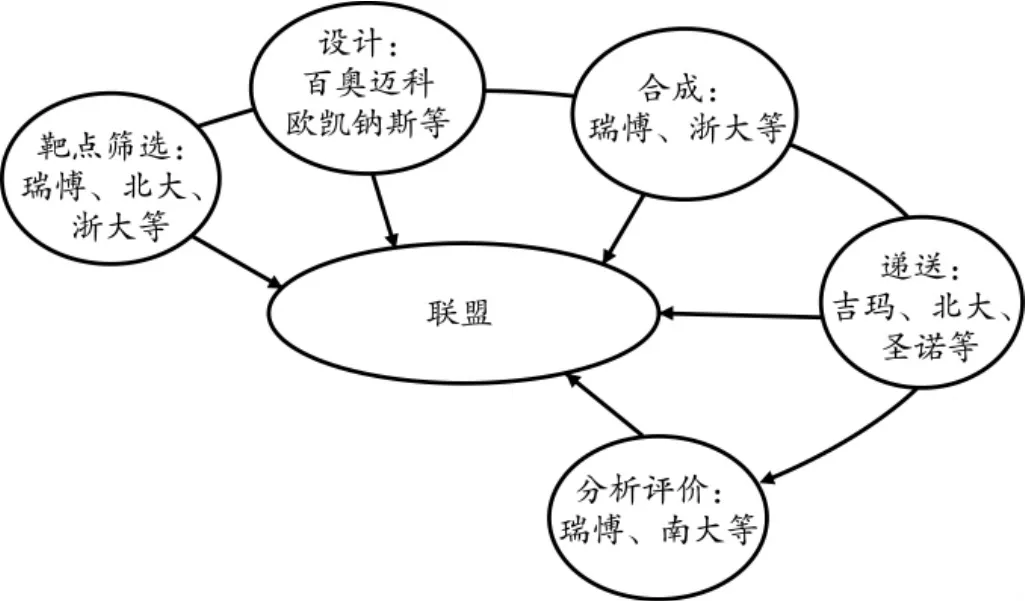
图4 多主体共同参与的链式发展的产业联盟模式

表5 现有发展模式的评价
目前,产业创新联盟是生物医药领域多主体共同参与链式发展模式的主要形式。通过组建国内小核酸产业创新联盟,发挥政府主导的举国体制优势,实现产业的技术共享和合作创新;发挥国内各个企业的技术研发优势,提高国内专利技术的产业化利用率,形成国内完整的小核酸药物开发技术链。在联盟模式的基础上,进行技术研发和合作,形成国内自有的药物开发技术路线;同时做好技术研发的风险规避和未来风险的预测,保证技术无风险实施。
参考文献:
[1]Couzin J.Breakthrough of the year:small RNAsmake big splash[J].Science,2002,298(5602):2296-2297.
[2]Dorsett Y,Tuschl T.siRNAs:applications in functional genomics and potential as therapeutics[J].Nature Reviews Drug Discovery,2004,3(4):318-329.
[3]张洪杰,殷勤伟.基于RNAi技术产品的商业化生物产业技术[J].生物化学与生物物理进展,2011(4):47-52.
[4]Fire A,Xu SQ,Montgomery MK,et al.Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans[J].Nature,1998,391(6669):806-811.
[5]Charlie S.Negotiating the RNAi patent thicket[J].Nature Biotechnology,2007,25:273-275.
[6]李玮婷,张才成,李俊明.小干扰RNA靶向系统的研究进展[J].广东医学,2013,34(17):2728-2730.
[7]毛金生,冯小兵,陈 燕.专利分析和预警操作事务[M].北京:清华大学出版社,2006:23.
[8]牛晓帆,朱睿倩,字来宏.最适生物医药产业发展模式比较研究[J].经济问题探索,2012(2):49-53.
