基层医院454例药品不良反应报告监测分析
2014-04-27蒙光义高春燕王冬晓庞家莲彭评志唐华斌陈靖辉
蒙光义,高春燕,王冬晓 ,庞家莲 ,彭评志,唐华斌,陈靖辉
(1.广西壮族自治区玉林市第一人民医院,广西 玉林 537000; 2.桂林医学院,广西 桂林 541004;3.广西壮族自治区玉林市妇幼保健院,广西 玉林 537000)
医疗系统的药品不良反应(ADR)监测工作越来越受到重视,加强ADR监测是促进医院合理用药和确保用药安全的重要方法和手段[1]。总结和分析ADR报告是探讨其发生规律、临床特点和防治措施的有效途径,对于临床安全用药和及时判断或预防新药所致ADR的发生具有积极的重要作用[2]。笔者通过对医院2012年上报国家药品不良反应监测系统的454例ADR报告进行统计和分析,观察其发生特点及规律,为医院合理用药和减少ADR的发生提供参考。
1 资料与方法
收集医院2012年门诊部和住院部上报药品不良反应监测系统ADR报告共454例,其中医师上报214例(47.14%),护士上报209例(46.04%),药师上报31例(6.83%)。按照《药品不良反应报告和监测管理办法》中的标准将ADR分类,分别从性别、年龄、药品种类、给药途径、主要临床表现、转归情况等方面进行统计和分析。
2 结果
2.1 患者年龄及性别
454例 ADR报告中,患者男 265例(58.37%),女 189例(41.63%),男性明显多于女性。患者年龄1天至87岁,60岁以上老年患者ADR发生率居首位,共140例(30.84%);18岁以下未成年人患者ADR发生率居第2位,共86例(18.94%)。见表1。

表1 ADR患者的年龄与性别分布情况(n=454)
2.2 用药情况
给药途径:见表2。

表2 引发ADR的给药途径分布(n=454)
药物类别:454例ADR报告中,抗菌药物引起的ADR最多,其次为抗肿瘤药物、中药制剂。见表3。
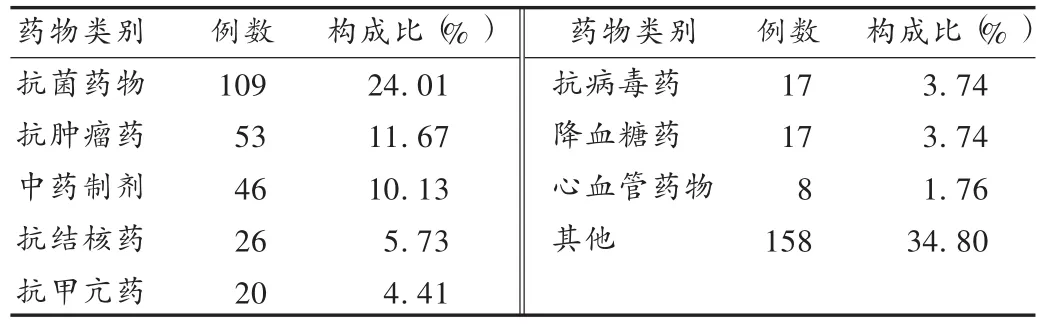
表3 引发ADR的药物类别及构成比(n=454)
2.3 ADR情况
累及器官/系统及主要临床表现:454例ADR临床表现主要为急性荨麻疹、红斑、皮疹及过敏样反应等累及皮肤及其附件损害的反应。见表4。

表4 ADR累及器官/系统及主要临床表现(n=454)
新的严重ADR及临床转归:454例ADR报告中,一般ADR 423 例(93.17% ),严 重 ADR 24 例 (5.29% ),新 的 ADR 7 例(1.54%)。其中新的严重ADR 4例,见表5。ADR转归方面,治愈253 例(55.73%),好转 194 例(42.73%),未好转 4 例(0.88%),不详3例(0.66%)。绝大部分ADR经过相关处理后都能治愈或好转。

表5 新的严重ADR详细报告情况
3 讨论
通常女性比男性更容易发生ADR,但本次调查中男性患者明显多于女性,具体原因不明。从454例ADR报告中患者年龄来看,ADR可能发生在任何年龄阶段。临床研究表明,ADR的发生除少数属于药效学方面原因以外,大多数属于药代动力学方面的原因[3]。本调查中60岁以上患者140例(30.84% ),位居各年龄阶段首位,表明老年患者容易发生ADR,推测与老年人的药效学特点和生理特点有关。老年患者常同时患有多种基础疾病,机体组织器官衰退和功能下降,免疫力降低,临床经常需要联合用药,增加了药物相互作用,且用药时间长,这些因素更容易导致ADR发生。因此,临床对于老年患者应尽量避免联合用药,在监测患者肝肾功能各项生理指标的同时,争取达到个体化给药方案。
ADR的发生与给药途径密切相关。本调查454例ADR报告中,有318例ADR是静脉滴注给药引起的,占70.04%,表明静脉滴注是最易引起ADR的给药途径,这与文献[4]报道相符。推测其原因可能有:静脉滴注使药物直接进入血液,特别是治疗窗较窄的药物,快速达到甚至超过有效浓度,导致血药浓度过高而发生不良反应;药物与溶剂配伍后受到光照、温度、酸碱度、微粒和内毒素等各种因素影响,增加ADR发生的危险。因此,选择合理的给药方式极其重要,建议临床用药时遵循“能口服尽量避免静脉给药”的原则,最大限度地降低ADR的发生[5]。
454例ADR中,抗菌药物是引发ADR药物类别中比例最高的一类,其中以头孢菌素类和喹诺酮类最多见,这与文献[6-9]报道一致。推测其原因可能与抗菌药物在临床应用中种类多、范围大有关,更可能与无指征使用抗菌药物、单次给药剂量偏大、未参照抗菌药物敏感性试验结果选药等滥用抗菌药物因素有关,这也是导致ADR发生率高的主要原因。因此,医院必须严格按照《抗菌药物临床应用管理办法》的要求规范医师使用抗菌药物。目前,抗菌药物普遍存在滥用等不合理现象,临床科室必须加强抗菌药物应用的监测,提高合理使用抗菌药物水平,减少抗菌药物所致ADR的发生。
454例ADR中,ADR累及器官/系统中皮肤及其附件损害的发生率最高,主要表现为急性荨麻疹、皮疹、红斑、瘙痒、过敏样反应等,这与文献[10-12]报道基本相同。推测其主要原因可能是皮肤反应为外在的直观反应,临床中易观察和发现。然而,内脏系统如肝肾功能损害、骨髓抑制等的临床反应比较隐秘,即使发生了ADR也不易观察和诊断,影响了ADR的及时上报。虽然皮肤及附件损害占主导地位,但一般易及时发现和治疗,而其他器官/系统因难以发现则需要医护人员或患者密切观察,本着“早发现早治疗”的原则,避免不可转归的不良反应,保障患者的用药安全。此外,ADR所致消化系统的反应如恶心、呕吐等症状,居第2位,主要为肿瘤化学治疗时所用抗肿瘤药物所致,与文献[13]报道一致。但ADR累及消化系统的反应在肿瘤专科医院的发生率最高,这与每个医院的具体情况有关[14]。
454例ADR中,一般ADR占93.17%,严重ADR占5.29%,新的ADR占1.54%,没有达到世界卫生组织对新的和严重ADR报告应达30%的标准[15],表明我院ADR的监测质量和上报工作有待进一步加强和提高。2012年,医院共发生新的严重ADR 4例,其中注射用苯磺酸阿曲库铵引起过敏性休克、支气管痉挛2例;钠钾镁钙葡葡糖注射液引起高热、寒战、心动过速1例;注射用复方三维B(Ⅱ)引起过敏性休克(严重)1例。从转归情况分析,我们必须高度关注新的严重ADR,并积极上报,再次遇到类似病情时,能提示医师综合考虑是否使用该类药物,从而达到安全、合理、有效用药。
总之,药品引起ADR的原因比较复杂,各种机理都有待深入研究。通过对ADR报告的统计、分析能对药源性损害事件起到预警作用,对医院合理使用药品特别是新购进药品起到积极的作用。因此,我们必须加强ADR的监测工作,提高合理用药水平,减少ADR的发生,促进医院诊疗水平的提高。
参考文献:
[1]赵珊珊,赵 平,张藜莉,等.我院259例药品不良反应报告分析[J].中国药房,2013,24(18):1704 - 1706.
[2]杨 威,吴丽华,黄伟侨,等.我院228例药品不良反应报告分析[J].中国医院药学杂志,2008,28(16):1431 -1432.
[3]陈新谦,金有豫,汤 光.新编药物学[M].第16版.北京:人民卫生出版社,2011:13 -14.
[4]周绣棣,李海燕,霍振洪,等.我院459例药品不良反应报告分析[J].中国药房,2012,23(38):3621 -3623.
[5]李立安.静脉输液治疗中应注意的问题及建议[J].中国医院药学杂志,2007,27(2):267 - 270.
[6]李 双.我院177例药品不良反应报告分析[J].中国新药杂志,2010,19(8):725.
[7]殷萍萍,王 坚,曹 辉,等.我院173例药品不良反应报告分析[J].中国药房,2012,23(38):3619 -3621.
[8]徐艳丽,吴玉波,蒋爱华,等.我院128例药品不良反应报告分析[J].哈尔滨医科大学学报,2012,44(1):88 -90.
[9]潘日兴,苏方华,王翠芬.我院171例药品不良反应报告分析[J].安徽医药,2011,15(1):119 -120.
[10]周 鹏,张 英,林建群,等.我院2010年453例药品不良反应报告分析[J]. 中国药业,2012,21(20):58 -59.
[11]马书田.我院125例药品不良反应报告分析[J].中国药房,2012,23(30):2861 - 2863.
[12]闻飞英.我院2011年药物不良反应报告分析[J].海峡药学,2012,24(10):264 - 265.
[13]黄建蓉,陈孟林.我院2011年135例药品不良反应报告分析[J].中国药业,2012,21(21):34 -36.
[14]王怡鑫,蒋 刚,蔡 红.我院2011年767例药品不良反应分析[J].中国药业,2013,22(2):66 -68.
[15]龚善初.我院142例药品不良反应报告分析[J].中国药房,2012,23(42):4002 - 4004.
