双侧睾丸支持细胞瘤1例报告并文献复习
2014-04-22满申兴斌李俊鹏王泽民赵立军李春辉
于 满申兴斌李俊鹏王泽民赵立军李春辉
1. 承德医学院附属医院泌尿外科(承德 067000); 2. 承德医学院附属医院病理科
双侧睾丸支持细胞瘤1例报告并文献复习
于 满1*申兴斌2李俊鹏1王泽民1赵立军1李春辉2
1. 承德医学院附属医院泌尿外科(承德 067000); 2. 承德医学院附属医院病理科
成人睾丸支持细胞瘤发病率较低,临床较为罕见,其恶性程度不高,临床预后较好。本院2006年11月收治1例双侧睾丸同时发生支持细胞瘤,结合文献进行讨论。
病例报告
患者,45岁,因双侧睾丸增大伴坠胀感3个月余,于2006年11月15日住院。入院时检查心肺无异常,体温36.9℃,外观双侧阴囊增大,右侧明显(图1)。体检时触及双侧睾丸增大,右侧约8.0cm ×7.0cm×7.0cm,左侧6.0cm×5.0cm×5.0cm,质地中等,表面光滑,轻触痛,有沉重感。双侧精索及附睾触之正常,双侧腹股沟未触及肿大的淋巴结。血清甲胎蛋白(AFP)、绒毛膜促性腺激素β-亚基(HCG)均正常;超声提示双侧睾丸实性占位,CT提示双侧睾丸实质内不均等实性占位,强化扫描时双侧睾丸占位性病变有强化(图2)。胸部X片未见异常。故诊断双侧睾丸肿瘤,行腹股沟切口双侧睾

图1 外观双侧阴囊增大,右侧明显
丸根治性切除术。术后大体标本见右侧睾丸8.0cm ×7.0cm×7.0cm,左侧睾丸5.5cm×5.0cm×5.0cm(图3)。术后病理镜下所见:肿瘤边界清楚,肿瘤细胞排列成巢状,细胞多角形,核呈椭圆形、圆形或长形,核仁不突出,未见核沟及核内包涵体,胞浆嗜酸性。细胞形态总体平和,相对一致,核分裂像<5个/10HPF(高倍视野法)。间质由中等量纤维和透明变性的组织构成,可见扩张的血管,间质水肿,少量炎细胞浸润,间质内残存的腺体结构完好(图4);免疫组化结果:肌特异性肌动蛋白(MSA)(-)、肌酸激酶(CK)(-)、Vimentin(+)、Desmin(+)、AFP(-)、NSE(+)(图5)。诊断双侧睾丸支持细胞瘤,明显核异性,有潜在恶性倾向。患者术后9个月时,诉腰痛,经CT检查,腰2、3椎体有破坏,考虑骨转移。虽经化疗和放疗,但于术后2年死亡。
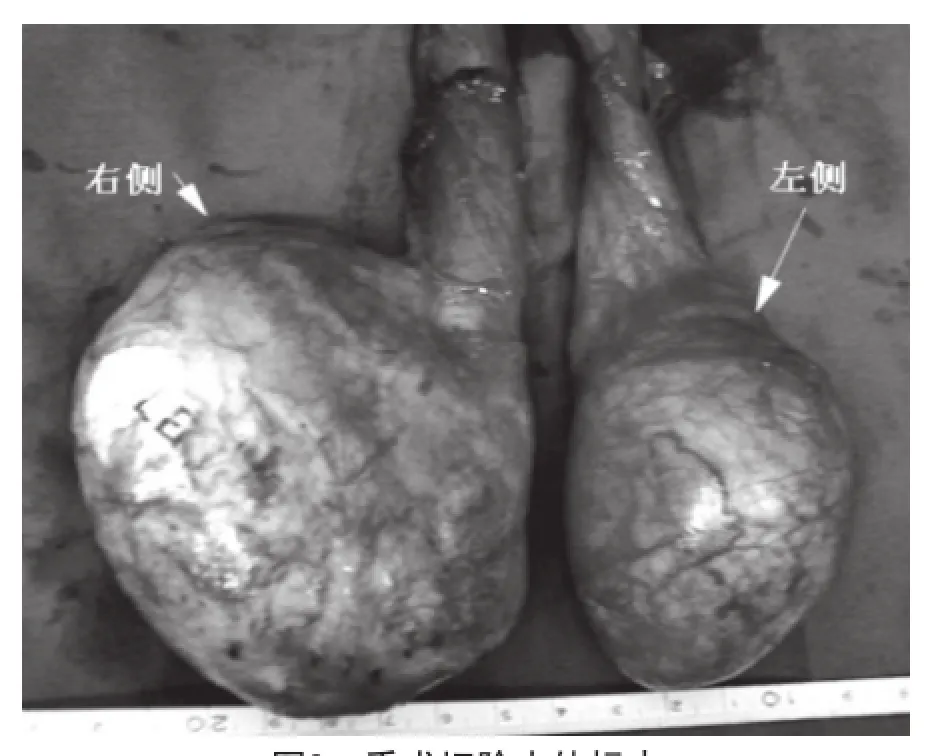
图3 手术切除大体标本
讨 论
一、发病情况
睾丸支持细胞瘤(Sertoli cell tumors)是一种罕见的性索间质肿瘤,睾丸支持细胞瘤又称男性母细胞瘤, 属于性腺基质肿瘤。一般认为起源于生殖嵴的原始性腺间质或颗粒细胞组成, 即生殖腺内生殖细胞的支持成分。大约占睾丸所有肿瘤的1%[1]。1944年Teilum首次报道了睾丸支持细胞瘤。此后陆续个案报告,到目前,文献显示全世界成组或个案报道不足400例[2]。搜集国内文献,自1989王麟根首先报道2例,到2013年底共计24例(见表1)[2-21]。本例为第25例。

图4 术后病理镜下所见

图5 免疫组化结果
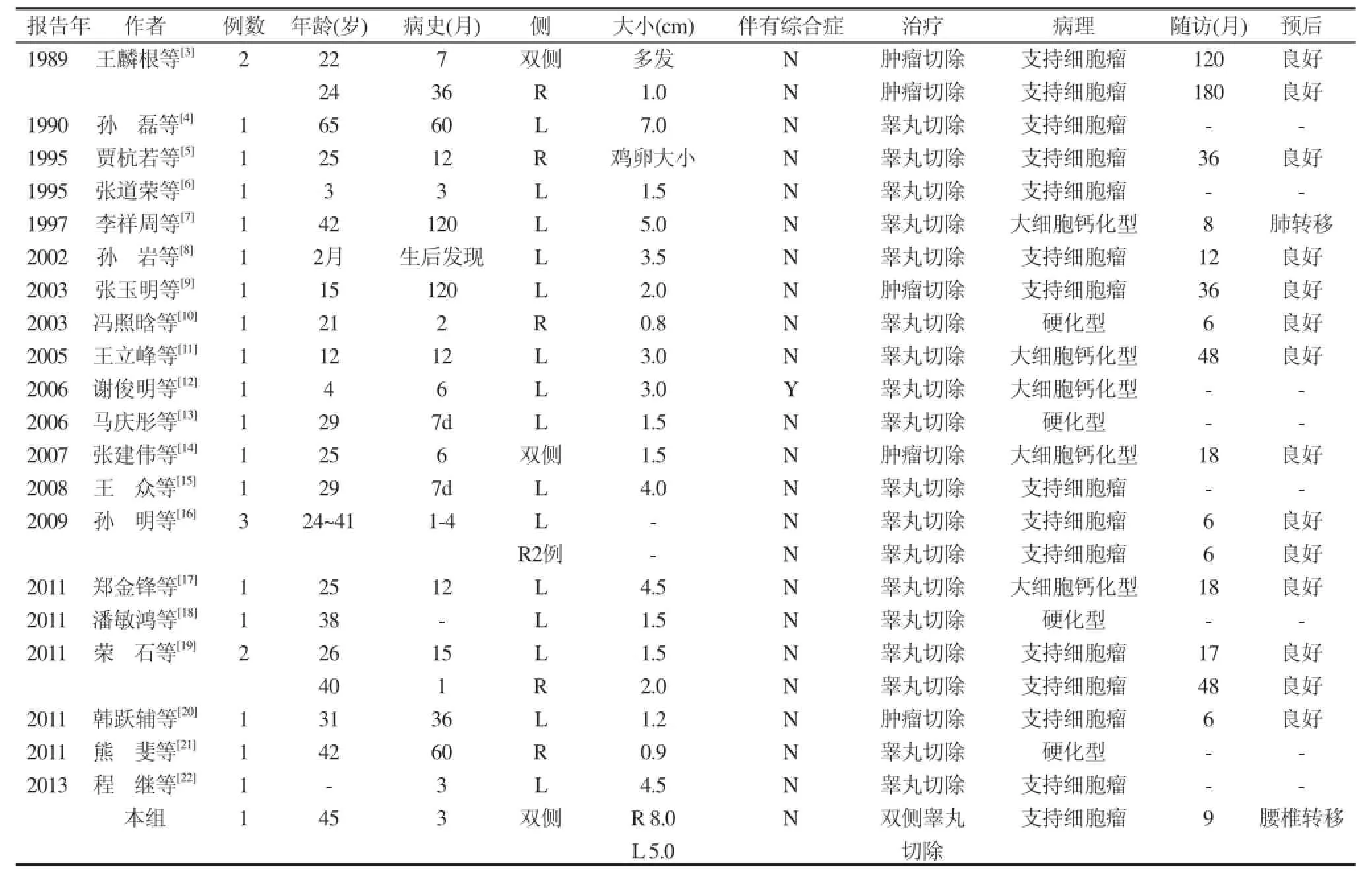
表1 国内报告的睾丸支持细胞瘤
睾丸支持细胞瘤可发生于各个年龄段,包括新生儿,但多见于中年人。国内25例中最小年龄2个月,最大年龄65岁,平均年龄27.3岁。原发性睾丸支持细胞瘤的病因至今尚不十分清楚,有多种因素参与。目前认为先天性因素中最主要的为隐睾和遗传因素。后天因素中较常见的为损伤、激素异常和感染[16]。临床上好发于隐睾及假两性畸形患者的睾丸,可能与睾丸损伤、炎症有关。
二、分类
睾丸支持细胞瘤被广泛接受的分型包括非特殊类型、硬化型和大细胞钙化型。这种组织学分类不是单纯的病理学分类,而是代表着不同的代谢及激素异常的临床特征,且有着不同的恶性潜能及预后意义。大多数睾丸支持细胞瘤属于“非特殊型”,即典型的睾丸支持细胞瘤;另有两种罕见亚型,即硬化型(Sclerosing Sertoli Cell Tumor,SSCT)和大细胞钙化型(Large Cell Calcifying Sertoli Cell Tumor,LCCSCT)。国内25例中,典型的睾丸支持细胞瘤为16例(64.0%),LCCSCT 5例(20.0%),硬化型4例(16.0%)。硬化型睾丸支持细胞瘤自Zukerberg等1991年首次报道10例至今英文文献共43例[1,22,23],国内共报道4例[10,13,18,21]。LCCSCT首例是由Proppe和 Scully在1980年描述,至2003年共有61例报道[24,25],到2014年2月仅增加了17例,目前在世界范围内英文文献共78例报道[26,27],国内有5例报道[7,11,12,14,17],是少见的亚型,大部分为散发,也可以是Carney和Pentz-Jeghers综合征的一部分。
三、病理
睾丸支持细胞瘤直径一般小于3cm,如果肿瘤较大,高度可疑恶性。肉眼观察肿瘤为实质性,呈灰白色,切面呈淡黄色,有砂砾感,有点状出血或坏死区域。镜下见最显著的特点是在丰富致密的纤维结缔组织中包绕着肿瘤性上皮细胞,细胞排列成实性或中空的小管状结构,小管通常较小且多为实性,分散或相互吻合,亦可呈不规则团簇状、片巢状、条索状聚集; 肿瘤细胞小至中等大,边界不清,胞质量中等、淡染,部分细胞含有偏心的大脂质空泡,核圆形、卵圆形,或呈不规则空泡状,有一个或多个小核仁,核染色质空泡状,细胞无异型或轻度异型性,核分裂象罕见。个别病例细胞有中度异型性,核分裂多见,肿瘤侵犯睾丸网、附睾和血管。
硬化型睾丸支持细胞瘤肉眼观为实性、白色或黄白色的结节。镜下见肿瘤呈条索状、实性癌巢或筛状分布于致密的胶原结缔组织之间。
LCCSCT肉眼观为灰白色或淡黄色结节,呈多灶性;镜下见黏液样或胶原性的间质中,肿瘤细胞呈巢状或条索状分布,胞质丰富,呈嗜酸性, 间质呈钙化或骨化,钙化是该瘤的一个重要特征。除恶性病例外,核分裂象少见。
免疫组化检查主要有助于区分睾丸的其他肿瘤,但有作者提出免疫组化 CK和vimentin有助于分型,CK的表达与小管的分化程度有关;大细胞钙化型vimentin阳性,低分子CK 灶性阳性。而硬化型CK常为阴性,vimentin强阳性。但国内24例中,做了免疫组化检查13例,vimentin阳性12例,阴性1例为非特殊型;CK阳性5例,阴性8例。本文1例vimentin阳性,CK呈阴性。Kao等[1]报告20例SSCT免疫组化检查结果,vimentin检查7例均为阳性,CK11例中阳性6例,inhibin15例阳性4例。免疫组化检查主要用于区分睾丸的其他肿瘤。如睾丸间质细胞瘤inhibin可呈强阳性。
四、临床表现
睾丸支持细胞瘤的临床表现随就诊时间而异, 左右睾丸的发病比例几乎相等;但国内25例中除3例为双侧同时发病外,其余22例左侧15例,右侧7例,左:右为2.1:1。主要临床表现为睾丸肿块,呈圆形或卵圆形,生长缓慢,质地韧,部分伴有疼痛或不适感,肿块生长缓慢,多为单发;也可出现内分泌变化,如男性乳房增大,约10%~38%有男性乳房发育,皮肤色素沉着等,青春期前患者偶有性早熟,雄激素、雌激素、促性腺激素升高,但也可正常。
硬化型睾丸支持细胞瘤见于青春期后,发病年龄18~80 岁,平均年龄为35岁。80%的肿瘤小于2.0cm,常为单一的无痛性肿块,无激素生成异常或伴发发育不良性综合征引起的性腺外症状,无遗传倾向。肿瘤均为单侧,左右睾丸的发病比例几乎相等;国内4例年龄21~42岁,平均年龄32.5岁。多数患者以发现睾丸肿物就诊, 均无激素异常的表现。
LCCSCT发病年龄多在20岁以下,平均年龄为16岁。国内5例中最小年龄4岁,最大年龄42岁,平均年龄21.6岁。以睾丸肿物为主要临床表现,少数乳房呈女性样发育或表现为性早熟。缓慢增长的睾丸肿块为其主要临床表现,偶伴有疼痛。部分患者有乳腺增生,尿中可排出大量雌激素。国内5例中有1例儿童先出现双侧乳房增大,进一步检查发现左侧睾丸肿瘤。婴幼儿患者可出现性早熟现象。其中40%与遗传性综合征或内分泌异常(包括性早熟和男性乳腺发育)有关,通常多见为Carney综合征,而Pentz-Jeghers综合征少见;约20%为双侧睾丸发病或睾丸多灶性病变,而双侧者Carney 综合征发生率更高[28]。Carney 综合征表现有:皮肤、软组织和心脏的黏液瘤,乳腺的黏液性病变,面部和口唇的雀斑,皮肤的蓝痣,色素性肾上腺皮质增生结节继发的Cushing综合征,垂体性激素腺瘤,砂砾体性黑色素性神经鞘瘤,LCCSCT 等。Pentz-Jeghers综合征,多见于儿童和青少年,是一种常染色体显性遗传病,患者有胃肠道多发性错构瘤性息肉,手足皮肤及口腔黏膜的色素沉着,故又称皮肤黏膜黑斑息肉病,息肉最常见于小肠[29]。需要注意LCCSCT有17%为恶性,恶性者发病年龄在20岁以上,肿瘤直径>4.0cm。
五、影像学表现
1. 超声检查表现:睾丸内低回声或等回声团块,边界清晰,内部回声欠均匀, 彩色多普勒显示肿物内部及周边可见少量血流信号,显示睾丸内占位病变,无明显特异性,而超声不能对本病作出明确诊断。
2. CT:CT平扫显示睾丸内实性占位,边缘清晰,包膜完整,内在密度均匀或欠均匀,可有囊变坏死钙化等。增强扫描显示睾丸病灶包膜略有强化,有时中央可见小片状不均匀强化影,但是确诊只能依靠病理学检查。
六、治疗与预后
因睾丸支持细胞瘤临床少见,在未获得组织病理学之前,很难与睾丸其他恶性肿瘤区别,所以,睾丸根治性切除仍是首选。对于年轻双侧睾丸的小肿瘤(<2.0cm的肿瘤)可做保留睾丸的肿瘤切除术[26]。硬化型较非特殊类型及大细胞钙化型预后要好,随访9个月至10 年,无一例复发或转移,即使年龄最大(80 岁)的患者其组织学形态表现为恶性(核分裂较多见,侵犯睾丸网、附睾和血管),术后5年死于心脏疾病,也没有睾丸肿瘤复发或转移的临床证据[22]。报道中肿瘤体积最大者7 cm,累及右侧整个睾丸,随访6年也无症状[30]。而非特殊类型及大细胞钙化型均有转移的报道[25,27,31,32]。文献报道年龄较大、或肿瘤超过4cm者,有恶性潜能,本组患者为45岁,在国内所有报告中除一例60岁者外是年龄最大者,而且双侧睾丸均弥漫性增大分别为8和5.5cm,该患者9个月时出现腰椎转移。表明硬化型睾丸支持细胞瘤恶性潜能极低,其预后要比其他两型好。因此,硬化型睾丸支持细胞瘤可以采取单纯肿块切除术,但由于术前往往明确诊断困难,根治手术仍为常用的术式。
睾丸肿瘤; 塞尔托利细胞瘤; 免疫组织化学
1 Kao CS, Kum JB, Idrees MT,et al. Sclerosing sertoli cell tumor of the testis: a clinicopathologic study of 20 cases.Am J Surg Pathol2014; 38(4):510-517
2 程继, 钟甘平, 董治龙. 睾丸支持细胞瘤1例报告. 中国男科学杂志 2013, 27(5): 65-66.
3 王麟根. 睾丸支持细胞瘤2例报道. 男性学杂志 1989; 3(2): 114-115
4 孙磊, 张林. 睾丸支持细胞瘤一例. 昆明医学院学报1990; 11(3): 78
5 贾杭若, 王爱忠. 睾丸支持细胞瘤一例. 中华病理学杂志1995; 24(6): 374
6 张道荣, 宋继渴, 张丽红. 睾丸支持一间质细胞肿瘤. 诊断病理学杂志 1995; 2(2): 99
7 李祥周, 石凤娟, 陆晓哲, 等. 睾丸恶性大细胞钙化性支持细胞瘤一例. 中华病理学杂志 1997; 26(4): 213
8 孙岩, 陶文芳, 李昭铸. 婴儿睾丸支持细胞瘤一例. 中华小儿外科杂志 2002; 23(1): 39
9 张玉明, 曲凯, 白鹏. 睾丸支持细胞瘤1例. 临床泌尿外科杂志 2003; 18(12): 727
10 冯照晗, 张钊, 姜永金. 睾丸支持细胞瘤一例报告. 中华泌尿外科杂志 2003; 24(3): 209
11 王立峰, 张淑杰, 戚基萍, 等. 睾丸大细胞钙化性支持细胞瘤一例. 中华病理学杂志 2005; 34(11): 761-762
12 谢俊明, 江少波, 邬贤德. 睾丸大细胞钙化型支持细胞瘤合并乳房发育. 现代泌尿外科杂志 2006; 11(1): 53-54
13 马庆彤, 赵英奇, 徐子强. 睾丸支持细胞瘤1例. 临床泌尿外科杂志 2006; 21(1): 76
14 张建伟, 苟新敏, 李智, 等. 睾丸大细胞钙化性支持细胞瘤一例. 中华病理学杂志 2007; 36(4): 281-282
15 王众. 睾丸支持细胞瘤的超声表现1例. 中国超声医学杂志 2008; 24(6Ⅱ): 28
16 孙明, 吴斌, 王鸿起, 等. 成人睾丸支持细胞瘤的诊断和治疗 (附3例报告并文献复习). 中华男科学杂志 2009; 15(10): 950- 951
17 郑金锋, 程童大, 刘晓红, 等. 睾丸大细胞钙化型支持细胞瘤临床病理观察. 中华男科学杂志 2011; 17(8): 730-733
18 潘敏鸿, 张智弘, 王聪, 等. 睾丸硬化型支持细胞瘤临床病理观察. 诊断病理学杂志 2011; 18(5): 368-370
19 荣石, 毛全宗, 严维刚, 等. 睾丸支持细胞瘤二例. 中华临床医师杂志(电子版) 2011; 5(24): 7459- 7460
20 韩跃辅, 吴宝国, 张朝胜, 等. 睾丸支持细胞瘤 1例报告并文献复习. 现代泌尿外科杂志 2011 16(3): 254-255
21 熊斐, 罗良平, 史长征. 硬化性睾丸支持细胞瘤 1 例. 中国医学影像技术 2011; 27(7): 1434
22 Zukerberg LR, Young RH, Scully RE. Sclerosing Sertoli cell tumor of the testis. A report of 10 cases.Am J Surg Pathol1991; 15(9): 829-834
23 Ishida M, Fujiwara R, Tomita K,et al.Sclerosing Sertoli cell tumor of the testis: a case report with review of the literature.Int J Clin Exp Pathol2013; 6(11): 2640-2643
24 Proppe KH, Scully RE. Large-cell calcifying Sertoli cell tumor of the testis.Am J Clin Pathol1980; 74(5): 607-619
25 De Raeve H, Schoonooghe P, Wibowo R,et al.Malignant large cell calcifying Sertoli cell tumor of the testis.Pathol Res Pract2003; 199(2): 113-117
26 Kaluzny A, Matuszewski M, Wojtylak S,et al. Organsparing surgery of the bilateral testicular large cell calcifying sertoli cell tumor in patient with atypical Peutz-Jeghers syndrome.Int Urol Nephrol2012; 44(4): 1045-1048
27 Petersson F, Bulimbasic S, Sima R,et al. Large cell calcifying Sertoli cell tumor: a clinicopathologic study of 1 malignant and 3 benign tumors using histomorphology, immunohistochemistry, ultrastructure, comparative genomic hybridization, and polymerase chain reaction analysis of the PRKAR1A gene.Hum Pathol2010; 41(4): 552-559
28 Halat SK, Ponsky LE, MacLennan GT. Large cell calcifying Sertoli cell tumor of testis.J Urol2007; 177(6): 2338
29 Gourgari E, Saloustros E, Stratakis CA. Large-cell calcifying Sertoli cell tumors of the testes in pediatrics.Curr Opin Pediatr2012; 24(4): 518-522
30 Abbas F, Bashir NW, Hussainy AS. Sclerosing Sertoli cell tumor of the testis.J Coll Physicians Surg Pak2005; 15(7): 437-438
31 Young RH, Koelliker DD, Scully RE. Sertoli cell tumors of the testis, not otherwise specif ed: a clinicopathologic analysis of 60 cases.Am J Surg Pathol1998; 22(6): 709-721
32 Henley JD, Young RH, Ulbright TM. Malignant Sertoli cell tumors of the testis: a study of 13 examples of a neoplasm frequently misinterpreted as seminoma. Am J Surg Pathol2002; 26(5): 541-550
(2014-05-20收稿)
10.3969/j.issn.1008-0848.2014.09.017
R 737.21
*通讯作者, Email: yumanok@126.com; Tel:13398692608
