特发性肺纤维化合并肺癌8例临床分析
2014-04-13沈凌夏俊波祁明浩王利民
沈凌 夏俊波 祁明浩 王利民
特发性肺纤维化合并肺癌8例临床分析
沈凌 夏俊波 祁明浩 王利民
吸烟不仅是肺癌(LC)的危险因素,还与特发性肺纤维化(IPF)的发病和预后相关。IPF患者合并LC的发生率明显高于普通吸烟人群。笔者现对我院近年来收治的8例有完整资料的IPF合并LC患者的临床资料作一回顾性分析,旨在提高临床对此病的认识,报道如下。
1 临床资料
1.1 一般资料 2007—2013年我院共收治8例男性IPF合并LC患者,年龄64~84岁,平均72.75岁。IPF诊断标准参考2011年美国胸科协会的诊断标准[1]。除外已知病因的间质性肺病:结缔组织病,药物和外源性过敏性肺炎、结节病、尘肺、肺朗格汉组织细胞增多症等。由有经验的放射科医生和2位呼吸科医生共同评价高分辨率CT资料,并参照相关标准[2]对肺纤维化的病变范围进行评分:0分:无,1分:1%~25%,2分:26%~50%,3分:51%~75%,4分:76%~100%。根据支气管镜和CT检查结果将LC分为中央型和周围型,肺段及肺段以上支气管腔内可见癌性浸润者归为中央型,肺段以下病变归为周围型。根据纵隔窗CT检查所示淋巴结数目>2枚、最大直径>1cm判断为纵隔淋巴结肿大。
1.2 临床表现 表现为咳嗽8例,呼吸困难6例,发热2例,杵状指5例,从出现咳嗽到确诊时间为1~30年,从出现呼吸困难到确诊时间为2个月~10年。血清肿瘤指标中癌胚抗原均增高(5.56~21.21μg/L,平均11.66μg/ L)。病理类型:鳞癌6例,腺癌2例。8例患者具体临床特点见表1。
1.3 影像学表现 主要表现为两下肺外周为主的网格影,蜂窝肺仅1例,评分2分者4例,1分者2例,4分者1例。LC部位以下叶多见,其中中央型5例,周围型3例;病灶数量:6例单发,2例多发;出现纵隔淋巴结肿大者5例。从形态上看,中央型LC表现为肿块,均伴有纵隔及肺门淋巴结肿大;周围型表现为结节,边界清楚。8例患者具体影像学特点见表2;图1-4。
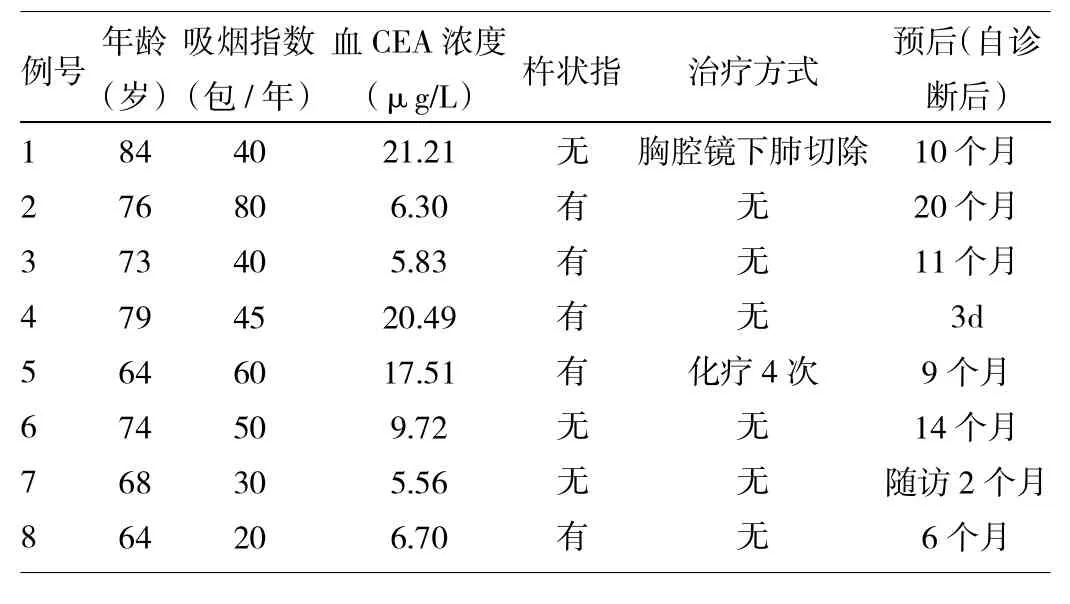
表1 8例患者具体临床特点
1.4 支气管镜下表现 6例完成支气管镜检查,其中5例中央型LC,均表现为气管或者支气管壁的浸润、增厚,均无新生物突出管腔;1例患者(例4)进行了肺泡灌洗检查;其他2例通过CT引导下经皮肺穿刺术获取病理标本确诊。
1.5 治疗及预后 仅2例患者在明确诊断后进行积极治疗:例1进行了胸腔镜下的右上肺切除术,例5进行了紫杉醇联合卡铂的化疗;其余6例均放弃治疗。例4患者在进行了肺泡灌洗后当天出现急性心肌梗死,并于术后第3天死亡;其余患者(除例7外)分别在诊断明确后的9~20个月死亡;例7已确诊2个月,目前仍有随访中。
2 讨论
目前LC的发病率逐年增高,而IPF是特发性间质性肺炎最常见的一类疾病,这两者的易感人群高度重叠,均以男性吸烟人群为主。2000年,英国的一项对队研究比较了890例IPF患者与5 884例对照者,发现前者的LC发生率4.4%,而后者为0.9%,差异有统计学意义(P<0.01),校正后的危险比达7.31[3]。韩国的一项回顾性分析发现,IPF患者中发生LC的比例高达22%[4]。这些都表明IPF合并LC并不少见,应引起临床上的广泛重视。
本组IPF合并LC患者均为男性吸烟者,75%的病理类型为鳞癌,高于文献报道(40%~50%),也明显高于其他LC人群(P<0.01)[5-6]。其临床症状以咳嗽和呼吸困难为主,杵状指的发生率为67%,与IPF人群相仿。英国一项对588例IPF患者11年的随访研究显示,其中合并LC的患者与其他IPF患者相比,男性所占比例更高(87%、63.6%),死亡时间提早(68.4岁、72.2岁),出现杵状指的机会更高(67.4%、49.7%)[7]。

表2 8例患者具体影像学特点
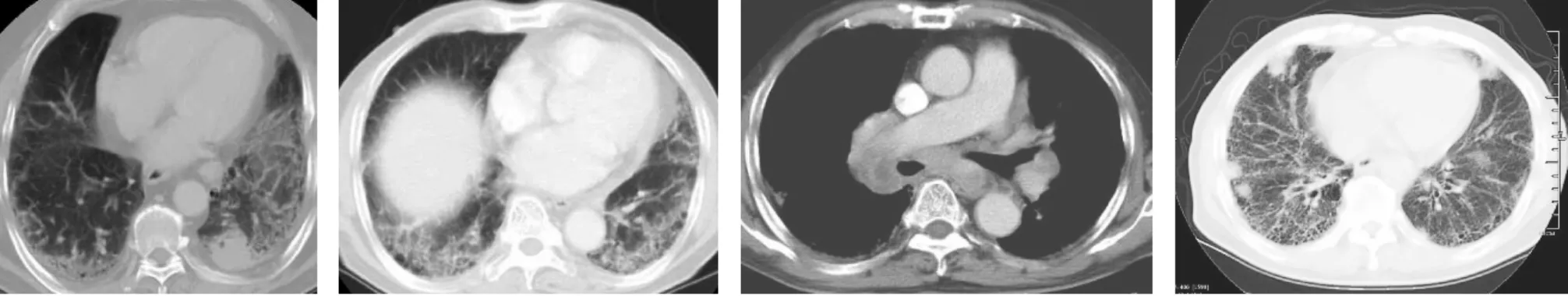
图1 病例2肺部CT示两肺下叶基底段外带网格影,左下叶后基底段见一肿块
Sakai[8]对47例IPF合并LC者的57例病理标本及高分辨CT片进行分析,发现其中82%的肿块位于周边,50份呈圆形或具有锐利边缘的分叶状,仅有7例(6例鳞癌,1例小细胞癌)侵及周边的蜂窝肺组织而使边界不清,有13份CT可见瘤内透光区。本组患者LC以下叶为主,与文献报道相似;中央型LC5例,3例外周型均在蜂窝肺部位,形态圆形、边界清楚,这与文献报道的大多数IPF相关LC多位于外周有所不同,可能与本组例数较少有关。此外,IPF合并LC还存在多发灶的特点。本组患者中有2例为多发病灶,较Mizushim等[9]报道的结果稍高,而未合并IPF的LC患者只有5%存在多发LC。
本组8例患者在就诊时同时发现IPF与LC,部分患者在其他医院长期作为“慢性支气管炎”治疗,由于缺乏资料因此无法判断IPF是否早于LC的发生。但有文献提示,对于IPF患者需要在病程发展过程中警惕LC的发生。Fujimoto等[10]报道了43例IPF患者中有16例(37%)在随访1~10年(平均4年)间发现LC的。因此对于IPF患者要动态观察影像学和肿瘤标记物的变化,及早地发现并诊断LC。目前,临床上尚缺乏肿瘤标记物在IPF合并LC中的系统研究,有部分文献报道IPF患者中LC的肿瘤标记物包括癌胚抗原(CEA)[11]、细胞角蛋白19片段(CYFRA21-1)[12]和糖蛋白CA19-9[13]可以增高。但本组8例患者的CEA均高于正常值,提示对于IPF患者应动态观察CEA的变化,将有助于早期发现IPF合并LC。
对于IPF合并LC的治疗,仍主要根据LC的分期进行。由于IPF患者肺功能状况相对较差以及所合并的LC处于进展期,因此手术的概率较非IPF合并LC的患者要小。本组仅1例患者进行手术,另外2例周围型LC患者均因考虑肺功能下降而取消手术。Usui等[14]报道,LC患者中合并有肺纤维化能进行手术的约35.3%,而无肺纤维化表现的则为57.3%。IPF合并LC患者术后急性肺损伤(IPF急性加重,简称AEIPF)的发生率(0%~25%)高于非IPF合并LC患者,而一旦发生AEIPF,病死率更是高达33.3~100%[5,15]。采用胸腔镜下辅助手术后AEIPF的发生率虽与直接开胸术无明显差异,但概率仍较少,推荐对IPF合并LC可予采用。
本组患者仅1例进行了化疗,但疗效并不理想,可能与其分期和肺纤维化程度严重有关,其余患者拒绝化疗和放疗。文献报道,与对照组比较,采用化疗药物和靶向药物治疗IPF合并LC,急性肺损伤的发生风险也要增加,发生率可达8.7%~11.5%[16-17]。有文献报道,28例IPF合并LC患者接受化疗,发生急性肺损伤8例(28%),死亡4例(14%)[18]。对合并IPF合并LC患者进行化疗时,不适合使用吉西他滨、阿霉素以及CPT-11,而紫杉醇[19]、长春新碱和铂类均可以谨慎使用。目前,表皮生长因子受体酪氨酸酶抑制剂在LC晚期治疗中的应用逐渐广泛,吉非替尼是其中代表药物,该药可能会导致急性间质性肺炎的发生,特别是已有肺纤维化的LC患者。日本的一项研究发现,既往有间质性肺炎病史的LC患者在使用吉非替尼时,发生急性间质性肺炎的比例高达13.9%,总体生存期仅103d,明显少于对照组[20]。吉非替尼在表皮生长因子受体突变的LC患者疗效较好,但是影像学有肺纤维化改变的患者EGFR突变概率较小,因此不建议给予IPF合并LC患者吉非替尼治疗。
Saito等[21]统计了350例Ⅰa期非小细胞肺癌手术切除患者,其中28例合并IPF,5年生存率为54.2%,而对照组则达到88.3%,差异有统计学意义(P<0.01)。Watanabe等[6]分别对不同分期LC患者按是否合并IPF分组,发现除Ⅲ期LC患者外,其余各期无IPF的原发性LC患者总生存期均明显好于合并IPF的LC患者,差异有统计学意义(P<0.01)。本组8例患者自诊断至死亡的时间为3d~2年(平均1年),总体预后较差,可能与确诊时患者属于LC晚期有关。
总之,目前临床对IPF合并LC的发病机制尚不完全清楚,其影像学表现有一定特殊性,易漏诊,治疗手段也较局限,而且并发症较多,预后较差,应引起临床重视。
[1]Raghu G,Collard H R,Egan J J,et al.An official ATS/ERS/JRS/ ALAT statement:idiopathic pulmonary fibrosis:evidence-based guidelines for diagnosis and management[J].Am J Respir Crit Care Med,2011,183(6):788-824.
[2]Kazerooni E A,Martinez F J,Flint A,et al.Thin-section CT obtained at10-mm increments versus limited three-level thin-section CT for idiopathic pulmonary fibrosis:correlation with pathologic scoring[J].AJR Am J Roentgenol,1997,169(4):977-983.
[3]Hubbard R,Venn A,Lewis S,et al.Lung cancer and cryptogenic fibrosing alveolitis.A population-based cohort study[J].Am J Respir Crit Care Med,2000,161(1):5-8.
[4]Park J,Kim D S,Shim T S,et al.Lung cancer in patients with idiopathic pulmonary fibrosis[J].Eur Respir J,2001,17(6):1216-1219.
[5]Kawasaki H,Nagai K,Yokose T,et al.Clinicopathological characteristics of surgically resected lung cancer associated with idiopathic pulmonary fibrosis[J].J Surg Oncol,2001,76(1):53-57.
[6]Watanabe A,Higami T,Ohori S,et al.Is lung cancer resection indicated in patients with idiopathic pulmonary fibrosis[J]?J Thorac Cardiovasc Surg,2008,136(5):1357-1363.
[7]Harris J M,Johnston I D,Rudd R,et al.Cryptogenic fibrosing alveolitis and lung cancer:the BTS study[J].Thorax,2010,65(1): 70-76.
[8]Sakai S,Ono M,Nishio T,et al.Lung cancer associated with diffuse pulmonary fibrosis:CT-pathologic correlation[J].J Thorac Imaging,2003,18(2):67-71.
[9]Mizushima Y,Kobayashi M.Clinical characteristics of synchronous multiple lung cancer associated with idiopathic pulmonary fibrosis.A review of Japanese cases[J].Chest,1995,108(5): 1272-1277.
[10]Fujimoto T,Okazaki T,Matsukura T,et al.Operation for lung cancer in patients with idiopathic pulmonary fibrosis:surgical contraindication[J]?Ann Thorac Surg,2003,76(5):1674-1678.
[11]Takahashi H,Nukiwa T,Matsuoka R,et al.Carcinoembryonic antigen in bronchoalveolar lavage fluid in patients with idiopathic pulmonary fibrosis[J].Jpn J Med,1985,24(3):236-243.
[12]Dobashi N,Fujita J,Ohtsuki Y,et al.Elevated serum and BAL cytokeratin 19 fragment in pulmonary fibrosis and acute interstitial pneumonia[J].Eur Respir J,1999,14(3):574-578.
[13]Kodama T,Satoh H,Ishikawa H,et al.Serum levels of CA19-9 in patients with nonmalignant respiratory diseases[J].J Clin Lab Anal,2007,21(2):103-106.
[14]Usui K,Tanai C,Tanaka Y,et al.The prevalence of pulmonary fibrosis combined with emphysema in patients with lung cancer[J].Respirology,2011,16(2):326-331.
[15]Yano M,Sasaki H,Moriyama S,et al.Post-operative acute exacerbation of pulmonary fibrosis in lung cancer patients undergoing lung resection[J].Interact Cardiovasc Thorac Surg, 2012,14(2):146-150.
[16]Nakagawa K,Yasumitsu T,Kotake Y,et al.Lung resection for lung carcinoma with idiopathic interstitial pneumonia[J].Nihon Kyobu Geka Gakkai Zasshi,1994,42(10):1933-1939.
[17]Ogura T,Kondo A,Sato A,et al.Incidence and clinical features of lung cancer in patients with idiopathic interstitial pneumonia[J].Nihon Kyobu Shikkan Gakkai Zasshi,1997,35(3):294-299.
[18]clinical characteristics of acute respiratory deterioration in pulmonary fibrosis associated with lung cancer following anti-cancer therapy[J].2009.
[19]Minegishi Y,Sudoh J,Kuribayasi H,et al.The safety and efficacy of weekly paclitaxel in combination with carboplatin for advanced non-small cell lung cancer with idiopathic interstitial pneumonias[J].Lung Cancer,2011,71(1):70-74.
[20]Ando M,Okamoto I,Yamamoto N,et al.Predictive factors for interstitial lung disease,antitumor response,and survival in non-small-cell lung cancer patients treated with gefitinib[J].JClin Oncol,2006,24(16):2549-2556.
[21]Saito Y,Kawai Y,Takahashi N,et al.Survival After Surgery for Pathologic Stage IA Non-Small Cell Lung Cancer Associated With Idiopathic Pulmonary Fibrosis[J].Ann Thorac Surg,2011, 92(5):1812-1817.
2013-09-12)
(本文编辑:欧阳卿)
310006 杭州市第一医院呼吸科
