铁铈钛复合氧化物催化剂的制备及其选择性催化还原NO的性能
2014-04-12史荣会董文威
史荣会,董文威,韩 祯,张 涛
(1. 天津大学 化工学院,天津 300072;2. 北洋国家精馏技术工程发展有限公司,天津 300072;3. 天津大学 精馏技术国家工程研究中心,天津 300072)
NOx可导致酸雨、光化学烟雾、臭氧层空洞等严重的环境问题,并对人类的身体健康造成危害[1]。因此,世界各国均通过制定环保法规和实施相应的措施严格控制NOx的排放。目前,以NH3为还原剂的选择性催化还原技术是去除NOx最有效的方法。用于该技术的商业催化剂主要有V2O5-WO3/TiO2和V2O5-MoO3/TiO2。该类催化剂价格昂贵、原料有毒且极易产生二次污染[2]。
CeO2由于具有独特的储氧性能和优良的氧化还原性能,已被广泛应用于脱硝反应[3-4]。Fe2O3常被作为助剂或活性组分应用于催化反应中,它的添加可以提高催化剂的活性和抗SO2中毒性[5]。TiO2具有良好的抗中毒性能,是商业脱硝催化剂的常用载体[6]。
本工作采用共沉淀法制备了一种新型催化剂——铁铈钛复合氧化物催化剂,研究了Fe掺加量、体积空速以及H2O和SO2的加入对其选择性催化还原NO性能的影响;采用XRD和SEM等手段对催化剂的结构和形貌进行了表征。
1 实验部分
1.1 试剂和仪器
Ce(NO3)3,Fe(NO3)3·9H2O,TiOSO4·2H2O,NH3·H2O:分析纯。
Kane KM9106型烟气分析仪:英国凯恩公司;Rigaku D/max-RB型X射线衍射仪:日本理学公司;S4800型场发射扫描电子显微镜:日本Hitachi公司。
1.2 催化剂的制备
铈钛复合氧化物催化剂的制备:按n(Ce)∶n(Ti)=0.2∶1,将Ce(NO3)3、TiOSO4·2H2O和去离子水混合,于室温下搅拌30 min。向混合液中滴加NH3·H2O至溶液pH=10.0,室温下静置2 h。过滤,洗涤,然后将滤饼置于烘箱中于110 ℃下干燥12 h,再在马弗炉中于500 ℃下焙烧5 h,最后经压片、破碎、过筛得到铈钛复合氧化物催化剂,记作Ce0.2TiOx。
铁铈钛复合氧化物催化剂的制备:采用与上述方法相同的共沉淀方法,以Ce(NO3)3,Fe(NO3)3·9H2O,TiOSO4·2H2O为原料,按n(Ce)∶n(Fe)∶n(Ti)分别为0.2∶0.4∶1,0.2∶0.8∶1,0.2∶1.2∶1制备铁铈钛复合氧化物催化剂,分别记作Ce0.2Fe0.4TiOx,Ce0.2Fe0.8TiOx,Ce0.2Fe1.2TiOx。
1.3 催化剂活性的评价
催化反应器采用长800 mm、内径10.0 mm的固定床反应器,进气流量为400 mL/min。模拟烟气组成(φ):NH35×10-4,NO 5×10-4,O25%,以N2作为平衡气。各路气体流量均由质量流量计控制。为减小因催化剂吸附NO引起的实验误差,实验前先将混合气通入反应器约2 h,使催化剂吸附饱和,待反应温度稳定后开始进行选择催化NO反应。
有研究表明[7],Fe可与Ti形成FeTiO3或Fe2TiO5晶体结构,从而限制活性组分的硫酸化,进而提高催化剂的抗H2O和SO2的能力。为此,考察了H2O和SO2的加入对Ce0.2Fe0.8TiOx催化活性的影响。在300℃下稳定反应3 h后,向反应体系中加入H2O 5%(φ)和SO21×10-4(φ),水蒸气由注射泵经加热器加热后注入反应器,反应16 h后停止添加。
1.4 分析方法
对催化剂的结构和形貌进行XRD和SEM表征。采用烟气分析仪测定NO的含量(φ),计算NO的去除率。
2 结果与讨论
2.1 催化剂的表征结果
2.1.1 XRD表征结果
Ce0.2Fe0.4TiOx,Ce0.2Fe0.8TiOx,Ce0.2Fe1.2TiOx,Ce0.2TiOx的XRD谱图见图1。由图1可见,Fe掺加前后催化剂的XRD谱图基本保持不变,未检测到Fe2O3和FeTiO3的特征衍射峰,说明Fe的加入对催化剂晶体的结构没有产生明显的影响,也表明Fe在催化剂上具有良好的分散性[8]。由图1还可见,XRD谱图中未出现CeO2和TiO2的相关衍射峰。这说明Fe,Ce,Ti均以不定形态存在,它们之间形成了良好的固溶体[9],且该固溶体的活性较规则晶体的活性高[10]。
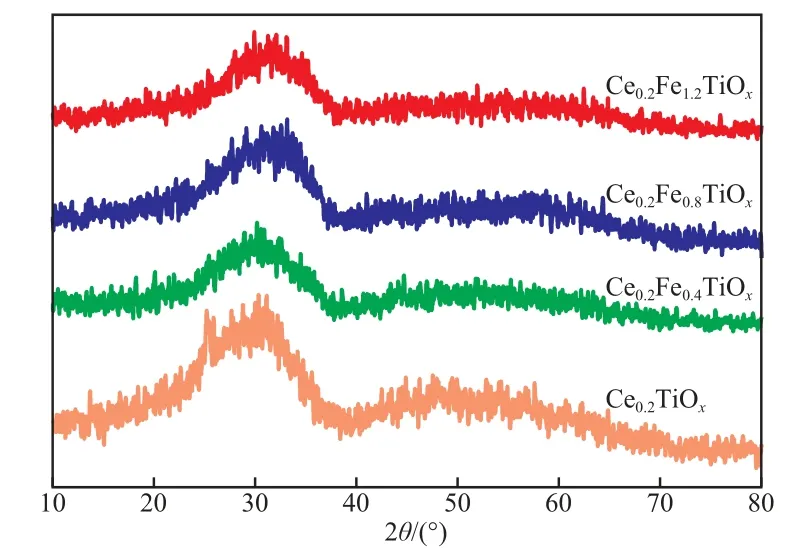
图1 不同催化剂的XRD谱图
2.1.2 SEM表征结果
Ce0.2Fe0.4TiOx,Ce0.2Fe0.8TiOx,Ce0.2Fe1.2TiOx,Ce0.2TiOx的SEM照片见图2。由图2可见:Fe的掺加使催化剂表面的颗粒更均匀,提高了催化剂的分散度;在3种Fe掺加的催化剂中,Ce0.2Fe0.8TiOx的粒径最小,且最为均匀。
2.2 Fe掺加量对催化剂性能的影响
2.2.1 Fe掺加量对NO去除率的影响
在反应时间3 h、体积空速25 000 h-1的条件下,Fe掺加量对NO去除率的影响见图3。由图3可见:NO去除率随反应温度的升高而逐渐增加;在4种催化剂中,未掺加Fe的催化剂(Ce0.2TiOx)的活性最低,这是由于Fe2O3的掺加可以增强反应组分在催化剂表面的吸附,增大NO的去除率;在Fe掺加的催化剂中,Ce0.2Fe0.8TiOx的催化效果最好,当反应温度为250 ℃时,NO的去除率达到99.8%;Ce0.2Fe1.2TiOx的催化活性较Ce0.2Fe0.8TiOx低,可能是由于掺加了过多的Fe使催化剂表面形成了Fe2O3,堵塞了催化剂的孔道,导致催化剂活性的降低。

图2 不同催化剂的SEM照片a Ce0.2TiOx;b Ce0.2Fe0.4TiOx;c Ce0.2Fe0.8TiOx;d Ce0.2Fe1.2TiOx
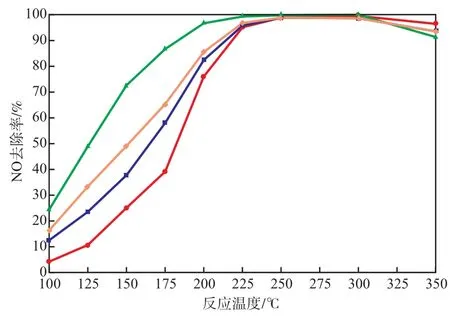
图3 Fe掺加量对NO去除率的影响● Ce0.2TiOx;■ Ce0.2Fe0.4TiOx;▲ Ce0.2Fe0.8TiOx;◆ Ce0.2Fe1.2TiOx
2.2.2 Fe掺加量对N2选择性的影响
在反应时间3 h、体积空速25 000 h-1的条件下,Fe掺加量对N2选择性的影响见图4。由图4可见:当反应温度为100~250 ℃时,4种催化剂的N2选择性基本保持在100%;当反应温度高于250 ℃后,随Fe掺加量的增加,N2选择性略有降低,但4种催化剂的N2选择性均在95%以上。综合考虑催化剂的性能,选择Ce0.2Fe0.8TiOx作为选择性催化还原NO的催化剂较为适宜。
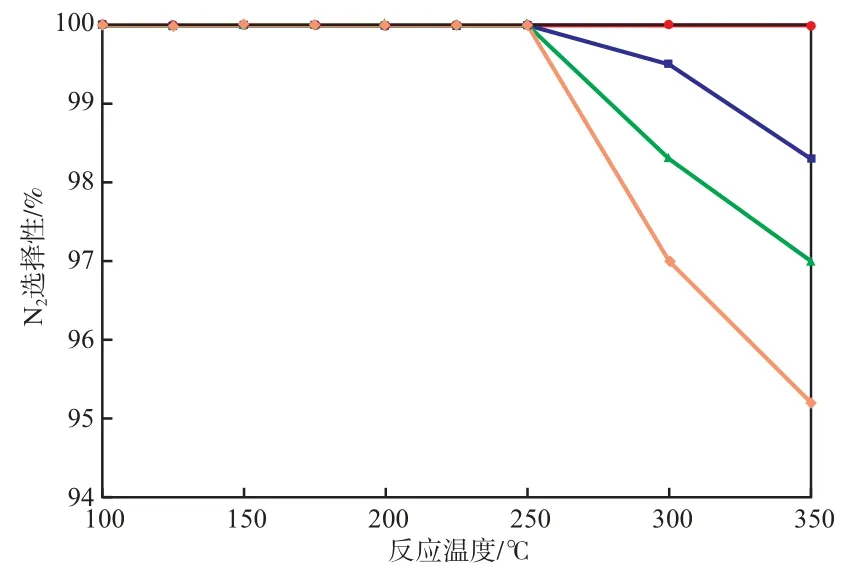
图4 Fe掺加量对N2选择性的影响● Ce0.2TiOx;■ Ce0.2Fe0.4TiOx;▲ Ce0.2Fe0.8TiOx;◆ Ce0.2Fe1.2TiOx
2.3 反应条件对Ce0.2Fe0.8TiOx催化活性的影响
2.3.1 体积空速对NO去除率的影响
在反应时间为3 h的条件下,体积空速对NO去除率的影响见图5。由图5可见:在反应温度为100℃的条件下,当体积空速由25 000 h-1提高至100 000 h-1时,NO去除率由24.4%降至6.7%;在反应温度为175 ℃的条件下,体积空速由25 000 h-1提高至100 000 h-1时,NO去除率的降幅最大;在反应温度为300 ℃的条件下,体积空速为25 000,50 000,100 000 h-1时的NO去除率分别为99.8%,99.1%,94.4%,均达90.0%以上。由此可见,Ce0.2Fe0.8TiOx催化剂在高空速条件下仍具有较好的催化性能。
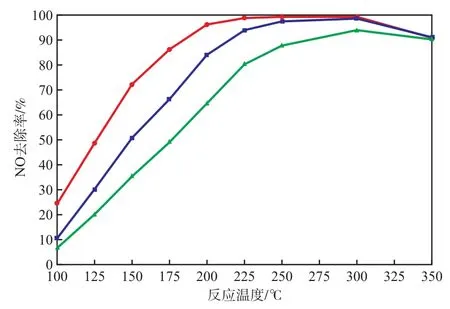
图5 体积空速对NO去除率的影响体积空速/h-1:● 25 000;■ 50 000;▲ 100 000
2.3.2 H2O和SO2的加入对NO去除率的影响
在反应温度300 ℃、体积空速25 000 h-1的条件下,H2O和SO2的加入对NO去除率的影响见图6。由图6可见:H2O和SO2的加入使NO去除率略有降低;同时加入H2O和SO2时的NO去除率略低于单独添加H2O或SO2时的NO去除率,但NO去除率均在90.0%以上;反应16 h后,停止添加H2O和SO2,NO去除率逐渐恢复。当SO2和H2O共同存在时,可与NH3发生反应,生成硫酸铵和硫酸氢铵类物质,沉积在催化剂表面使催化剂失活。SO2和H2O还可使催化剂的活性组分硫酸化,造成催化活性的下降[11]。Fe的掺加在一定程度上抑制了催化剂活性组分的硫酸化,同时也可促进硫酸铵盐类物质的分解[12]。
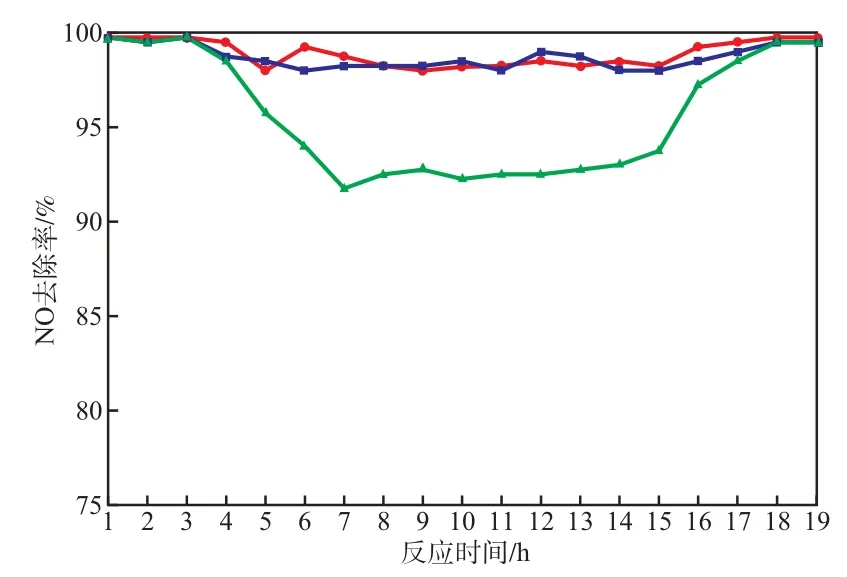
图6 H2O和SO2的加入对NO去除率的影响● SO2;■ H2O;▲ SO2+H2O
3 结论
a)XRD和SEM表征结果显示,Fe的掺加使铁铈钛复合氧化物催化剂表面的颗粒更均匀,提高了催化剂的分散度。
b)Fe的掺加显著提高了铁铈钛复合氧化物催化剂的活性。以Ce0.2Fe0.8TiOx为催化剂,在反应温度250 ℃、反应时间3 h、体积空速25 000 h-1的条件下,NO去除率达99.8%,N2选择性为100%。
c)Fe的掺加显著提高了Ce0.2Fe0.8TiOx催化剂的抗H2O和SO2的能力。在反应温度300 ℃、体积空速25 000 h-1的条件下,向反应体系中同时加入H2O和SO2,催化剂活性受到明显抑制,但NO去除率仍达90.0%以上,停止添加H2O和SO2时NO的去除率又逐渐恢复。
[1] Bosch H,Janssen F. Catalytic reduction of nitrogen oxides:A review on the fundamentals and technology[J].Catal Today,1988,2(4):369-521.
[2] Lietti L,Ramis G,Berti F,et al. Chemical and mechanistic aspects of the selective catalytic reduction of NOxby ammonia over oxide catalysts:A review[J]. Appl Catal,B,1998,18(1/2):1-36.
[3] Shan Wenpo,Liu Fudong,He Hong,et al. Novel cerium-tungsten mixed oxide catalyst for the selective catalytic reduction of NOxwith NH3[J]. Chem Commun,2011,47:8046-8048.
[4] Chen Xiongbo,Gao Shan,Wang Haiqiang,et al. Selective catalytic reduction of NO over carbon nanotubes supported CeO2[J]. Catal Commun,2011,14(1):1-5.
[5] Wu Zhongbiao,Jiang Boqiong,Liu Yue. Effect of transition metals addition on the catalyst of manganese/titania for low-temperature selective catalytic reduction of nitric oxide with ammonia[J]. Appl Catal,B,2008,79(4):347-355.
[6] Xu Wenqing,Yu Yunbo,Zhang Changbin,et al. Selective catalytic reduction of NO by NH3over a Ce/TiO2catalyst[J]. Catal Commun,2008,9(6):1453 -1457.
[7] Liu Fudong,He Hong,Zhang Changbin,et al. Mechanism of the selective catalytic reduction of NO with NH3over environmental-friendly iron titanate catalyst[J]. Catal Today,2011,175(1):18-25.
[8] 熊志波,路春美. 铁铈复合氧化物催化剂SCR脱销的改性研究[J]. 燃料化学学报,2013,41(3):361 -367.
[9] Liu Fudong,He Hong,Zhang Changbin,et al. Selective catalytic reduction of NO with NH3over iron titanate catalyst:Catalytic performance and characterization[J]. Appl Catal,B,2010,96(3/4):408-420.
[10] Pena D A,Uphade B S,Smirniotis P G. TiO2-supported metal oxide catalysts for low-temperature selective catalytic reduction of NO with NH3:I. Evaluation and characterization offirst row transition metals[J]. J Catal,2004,221(2):421-431.
[11] Xu Wenqing,He Hong,Yu Yunbo. Deactivation of a Ce/TiO2catalyst by SO2in the Selective Catalytic Reduction of NO by NH3[J]. J Phys Chem C,2009,113(11):4426-4432.
[12] Liu Fudong,He Hong,Zhang Changbin. Novel iron titanate catalyst for the selective catalytic reduction of NO with NH3in the medium temperature range[J].Chem Commun,2008,17:2043-2045.
