改良FLAG方案治疗难治性急性髓系白血病的临床观察
2014-04-12张开峰韦菊英肖峰孟海涛钱文斌
张开峰 韦菊英 肖峰 孟海涛 钱文斌
改良FLAG方案治疗难治性急性髓系白血病的临床观察
张开峰 韦菊英 肖峰 孟海涛 钱文斌
目的 探讨阿糖胞苷(Ara-C)联合氟达拉滨(Flu)组成的改良FLAG方案治疗难治性急性髓系白血病(AML)患者的疗效及安全性。方法采用改良FLAG方案治疗难治性AML患者14例,其中原发难治性AML 8例,复发难治性AML 6例。具体方案为氟达拉滨(Flu)30mg/(m2·d),静脉滴注,d1~5;阿糖胞苷(Ara-C)1g/(m2·d),静脉滴注,d1~5;粒细胞集落刺激因子(G-CSF)5μg/(kg·d),皮下注射,d0~5。结果治疗1个疗程后,14例患者中7例获得完全缓解(CR),CR率50%;2例部分缓解(PR),PR率14.3%;5例未缓解(NR);总有效率(CR+PR)为64.3%。无一例治疗相关性死亡。结论改良FLAG方案是治疗难治性AML的有效方案,且安全性良好。
急性髓系白血病 难治性 FLAG方案
成人急性髓细胞白血病(AML)在联合化疗诱导治疗后缓解率可达60.0%~80.0%,但是仍有20.0%~40.0%的成人AML患者归为难治,难治性AML的治疗已成为AML治疗中的重点和难点。标准剂量的FLAG方案在难治性AML中有较好的疗效,但化疗相关不良反应较大,早期病死率较高。为使之更适合临床应用,笔者将其中阿糖胞苷(Ara-C)的剂量减低为1g/(m2·d),以改良FLAG方案治疗了难治性AML患者14例,并观察其疗效及安全性,现报道如下。
1 资料和方法
1.1 一般资料 选择2009-03—2013-03浙江大学医学院附属第一医院血液科符合条件的患者共14例,其中男9例,女5例,年龄23~63岁,中位年龄47.6岁。原发难治性AML 8例,复发难治性AML 6例。FAB分型:原发难治性AML中M2型3例,M5型4例,M0型1例;复发难治性AML中M2型4例,M5型2例。所有患者均符合难治性AML诊断标准[1]:(1)原发难治性AML:经典方案诱导化疗2个疗程未获完全缓解(CR)者,或者髓外白血病持续存在者;(2)复发难治性AML:第1次CR后6个月内复发者,或者第1次CR后6个月后复发、经正规诱导化疗失败者,以及2次或2次以上复发者。入选患者一般状况尚可,美国东部肿瘤协作组体能状态(ECOG)评分≤2分,并除外急性早幼粒细胞白血病。
1.2 治疗方案 14例患者均采用改良FLAG方案诱导化疗1个疗程,具体为氟达拉滨(Flu)30mg(/m2·d),静脉滴注,d1~5;Ara-C 1g(/m2·d),静脉滴注,d1~5;粒细胞集落刺激因子(G-CSF)5μg(/kg·d),皮下注射,d0~5。所有患者均给予预防感染措施如口腔护理、坐浴、空气消毒
等,对于重度贫血及血小板<20×109/L的患者给予相应的成分输血。
1.3 观察指标 化疗前给予完善各项检查:血常规、肝肾功能、心电图、心脏B超、胸部CT、骨髓常规及微小残留白血病、染色体。化疗开始后每周检查血常规2次,肝肾功能1次;待血象恢复后,复查骨髓常规及微小残留白血病评估疗效。
1.4 疗效判定 参照张之南《血液病诊断及疗效标准》第3版[1],将患者疗效分为CR、部分缓解(PR)、未缓解(NR),CR和PR均归为有效。治疗不良反应按WHO不良反应分级标准进行评估。
2 结果
2.1 14例难治性AML患者的临床资料 见表1。
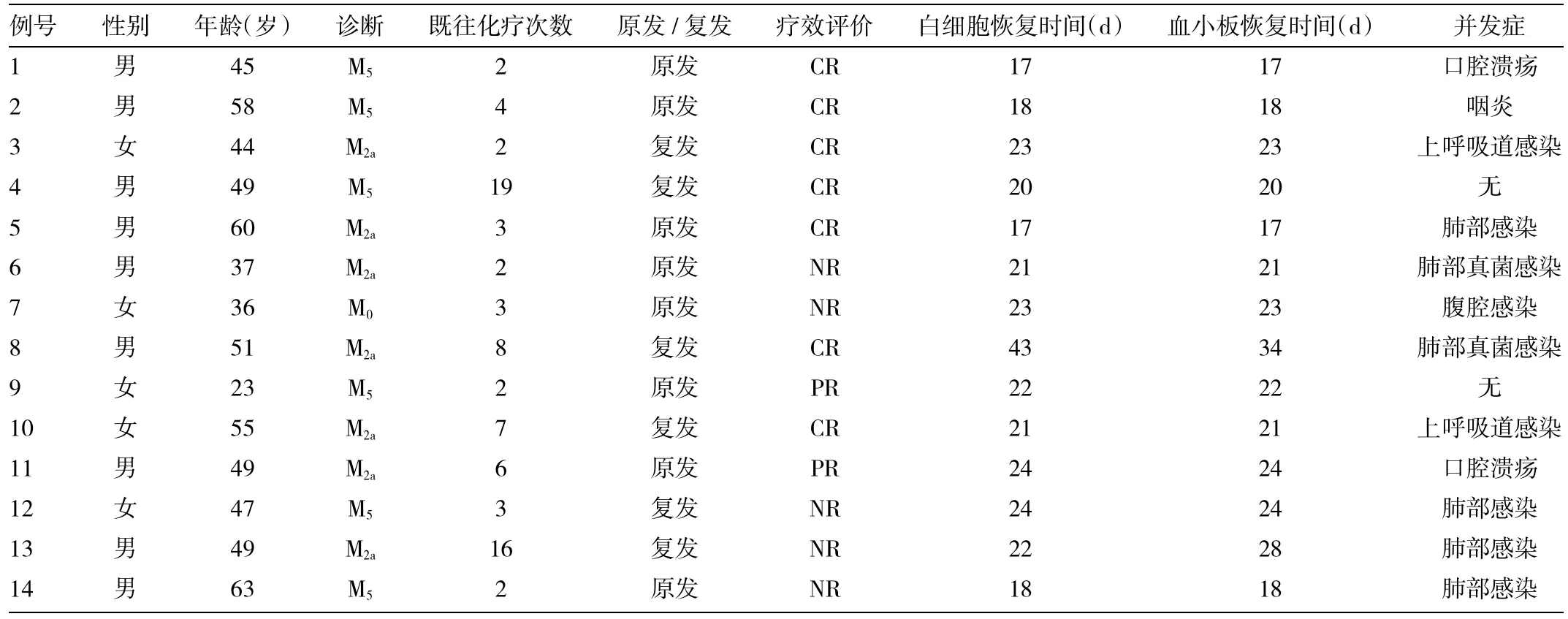
表1 14例难治性AML患者的临床资料
2.2 治疗效果 14例患者中7例CR(50.0%),PR 2例(14.3%),NR 5例(35.7%),有效率为64.3%,早期死亡0例(0.0%)。其中8例原发难治AML患者中CR 3例(37.5%);PR 2例(25.0%),有效率62.5%;6例复发难治AML患者中CR 4例(66.7%);PR 0例(0.0%),有效率 66.7%。14例患者的总生存率在 36个月时为55.4%,48个月时为36.9%;FLAG方案化疗后12个月时的总生存率为 50.0%,24个月时的总生存率为33.3%,见图1-2。
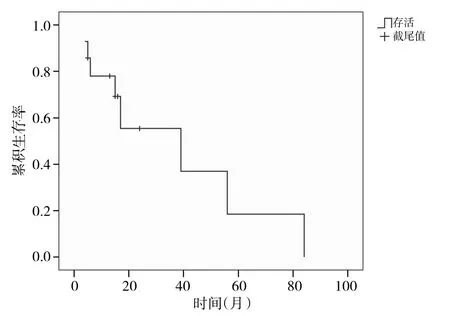
图1 患者总生存曲线
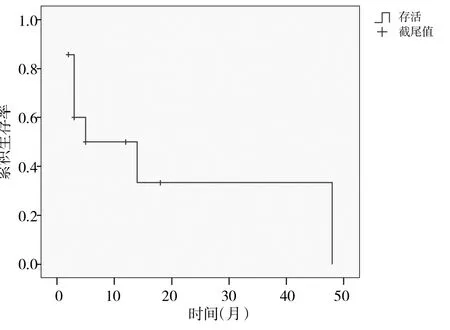
图2 FLAG方案化疗后患者生存曲线
2.3 不良反应 14例患者均出现4级血液学不良反应,其中12例发生感染。CR患者中性粒细胞计数恢复≥1.0×109/L的中位时间为21.5d,血小板计数恢复≥30× 109/L的中位时间为21.5d,无一例治疗相关性死亡。非血液学不良反应包括胃肠道反应、口腔溃疡、肝功能损害、肾功能不全、脱发等,多为轻、中度或暂时性反应,对症处理后好转,未发现心脏和中枢神经系统不良反应。
3 讨论
难治性AML对常规化疗反应差,缓解率低,是临床治疗的一个难点。目前对于难治性AML的治疗手段包括选用二线化疗药物、加大化疗药物剂量、联合新药、分子靶向治疗以及多药耐药逆转剂等,这些方案对于难治性AML疗效各异,大部分疗效欠佳[2-3]。Ara-C是目前治疗难治性AML最重要的药物之一,其疗效与渗入到细胞内形成三磷酸阿糖胞苷(Ara-CTP)的浓度有关。Flu是氟化嘌呤类免疫抑制剂,与Ara-C具有协同作用,在Ara-C前4h使用Flu可显著提高白血病细胞内Ara-CTP浓度,与G-CSF组成FLAG方案治疗难治性AML,具有更好治疗效果[4]。
国内外临床研究中,标准FLAG方案中的Ara-C用量多为2~3g/(m2·d),连用4~5d,其CR率约在50.0%~64.0%。Lee等[5]用Ara-C 2g/(m2·d)的标准方案治疗29例难治、复发AML,CR率为47.5%。采用大剂量Ara-C的方案骨髓抑制明显,造血恢复中位时间可长达25d左右[6],治疗相关性病死率达10.0%~15.0%[7-8],使其临床应用受到一定的限制。本研究中将Ara-C的剂量减低为1g/(m2·d)之后,CR率仍达50.0%;其中在复发难治性患者中CR率可达66.7%,疗效与含有大剂量Ara-C的标准FLAG方案[7-8]相似,且无一例化疗相关性死亡,提示1g/(m2·d)Ara-C组成的改良FLAG方案不良反应更低,临床应用更安全。
本研究还发现,改良FLAG方案治疗后原发难治性AML组患者CR率为37.5%,明显低于复发难治性AML组(CR率66.7%),但病例数太少,无法进行统计学分析。Lee等[5]以FLAG方案治疗后原发难治组CR率为38.9%;复发难治组CR率为66.7%,与本研究结果类似,提示FLAG方案更适合于复发难治性AML患者的治疗。
Becker等[9]报道,标准FLAG方案治疗难治、复发AML患者的平均生存期仅为3~8个月;Lee等[5]报道为14.3个月。Wierzbowska等[10]采用克拉屈滨代替Flu联合Ara-C和米托蒽醌组成CLAG-M方案治疗75例难治性AML患者,CR率为50.7%,但化疗后仅21.0%的患者生存期超过2年。本研究中患者行改良FLAG方案化疗后的12个月总生存率为50.0%,24个月为33.3%;提示嘌呤类药物联合Ara-C的化疗方案中Ara-C剂量减低为1g/(m2·d)能显著减少治疗相关性死亡,延长患者生存时间。
综上所述,本研究发现1g/(m2·d)Ara-C组成的改良FLAG方案对难治性AML治疗有较高的CR率,早期病死率较低,患者总生存率较高,但由于本研究病例数较少,故其远期疗效和不良反应有待于扩大病例数,进行多中心研究进一步证实。
[1]张之南,沈悌.血液病诊断及疗效标准[M].3版.北京:科学出版社, 2007:103-134.
[2]王季石,卢英豪.难治性白血病诊治进展[J].白血病·淋巴瘤,2009,18 (6):367-371.
[3]朱雄鹏,马跃华,刘德龙.急性髓细胞白血病治疗新进展:第51届美国血液学年会热点[J].白血病·淋巴瘤,2010,19(2):97-102.
[4] Bashey A,Liu L,Ihasz A,et al.Non-anthracycline based remission induction therapy for newly diagnosed patients with acute myeloid leukemia aged 60 or older[J].Leuk Res,2006,30(4):503-506.
[5] Lee S R,Yang D H,Ahn J S,et al.The clinical outcome of FLAG chemotherapy without idarubicin in patients with relapsed or refractory acute myeloid leukemia[J].J Korean Med Sci,2009,24(3):498-503.
[6]姚鲲,廖爱军,杨威,等.FLAG方案治疗复发、难治急性白血病的疗效观察[J].临床血液学杂志,2011,24(9):548-549.
[7] Ferrara F,Palmieri S,Pocali B,et al.De novo acute myeloid leukemia with multilineage dysplasia;treatment results and prognostic evaluation from a series of 44 patients treated with fludarabine,cytarabine and G-CSF(FLAG)[J].Eur J Haematol,2002,68 (4):203-209.
[8] Jackson G,Taylor P,Smith G M,et al.A multicentre,open,noncomparative phase II study of a combination of fludarabine phosphate,cytarabine and granulocyte colony-stimulating factor in relapsed and refractory acute myeloid leukemia and de novo refractory anaemia with excess of blasts in transformation[J].Br J Haematol,2001,112(1):127-137.
[9]Becker P S,Kantarjian H M,Appelbaum F R,et al.Retrospective comparison of clofarabine versus fludarabine in combination with high-dose cytarabine with or without granulocyte colony-stimulating factor as salvage therapies for acute myeloid leukemia[J].Haematol,2013,98(1):114-118.
[10]Wierzbowska A,Robak T,Pluta A,et al.Cladribine combined with high doses of arabinoside cytosine,mitoxantrone,and G-CSF (CLAG-M)is a highly effective salvage regimen in patients with refractory and relapsed acute myeloid leukemia of the poor risk:a final report of the Polish Adult Leukemia Group[J].Eur J Haematol,2008,80(2):115-126.
Modified FLAG regimen in treatment for refractory acute myeloid leukemia
ObjectiveTo investigate the efficacy and safety of modified FLAG regimen in treatment of refractory acute myeloid leukemia(AML).MethodsFourteen patients with refractory AML,including 8 cases of primary refractory AML and 6 cases of relapsed refractory AML,were treated with modified FLAG regimen consisting of fludarabine(Flu)30mg/(m2·d),d1~5, cytarabine(Ara-C)1g/(m2·d),d1~5,granulocyte colony-stimulating factor(G-CSF)5μg/(kg·d),d0~5.ResultsThere were 7 cases of complete remission(CR),2 cases of partial remission(PR)and 5 patients had no response(NR)in this series,with a CR rate of 50.0%and an overall response rate of 64.3%.ConclusionThe modified FLAG regimen is safe and effective for treatment of refractory AML.
Acute myeloid leukemia Refractory FLAG regimen


2013-10-18)
(本文编辑:胥昀)
浙江省卫生厅课题资助项目(2012KYA069)
310003 杭州,浙江大学医学院附属第一医院血液科(张开峰系进修医师,现在嵊州市人民医院血液科工作)
韦菊英,E-mail:weijuy@hotmail.com
