天山花楸平喘胶囊的质量标准研究
2014-04-11李改茹刘玉花常军民程煜凤何家伟
李改茹, 刘玉花, 常军民*, 程煜凤, 何家伟
(1.新疆医科大学药学院, 新疆 乌鲁木齐 830011;2.新疆医科大学第一附属医院,新疆 乌鲁木齐830054)
天山花楸平喘胶囊的质量标准研究
李改茹1, 刘玉花2, 常军民1*, 程煜凤1, 何家伟2
(1.新疆医科大学药学院, 新疆 乌鲁木齐 830011;2.新疆医科大学第一附属医院,新疆 乌鲁木齐830054)
目的 建立天山花楸平喘胶囊的质量标准。 方法 用薄层色谱法 (TLC) 对胶囊内容物中金丝桃苷、 苦杏仁苷进行定性鉴别; 采用高效液相色谱法测定金丝桃苷、 槲皮素和山柰素的量。 结果 TLC鉴别专属性强, 斑点清晰、 分离度好, 阴性对照无干扰; 金丝桃苷、 槲皮素和山柰素进样量分别在 3.72 ~74.4 μg(r=0.999 9)、 8.00 ~64.00 μg(r=0.999 3)、 2.00 ~16.00 μg(r=0.999 3) 范围内与其峰面积积分值呈良好的线性关系, 平均回收率分别为101.2%、 97.3%和 93.7%, RSD分别为 1.4% (n=9)、 2.6%和 1.9% (n=6)。 结论 所建标准可用于天山花楸平喘胶囊的质量控制。
天山花楸; 平喘胶囊; 质量标准; TLC; HPLC
天山花楸 Sorbus tianshanica Ruper.为新疆民间特有天然植物药,维吾尔和哈萨克族常以其嫩枝、叶和果实入药,具有清肺止咳,补脾生津,补血补气的功效[1-3]。根 据天然 药物 5 类新药 的申报要求,在前期对天山花楸药用部位的提取分离工艺研究和天山花楸平喘胶囊的成型工艺的研究基础上,为保证该新药制剂的安全性和临床有效性,对其进行了质量标准的临床前研究[4-9]。
1 仪器与试药
高效液相色谱仪 ( 日本 岛津, LC-20AB泵,SPD-20A紫 外 检 测 器), 色 谱 柱 ( shim-pack Vp-ODS 柱,150 mm×4.6 mm, 5 μm), Lcsolution 工作站, CAMAG LIONMAT 5 薄层色谱半自动点样仪(瑞士卡玛公司), CAMAG REPROSTAR 3 薄层色谱数码成像系统 (瑞士卡玛公司),DHO-9075A型电热鼓风干燥箱 (上海恒科仪器有限公司), AB-135-S 型 电 子 分 析 天 平 ( 托 利 多-梅 特 勒 有 限 公司), SHH-500SD药品稳定性试验箱 (重庆永生实验仪器厂),KQ-500DZ超声清洗器 (昆山市超声仪器有限公司, 500 W, 40 kHz), 聚酰胺薄膜薄层板 (浙江台州市路桥四甲塑料厂), GF254薄层板 (Merck 公司)。
金丝桃苷对照品 (中国固体制剂制造技术国家工程研究中心, 批号 J20-110411 )) ; 苦杏仁苷对照品 (中国药品生物制品检定所, 批号 110820-200403); 槲皮素对照品 (中国食品药品检定研究院, 批号 100081-200406); 山柰素对照品 (中国食品药品检定研究院,批号 110861-200808);天山花 楸 平 喘 胶 囊 ( 批 号 20121029、 20121030、20121031) 及阴性样品由新疆医科大学药物分析教研室提供; 甲醇 ( Burdick&Jackson 色谱纯), 乙腈 (Burdick&Jackson 色谱纯), 超纯水, 其他试剂均为分析纯。
2 方法与结果
2.1 薄层鉴别
2.1.1 金丝桃苷的薄层鉴别 分别称取 3 批天山花楸平喘胶囊内容物各 40 mg, 加甲醇 4 mL经超声溶解后过滤,将滤液作为供试品溶液;称取金丝桃苷对照品2mg, 加甲醇制成每1mL含1mg的对照品溶液;取天山花楸平喘胶囊阴性处方样品,将内容物按供试品溶液的制备方法,制成阴性样品溶液。 吸取上述溶液各 2 μL, 分别点于同一聚酰胺薄膜薄层板上,分别以乙酸乙酯-甲酸-水 (8 ∶1 ∶1) 和乙酸乙酯-甲醇-甲酸 (10 ∶5 ∶3) 为展开剂,展开, 取出, 晾干, 喷以 5%AlCl3乙醇溶液, 晾干, 电吹风吹至斑点显色清晰, 紫外光灯 (366 nm) 下检视。 结果, 在 2 种展开条件的供试品色谱中,均在与对照品色谱相应位置处显相同颜色的斑点, 阴性对照无干扰。 见图1。

图1 金丝桃苷的 TLC图Fig.1 TLC diagram of hyPerin
2.1.2 苦杏仁苷的薄层鉴别 分别称取 3 批天山花楸平喘胶囊内容物各 160 mg, 加甲醇 8 mL行超声溶解后过滤,将滤液蒸干, 加入2 mL甲醇作为供试品溶液; 称取苦杏仁苷对照品 3 mg, 加甲醇制成每1 mL含3 mg的对照品溶液; 取天山花楸平喘胶囊阴性处方样品,将内容物按供试品溶液的制备方法,制成阴性样品溶液。吸取阳性、阴性对照品溶液各 3 μL, 供试品溶液各 2 μL, 分别点于同一 GF254薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15 ∶40 ∶22 ∶10)在 5 ~10 ℃放置 12 h 的下层为展开剂, 展开, 取出, 立即喷以 0.8%磷钼酸的15%硫酸乙醇溶液 (临用现配), 105 ℃加热 3 ~4 min 显色, 白光下检视; 吸取阳性、 阴性对照品溶液各 3 μL,供试品溶液各 2 μL, 分别点于同一GF254薄 层 板 上, 以 三 氯 甲 烷-乙 酸 乙 酯-甲 醇-水(3 ∶8 ∶5 ∶2) 在 5 ~10 ℃放置 12 h 的下层为展开剂, 展开, 取出, 晾干, 喷以磷钼酸显色剂 (2 g磷钼酸溶于 20 mL水中, 再缓缓加入 30 mL硫酸,临用现配), 105 ℃加热 3 ~4 min 显色, 白光下检视。结果,在2种展开条件的供试品色谱中,均在与对照品色谱相应位置处显相同颜色的斑点,阴性对照无干扰。见图2。

图2 苦杏仁苷的 TLC图Fig.2 TLC diagram of am ygdaline
2.2 金丝桃苷的测定
2.2.1 色 谱条件与系统适用性试 验 shim-pack Vp-ODS 色谱柱 (150 mm×4.6 mm,5 μm); 流动相为乙腈-0.1% 磷酸 (26 ∶84); 检测波长 360 nm, 体积流量 1 m L/min; 柱温 30 ℃; 进样量 10 μL。 在此色谱条件下, 供试品中金丝桃苷色谱峰与其他组分色谱峰能够达到基线分离,与对照品色谱峰保留时间一致;理论塔板数按金丝桃苷峰计算应不低于4 000。 结果见图 3。
2.2.2 对照品溶液的制备 精密称取金丝桃苷对照品适量, 置25 mL量瓶中, 加甲醇制成每 1 m L含 0.186 mg的溶液, 即得。
2.2.3 供试品溶液的制备 精密称取本品内容物100 mg, 置具塞锥形瓶中, 加40 mL甲醇,超声处理 30 min 后过滤, 置 50 mL量瓶中, 放冷, 加甲醇定容至刻度, 进样前 过 0.2 μm 微孔滤膜,即得。
2.2.4 阴性对照品溶液的制备 取阴性样品, 按“2.2.3” 项下方法配制阴性对照溶液。
2.2.5 线性关系考察 精密量取金丝桃苷对照品溶液 0.2、 0.5、 1、 2、 3、4 mL分别置 10mL量瓶中, 用甲醇定容至刻度, 摇匀, 分别进样 10 μL。以峰面积积分值对质量浓度进行线性回归,得方程Y=21 760X+2 669.5 (r=0.999 9)。 结果表明,金丝桃苷在 3.72 ~74.4 μg/mL范围内与峰面积的线性关系良好。
2.2.6 精密度试验 精密量取金丝桃苷对照品溶液适量,在上述色谱条件下连续进样6次,记录峰面积。 结果, RSD为 1.32% (n=6), 表明仪器精密度良好。
2.2.7 稳定性试验 精密称取批号为 20121029 的胶囊内容物适量, 按照 “2.2.3” 项制备, 上述色谱条件, 分别于 0、 2、 4、 6、 8、 10、 12 h 测定金丝桃苷。 结果, RSD为 3.55% (n=6), 表明供试品溶液在12 h内基本稳定。
2.2.8 重复性试验 精密称取批号为 20121029 的胶囊内容物适量, 按 “2.2.3” 项下方法平行制备6份供试品溶液,照上述色谱条件测定。结果,金丝桃苷的平均含有量为 9.09 mg/g, RSD为 1.77%(n=6), 表明方法重复性良好。
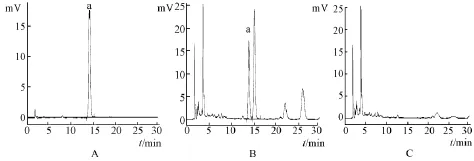
图3 金丝桃苷 HPLC色谱图Fig.3 HPLC chromatogram s of hyPerin
2.2.9 加 样 回 收 率 试 验 精 密 称 取 批 号 为20121029 的胶囊内容物 (含有量为 9.09 mg/g) 适量,加入高、中、低剂量的金丝桃苷对照品溶液,各平行 3 份,按照 “2.2.3”项下方法操作, 在此色谱条件下,用外标法计算回收率。结果,见表1。
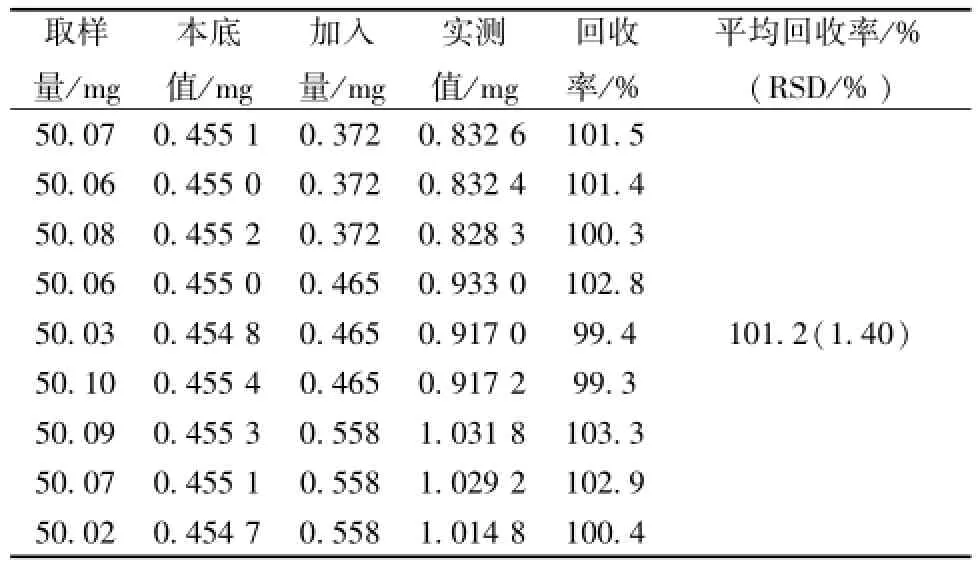
表 1 金丝桃苷的加样回收率考察 (n=9)Tab.1 Results of recovery tests for hyPerin(n=9)
2.2.10 样 品 测 定 分 别 取 批 号 为 20121029、20121030、 20121031 的 3 批天山花楸平喘胶囊内容物, 按上述 “2.2.3” 项操作制备供试品溶液,平行3份,在该色谱条件下进行测定。结果,见表2。
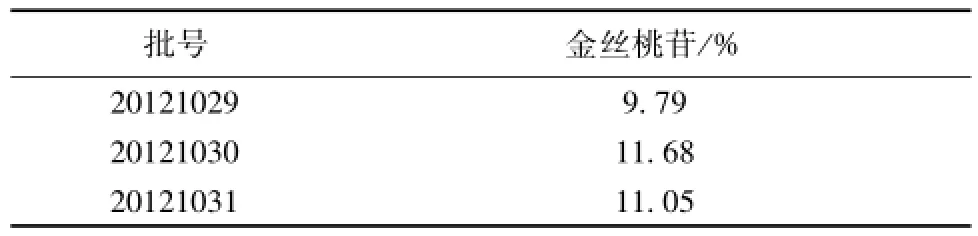
表 2 样品测定 (n=3)Tab.2 Results of conten t determ ination of sam Ples( n= 3)
2.3 黄酮苷的测定
2.3.1 色 谱条件与系统适用性试验 shim-pack Vp-ODS 色谱柱 (150 mm×4.6 mm,5 μm); 流动相为甲醇-0.1% 磷酸 (52 ∶48); 检测波 长 360 nm; 体积流量 1 m L/min; 柱温 30 ℃; 进样量 10 μL。 在此色谱条件下, 供试品中槲皮素、 山柰素的色谱峰与其他组分色谱峰能够达到基线分离,与对照品色谱峰保留时间一致;理论塔板数按槲皮素峰计算应不低于 4 000。 结果见图4。

图4 槲皮素、 山柰素 HPLC色谱图Fig.4 HPLC chromatogram s of quercetin and kaem Pferol
2.3.2 混合对照品溶液的制备 分别精密称取槲皮素、山柰素适量,加甲醇使成每1 mL含槲皮素为160 μg、山柰素为40 μg的混合对照品溶液, 即得。
2.3.3 供试品溶液的制备 精密称取本品 80 mg,置圆底烧瓶中, 加甲醇30 mL, 25%盐酸5 mL, 85℃水浴回流 60 min, 冷却, 转移至 50 mL量瓶中,用甲醇稀释至刻度,摇匀,过滤取续滤液,即得。
2.3.4 阴性对照品溶液的制备 取阴性样品,按“2.3.3” 项下方法制备阴性对照溶液。
2.3.5 线性关系考察 分别精密量取混合对照品贮备液0.5、 1、 2、 3、 4 m L置 10 m L量瓶中, 用甲醇稀释定容。在上述色谱条件下,以槲皮素、山柰素的对照品色谱峰面积 (A) 对进样质量浓度进行线性回归,绘制标准曲线。槲皮素、山柰素的回归方程、 相关系数、线性范围见表3。
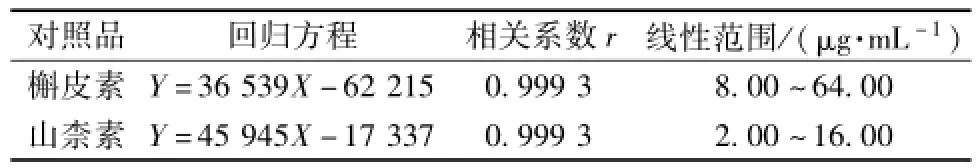
表3 槲皮素、 山柰素的回归方程、 相关系数、线性范围Tab.3 Regression equations, correlation coefficient and linearity ranges of the quercetin, kaem Pferol
2.3.6 精密度试验 精密量取混合对照品溶液(槲皮素 32 μg/mL,山柰素 8 μg/mL),按上述色谱条件测定,记录峰面积值。结果,槲皮素、山柰素的 RSD分别为 1.51%、 1.05% (n=6), 表明仪器精密度良好。
2.3.7 稳定性试验 按照 “2.3.3” 项下方法制备供试品溶液,分别于 0、 2、4、 6、 8、 10 h 进样,按上述色谱条件测定,记录峰面积值。结果,槲皮素、 山柰素 的 RSD分 别为 2.10%、 2.31%(n=6), 表明供试品溶液在 10 h 内基本稳定。
2.3.8 重复性试验 按照 “2.3.3” 项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积值。结果,槲皮素、山柰素的平均含有量为30.63、 7.93 mg/g, RSD分别为 2.03%、 1.86%(n=6), 表明方法重复性良好。
2.3.9 加样回收率试验 精密称取样品 25 mg,平行 6 份, 分别置 100 mL圆底烧瓶中, 分别加入质量浓度为 0.644 mg/mL槲皮素、 0.535 mg/mL山柰素各1 m L, 按照 “2.3.3” 项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积值,用外标法计算回收率。结果,槲皮素、山柰素的平均回 收 率 分 别 为 97.3%、93.7%,RSD 分 别 为2.61%、1.88% (n=6)。

表 4 槲皮素的回收率试验 (n=6)Tab.4 Results of recovery tests for quercetin ( n=6)
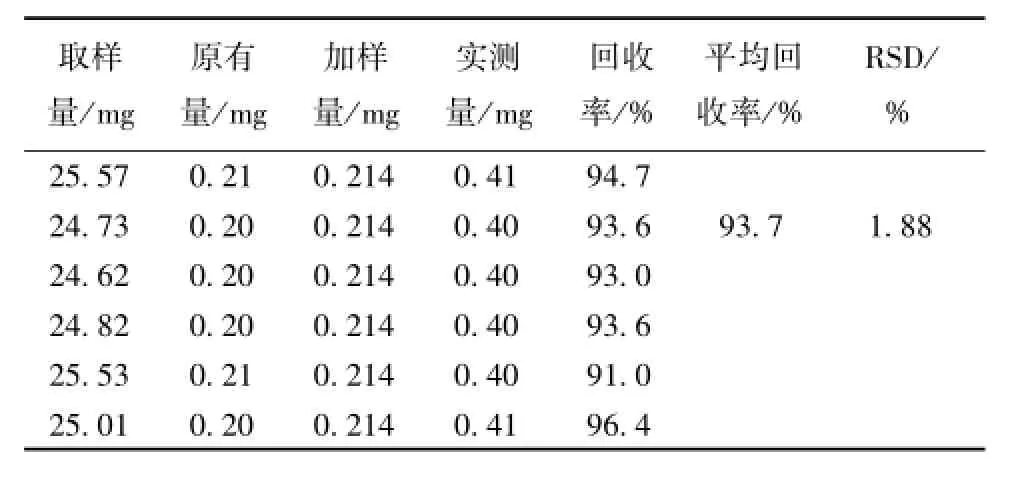
表 5 山柰素回收率试验 (n=6)Tab.5 Resu lts of recovery tests for kaemPferol(n=6)
2.3.10 样 品 测 定 分 别 取 批 号 为 20121029、20121030、 20121031 的 3 批天山花楸平喘胶囊内容物, 按上述 “2.3.3” 项操作制备样品溶液, 平行 3份,按上述色谱条件测定,记录峰面积值,计算天山花楸平喘胶囊内容物中黄酮苷的量 (天山花楸黄酮苷的量 =槲皮素量 ×2.02+山柰素量 ×1.87)。 结果见表 6, 天山花楸中试提取物测定结果见表7。
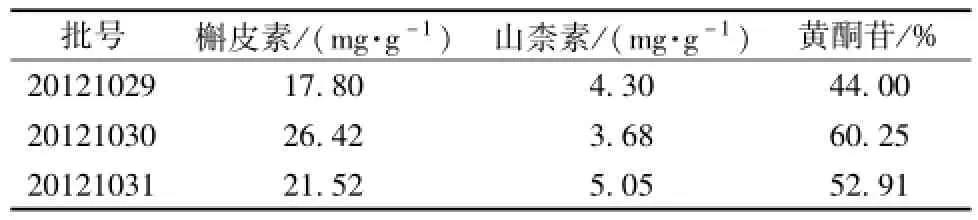
表6 样品测定结果 (n=3)Tab.6 Results of content determ ination of samPles( n= 3)

表7 天山花楸中试提取物测定结果Tab.7 Results of content determ ination of extract
3 讨论
根据 《中国药典》 2010 年版中有关 TLC鉴别的要求, 经过预实验及有关文献的查阅[10], 分别对不同的薄层板、不同的展开剂、点样量等展开条件进行了考察,确定了两种不同的展开条件来定性鉴别天山花楸平喘胶囊中有效成分金丝桃苷和苦杏仁苷。结果,该方法具有较好的重复性和专属性,可快速有效地对胶囊的安全性和有效性进行质量控制。
天山花楸药材中含有的金丝桃苷和苦杏仁苷两种有效成分具有明确的止咳平喘的药理作用。金丝桃苷成分稳定,用等度洗脱方法干扰少,分离度、重现性好, 操作简便, 可快速用 RP-HPLC对其进行分离检测;但苦杏仁苷成分不稳定,对温度敏感,易水解,所以天山花楸药材经提取分离后,含苦杏仁苷量较低, 尝试采用 RP-HPLC分析方法,用不同的梯度洗脱方法来同时对金丝桃苷和苦杏仁苷两种有效 成 分 进行 测 定[10-13],苦 杏 仁 苷的 分 离度都达不到要求, 而采用液-质连用的分析方法达不到快速、操作简单易行的特点,适用范围窄,所以本研究只对苦杏仁苷进行了定性鉴别。
天山花楸药材中含有多种黄酮类化合物,不能进行一一控制, 据文献报道, 采用 RP-HPLC法对两种主要的水解苷元槲皮素和山柰素进行分离检测,用外标法来计算各苷元的量,再利用相对分子质量为610 的芦丁对槲皮素的转换因子 2.02 和相对分子质量为 534 的山柰素糖苷 (山柰素-葡萄糖苷-丙二酸酯) 对山柰素的转换因子 1.87 的转换关系来计算 天山 花 楸 黄酮 苷 的 量[14-16]。 本 法采 用 等度洗脱,重复性好,操作简便,可快速、准确地测定成分含有量,能在一定程度上对天山花楸平喘胶囊进行质量控制。
[ 1 ] 新疆自治区卫生厅.新疆自治区药品标准 [S] 1987 : 14.
[2] 新疆植物志编辑委员会.新疆植物志:第二卷第二分册[M].乌鲁木齐: 新疆人民出版社, 1973: 62-65.
[3] 新疆自治区卫生厅革命委员会.新疆中草药 (维文)[M].乌鲁木齐: 新疆人民出版社, 1973: 77-79.
[4] 赵雪丽,宋 英,谈 静,等.颈康舒胶囊质量标准研究[J].中成药, 2012, 34(3): 494-496.
[5] 王智森, 高 飞, 安丽娜, 等.培根胶囊的质量标准研究[J].中国药房, 2012, 23(7): 635-637.
[6] 周 滢,曹佩雪, 梁光义, 等.芍石护睛胶囊质量标准研究[J].中国实验方剂学杂志, 2011, 17(3): 113-115.
[ 7 ] 范永春.乳欣安胶囊质量标准研究[J].中成药, 2009, 32(5): 786-789.
[8] 张华峰,贾恒明, 赵 广, 等.祛湿止痒颗粒的质量标准[J].中草药, 2011, 42(1): 85-87.
[9] 匡菊香,刘远文, 张倩茹, 等.舍莲胃康胶囊的质量标准研究[J].中国药房, 2012, 23(3): 248-249.
[10] 国家药典委员会.中华人民共和国药典: 2010 年版一部[S].北京: 中国医药科技出版社, 2010.
[11] 李景庄, 胡君萍, 杨建华, 等.HPLC-UV法测定天山花楸金丝桃苷和芦丁的含量[J].药物分析杂志, 2009, 29(2):310-312.
[12] 张 薇, 常军民, 沈美英, 等.RP-HPLC法测定天山花楸果实中苦杏仁苷、 芦丁、 金丝桃苷和橙皮苷的含量[J].药物分析杂志, 2011, 31(5): 935.
[13] 郭 静, 常军民, 孟 磊.HPLC同时测定天山花楸中苦杏仁苷和金丝桃苷[J].中成药, 2009, 31(9): 1451
[14] 李爱红, 胡文军.HPLC法测定银杏叶胶囊中总黄酮苷的含量[ J] .中国药房, 2008, 19(12) : 927-928.
[15] 郑永刚, 郁长治, 王 欢, 等.HPLC法测定天山花楸叶提取物黄酮苷的含量[ J].广州化工, 2012, 40 (15):161-163.
[16] 郁长治, 郑永刚, 吴旭东, 等.HPLC法测定沙棘叶黄酮苷的含量[J].中国当代医药, 2012, 19(11): 51-54.
Quality control for Tianshan Huaqiu Asthm a CaPsules
LIGai-ru1, LIU Yu-hua2, CHANG Jun-min1*, CHENG Yu-feng1, HE Jia-wei2
(1.College of Pharmacy, Xinjiang Medical University, Urumqi 830011, China; 2.First Affiliated Hospital of Xinjiang Medical University, Urumqi 830054, China)
Sorbus tianschanica Ruper.; asthma capsule; quality criteria;TLC;HPLC
R927.2
: A
: 1001-1528(2014)01-0106-06
10.3969/j.issn.1001-1528.2014.01.026
2013-04-18
新疆维吾尔自治区科技支撑计划 (201133127)
李改茹 (1975—) , 女, 副教授, 研究方向: 天然药物分析。 E-mail: 164232309@qq.com
*通信作者: 常军民 (1965—) , 男, 教授, 博士, 硕士生导师, 研究方向: 天然药物分析。 E-mail: 1617265908@qq.com
