HPLC-ELSD法同时测定心脑舒口服液中 7 种皂苷类成分
2014-04-11刘广桢刘洪超徐丽华
林 林, 刘广桢, 刘洪超, 徐丽华
(山东省食品药品检验所,山东 济南 250101)
[质 量]
HPLC-ELSD法同时测定心脑舒口服液中 7 种皂苷类成分
林 林, 刘广桢, 刘洪超, 徐丽华
(山东省食品药品检验所,山东 济南 250101)
目的 建立同时测定心脑舒口服液 (人参、 黄芪、 五味子、 党参、 麦冬) 中人参皂苷 Rg; 人参皂苷 Re; 人参皂苷 Rf; 人参皂苷 Rb1; 人参皂苷 Rb2; 人参皂苷 Rb3; 黄芪甲苷的方法。 方法 采用 HPLC-ELSD法; Kromasil C18色谱柱; 乙腈-水为流动相; 体积流量为 1mL/min。 结果 根据回归方程, 7 种成分人参皂苷 Rg1、 人参皂苷 Re、 人参皂苷 Rf、 人参皂苷 Rb1、 人参皂苷 Rb2、 人参皂苷 Rb3、 黄芪甲苷分别在 0.202 8 ~2.028 μg( r=1.00), 0.378 8 ~3.788 μg(r=1.00), 1.686 2 ~16.862 μg(r=1.00), 0.843 4 ~8.434 μg(r=1.00), 0.204 8 ~2.048 μg(r= 1.00), 0.181 6 ~1.816 μg(r=1.00) 和 0.116 6 ~1.166 μg(r=1.00) 范围内呈良好的线性关系, 平均回收率分别为 98.1% (RSD为 1.1%), 98.1% (RSD为 0.87%), 98.5% (RSD为 0.58%),98.2% (RSD为 0.58%),98.6%(RSD为 0.49%),98.7% (RSD为 1.1%), 98.5% (RSD为 0.42%)。 结论 该方法多种成分同时测定, 操作简便、准确、重复性好,可用于心脑舒口服液的质量控制。
心脑舒口服液; 人参皂苷 Rg1; 人参皂苷 Re; 人参皂苷 Rf; 人参皂苷 Rb1; 人参皂苷 Rb2; 人参皂苷 Rb3;黄芪甲苷
心脑舒口服液由人参、黄芪、五味子、党参、麦冬五味药组成,具有补气养阴的作用,主要用于气阴两虚而致的头晕目眩,失眠健忘,心悸怔仲,短气肢倦,自汗盗汗,不耐烦劳等症。现行质量标准收载于 《卫生部药品标准》 中药成方制剂第 17册,仅有人参中人参二醇、人参三醇的薄层鉴别项。为进一步提高该制剂的质量控制,本实验基于中药配伍君臣佐使的基本原则,参考相关文献[1-15], 建立了心脑舒口服液中主要药味人参、 黄芪中 7 种皂苷类成分人参皂苷 Rg1、人参皂苷 Rb1、人参皂苷 Rb2、 人参皂苷 Rb3、 人参皂苷 Re、 人参皂苷 Rf和黄芪甲苷的同时测定方法。 通过方法学验证,该方法操作简便、准确、重复性好,为全面控制心脑舒口服液的质量提供参考依据。
1 仪器与试药
Agilent1200 高效液 相色谱 仪 ( 四元梯 度泵、自动进样器、 蒸发光散射检测器、 Agilent色谱工作站), Mettler AE240 电子天平 ( 瑞 士 梅 特勒公司); 黄芪甲苷对照品 (批号 110781-200613)、人参皂苷 Rg1对照品 ( 批号 110703-200424 )、 人参皂苷 Rb1对照品 (批号 110704-200420)、 人参皂苷 Rb2对照品 ( 批号 111715-200501)、人参皂苷Rb3对照品 (批号 111686-200501)、 人参皂苷 Re对照品 (批号 110754-200421)、 人参皂苷 Rf对照品 (批号 111719-200502) 均购自中国食品药品检定研究院;乙腈为色谱纯;其他试剂为分析纯。心脑舒 口 服 液 ( 批 号 分 别 为: 120301、 120302、120303) 由荣昌制药 (淄博) 有限公司提供。
2 方法与结果
2.1 色谱条 件 Kromasil C18色谱 柱 ( 250 mm× 4.6 mm, 5 μm); 以乙腈为流动相 A, 水为流动相B, 梯度洗脱 ( 表 1); 体积流量 1 mL/min, 柱温35℃。
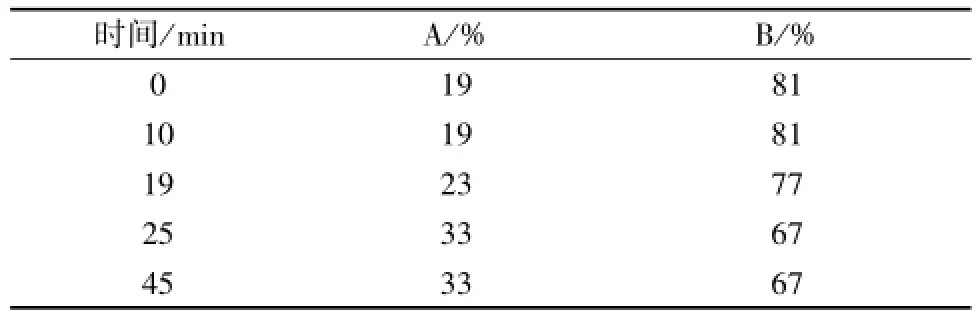
表1 梯度洗脱程序Tab.1 Gradient elution mode ofmobile Phase
2.2 对照品溶液的制备 分别精密称取人参皂苷Rg1、 人参皂苷 Re、 人参皂苷 Rf、 人参皂苷 Rb1、人参皂苷 Rb2、 人参皂苷 Rb3和黄芪甲苷对照品适量, 加甲醇制成质量浓度 为 0.101 4、 0.189 4、 0.843 1、 0.421 7、 0.102 4、 0.090 8、 0.058 3 mg/mL的混合溶液, 作为对照品溶液。
2.3 供试品溶液的制备 取供试品适量, 混匀,精密量取 10 mL, 置分液漏斗中, 加水 10 mL,用正丁醇振摇提取 4 次, 每次 20 mL, 合并正丁醇提取液, 用浓氨试液洗涤 2 次, 每次 30 m L, 弃去氨洗液,正丁醇液蒸干,残渣加甲醇适量使溶解,转移至5 mL量瓶中, 加甲醇至刻度, 摇匀, 滤过,即得。
2.4 阴性溶液的制备 分别取不加黄芪、 人参的空白样品,按供试品溶液的制备项下的方法,制得阴性对照溶液,即得。
2.5 方法的专属性考察 分别精密吸取混合对照品溶液、 供试品溶液及阴性对照溶液各 5 μL, 按“2.1” 项色谱条件分析, 结果见图 1。 人参皂苷Rg1、 人参皂苷 Re、 人参皂苷 Rf、 人参皂苷 Rb1、人参皂苷 Rb2、 人参皂苷 Rb3和黄芪甲苷与其相邻色谱峰的分离度均大于 1.5, 拖尾因子在 0.90 ~1.10, 理论板数以各峰计均在 5 000 以上。阴性对照在相应位置上未见色谱峰,心脑舒口服液中其他组分不干扰7种成分的测定,方法专属性良好。
2.6 线性关系考察 精密量取混合对照品溶液,分别进样 2、 5、 10、 15、 20 μL, 按 “2.1” 项色谱条件分析, 以进样量 (C) 的对数值为横坐标, 峰面积 (A) 的对数值为纵坐标, 进行线性回归, 得到回归方程。 人参皂苷 Rg1回归方程为 ln A=1.23 ln C+5.64 (r=1.00), 人参皂苷 Re回归方程为ln A=1.61 ln C+4.56 ( r=1.00), 人参皂苷 Rf回归方程为 ln A=1.27 ln C+5.51 ( r=1.00), 人参皂苷 Rb1回归方程为 ln A=1.52 ln C+4.71 ( r= 1.00), 人参皂苷 Rb2回归方程为 ln A=1.21 ln C+ 6.34 (r=1.00), 人参皂苷 Rb3回归方程为 ln A= 1.20 ln C+6.44 (r=1.00), 黄芪甲苷回归方程为ln A=1.24 ln C+6.92 (r=1.00)。 结果表明人参皂苷 Rg1、 人 参 皂 苷 Re、 人 参 皂 苷 Rf、 人 参 皂 苷Rb1、 人参皂苷 Rb2、 人参皂苷 Rb3和黄芪甲苷分别在 0.202 8 ~2.028 μg, 0.378 8 ~3.788 μg,1.686 2 ~16.862 μg, 0.843 4 ~ 8.434 μg,0.204 8 ~2.048 μg, 0.181 6 ~ 1.816 μg 和0.116 6 ~1.166 μg范围内线性关系良好。
2.7 精密度试验 取混合对照品溶液, 按 “2.1”项色谱条件分析, 连续进样6次测定, 每次 5 μL,测定峰面积值, 结果人参皂苷 Rg1、 人参皂苷 Re、人参皂苷 Rf、 人参皂苷 Rb1、 人参皂苷 Rb2、 人参皂苷 Rb3和 黄 芪 甲 苷的 RSD值分别为 0.86%、1.2%、 0.76%、 0.84%、 0.59%、 0.87%、1.2%, 表明精密度良好。
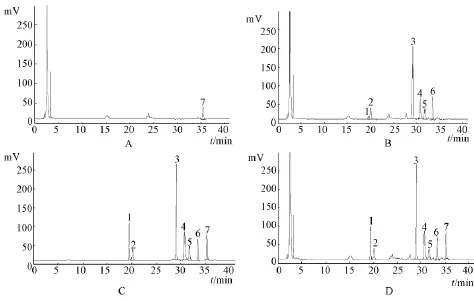
1.人参皂苷 Rg12.人参皂苷 Re 3.人参皂苷 Rf 4.人参皂苷 Rb15.人参皂苷 Rb26.人参皂苷 Rb37.黄芪甲苷1.ginsenoside Rg12.ginsenoside Re 3.ginsenoside Rf 4.ginsenoside Rb15.ginsenoside Rb26.ginsenoside Rb37.astragaloside
2.8 稳定性试验 取同一供试品溶液, 按 “2.1”项色谱条件,分别于 0、 3、6、9、12、 15 h 测定,结果人参皂苷 Rg1、 人参皂苷 Re、 人参皂苷 Rf、人参皂苷 Rb1、 人参皂苷 Rb2、 人参皂苷 Rb3和黄芪甲苷的 RSD值分别为 0.78%、 1.4%、 0.86%、0.59%、 0.79%、0.74%、 0.78%,说明供试品中的7种指标成分在室温条件下15 h内稳定。
2.9 重复性试验 取同一批心脑舒口服液 (批号20120301), 平行制备 6 份供试品溶液, 按 “2.1”项色谱条件分析, 结果人参皂苷 Rg1平均质量浓度为 0.090 4 mg/mL, RSD为 0.76%; 人参皂苷 Re平均质量浓度为 0.204 3 mg/mL, RSD为 1.1%;人参皂苷 Rf平均质量浓度为 0.801 7 mg/mL, RSD为 0.71%; 人参皂苷 Rb1平均质量浓度为 0.428 6 mg/mL, RSD为 1.0%; 人参皂苷 Rb2平均质量浓度为 0.098 8 mg/mL, RSD为0.69%; 人参皂苷 Rb3平均质量浓度为 0.098 1 mg/mL, RSD为 0.84%;黄芪甲苷平均质量浓度为 0.062 9 mg/mL, RSD为0.89%。 结果表明方法的重复性良好。
2.10 加样回收试验 取心脑舒口服液 (批号20120301) 适量, 精密量取 6 份, 每份 5 mL, 置具塞锥形瓶中,分别精密加入 “2.2” 项下的对照品溶液 5 m L(含人参皂苷 Rg10.507 0 mg、 人参皂苷 Re 0.947 0 mg、人参皂苷 Rf 4.215 5 mg、 人参皂苷 Rb12.108 5 mg、 人参皂苷 Rb20.512 0 mg、人参皂苷 Rb30.454 0 mg和黄芪甲苷 0.291 5mg),制备供试品溶液, 进样 5 μL, 按 “2.1” 项色谱条件分析。 回收率分别为 98.1%、 98.1%、 98.5%、98.2%、 98.6%、 98.7%、 98.5%, RSD 分 别 为1.1%、 0.87%、 0.58%、 0.58%、 0.49%、1.1%、 0.42%, 结果表明该方法的回收率良好。结果见表2。
2.11 样品的测定 分别取 3 批心脑舒口服液样品制成的供试品溶液各5 μL, 以及 “2.1”项下的对照品溶液 5 μL、10 μL、 15 μL注入液相色谱仪,测定,按外标三点法对数方程进行计算。结果见表3。
3 讨论
3.1 样品测定结果显示不同批次样品中各待测成分的量存在较大差异,这可能与药材质量存在较大联系,进一步提示测定该制剂中7种成分的必要性,对保证制剂的质量和临床疗效的稳定可靠有着重要影响。

表 2 加样回收率试验结果 (n=6)Tab.2 Results of recovery tests(n=6)
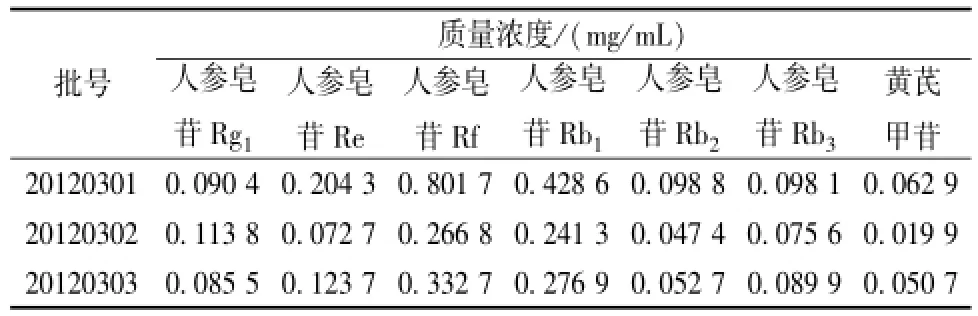
表3 心脑舒口服液中有效成分的测定结果 (n=3)Tab.3 Determ ination of active com Ponents in Xinnaoshu O ral Liquid( n=3)
3.2 目前的文献报道中仅有心脑舒口服液中人参皂苷 Rg1与人参皂苷 Re的定量测定, 本实验将心脑舒口服液中人参中人参皂苷 Rg1、 人参皂苷 Rb1、人参皂苷 Rb2、 人参皂苷 Rb3、 人参皂苷 Re、 人参皂苷 Rf等 6 种成分和黄芪中黄芪甲苷共7 种成分的量进行同时测定。
3.3 在色谱条件的选择中, 由于使用蒸发光检测器,不能使用非挥发性的试剂,参考相关文献,可选择的流动相只有甲醇-水、 乙腈-水两种, 综合实验结果, 以乙腈-水为流动相, 色谱行为更理想。
3.4 在供试品溶液的制备过程中, 曾考察过直接加水饱和的正丁醇提取与加水稀释后用水饱和正丁醇提取,由于本品含糖量较高,加水稀释后有利于萃取分层。
3.5 在供试品溶液的制备过程中, 正丁醇液的洗涤曾考察过浓氨试液、 氨试液以及1%氢氧化钠溶液,由于黄芪甲苷在碱性环境中存在转化的过程,综合试验结果以及操作过程,最后选择以浓氨试液作为洗涤溶剂。
[ 1 ] 国家药典委员会.中华人民共和国药典: 2010 年版一部[S].北京: 中国医药科技出版社, 2010.
[ 2 ] 李红月, 李 军.心脑舒口服液中人参皂苷 Rg1、 人参皂苷 Re的含量测定[J].黑龙江科技信息, 2011(15): 24.
[3] 郑先华, 于 伟, 陈 桦.心脑舒口服液质量标准的研究[J].云南中医中药杂志, 2006, 27(4): 41-42.
[4] 刘浩文,刘嘉仪.黄芪药材中黄芪甲苷含量测定的两种方法的比较 [J].中药新药与临床药理, 2011, 22 (6):659-662..
[ 5 ] 范 辉, 顾泉琳, 贝伟剑, 等.HPLC法测定乌参醒脑滴丸中人参皂苷 Rg1、 Re、 Rb1和 Rd [J].中成药, 2012,34(8): 1280-1283.
[ 6 ] 刘 志, 阮长春, 刘天志, 等.HPLC法同时测定林下参、鲜人参、 生晒参和红参中 14 种人参皂苷[J].中草药,2012, 43(7): 2431-2434.
[ 7 ] 曹树萍, 聂黎行, 王钢力, 等.HPLC法同时测定参麦注射液中 9 个人参皂苷的含量[J].药物分析杂志, 2011, 41(8): 476-479.
[ 8 ] 汪 冰, 尤慧莲, 徐丽华.HPLC法测定芪参胶囊中五种成分的含量[J].中成药, 2012, 34(3): 483-486.
[ 9 ] 代 龙.HPLC法测定血塞通分散片中三七皂苷 R1及人参皂苷 Rg1、 Rb1的 含 量 [ J].齐 鲁 药 事, 2009, 28 ( 6 ):333-335.
[10] 刁保忠, 靳维荣, 王登旭, 等.RP-HPLC法测定生津益气口服液中黄芪甲苷的含量[J].齐鲁药事, 2012, 31(10):588-589.
[11] 陈祖云, 石凌云, 黄 勇, 等.HPLC-ELSD法测定脑通颗粒中黄芪甲苷和人参皂苷 Rb1的含量及稳定性[J].中国药房, 2011, 22(23): 2164-2166.
[12] 冯向东, 黄海欣, 高光伟, 等.HPLC-ELSD测定心宁片中三七皂苷 R1、 人参皂苷 Rg1、 人参皂苷 Rb1的含量[J].中成药, 2007, 29(12): 1786-1789.
[13] 曹湘萍, 梁建宁, 何晓艳, 等.HPLC-ELSD法测定乙肝宁颗粒中黄芪甲苷的含量[ J].中成 药, 2005, 27 (2):165-167.
[14] 林 雅, 施 红.HPLC-ELSD法测定石斛合剂中黄芪甲苷的含量[ J].福建中医学院学报, 2008, 18(1) : 31-32.
[15] 刘元媛, 张振秋.HPLC-ELSD测定康艾扶正片中黄芪甲苷的含量[J].中成药, 2007, 29(11): 1705-1706.
Determ ination of seven saPonins in Xinnaoshu Oral Liquid by HPLC-ELSD
LIN Lin, LIU Guang-zhen, LIU Hong-chao, XU Li-hua
(Shandong Provincial Institute for Food and Drug Control, Jinan 250101, China)
AIM To develop amethod for determining seven kinds of saponins in Xinnaoshu Oral Liquid ( Astragali Radix, Ginseng Radix et Rhizoma, Schisandrae Chinensis Fructus, Codonopsis Radix,Ophiopogonis Radix).METHODS The quantative analysiswas carried outon a column of Kromasil C18by HPLC-ELSD, using a mobile phase of acetonitrile-water under a flow rate of 1 m L/min.RESULTS The linear ranges of ginsenoside Rg1, ginsenoside Re, ginsenoside Rf, ginsenoside Rb1, ginsenoside Rb2, ginsenoside Rb3and astragaloside fell within the ranges of 0.202 8-2.028 μg, 0.378 8-3.788 μg, 1.686 2-16.862 μg, 0.843 4-8.434 μg, 0.204 8-2.048 μg, 0.181 6-1.816 μg, 0.116 6-1.166 μg,respectively, The seven components showed good linear correlations(r=1.00, r=1.00, r=1.00, r=1.00, r=1.00, r=1.00, r=1.00) .The recoveries were 98.1%for ginsenoside Rg1, 98.1%for ginsenoside Re, 98.5%for ginsenoside Rf, 98.2%for ginsenoside Rb1, 98.6%for ginsenoside Rb2, 98.7%for ginsenoside Rb3, and 98.5%for astragaloside, respectively.The relative standard deviationswere 1.1%,0.87%, 0.58%, 0.58%, 0.49%, 1.1%, 0.42%,respectively(n=6 ).CONCLUSION Thismethod is simple, accurate, reproducible and convenient for the quality control over Xinnaoshu Oral Liquid.
Xinnaoshu Oral Liquid; ginsenoside Rg1; ginsenoside Re;ginsenoside Rf;ginsenoside Rb1;ginsenoside Rb2; ginsenoside Rb3; astragaloside
R927.2
: A
: 1001-1528(2014)01-0090-05
10.3969/j.issn.1001-1528.2014.01.022
2013-03-18
基鑫项目: 2013 年山东省自然科学基金 (ZR2013HM074)
林 林 (1980—) , 女, 主管药师, 硕士, 研究方向: 中药分析。 Tel(0531) 81216523, E-mail: linlinsfda@163.com
