头痛滴丸不同提取工艺指纹图谱比较研究
2014-04-11龚苏晓张铁军王思路
刘 悦, 龚苏晓, 张铁军*, 王思路, 胡 乔
(1.天津中医药大学, 天津 300070; 2.天津药物研究院释药技术与药物代谢动力学国家重点实验室,天津 300193; 3.天津药物研究院中药现代制剂与中药质量控制技术国家和地方工程实验室, 天津 300193)
头痛滴丸不同提取工艺指纹图谱比较研究
刘 悦1,2,3, 龚苏晓2,3, 张铁军2,3*, 王思路1,2,3, 胡 乔1,2,3
(1.天津中医药大学, 天津 300070; 2.天津药物研究院释药技术与药物代谢动力学国家重点实验室,天津 300193; 3.天津药物研究院中药现代制剂与中药质量控制技术国家和地方工程实验室, 天津 300193)
目的 优选头痛滴丸 (川芎、藁本、 菊花、 白芷、 钩藤) 最佳提取方法。方法 采用高效液相色谱法, 建立头痛滴丸的化学成分指纹图谱的测定方法,以阿魏酸、木犀草苷、藁本内酯3种对照品进行色谱峰指认,确定特征色谱峰的药材归属, 比较头痛滴丸的水回流提取、 传统水煎煮、 80%乙醇回流提取、 80%乙醇渗漉提取 4 种提取方法的特征色谱峰数目和相对峰面积大小, 优选出最佳提取方法。 结果 醇渗漉提取工艺样品中共标记了45个色谱峰, 其中有21个药材特征峰, 且醇渗漉提取工艺相比其他提取工艺, 特征色谱峰的数量和相对峰面积均具有明显优势, 其中有19个药材特征峰相对峰面积最大。 结论 通过头痛滴丸4种不同的提取工艺的对比, 确定醇渗漉提取工艺优于其他工艺。
头痛滴丸;化学成分;指纹图谱;提取工艺
头痛滴丸方为临床经验方,由川芎、藁本、菊花、白芷、钩藤等8味药组成,具有疏风止痛、清热平肝熄风的功效,临床常用来治疗偏头痛。川芎、藁本中的有机酸和挥发油类成分,菊花中黄酮及苷类成分,白芷中的挥发油和香豆素类成分以及钩藤中的生物碱类成分均为治疗头痛的主要指标成分[1-5]。 方中川芎、 藁本为君药, 阿魏酸、 藁本内酯是两药的共有成分,阿魏酸能够抗凝血,具有抗炎镇痛的作用[6]。 藁本内酯具有镇静、 镇痛、 解痉、抗惊厥等作用,被认为是治疗偏头痛的物质基础[7]。 菊花为臣药, 疏散清热,主要药效成分为木犀草苷, 具有抗炎和镇痛作用[8]。 中药药效是多成分、多靶点整体作用的结果,在对中药的提取工艺筛选过程中,若只采用某单一化学成含有量为指标,不能较全面地表征出复方全貌的特点,具有一定的局限性。本实验运用高效液相色谱法建立了头痛滴丸不同提取工艺的化学成分指纹图谱,尽可能多的得到各成分的色谱峰,相对完整地反映出全方的化学成分,以不同提取工艺的特征峰面积的数量和相对峰面积 (以相应对照药材色谱图为基准计算)的大小为依据来评价不同提取工艺的优劣,并用各单一对照药材对全方化学成分指纹图谱峰进行镜像比对,以确定不同特征峰归属。
1 仪器与试药
Dionex Summit高效液相色谱仪 (美国戴安公司); Lab Alliance高效液相色谱仪 ( 美国兰博公司); 超声波提取器 AS3120 (江苏汉邦科技有限公司) ; AB204-N电 子 天 平 ( 万 分 之 一, Mettler-Toledo); BP211D电子天平 ( 十万分之一,Sarlorius);R501B星海旋转蒸发器 (无锡市星海王生化设备有限公司); 电加热套 PTHW型 (河南豫华仪器有限公司)。
阿魏酸对照品 (批号 110773-200611, 购自中国药品生物制品检定所)、木犀草苷对照品 (批号11720-201106, 购自中国食品药品检定研究院)、藁本内酯对照品 (自制, 批号 20130301)。 甲醇(天津市康科德科技有限公司) 为分析纯和色谱纯,水为娃哈哈纯净水,其余试剂均为分析纯。
方中各味药材均购自天津中药饮片厂,经天津药物研究院张铁军研究员鉴定, 均符合 2010 年版《中国药典》 规定。
2 方法与结果
2.1 对照品的制备 精密称取阿魏酸、 木犀草苷、藁本内酯对照品适量, 置于25 m L量瓶中, 加甲醇溶解,定容并稀释至刻度,摇匀,得混合对照贮备液; 取其中1 mL贮备液置10 m L量瓶中, 加甲醇稀释至刻度, 摇匀, 得每 1 m L含阿魏酸20.56 μg、木犀草苷 26.80 μg、 藁本内酯 34.10 μg的混合对照品溶液。
2.2 供试品溶液的制备
2.2.1 工艺 1 样品的制备 称取 6 倍处方量的川芎、 藁本、 白芷、 菊花等药材, 砸碎, 10 倍量水冷浸 60 min, 回流提取 3 次, 每次 1.5 h, 合并 3次提取液放冷,减压浓缩得稠膏,作为样品1 (每1 g稠膏约含2 g生药)。
2.2.2 工艺 2 样品的制备 称取 6 倍处方量的川芎、藁本、白芷、菊花等药材,砸碎,加水冷浸30 min, 加水量为没过药材 5 cm, 煎煮 2 次, 第 1煎 30 min, 加水量为 2 000 m L, 纱布过滤。 第 2 煎20 min, 加水量为 1 200 mL, 纱布过滤。 合并两次滤液, 减压浓缩至稠膏, 作为样品2 (每1 g稠膏约含2 g生药)。
2.2.3 工艺 3 样品的制备 称取 6 倍处方量的川芎、 藁本、 白芷、 菊花等药材, 砸碎, 10 倍量80%乙醇冷浸 60 min, 回流提取 3 次, 每次 1.5 h,合并3次提取液放冷,减压浓缩得稠膏,作为样品3 (每1 g稠膏约含2 g生药)。
2.2.4 工艺 4 样品的制备 称取 6 倍处方量的川芎、藁本、白芷、菊花等药材,粉碎成粗粉,过10 目筛, 3 倍量 80%乙醇浸泡过夜后, 开始渗漉,渗漉体积流量为 5 m L/( min·kg), 溶剂用量为 14倍量,收集渗漉液,混匀,减压浓缩得稠膏,作为样品4 (每1 g稠膏约含2 g生药)。
2.2.5 对照药材溶液制备 称取川芎对照药材,按照混合提取工艺中相应工艺进行提取,制得川芎对照药材溶液;同法制得藁本、菊花、白芷、钩藤、全蝎、郁金、细辛对照药材溶液。
2.3 色谱条件与系统适应性 Dikma Diamonsil-C18色谱柱 (250 mm×4.6 mm, 5 μm), 流动相为甲醇 (A)-0.05%磷酸溶液 (B) 梯度洗脱 (0 ~14 min, 35%→50%A; 14 ~16 min, 50% →75%A;16 ~35 min, 75% →77%A; 35 ~36 min, 77%→35%A; 36 ~40 min, 35%A)。 柱温 30 ℃, 体积流量 1 mL/min, 波长 282 nm。
2.4 方法学考察
2.4.1 精密度试验 取工艺 4 样品,连续进样 6次, 按 “2.3” 项色谱条件进行测定, 计算各特征色谱峰的相对保留时间和相对峰面积的 RSD值,结果分别为 0.65% ~1.86%、1.23% ~2.34%,表明该仪器精密度良好 (相对峰面积以 39 号峰藁本内酯为参比峰)。
2.4.2 稳定性试验 取工艺 4 样品, 室温放置, 分别于 0、 2、4、 8、 16、 24 h 取样, 按 “2.3”项色谱条件测定,每次进样量均为 10 μL, 计算各特征色谱峰的相对保留时间和相对峰面积的 RSD值,结果分 别为 0.78% ~1.92%、 1.42% ~2.44%,表明供试品溶液室温放置 24 h 内稳定 (相对峰面积以 39 号峰藁本内酯为参比峰)。
2.4.3 重复性试验 取工艺 4 样品, 按供试品溶液制备方法制备 6 份, 按 “2.3” 项下色谱条件测定,计算各特征色谱峰的相对保留时间和相对峰面积 的 RSD 值,结 果 分 别 为 0.87% ~1.76%、1.56% ~2.63%, 表明该方法的重复性良好 (相对峰面积以 39 号峰藁本内酯为参比峰)。
2.5 样品测定
2.5.1 不同提取工艺样品指纹图谱比较 取等生药量样品, 溶于 25 mL甲醇中, 超声处理 30 min,过 0.45 μm微孔滤膜, 备用。 按 “2.3” 项色谱条件进行测定, 并进行主要色谱峰的指认。 如图1、2所示。

图1 混合对照品色谱图Fig.1 Chromatogram ofm ixed reference substances

图2 头痛滴丸不同提取方法的 HPLC指纹图谱Fig.2 HPLC fingerPrints of Toutong DroPPing Pills sam Ples w ith d ifferent extraction methods
2.5.2 特征峰的药材归属 醇渗漉工艺共标记了45个色谱峰, 以醇渗漉提取工艺为基准, 分别对各药材工艺样品进行镜像比对,确定了21个色谱峰的药材归属,如图3~8所示。归属的特征峰如表1所示。
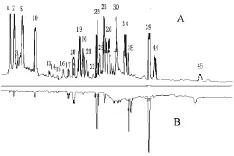
图3 头痛滴丸醇渗漉提取和川芎镜像图Fig.3 Ethanol Percolation extraction of Toutong DroPPing Pills and Chuanxiong Rhizoma comParison chart
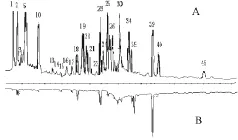
图4 头痛滴丸醇渗漉提取和藁本镜像图Fig.4 Ethanol Percolation extraction of Toutong DroPPing Pills and Ligustici Rhizoma com Parison chart

图5 头痛滴丸醇渗漉提取和白芷镜像图Fig.5 Ethanol Percolation extraction of Toutong D roPPing Pills and Angelica dahurica Rhizoma com Parison char t
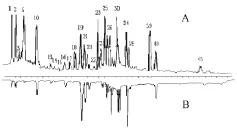
图6 头痛滴丸醇渗漉提取和菊花镜像图Fig.6 Ethanol Percolation extraction of Tou tong DroPPing Pills and Chrysanthem i Flos com-Parison chart
2.5.3 不同工艺样品特征峰的相对峰面积比较以相应的对照药材色谱图为基准,计算4个不同工艺样品相应特征峰的相对峰面积,如表2所示。
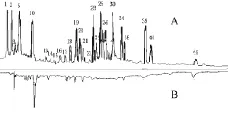
图7 头痛滴丸醇渗漉提取和钩藤镜像图Fig.7 Ethanol Percolation extraction of Toutong DroPPing Pills and Uncaria rhynchophylla com Parison char t
2.5.4 数据分析 通过药材归属和各工艺特征峰的相对峰面积的计算,得出工艺4样品的特征色谱峰数目和相对峰面积均具有明显优势。工艺3和工艺4的特征色谱峰为 16个。 疏风止痛类药材共归属了11个色谱峰, 其中工艺4样品 9个峰的相对峰面积最大, 2个峰的相对峰面积略小于工艺3。清热平肝熄风类药材共归属了 12个色谱峰, 其中工艺4样品8个峰的相对峰面积最大,2个峰的相对峰面积略小于工艺3, 另2个峰的相对峰面积略小于工艺 1。温经散寒类药材共归属了 4个色谱峰,其中工艺4样品3个峰的相对峰面积最大,1个峰的相对峰面积略小于工艺一。

图8 头痛滴丸醇渗漉提取和细辛镜像图Fig.8 Ethanol Percolation extraction of Toutong DroPPing Pills and Asari Herba com Parison chart
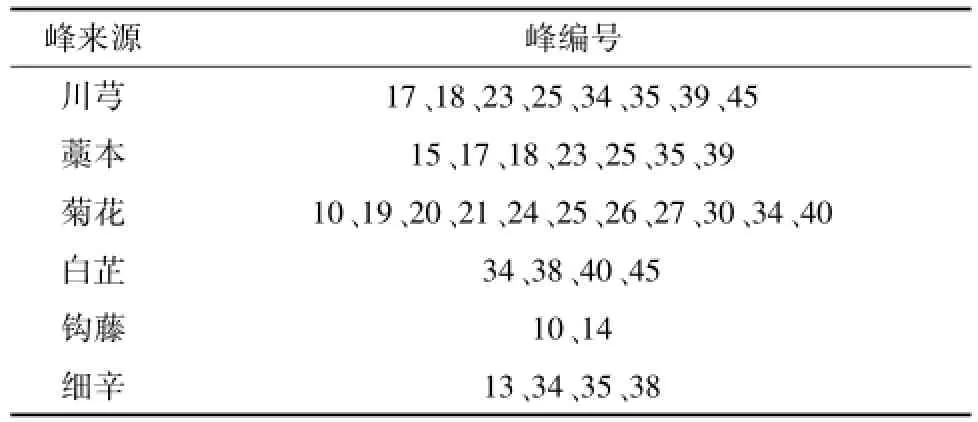
表1 色谱峰的药材归属Tab.1 ChromatograPhic Peaks belonging to herbs
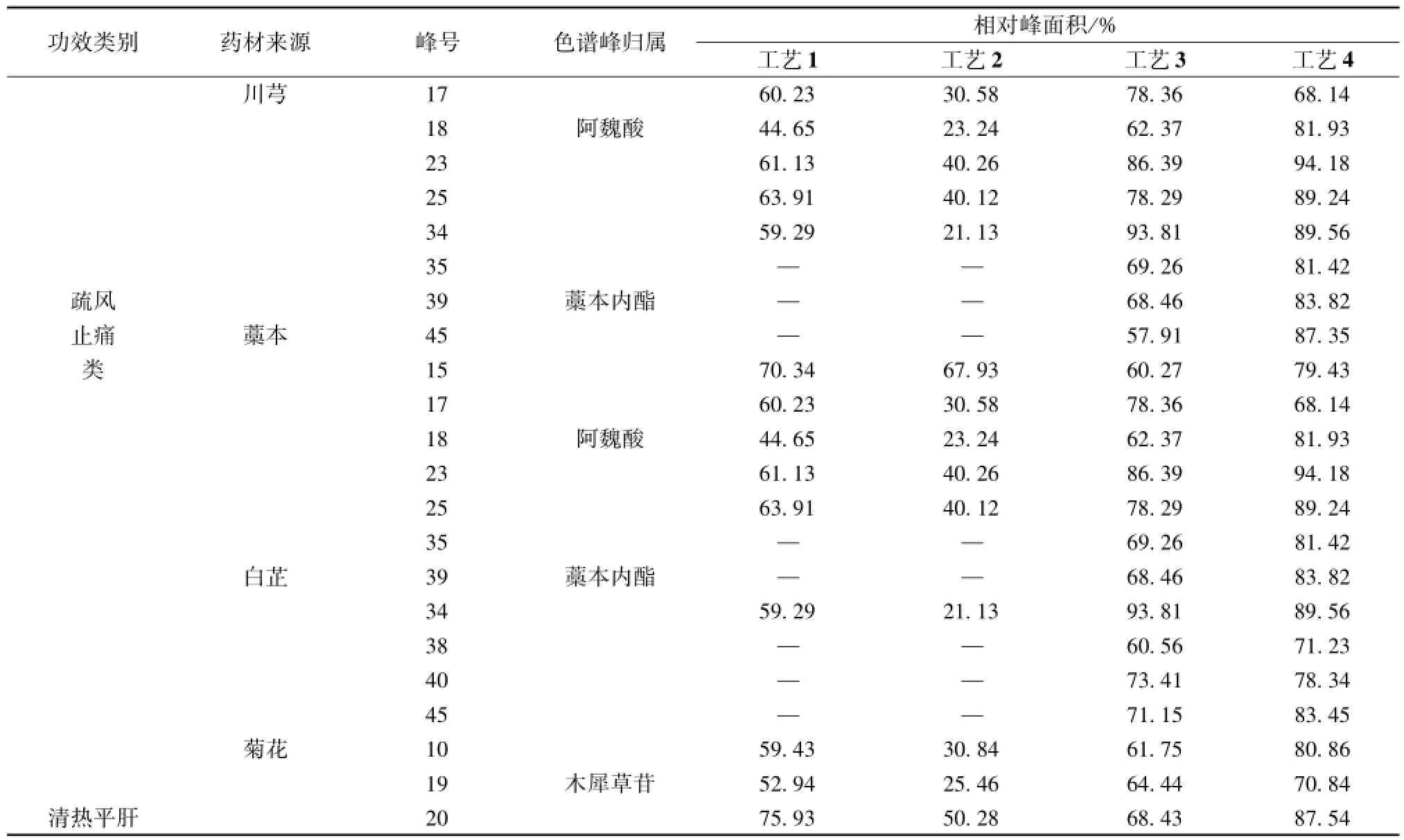
表2 不同提取方法样品色谱峰相对峰面积比较Tab.2 Relative Peak areas of different sam Ples
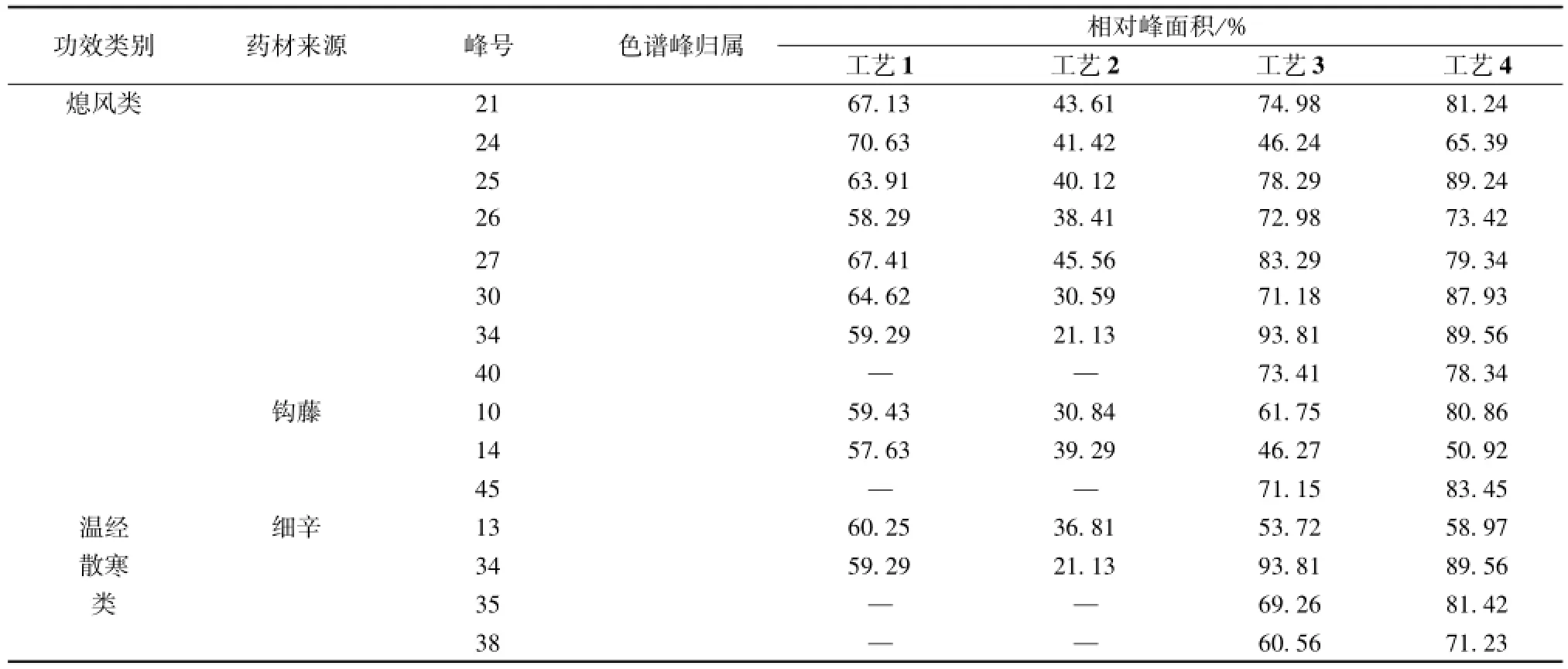
续表2
3 结论与讨论
3.1 在中药复方提取工艺的筛选过程中, 目前多以干浸膏得率、单体含有量和化学部位含有量为指标评价不同工艺的优劣,此种方法不能较全面地表征出中药复方的全貌,具有一定局限性。指纹图谱技术是目前公认的能较全面反映中药整体化学特征的手段[9]。 本实验建立了头痛滴丸方不同提取工艺的指纹图谱,测定了复方提取液的高效液相色谱(HPLC) 指纹图谱数据, 并结合功效类别对其进行信息提取和统计,较之于以往可以更全面地掌握复方多成分的信息。
3.2 本实验的复方化学成分较多,各特征峰吸收波长不一致, 通过DAD检测器, 进行全波长扫描,结果发现 282 nm下色谱峰信息较全面, 故确定检测波长为 282 nm。
3.3 根据复方中各药材的化学成分及其药理作用,初步拟定了4种不同的提取工艺,建立了不同提取工艺的 HPLC图谱, 之后进行了药材归属。 通过图谱可知,醇渗漉提取和醇回流提取工艺的特征色谱峰多于传统水煎和水回流提取工艺,醇渗漉提取工艺的特征色谱峰数目和相对峰面积明显优于其他工艺,故初步确定醇渗漉提取工艺为最佳提取工艺,为后期的制剂工艺和药效学实验研究奠定了基础。
3.4 虽然此化学成分指纹图谱可以提供较为丰富的中药提取物信息,但本实验采用紫外检测器,只能提供提取液中具有紫外吸收的成分的相对含量信息,且色谱峰所对应成分的药效作用尚不完全清楚,今后有待于建立药液的液质联用指纹图谱,借助质谱等更加灵敏、通用的检测系统,进行全成分的高效分析、检测,提高中药复方的提取效率,为制剂的前处理提供更多的理论依据。
[ 1 ] 裴艳霞.川芎的药理作用及临床应用 [J].中国医药指南,2011, 9(34): 197-198.
[ 2 ] 唐 忠.藁本化学成分及药理研究[J].中国医药指南,2011, 9(30): 34-35.
[3] 张晓媛,段立华,赵 丁.菊花化学成分及药理作用的研究[ J] .时珍国医国药, 2008, 19(7) : 1702-1704.
[4] 崔秋兵, 张 艺, 兰 莎.白芷镇痛作用物质基础研究[J].中国实验方剂学杂志, 2010, 16(12): 102-104.
[5] 叶 齐, 齐荔红.钩藤的主要成分及生物活性研究进展[J].西北药学杂志, 2012, 27(5): 508-510.
[ 6 ] 曲培向.川芎药理作用研究进展[J].内蒙古中医药,2010, 3: 78-79.
[7] 左爱华,王 莉,肖红斌.藁本内酯药理学和药代动力学研究 进 展 [ J]. 中 国 中 药 杂 志, 2012, 37 ( 22 ):3350-3353.
[8] 刘 圆,李园园, 冯婷婷, 等.木犀草素镇痛抗炎作用的实 验 研 究 [ J]. 齐 齐 哈 尔 医 学 院 学 报, 2010, 31(15): 2370.
[ 9 ] Sun G X, Bi K S.Effect of fingerprintology of traditional Chinesemedicine( TCM) in the innovative development of TCM[ J] .Chin JChromatogr, 2008, 26(2) : 172-179.
Com Parison of fingerPrints of different extraction Processes of Toutong DroPPing Pills
LIU Yue1,2,3, GONG Su-xiao2,3, ZHANG Tie-jun2,3, WANG Si-lu1,2,3, HU Qiao1,2,3
(1.Tianjin University of Traditional ChineseMedicine, Tianjin 300073, China; 2.Tianjin Instituteof Pharmaceutical Research, State Key Laboratory of Drug Delivery Technologies and Drug Metabolism, Tianjin 300193, China; 3.Tianjin Instituteof Pharmaceutical Research, The National and Local Engineering Laboratory of the Modernized Chinese Medicine and Chinese Medicine Quality Control Techniques, Tianjin 300193, China)
Toutong Dropping Pills; chemical constituent;chromatographic fingerprint; extraction process
R284.2
: A
: 1001-1528(2014)01-0085-05
10.3969/j.issn.1001-1528.2014.01.021
2013-03-14
刘 悦 (1987—) , 女, 硕士生, 研究方向: 中药制剂。 Tel: 15822365678, E-mail: ldkmeng@sina.com
*通信作者: 张铁军 Tel: (022) 23006848
